BIOENERGTICA BIOQUMICA IZPS D PH PERLA LUCA ORDEZ

BIOENERGÉTICA BIOQUÍMICA IZPS D. PH. PERLA LUCÍA ORDÓÑEZ BAQUERA

• • • INTRODUCCIÓN La TERMODINÁMICA describe y relaciona las propiedades físicas de la materia y sus cambios de ENERGÍA. Los seres vivos requieren energía y debe existir un balance energético entre la célula y su entorno (1 era ley). Cualquier proceso que sucede en la célula PRODUCE o CONSUME energía. Los Sistemas Biológicos forman biomoléculas que interaccionan para producir organismos complejos. La CÉLULA es una gran fábrica química donde cada segundo se realizan miles de reacciones que requieren una fuente de materia (átomos de los nutrientes) y una fuente de energía (que al final de cuentas proviene del Sol). El objetivo general de un ser vivo es generar orden para que el vida sea posible.

ENERGÍA EN LAS MOLÉCULAS • • • ENERGÍA: Capacidad de producir un cambio y se mide por la cantidad de trabajo realizado durante el periodo del cambio. La presencia de energía solo se observa cuando ocurre el cambio. ENERGÍA POTENCIAL: Cantidad de trabajo que puede realizarse al liberar la energía almacenada en un determinado lugar. ENERGÍA DE COMBUSTIÓN: Energía contenida en los enlaces de Carbono de los combustibles y que se libera por el proceso de combustión. ENERGÍA QUÍMICA EN LA CÉLULA: Energía que se obtiene a partir de la combustión de los nutrientes y que se utiliza para realizar un TRABAJO CELULAR.

TIPOS DE TRABAJO CELULAR QUE REQUIEREN ENERGÍA • Reacciones química no favorables o • Movimiento de moléculas a través de espontáneas. membranas. • Reacciones que generen orden y por lo tanto un alto contenido de información. • Crecimiento y división celular.
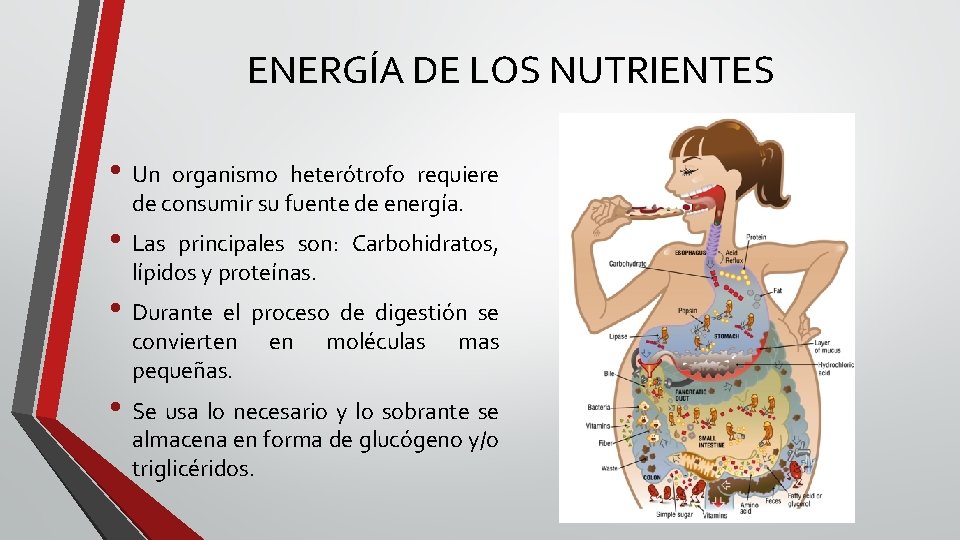
ENERGÍA DE LOS NUTRIENTES • Un organismo heterótrofo requiere de consumir su fuente de energía. • Las principales son: Carbohidratos, lípidos y proteínas. • Durante el proceso de digestión se convierten pequeñas. en moléculas mas • Se usa lo necesario y lo sobrante se almacena en forma de glucógeno y/o triglicéridos.

ENERGÍA DE LOS NUTRIENTES • • RENDIMIENTO ENERGÉTICO: Depende de lo eficiente del proceso digestivo. No solo se toma en cuenta el contenido calórico. Un elevado contenido de energía depende de los enlaces químicos que al romperse liberan energía.

COMBUSTIÓN • Los H unidos al C se liberan y se unen al O para formar agua. • Se libera energía en forma de calor. • La celulosa al quemarse se convierte en CO 2
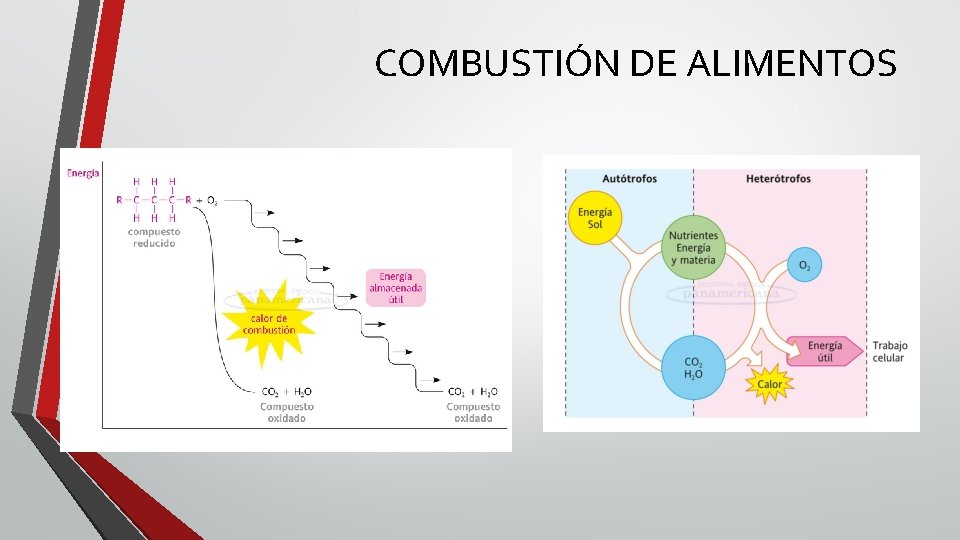
COMBUSTIÓN DE ALIMENTOS

SISTEMAS BIOLÓGICOS • • Un SISTEMA es una pequeña parte del UNIVERSO que se aísla para someterla a estudio (célula, rx química). Todo lo que rodea al sistema es el ENTORNO. El ENTORNO mas el SISTEMA se denomina UNIVERSO. Puede haber sistemas: Aislados, Cerrados o Abiertos.
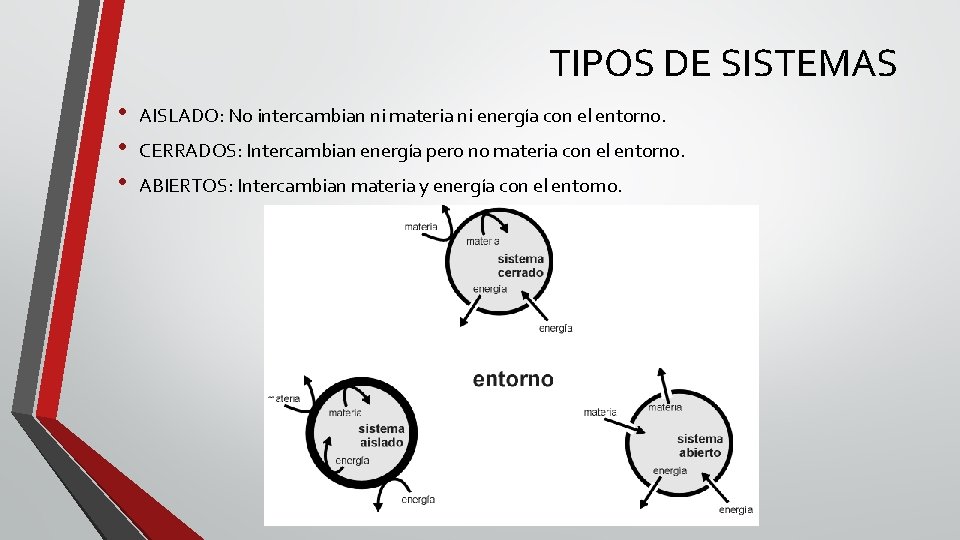
TIPOS DE SISTEMAS • • • AISLADO: No intercambian ni materia ni energía con el entorno. CERRADOS: Intercambian energía pero no materia con el entorno. ABIERTOS: Intercambian materia y energía con el entorno.

FUNCIÓN DE ESTADO • Magnitud física que caracteriza el estado de un sistema en equilibrio. (Variables que nos indican como se comportaría el sistema). • Entalpía (H) Entropía (S) Energía libre de Gibbs (G). • Se miden según el cambio que se produce para que el sistema alcance el equilibrio y se representan por : Δ (ΔH, ΔS y ΔG). • Δ=incremento= Estado final –Estado inicial
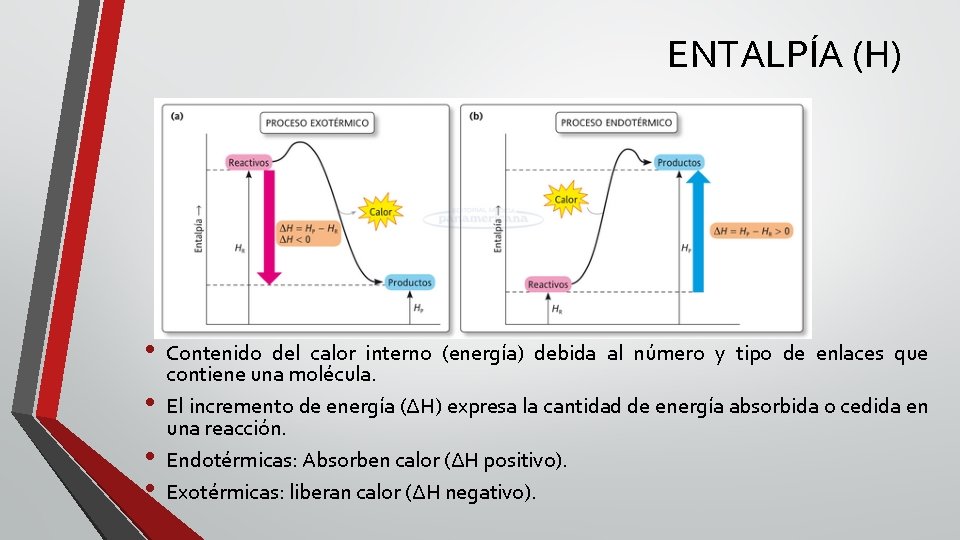
ENTALPÍA (H) • • Contenido del calor interno (energía) debida al número y tipo de enlaces que contiene una molécula. El incremento de energía (ΔH) expresa la cantidad de energía absorbida o cedida en una reacción. Endotérmicas: Absorben calor (ΔH positivo). Exotérmicas: liberan calor (ΔH negativo).
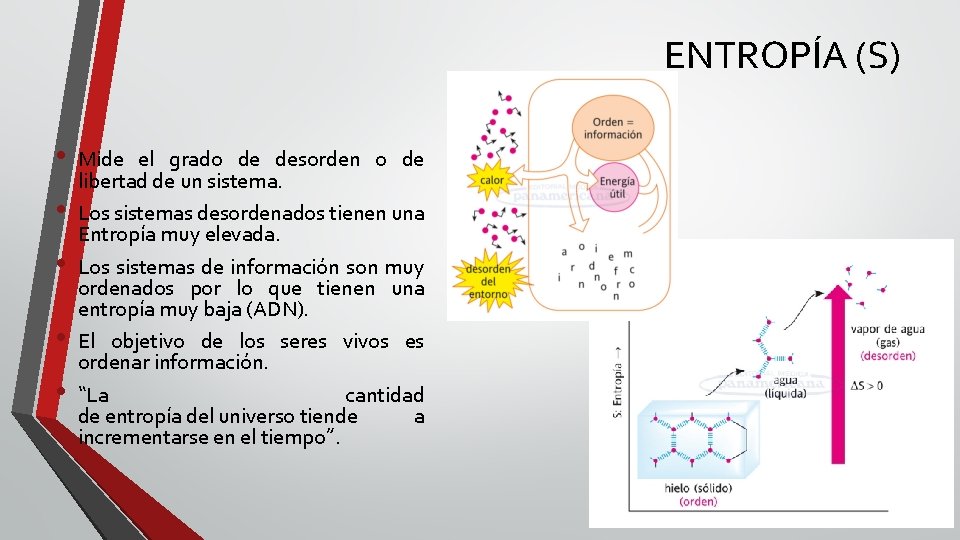
ENTROPÍA (S) • • • Mide el grado de desorden o de libertad de un sistema. Los sistemas desordenados tienen una Entropía muy elevada. Los sistemas de información son muy ordenados por lo que tienen una entropía muy baja (ADN). El objetivo de los seres vivos es ordenar información. “La cantidad de entropía del universo tiende a incrementarse en el tiempo”.

ENTROPÍA (S) • En los sistemas abiertos hay que tomar en cuenta el intercambio de entropía con el entorno. • En las reacciones exotérmicas aumenta la entropía del entorno. • En las reacciones endotérmicas disminuye la entropía del entorno. • Una reacción es mas problable si se da en situaciones de aumento de entropía.

ENERGÍA LIBRE DE GIBBS • Permite predecir la dirección de las reacciones químicas, su posición exacta en el equilibrio y la cantidad de trabajo que pueden llevar a cabo. • Indica que si una reacción va a ser espontánea o no. ΔG = ΔH –T ΔS

TAREA • Investigar que es la cinética enzimática. • Mecanismos de acción de las enzimas. • Clasificación de las enzimas (con descripción)
- Slides: 16