Biochimica clinica Il laboratorio nelle malattie del fegato

Biochimica clinica Il laboratorio nelle malattie del fegato
Fegato umano; Reperto autoptico
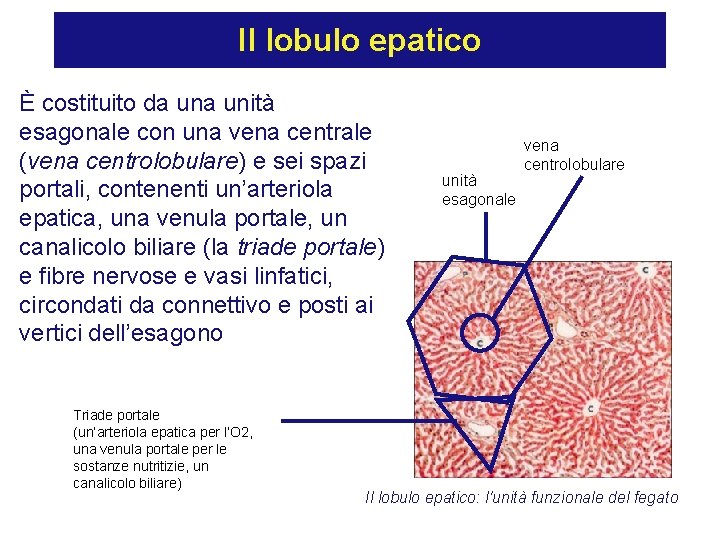
Il lobulo epatico È costituito da unità esagonale con una vena centrale (vena centrolobulare) e sei spazi portali, contenenti un’arteriola epatica, una venula portale, un canalicolo biliare (la triade portale) e fibre nervose e vasi linfatici, circondati da connettivo e posti ai vertici dell’esagono Triade portale (un’arteriola epatica per l’O 2, una venula portale per le sostanze nutritizie, un canalicolo biliare) unità esagonale vena centrolobulare Il lobulo epatico: l'unità funzionale del fegato
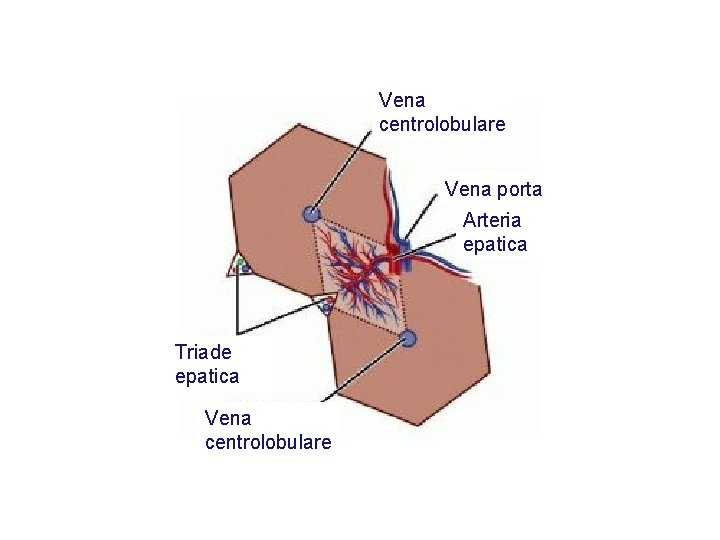
Vena centrolobulare Vena porta Arteria epatica Triade epatica Vena centrolobulare

Cellule del fegato cellule parenchimali (65% volume del fegato): epatociti cellule non parenchimali (35% volume del fegato): cellule endoteliali cellule del sistema reticolo-endoteliale (di Kupffer) cellule stellate o cellule di Ito cellule dei dotti biliari

Le vie metaboliche della glicolisi del ciclo di Krebs, della sintesi degli amminoacidi e dei processi di fosforilazione ossidativa avvengono tutti all’interno degli epatociti, che sono particolarmente ricchi di mitocondri.

L’irrorazione del fegato Gli epatociti sono irrorati da un duplice sistema di vasi afferenti (sinusoidi): ■ rami dell’arteria epatica (O 2) ■ rami del sistema venoso portale (sostanze assorbite)
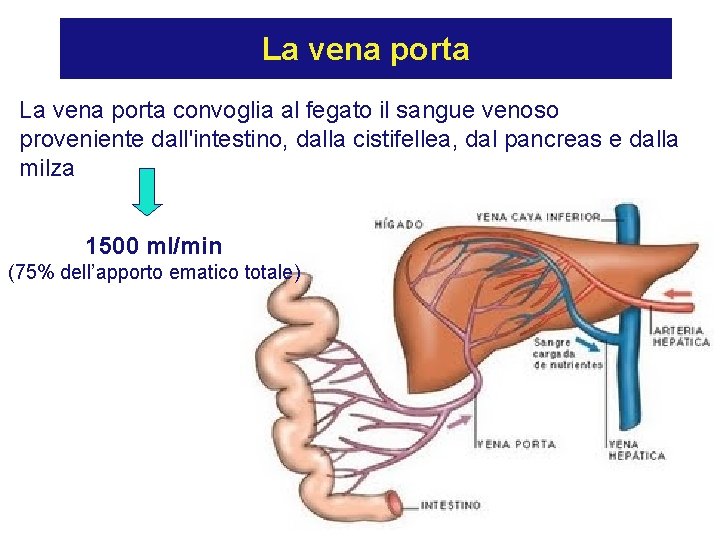
La vena porta convoglia al fegato il sangue venoso proveniente dall'intestino, dalla cistifellea, dal pancreas e dalla milza 1500 ml/min (75% dell’apporto ematico totale)
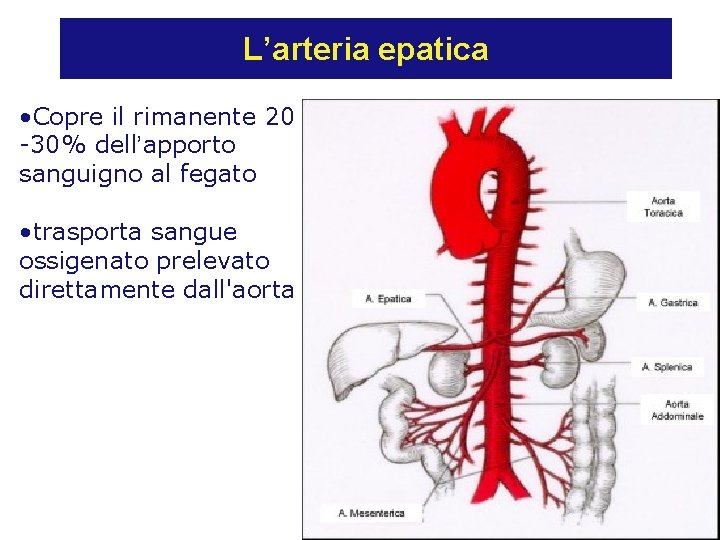
L’arteria epatica • Copre il rimanente 20 -30% dell’apporto sanguigno al fegato • trasporta sangue ossigenato prelevato direttamente dall'aorta
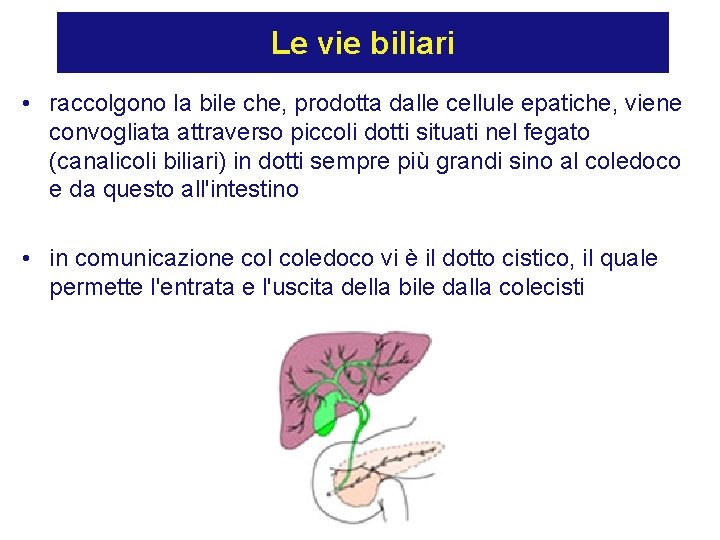
Le vie biliari • raccolgono la bile che, prodotta dalle cellule epatiche, viene convogliata attraverso piccoli dotti situati nel fegato (canalicoli biliari) in dotti sempre più grandi sino al coledoco e da questo all'intestino • in comunicazione coledoco vi è il dotto cistico, il quale permette l'entrata e l'uscita della bile dalla colecisti
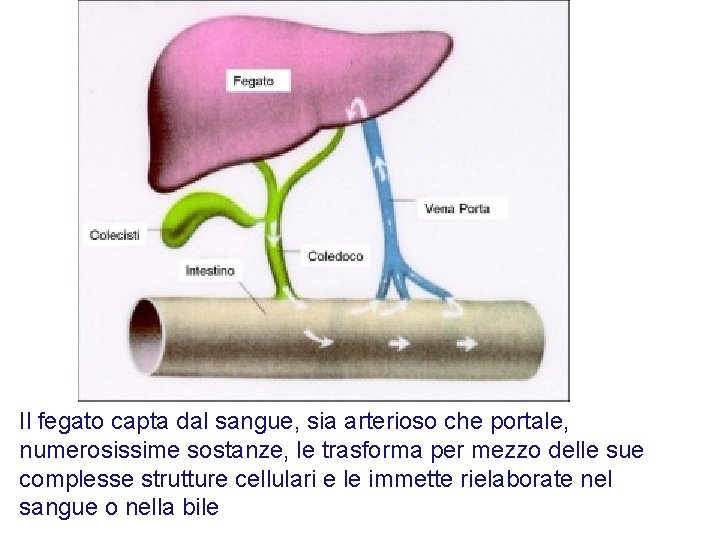
Il fegato capta dal sangue, sia arterioso che portale, numerosissime sostanze, le trasforma per mezzo delle sue complesse strutture cellulari e le immette rielaborate nel sangue o nella bile
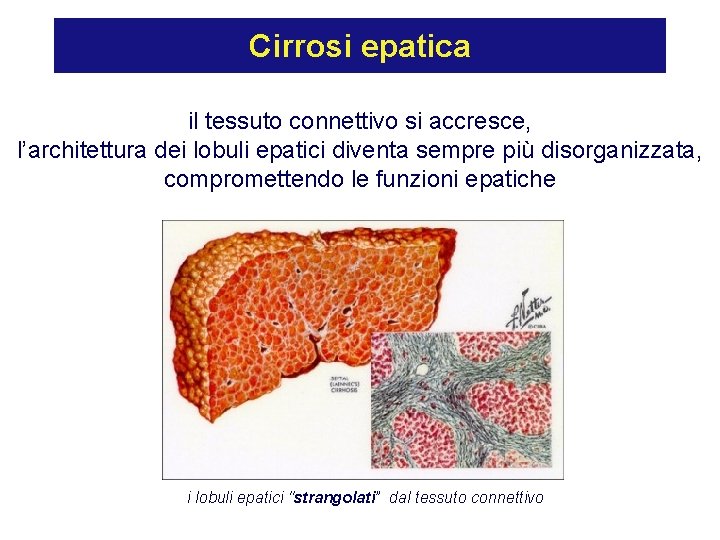
Cirrosi epatica il tessuto connettivo si accresce, l’architettura dei lobuli epatici diventa sempre più disorganizzata, compromettendo le funzioni epatiche i lobuli epatici "strangolati” dal tessuto connettivo
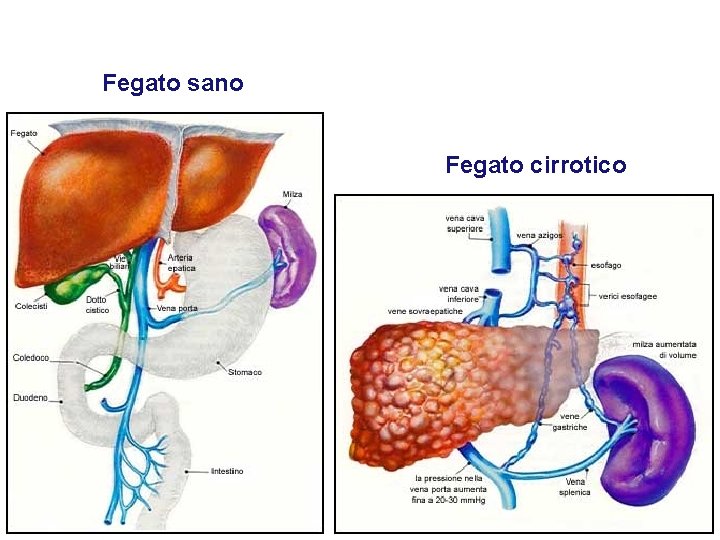
Fegato sano Fegato cirrotico
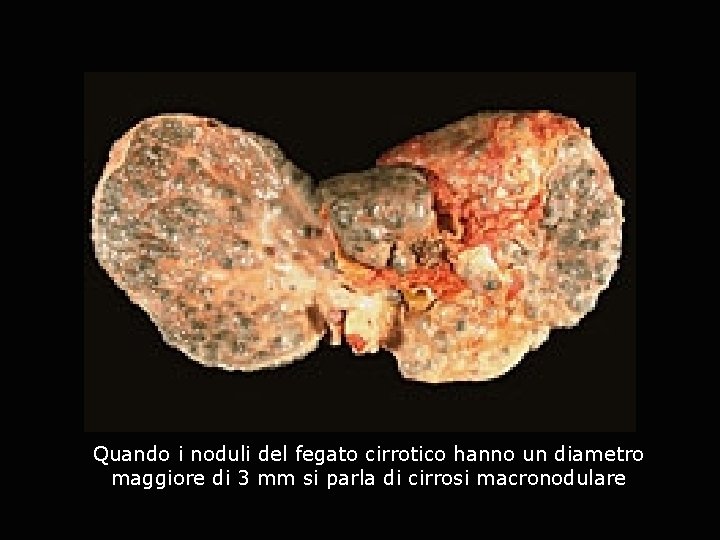
Quando i noduli del fegato cirrotico hanno un diametro maggiore di 3 mm si parla di cirrosi macronodulare
Pool metabolico del fegato Dobbiamo immaginare il fegato come un grande laboratorio chimico dove arrivano materia prima (carboidrati, grassi, proteine, vitamine sali minerali) ed anche sostanze tossiche

Principali funzioni del fegato (a) Deposito di glicogeno che può essere usato come sorgente di glucosio plasmatico (b) Controllo dell’assorbimento del glucosio (c) Sintesi di acidi grassi come forme di deposito di calorie in eccesso (d) Metabolismo di acidi grassi a chetoni (e) Deposito e metabolismo di vitamine (f) Sintesi di proteine plasmatiche (g) Detossificazione chimica di tossine chimiche prodotte endogenamente e somministrate esogenamente e filtrazione meccanica di batteri (h) Mantenimento del normale equilibrio idrosalino (i) Secrezione della bile

Normale funzionalità epatica Sintesi: proteine plasmatiche, fatt. della coagulazione, composti azotati non proteici (urea, ac. urico, purine, pirimidine, glutatione, …) Accumulo: glicogeno, trigliceridi, ac. grassi, colesterolo, vitamine, ferro, rame, ac. folico, vit. B 12, proteine plasmatiche, fosfolipidi Catabolismo: insulina, glucagone, glucocorticoidi, progesterone, estrogeni, farmaci. Escrezione: bile
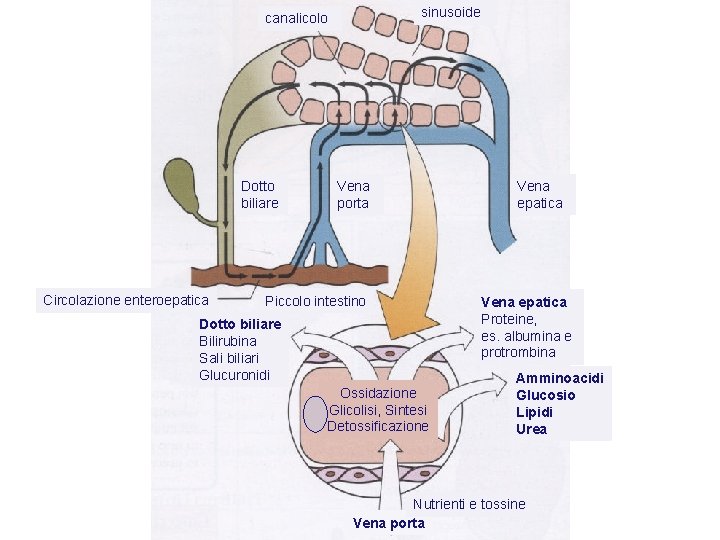
sinusoide canalicolo Dotto biliare Circolazione enteroepatica Vena porta Piccolo intestino Dotto biliare Bilirubina Sali biliari Glucuronidi Ossidazione Glicolisi, Sintesi Detossificazione Vena epatica Proteine, es. albumina e protrombina Amminoacidi Glucosio Lipidi Urea Nutrienti e tossine Vena porta

Principali funzioni del fegato • Metabolismo dei Carboidrati • Metabolismo dei Lipidi • Metabolismo delle Proteine – Sintesi delle Plasmaproteine – Sintesi dei Fattori della coagulazione – Trasformazione dello ione Ammonio • Funzioni di coniugazione e detossificazione • Funzioni di deposito

Specifiche malattie tendono a interessare le diverse componenti epatiche con quadri clinici prevedibili spesso conseguenze cliniche e biochimiche caratteristiche l'epatite acuta virale si manifesta principalmente con un danno epatocellulare la cirrosi biliare primitiva con un'alterazione della secrezione biliare

I sintomi di una malattia epatica riflettono in genere la necrosi epatocellulare o la compromissione della secrezione biliare Se le cause della malattia epatica regrediscono il fegato si rigenera Il mito del titano Prometeo rappresentato in un quadro fiammingo del '600

……in alcune malattie tutte le strutture epatiche possono essere interessate causando degli sconvolgimenti funzionali multipli l'epatopatia alcolica grave Caravaggio: Bacco

Le indagini di laboratorio per la valutazione della funzionalità epatica Non valutano, in maniera qualitativa, la capacità del fegato di svolgere le sue numerosi funzioni, ma danno un’indicazione per l’esistenza, l’estensione e il tipo di danno epatico. Le indagini di laboratorio sono per differenziare i seguenti quadri clinici: Ostruzione del tratto biliare Danno acuto epatocellulare Malattia epatica cronica Nessun test è in grado da solo di valutare la funzione epatica in maniera globale L'uso di più esami di laboratorio: • migliora le possibilità di rilevare anomalie epatobiliari • aiuta nel differenziare le patologie sospettate clinicamente • definisce la gravità della malattia epatica

Marcatori biochimici per lo studio del fegato • Coniugazione – Bilirubina totale e frazionata (coniugata e non coniugata) • Citolisi – Alanina Amminotrasferasi (ALT, GPT) – Aspartato Amminotrasferasi (AST, GOT) – Lattato Deidrogenasi (LDH) • Colestasi – Fosfatasi Alcalina (AP) – -Glutamiltrasferasi ( -GT) • Protidosintesi – Albumina e altre sieroproteine – Pseudocolinesterasi – Tempo di Quick

Secrezione biliare Funzione della bile -ruolo chiave nella digestione dei lipidi: assorbimento intestinale dei lipidi e sostanze lipofile per azione dei sali biliari -veicolo attraverso cui vengono eliminati: • la bilirubina • alcuni metalli pesanti (Cu, Fe, Mn, Zn) • sostanze potenzialmente tossiche • numerosi anioni e cationi organici (ormoni, farmaci, ecc) • il colesterolo (regolazione della quantità di colesterolo presente nell’organismo, attraverso la sintesi di sali biliari e l’escrezione biliare del colesterolo) -protezione da infezioni intestinali, attraverso l’escrezione di Ig. A e di citochine -protezione dell’epatocita e delle cellule dei duttuli e della mucosa intestinale dall’azione tossica dei sali biliari.

Composizione della bile • • • acqua ed elettroliti (82 %), acidi biliari (12 %), fosfolipidi (4 %), colesterolo non esterificato (<1 %), bilirubina coniugata proteine sintetizzate dal fegato (es. Ig. A secretorie) o da esso escrete • farmaci ed altre sostanze esogene e/o loro cataboliti Flusso biliare totale: 600 ml/die

Origine della secrezione biliare A) Bile di origine epatocitaria: -frazione dipendente dai Sali biliari (BADF) -frazione indipendente dai Sali biliari (BAIF) La bile epatica ha contenuto elettrolitico simile a quello del plasma; B) Bile di origine duttale: -frazione prodotta dai dotti biliari, per azione della secretina. Dipende dall’alimentazione Nei dotti biliari la composizione è modificata dalle cellule duttulari: aumento del contenuto biliare di bicarbonato. (A) componente organica dagli epatociti (B) componente idroelettrolitica dagli epatociti e dalle cellule dei dotti biliari

Bilirubina • La bilirubina è un prodotto catabolico del metabolismo dell’eme • È una molecola lipofila poco solubile in acqua, è veicolata nel plasma dall’albumina con cui ha un legame ad alta affinità che ne impedisce l’escrezione urinaria. • È presente nei liquidi corporei (liquido cefalo-rachidiamo, versamenti articolari, cisti, ecc. ) in proporzione al loro contenuto di albumina ed è assente nelle secrezioni quali le lacrime, la saliva e il succo pancreatico. • Nel plasma, in condizioni normali, la bilirubina è presente alla concentrazione di 0, 4 -1 mg/dl (7 -17 mol/l)

Metabolismo della bilirubina In condizioni fisiologiche, nell’adulto la produzione di bilirubina è di 250 -350 mg/24 h Distruzione di eritrociti senescenti Distruzione di eritrociti in maturazione 80 -85% Sistema Reticolo Endoteliale Turnover dell’eme e dei suoi prodotti 15 -20% emoglobina eme Midollo Osseo globina Eme ossigenasi biliverdina Biliverdina riduttasi bilirubina Fegato Le fonti di origine della bilirubina possono essere distinte in: -quota emocateretica: proviene dalla distruzione fisiologica dei globuli rossi -quota eritropoietica: proviene dalla eritropoiesi inefficace (cioè dal catabolismo midollare di molecole di eme non utilizzate nell’eritropoiesi e dalla distruzione di eritroblasti, reticolociti e globuli rossi neoformati) -quota epatica: deriva dal catabolismo di molecole dell’epatocita (essenzialmente enzimi che contengono l’eme)
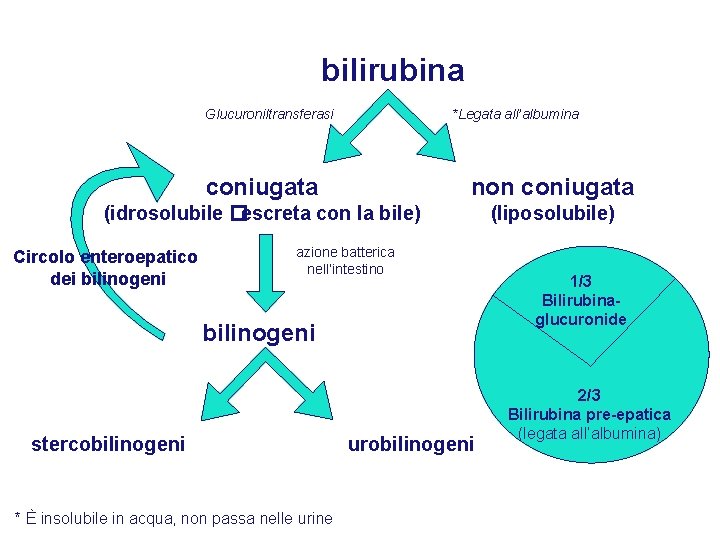
bilirubina Glucuroniltransferasi *Legata all’albumina coniugata non coniugata (idrosolubile �escreta con la bile) (liposolubile) Circolo enteroepatico dei bilinogeni azione batterica nell’intestino bilinogeni stercobilinogeni * È insolubile in acqua, non passa nelle urine urobilinogeni 1/3 Bilirubinaglucuronide 2/3 Bilirubina pre-epatica (legata all’albumina)
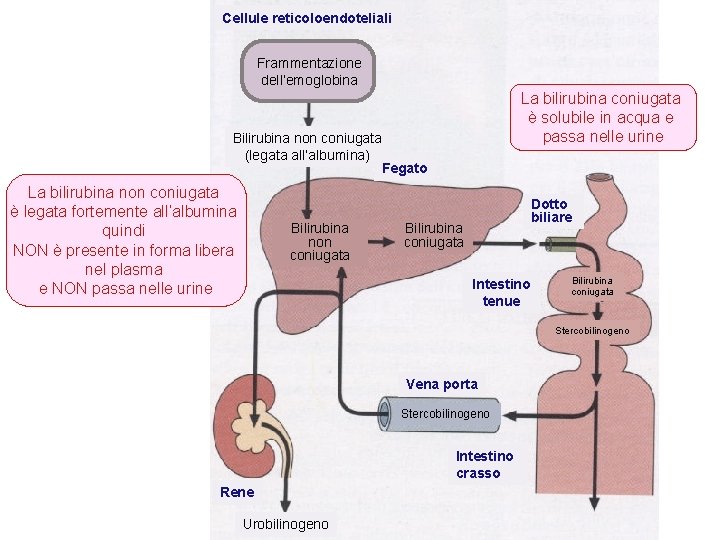
Cellule reticoloendoteliali Frammentazione dell’emoglobina La bilirubina coniugata è solubile in acqua e passa nelle urine Bilirubina non coniugata (legata all’albumina) Fegato La bilirubina non coniugata è legata fortemente all’albumina quindi NON è presente in forma libera nel plasma e NON passa nelle urine Bilirubina non coniugata Dotto biliare Bilirubina coniugata Intestino tenue Bilirubina coniugata Stercobilinogeno Vena porta Stercobilinogeno Intestino crasso Rene Urobilinogeno
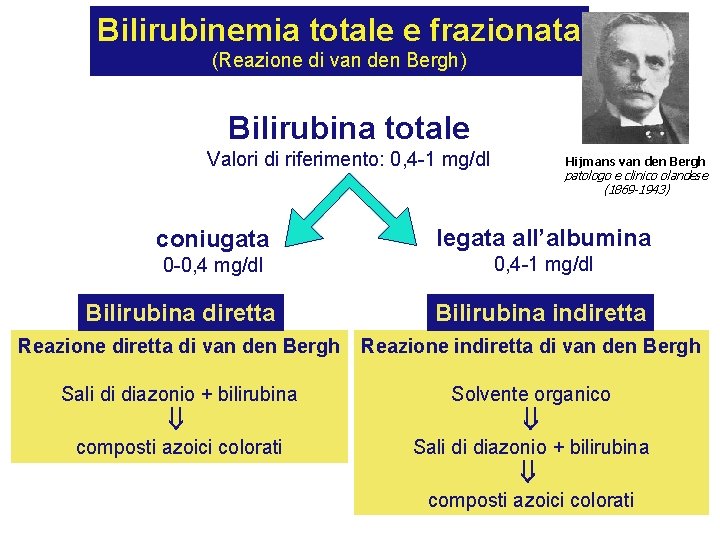
Bilirubinemia totale e frazionata (Reazione di van den Bergh) Bilirubina totale Valori di riferimento: 0, 4 -1 mg/dl Hijmans van den Bergh patologo e clinico olandese (1869 -1943) coniugata legata all’albumina 0 -0, 4 mg/dl 0, 4 -1 mg/dl Bilirubina diretta Bilirubina indiretta Reazione diretta di van den Bergh Reazione indiretta di van den Bergh Sali di diazonio + bilirubina composti azoici colorati Solvente organico Sali di diazonio + bilirubina composti azoici colorati

Bilirubina libera circolante Cause di separazione della bilirubina dall’albumina: -alterazioni albumina -alterazioni del p. H ematico -sostanze endogene o esogene a maggiore affinità per l’albumina: acidi biliari, acidi grassi a catena lunga, salicilati, furosemide, gentamicina, sulfamidici , fenilbutazone (meccanismo competitivo)

Conseguenze patologiche della presenza di Bilirubina libera circolante Inibizione degli enzimi mitocondriali, alterazione della sintesi del DNA, inibizione della sintesi delle proteine Danni più gravi: (a) SNC, in particolare nuclei della base (ittero nucleare) Interferenza nella trasmissione dei segnali neuro-eccitatori a livello sinaptico e nella conduzione dell’impulso nervoso, particolarmente a livello del nervo uditivo. Clinica: iperriflessia; ritardo mentale, diplegia spastica, coreoatetosi. (b) A livello renale interferenza con il metabolismo idroelettrolitico (es. edema neuronale).

Metabolismo dei sali biliari Quantità totale o pool dei sali biliari: variabile fra 2 e 5 g, ed è mantenuta costante dalla sintesi di sali biliari (400 -500 mg/24 h) La sintesi sali biliari avviene negli epatociti, a partire del colesterolo -I° tappa: nel citoplasma idrossilazione in posizione 7 (feed-back -) -trasporto nei mitocondri: acidi biliari primari, colico (acido 3 , 7 , 12 -triidrossi-5 colanico) e cheno-deossicolico o chenico (acido 3 , 7 -diidrossi-5 -colanico) (rapporto 2: 1) -trasporto nel citoplasma: coniugazione con glicina o taurina (rapporto glico/tauro-coniugati = 3: 1), -bile -lume intestinale: acidi biliari secondari= a. b. primari deconiugati e deidrossilati in posizione 7 = deossicolico e litocolico; in alternativa, ossidazione dell’acido chenodeossicolico= acido chenolitocolico (3 -idrossi-7 cheto-5 -colanico). -ileo e colon: a. b. primari e secondari riassorbiti (meccanismo attivo nell’ileo distale, passivo facilitato nelle altre porzioni). -fegato: captazione (70 - 90 % al primo passaggio) -a. b. primari: coniugazione con colina o taurina ed escrezione bile -a. b. secondari: trasformazione (1) acido litocolico in acido solfolitocolico, idrosolubile, circolo, urine. (2) L’acido chetolitocolico in acido ursodesossicolico, coniugato con glicina o con taurina, bile= acidi biliari terziari =circolo entero-epatico dei sali biliari : 5 -10 volte/die.

Funzioni/Correlati patologici dei Sali Biliari -Emulsione/assorbimento dei grassi alimentari nell’intestino (sali biliari + colesterolo e fosfolipidi=soluzione micellare) Ridotta secrezione = steatorrea e dimagrimento -Favoriscono l’assorbimento di vitamine liposolubili (D, E, K, A) Ridotta secrezione= osteomalacia, manifestazioni emorragiche -Stimolazione del flusso di bile nel sistema biliare (aumento escrezione biliare di acqua, lecitina, colesterolo e bilirubina coniugata) - Mantenimento omeostasi colesterolo - Stimolazione peristalsi/azione batteriostatica -Rilascio ormoni gastrointestinali - possibile responsabilità in patogenesi colestasi- prurito

Iperbilirubinemia Quando la concentrazione di bilirubina nel sangue supera 1 mg/dl Tre cause principali: • Emolisi • Blocco del meccanismo di coniugazione all’interno dell’epatocita • Ostruzione del sistema biliare
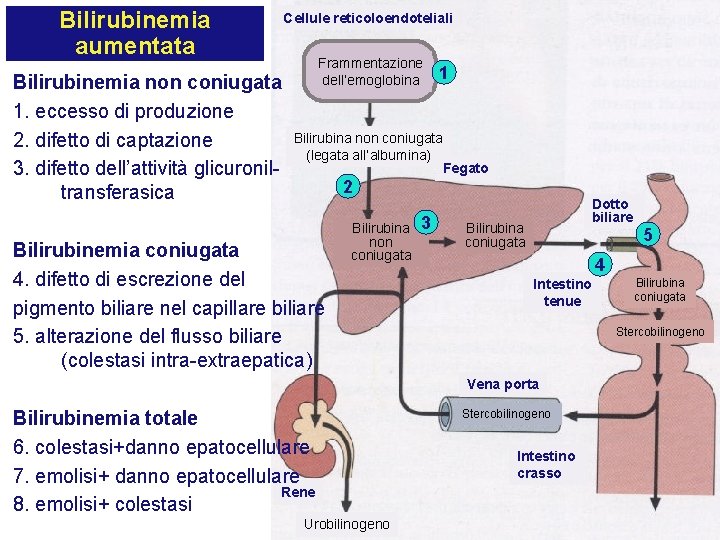
Bilirubinemia aumentata Bilirubinemia non coniugata 1. eccesso di produzione 2. difetto di captazione 3. difetto dell’attività glicuroniltransferasica Cellule reticoloendoteliali Frammentazione dell’emoglobina 1 Bilirubina non coniugata (legata all’albumina) Fegato 2 Bilirubinemia coniugata 4. difetto di escrezione del pigmento biliare nel capillare biliare 5. alterazione del flusso biliare (colestasi intra-extraepatica) Bilirubina non coniugata 3 Dotto biliare Bilirubina coniugata 4 Intestino tenue Urobilinogeno Bilirubina coniugata Stercobilinogeno Vena porta Bilirubinemia totale 6. colestasi+danno epatocellulare 7. emolisi+ danno epatocellulare Rene 8. emolisi+ colestasi 5 Stercobilinogeno Intestino crasso
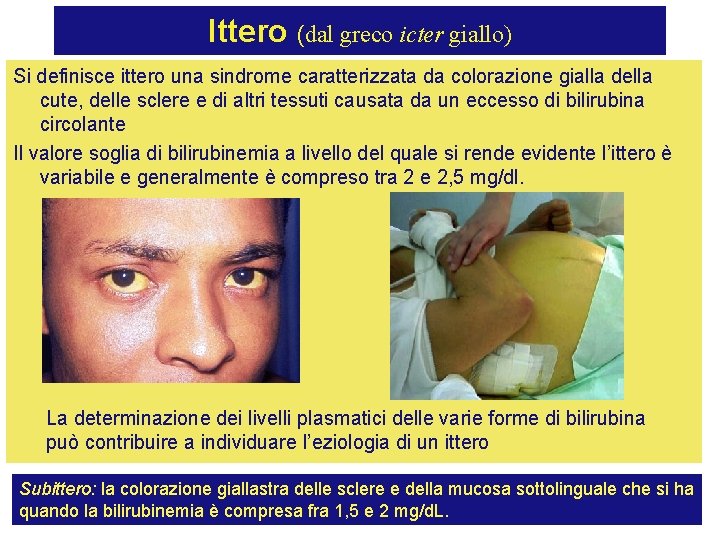
Ittero (dal greco icter giallo) Si definisce ittero una sindrome caratterizzata da colorazione gialla della cute, delle sclere e di altri tessuti causata da un eccesso di bilirubina circolante Il valore soglia di bilirubinemia a livello del quale si rende evidente l’ittero è variabile e generalmente è compreso tra 2 e 2, 5 mg/dl. La determinazione dei livelli plasmatici delle varie forme di bilirubina può contribuire a individuare l’eziologia di un ittero Subittero: la colorazione giallastra delle sclere e della mucosa sottolinguale che si ha quando la bilirubinemia è compresa fra 1, 5 e 2 mg/d. L.

Classificazione tradizionale degli itteri preepatici, dovuti ad iperproduzione della bilirubina epatocellulari, dovuti a lesioni parenchimali del fegato che compromettono il metabolismo epatico della bilirubina postepatici, provocati da ostruzione delle vie biliari intra- e/o extraepatiche

Classificazione fisiopatologica degli itteri Aumentata produzione di bilirubina – Emolisi – Eritropoiesi inefficace Itteri congeniti –Diminuzione dell’uptake (Sindrome di Gilbert) –Difetto di coniugazione (Ittero fisiologico del neonato, Sindrome di Crigler-Najjar I e II) –Difetto di escrezione (Sindrome di Dubin-Johnson, Sindrome di Rotor) Itteri acquisiti – Diminuzione dell’uptake e del trasporto (Farmaci, Epatiti acute e croniche, Cirrosi epatica) – Difetto di coniugazione (Farmaci, allattamento al seno, Cirrosi epatica) – Difetto di escrezione (Cirrosi epatica, Ostruzione delle vie biliari)

Classificazione degli itteri in base alla coniugazione della bilirubina vena epatocita canalicolo Bilirubina non coniugata 0, 4 -1 mg/dl Reticolo endoplasmatico Bilirubina coniugata (diretta) 0 -0, 4 mg/dl Ittero da bilirubina non coniugata Ittero da bilirubina coniugata

Ittero da bilirubina non coniugata • Iperproduzione di bilirubina Emolisi intra o extravascolare Eritropoiesi inefficace • Difetti di captazione a livello epatico • Difetti di coniugazione della bilirubina congenite (ittero neonatale, S. di Gilbert, S. di Crigler-Najjar) acquisite La bilirubina non coniugata è legata all’albumina: • non passa nelle urine • alta affinità per i lipidi di membrana, causando alterazioni delle membrane cellulari soprattutto a livello del sistema nervoso

Ittero da bilirubina coniugata • Alterata escrezione epatica • Disordini familiari o ereditari (S. di Dubin-Jonson, S. di Rotor, colestasi familiare ricorrente benigna, ittero gravidico ricorrente) • Disordini acquisiti (colestasi da farmaci, ittero post-operatorio, epatite e cirrosi, ostruzione biliare extraepatica) La bilirubina coniugata non è lagata all’albumina, quindi è solubile in acqua • passa nelle urine • colore giallo-marrone

Itteri neonatali non costituzionali Ittero fisiologico dei neonati e ittero dei prematuri Nei primi giorni dopo la nascita si ha, anche nel nato a termine, un aumento della concentrazione della bilirubina circolante, con netta prevalenza della quota non coniugata. Ciò è dovuto a: aumento della produzione della bilirubina: quota emocateretica (inferiore vita media gr) ed epatica. insufficienza delle capacità metaboliche del fegato: insufficienti il contenuto epatico di ligandina, acido glicuronico, UGT-1. insufficiente sviluppo della flora batterica intestinale: insufficiente produzione bilinogeni Aumento della bilirubina sierica nel 2° giorno, massimo livello (fino ad 8 -9 mg/d. L) nel 3° - 5° giorno, normale nel corso della 2° settimana. Nel prematuro: (a) più lunga durata (b) concentrazione dell’albumina inferiore= facile deposito nei tessuti di bilirubina non coniuata (c) immaturità della barriera ematoencefalica= ittero nucleare Elementi che suggeriscono che l’ittero del neonato non sia “fisiologico” (nel nato a termine) o “parafisiologico” (nel prematuro): - comparsa dell’ittero nelle prime 24 ore dalla nascita; - livelli di bilirubina non coniugata superiori a 9 (nato a termine) o 14 mg/d. L (prematuro); - livelli di bilirubina coniugata superiori a 2 mg/d. L.
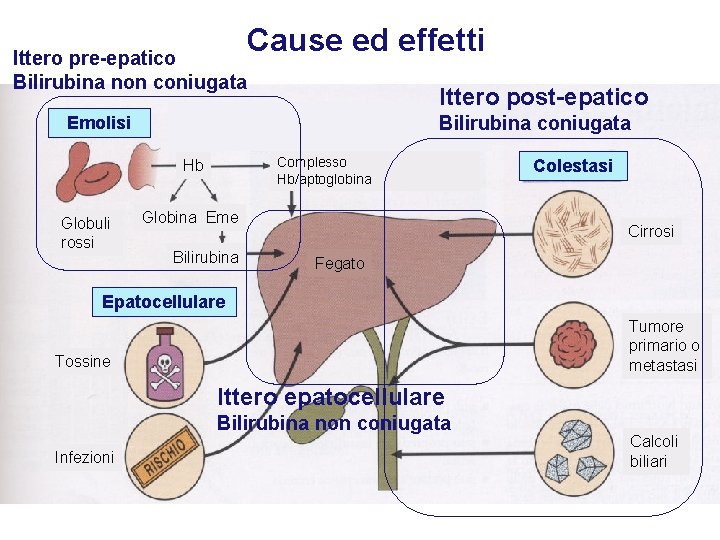
Cause ed effetti Ittero pre-epatico Bilirubina non coniugata Ittero post-epatico Bilirubina coniugata Emolisi Complesso Hb/aptoglobina Hb Globuli rossi Globina Eme Bilirubina Colestasi Cirrosi Fegato Epatocellulare Tumore primario o metastasi Tossine Ittero epatocellulare Bilirubina non coniugata Infezioni Calcoli biliari
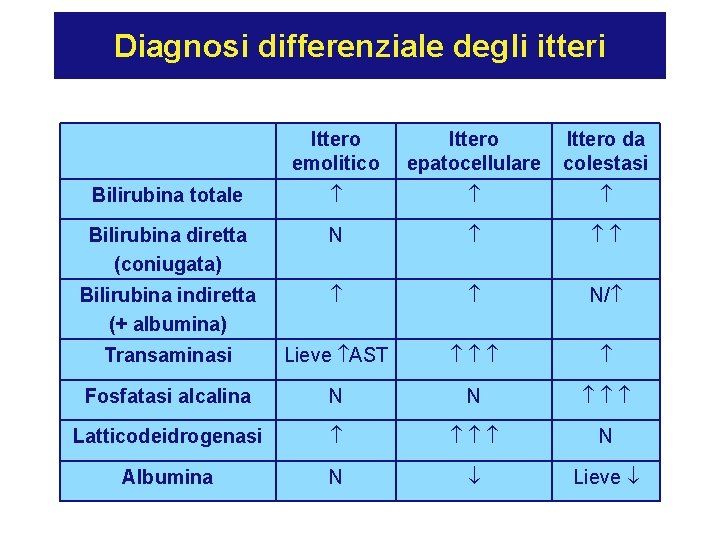
Diagnosi differenziale degli itteri Ittero emolitico Ittero epatocellulare Ittero da colestasi Bilirubina totale Bilirubina diretta (coniugata) N Bilirubina indiretta (+ albumina) N/ Transaminasi Lieve AST Fosfatasi alcalina N N Latticodeidrogenasi N Albumina N Lieve

Marcatori biochimici per lo studio del fegato • Coniugazione – Bilirubina • Citolisi – Alanina Amminotrasferasi (ALT, GPT) – Aspartato Amminotrasferasi (AST, GOT) – Lattato Deidrogenasi (LDH) • Colestasi – Fosfatasi Alcalina (AP) – -Glutamiltrasferasi ( -GT) • Protidosintesi – Albumina e altre sieroproteine – Pseudocolinesterasi – Tempo di Quick

Transaminasi sieriche (Aminotrasferasi) • Sono enzimi che appartengono alla classe delle trasferasi e catalizzano la reazione di trasferimento di un gruppo aminico da un aminoacido ad un chetoacido • Nel siero sono presenti due forme che differiscono per substrato e localizzazione: Aspartato aminotrasferasi (AST) detta anche transaminasi glutammico ossalacetica (GOT) Valori di riferimento Maschi: 10 -45 UI/l Femmine: 5 -30 UI/l Alanina aminotrasferasi (ALT) detta anche transaminasi glutammico piruvica (GPT) Valori di riferimento Maschi: 10 -40 UI/l Femmine: 5 -35 UI/l Rapporto AST/ALT Valori di riferimento: 0, 7 -1, 4
Espressione d’organo delle Transaminasi ALT AST AST

AST Citoplasma Mitocondri ALT Citoplasma • AST, enzima sia citoplasmatico sia mitocondriale, é riscontrabile soprattutto nel cuore, fegato, muscolo scheletrico e rene • ALT, enzima esclusivamente citoplasmatico, é presente soprattutto nel fegato e nel rene e meno nel cuore e nel muscolo scheletrico
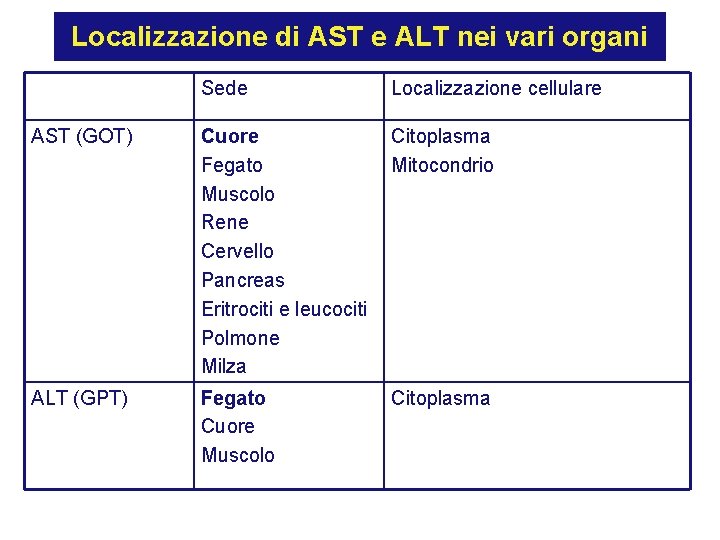
Localizzazione di AST e ALT nei vari organi Sede Localizzazione cellulare AST (GOT) Cuore Fegato Muscolo Rene Cervello Pancreas Eritrociti e leucociti Polmone Milza Citoplasma Mitocondrio ALT (GPT) Fegato Cuore Muscolo Citoplasma

Orientamento diagnostico nell’aumento delle transaminasi Anamnesi farmacologica negativa Transaminasi di origine extra-epatica: ALT AST + Patologia cardiaca o muscolare Anamnesi farmacologica positiva Transaminasi di origine epatica: ALT + AST + Epatite tossica* *ALT nelle epatiti acute (sia su base virale che tossica) aumenta nel siero molto più rapidamente della AST, sia perchè l’AST è inattivata più rapidamente, sia perchè l’ALT, che è presente perlopiù nel citoplasma, diffonde più rapidamente attraverso la membrana cellulare.

Marcatori di Citolisi (AST, ALT, LDH) ↑ ↑ ↑ Epatite virale acuta ↑ ↑ ↑ Epatite acuta alcool ↑ ↑ Epatite cronica autoimmunitaria ↑ ↑ Epatite cronica attiva ↑ Insufficienza cardiaca dx ↑ Colestasi Falsi positivi Infarto Citolisi muscolare
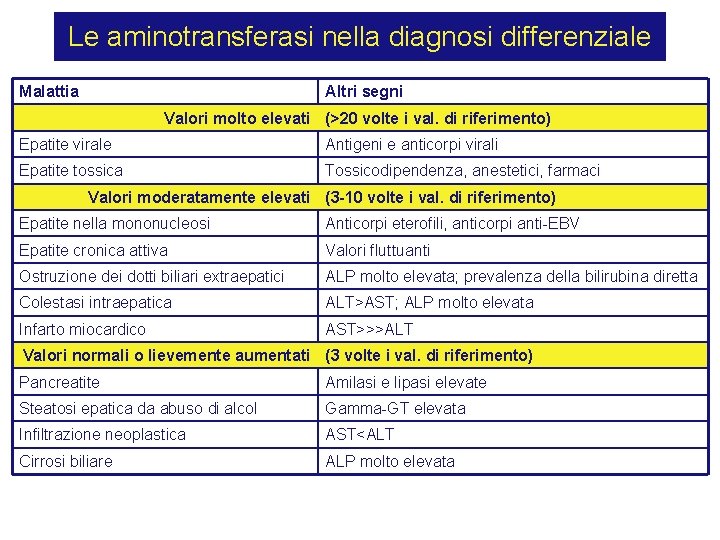
Le aminotransferasi nella diagnosi differenziale Malattia Altri segni Valori molto elevati (>20 volte i val. di riferimento) Epatite virale Antigeni e anticorpi virali Epatite tossica Tossicodipendenza, anestetici, farmaci Valori moderatamente elevati (3 -10 volte i val. di riferimento) Epatite nella mononucleosi Anticorpi eterofili, anticorpi anti-EBV Epatite cronica attiva Valori fluttuanti Ostruzione dei dotti biliari extraepatici ALP molto elevata; prevalenza della bilirubina diretta Colestasi intraepatica ALT>AST; ALP molto elevata Infarto miocardico AST>>>ALT Valori normali o lievemente aumentati (3 volte i val. di riferimento) Pancreatite Amilasi e lipasi elevate Steatosi epatica da abuso di alcol Gamma-GT elevata Infiltrazione neoplastica AST<ALT Cirrosi biliare ALP molto elevata

Marcatori biochimici per lo studio del fegato • Coniugazione – Bilirubina • Citolisi – Alanina Amminotrasferasi (ALT, GPT) – Aspartato Amminotrasferasi (AST, GOT) – Lattato Deidrogenasi (LDH) • Colestasi – Fosfatasi Alcalina – -Glutamiltrasferasi ( -GT) • Protidosintesi – Albumina e altre sieroproteine – Pseudocolinesterasi – Tempo di Quick

La colestasi È la condizione in cui la bile non può fluire dal fegato al duodeno Fegato Colecisti Dotto biliare comune Papilla duodenale

La Sindrome Colestatica Definizione: La colestasi deriva da un'interferenza con il flusso biliare che si può verificare ovunque, dalla membrana basolaterale dell'epatocita fino allo sbocco del coledoco in duodeno. Si può distinguere così una colestasi intra- ed una extraepatica. Morfologicamente: la colestasi si definisce come un accumulo di bile nelle cellule epatiche e nei dotti biliari. Clinicamente: la colestasi è caratterizzata dalla ritenzione nel sangue di sostanze normalmente escrete con la bile = l livelli sierici degli acidi biliari sono aumentati. Funzionalmente: la colestasi rappresenta una riduzione del flusso di bile canalicolare. Si associa ad una ridotta escrezione epatica di acqua e/o di soluti organici (bilirubina, sali biliari). L'alterazione del flusso biliare è di tipo multifattoriale
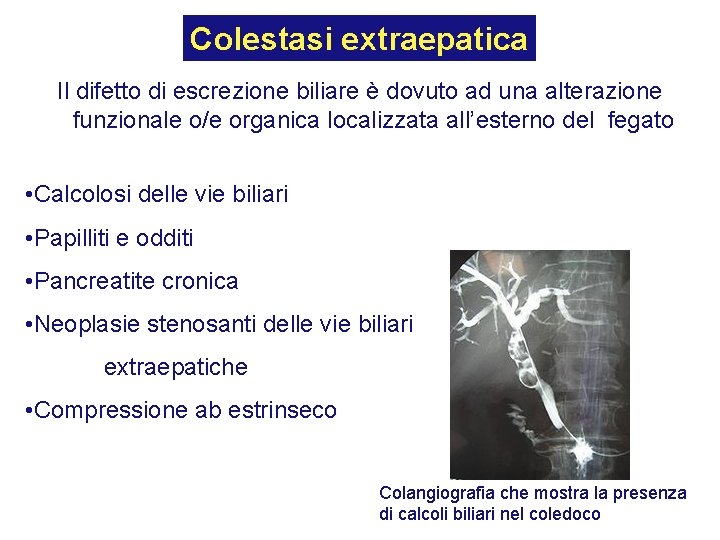
Colestasi extraepatica Il difetto di escrezione biliare è dovuto ad una alterazione funzionale o/e organica localizzata all’esterno del fegato • Calcolosi delle vie biliari • Papilliti e odditi • Pancreatite cronica • Neoplasie stenosanti delle vie biliari extraepatiche • Compressione ab estrinseco Colangiografia che mostra la presenza di calcoli biliari nel coledoco
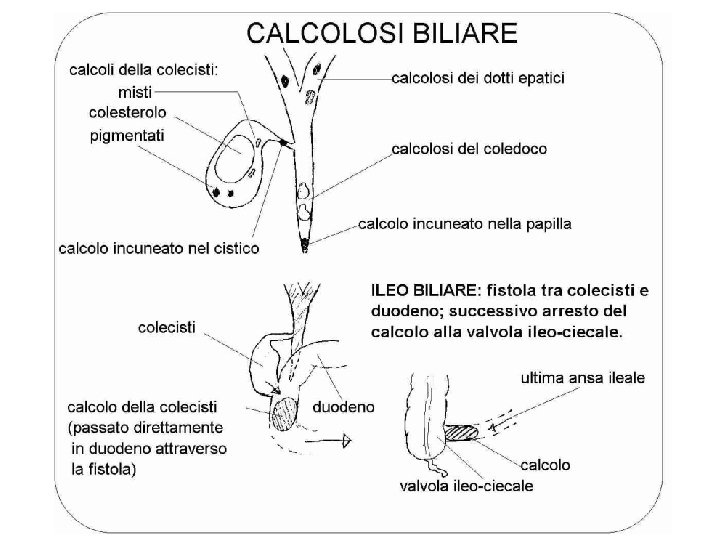
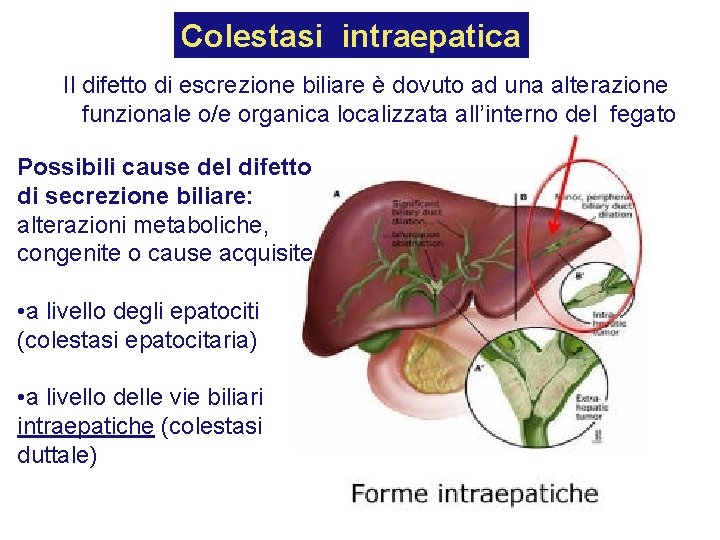
Colestasi intraepatica Il difetto di escrezione biliare è dovuto ad una alterazione funzionale o/e organica localizzata all’interno del fegato Possibili cause del difetto di secrezione biliare: alterazioni metaboliche, congenite o cause acquisite • a livello degli epatociti (colestasi epatocitaria) • a livello delle vie biliari intraepatiche (colestasi duttale)

Principali conseguenze fisiopatologiche della colestasi intraepatica -danno a livello epatico -malassorbimento dei lipidi e delle vitamine liposolubili: steatorrea e dimagrimento, osteomalacia, manifestazioni emorragiche, emeralopia -sofferenza dei tubuli renali per l’azione tossica dei sali biliari e della bilirubina fino alla necrosi tubulare

Marcatori di Colestasi Fosfatasi alcalina Gamma-glutamiltranspeptidasi ( -GT)

Fosfatasi alcalina È un enzima che appartiene alla classe delle idrolasi Valori di riferimento Adulto: 50 -190 UI/l Lattante: 110 -700 UI/l Bambino (1 -10 anni): 110 -550 UI/l Adolescente: 130 -700 UI/l Livelli elevati si trovano in tutte le cellule in fase di proliferazione o con un attivo metabolismo, come gli epatociti, le cellule dell’epitelio delle vie biliari, gli osteoblasti, le cellule epiteliali intestinali, della placenta, nonchè i granulociti circolanti.

Espressione delle isoforme della fosfatasi alcalina Le fosfatasi alcaline sono prodotte da geni diversi e classificate in: FA tessuto-specifica: isoenzima principale, correlato al metabolismo osseo e alle lesioni epato-biliari FA intestinale: non è un marcatore specifico 1) in molte malattie epatiche si ha un incremento sierico di questo isoenzima; 2) è metabolizzata più velocente degli altri due isoenzimi e per questo ha una bassa concentrazione sierica FA placentare e simil-placentare: in gravidanza, prodotte dalla placenta Nel siero umano sono presenti le diverse forme isomeriche della FA

Condizioni associate ad aumento dei livelli sierici di fosfatasi alcalina Concentrazione nel siero >10 volte i val. di riferimento Ostruzione delle vie biliari extraepatiche da tumore Infiltrazione neoplastica delle aree portali Atresia congenita dei dotti biliari intraepatici Concentrazione nel siero da 3 a 10 volte i val. di riferimento Ostruzione dei dotti biliari extraepatici per calcolosi Ostruzione parziale dei dotti biliari intra- o extraepatici Concentrazione normale o leggermente aumentata Epatopatie da alcol, epatite cronica attiva, epatite virale

Un aumento del valore necessita perciò sempre di un'indagine più approfondita e di un'attenta comparazione con altri valori di laboratorio

Valori di riferimento Gamma-glutamiltranspeptidasi Uomo: 6 -28 UI/l È un enzima che appartiene alla classe delle transferasi, Donna: 4 -18 UI/l Neonato: 10 -100 UI/l fa parte della membrana cellulare e catalizza il trasferimento di un gruppo glutammico tra peptidi e aminoacidi È presente in grande quantità nel fegato e nell’epitelio tubulare renale Invece, nel tessuto osseo i livelli della gamma-GT non sono elevati come quelli della fosfatasi alcalina Per la diagnosi di malattie epatiche la gamma-GT è poco specifico e non aggiunge nulla alle informazioni che si ottengono con il dosaggio delle aminotransferasi e dell’ALP È utile quando si riscontra un aumento della concentrazione sierica di fosfatasi alcalina di natura dubbia (es. , patologia ossea): il concomitante aumento della gamma-GT conferma l’origine epatica della patologia!
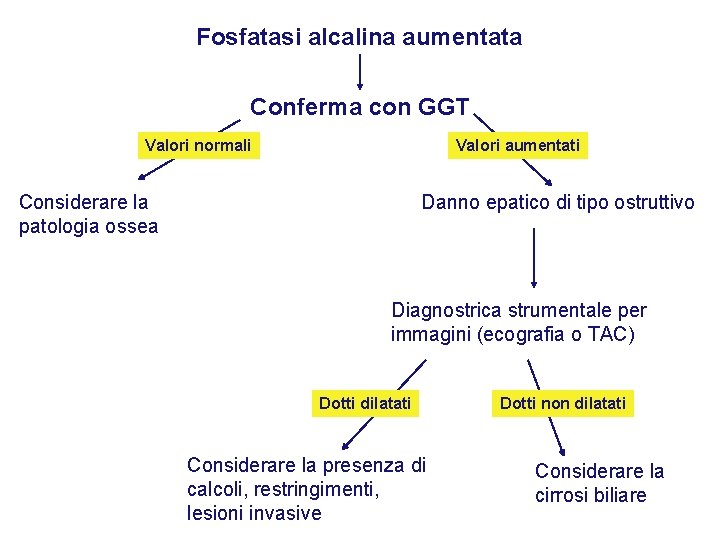
Fosfatasi alcalina aumentata Conferma con GGT Valori normali Valori aumentati Danno epatico di tipo ostruttivo Considerare la patologia ossea Diagnostrica strumentale per immagini (ecografia o TAC) Dotti dilatati Considerare la presenza di calcoli, restringimenti, lesioni invasive Dotti non dilatati Considerare la cirrosi biliare

• La GGT aumenta nelle epatopatie con stasi biliare: ittero da ostruzione delle vie biliari, metastasi epatiche e colestasi intraepatica. • È un enzima di induzione (farmaci, alcol) L’aumento isolato della GGT si osserva in soggetti alcolisti, anche in assenza di un’epatopatia, ed è dovuto sia all’azione induttiva dell’alcool sull’enzima sia al danno epatico. Non esiste un rapporto diretto tra l’aumento della GGT, la quantità di alcol assunta e la durata del consumo di alcol. Drinkers, Vincent van Gogh

Positività dei marcatori di Colestasi • • • Colelitiasi Tumori epatici Neoplasie biliari Tumori della testa del pancreas Cirrosi biliare • Falsi positivi – -GT • Alcoolismo • Epatite cronica • Cirrosi • Falsi positivi – FA • Gravidanza • Malattie ossee • Tumori ovarici

La Sindrome Colestatica: principali aspetti clinici Prurito: in passato attribuito direttamente all’azione dei sali biliari sulle terminazioni nervose, è dovuto agli oppioidi endogeni, provocato dai sali biliari Ittero: per iperbilirubinemia prevalentemente coniugata= urine “color marsala” , feci ipocoliche. Steatorrea: malassorbimento dei lipidi per carenza di sali biliari nel duodeno Sindrome emorragica da carenza di vitamina K od altre manifestazioni cliniche della carenza delle vitamine liposolubili etc. *

La Sindrome Colestatica: principali aspetti di lab. • iperbilirubinemia prevalentemente coniugata • fosfatasi alcalina (FA): la sintesi epatocellulare aumenta in corso di colestasi • -glutamil-transpeptidasi ( -GT), aumento segno di danno e/o di proliferazione della membrana canalicolare e/o duttulare • aumento in circolo dei sali biliari Aumento nel siero dei trigliceridi e del colesterolo* comparsa in circolo di una lipoproteina specifica per la colestasi, la lipoproteina X* (xantomi; cellule a bersaglio/emolisi) aumento nel sangue e nell’epatocita del rame per mancata escrezione

Marcatori biochimici per lo studio del fegato • Coniugazione – Bilirubina • Citolisi – Alanina Amminotrasferasi (ALT, GPT) – Aspartato Amminotrasferasi (AST, GOT) – Lattato Deidrogenasi (LDH) • Colestasi – Fosfatasi Alcalina – -Glutamiltrasferasi ( -GT) Protidosintesi –Albumina e altre sieroproteine –Pseudocolinesterasi –Tempo di Quick
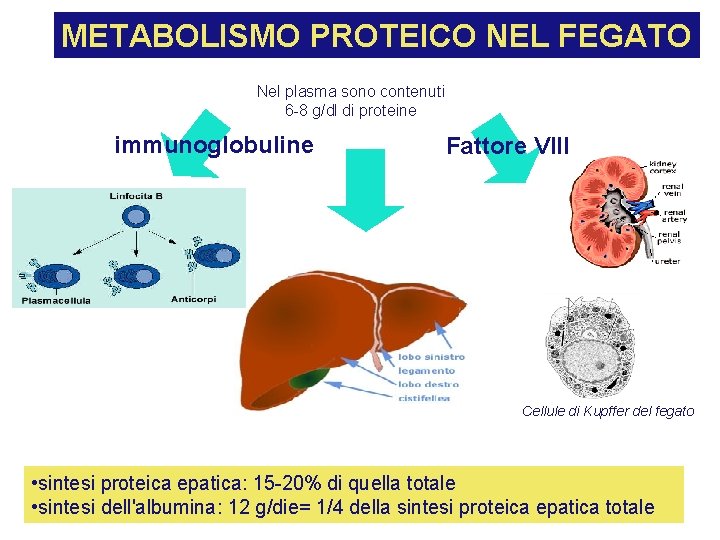
METABOLISMO PROTEICO NEL FEGATO Nel plasma sono contenuti 6 -8 g/dl di proteine immunoglobuline Fattore VIII Cellule di Kupffer del fegato • sintesi proteica epatica: 15 -20% di quella totale • sintesi dell'albumina: 12 g/die= 1/4 della sintesi proteica epatica totale

Il FEGATO e le proteine • funzione di deposito proteico (pool aminoacidico) -riutilizzazione in corso di digiuno= trasformazione in AA ( processo di idrolisi, catalizzato dalle catepsine) – uso degli AA per la gluconeogenesi (concorso anche di AA assorbiti e del t. muscolare: glutammina e alanina importanti fonti per gluconeogenesi e ureogenesi) • immissione in circolo di AA La quota di AA aumenta notevolmente in corso di necrosi epatica oppure nella cirrosi avanzata (possibile aminoaciduria) • sintesi di proteine plasmatiche albumina, alfa e beta globuline, fattori della coagulazione, frazioni del complemento, ecc. , immesse nel sangue circolante (esclusivamente negli epatociti sotto il controllo ormonale - somatotropo e probabilmente insulina) • reazioni di transaminazione

DIGESTIONE/ASSORBIMENTO AMINOACIDI -Idrolisi macromolecole proteiche: enzimi digestivi. = numerose proteasi e peptidasi es. proteasi gastriche (pepsinogeno convertito in pepsina in ambiente acido), pancreatiche (tripsina, chimotripsina e carbossipeptidasi), peptidasi intracellulari degli enterociti. -prodotti della digestione enzimatica: peptidi ed AA -assorbimento nel tratto prossimale del digiuno. -assorbimento AA: almeno 7 specifici sistemi di trasporto attivo (alcuni trasportano più di un aminoacido) -assorbimento di peptidi: attraverso carrier specifici (soprattutto di- e tripeptidi) (in patologie congenite in cui l’assorbimento di AA dibasici e cisteina è compromesso il fabbisogno protidico è assicurato in gran parte dai peptidi assorbiti= cistinuria e sindrome di Hartnup)

Il fegato come sede di trasformazione di aa (A) triptofano ad acido nicotinico (in presenza di vitamina B 6) (B) fenilalanina a tirosina (C) metabolismo della glicina, aminoacido che può subire diversi processi: a) ossidazione ad acido gliossilico b) conversione reversibile a serina c) coniugazione con acido benzoico: acido ippurico d) coniugazione con acido colico e chenodesoscicolico e) sintesi del glutatione f) sintesi della creatina g) sintesi di anelli pirrolici (D) sintesi della colina e fosforilazione della colina stessa a fosforilcolina (sintesi dei fosfolipidi) (E) metabolismo della metionina

Reazioni di Transaminazione Aspartato aminotrasferasi (AST) Alanina aminotrasferasi (ALT) Gli AA epatocitari possono derivare dalla sintesi locale degli a -chetoacidi, che vanno incontro al processo di transaminazione e vengono quindi trasformati in AA= es. reazione reversibile di transaminazione effettuata dai due enzimi AST e ALT che a partire dall’alfa-chetoacido alfa chetoglutarico, portano alla sintesi dell’acido glutammico.

Correlati Patologici -insufficienza epatica: carenza di ATP= accumulo di NH 3 (ammoniaca) da deficit di ureogenesi -produzione anche intestinale dell’ammonio (ureasi batteriche e aminoacido ossidasi)= nella cirrosi l’NH 3 nel sangue portale non entra nel parenchima epatico per essere detossificato tramite la conversione ad urea, ma, attraverso la circolazione sistemica, raggiunge il Sistema Nervoso Centrale Importanza nella patogenesi dell'encefalopatia epatica
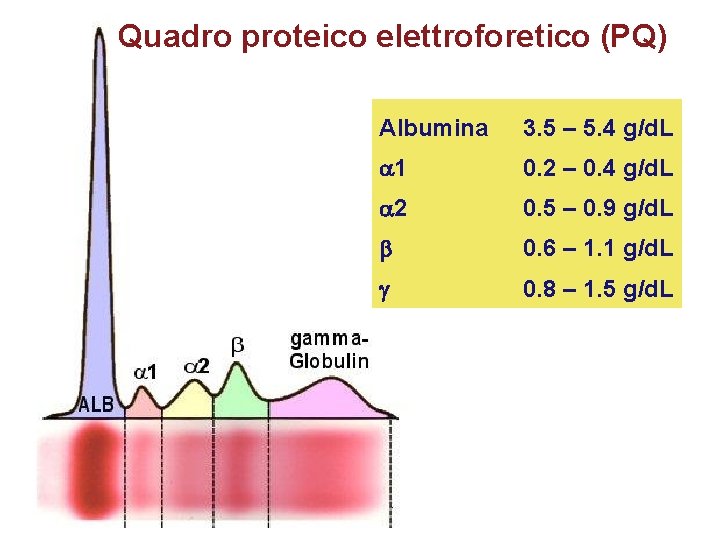
Quadro proteico elettroforetico (PQ) Albumina 3. 5 – 5. 4 g/d. L a 1 0. 2 – 0. 4 g/d. L a 2 0. 5 – 0. 9 g/d. L 0. 6 – 1. 1 g/d. L 0. 8 – 1. 5 g/d. L
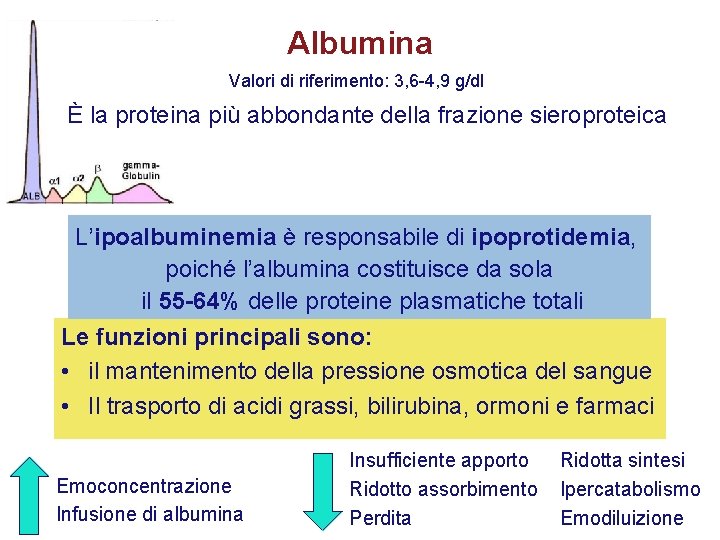
Albumina Valori di riferimento: 3, 6 -4, 9 g/dl È la proteina più abbondante della frazione sieroproteica L’ipoalbuminemia è responsabile di ipoprotidemia, poiché l’albumina costituisce da sola il 55 -64% delle proteine plasmatiche totali Le funzioni principali sono: • il mantenimento della pressione osmotica del sangue • Il trasporto di acidi grassi, bilirubina, ormoni e farmaci Emoconcentrazione Infusione di albumina Insufficiente apporto Ridotto assorbimento Perdita Ridotta sintesi Ipercatabolismo Emodiluizione

Alfa 1 -globuline Valori di riferimento: 0, 2 -0, 4 g/dl Tale frazione elettroforetica esprime principalmente il comportamento dell’ 1 -glicoproteina, dell’ 1 -fetoproteina, dell’ 1 -lipoproteina Gravidanza Malattie infettive Malattie infiammatorie croniche Infarto del miocardio Neoplasie Carenza congenita di 1 -antitripsina Sclerodermia Sindrome nefrosica

Alfa 2 -globuline Valori di riferimento: 0, 4 -0, 8 g/dl Tale frazione elettroforetica esprime principalmente il comportamento dell’ 2 -macroglobulina, dell’aptoglobina, dell’antitrombina III, protrombina, ceruloplasmina, colinesterasi, pre- -lipoproteine Infezioni acute batteriche Traumi Interventi chirurgici Infarto del miocardio Neoplasie Epatopatie croniche Diabete mellito Epatite virale Sindrome di Down Collagenopatie Pancreatite
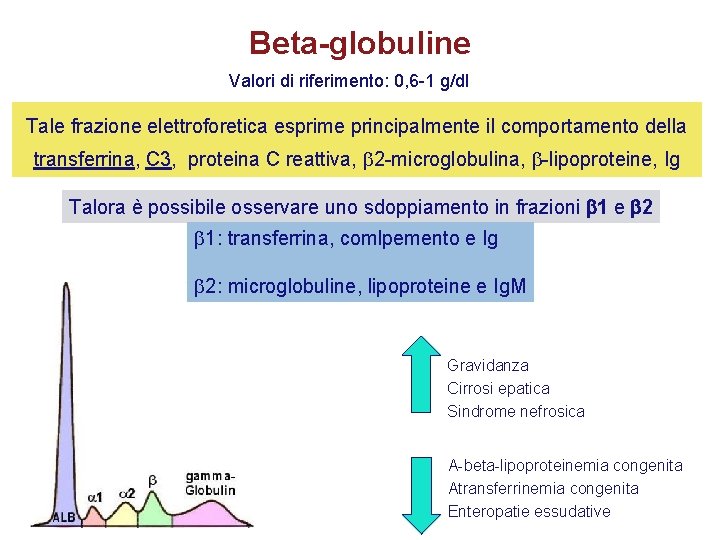
Beta-globuline Valori di riferimento: 0, 6 -1 g/dl Tale frazione elettroforetica esprime principalmente il comportamento della transferrina, C 3, proteina C reattiva, 2 -microglobulina, -lipoproteine, Ig Talora è possibile osservare uno sdoppiamento in frazioni 1 e 2 1: transferrina, comlpemento e Ig 2: microglobuline, lipoproteine e Ig. M Gravidanza Cirrosi epatica Sindrome nefrosica A-beta-lipoproteinemia congenita Atransferrinemia congenita Enteropatie essudative

Gamma-globuline Valori di riferimento: 0, 9 -1, 4 g/dl Comprendono le immunoglobiline (G, M, A, D, E) In particolare la frazione Ig. G, in condizioni normali, è prevalente sulle altre Un aumento delle -globuline può essere distinto nei quadri della gammopatia policlonale o monoclonale Policlonale: con aumento di molte classi di immunoglobuline Epatopatie croniche (epatite cronica, cirrosi epatica) Infezioni congenite Infezioni batteriche acute e croniche Parassitosi Monoclonale: con aumento di un unico tipo di immunoglobulina Malnutrizione Ustioni Terapia immunosoppressiva Sindrome nefrosica

Profilo normale Albumina a 1 a 2 3. 5 – 5. 4 g/d. L 0. 2 – 0. 4 g/d. L 0. 5 – 0. 9 g/d. L 0. 6 – 1. 1 g/d. L 0. 8 – 1. 5 g/d. L Cirrosi
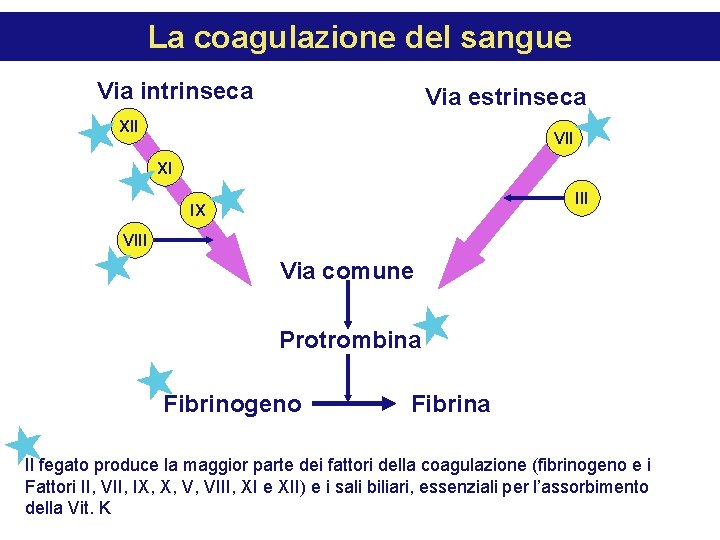
La coagulazione del sangue Via intrinseca Via estrinseca XII VII XI III IX VIII Via comune Protrombina Fibrinogeno Fibrina Il fegato produce la maggior parte dei fattori della coagulazione (fibrinogeno e i Fattori II, VII, IX, X, V, VIII, XI e XII) e i sali biliari, essenziali per l’assorbimento della Vit. K

Fibrinogeno (Fatt. I) Valori di riferimento: 200 -400 mg/dl • Glicoproteina sintetizzata dal fegato, che svolge un ruolo essenziale nel processo coagulativo • È una proteina solubile, che si trasforma in un prodotto insolubile e fibroso, la fibrina • È il substrato fisiologico della trombina Malattie infettive acute e croniche Necrosi tessutale Neoplasie Gravidanza Ustioni Congenita Acquisita: epatopatie eccesso di eparina

Trombina (Fatt. IIa) È l’enzima responsabile della conversione del fibrinogeno in fibrina • Circola nel plasma come protrombina • È sintetizzata dal fegato • La sua formazione è condizionata dall’apporto di vitamina K La trombina catalizza la scissione poteolitica dei fibrino peptidi del fibrinogeno in polipeptidi detti fibrin monomers, che a loro volta polimerizzano e infine vengono stabilizzati dal fattore XIII in presenza di ioni calcio.

Tempo di protrombina (PT) o tempo di Quick Valori di riferimento: 12 -14’’ • Il tempo, in secondi, necessario alla formazione del coagulo quando al plasma si aggiunge tromboplastina e ioni calcio a 37°C. • Valuta il meccanismo estrinseco e comune della coagulazione del sangue e può essere alterato in presenza di deficit dei Fattori I, II, V, X (prodotti a livello epatico). La valutazione seriale del PT può essere utilizzata per distinguere tra colestasi e malattia epatocellulare grave Carenza o alterazione congenita dei Fattori I, II, V, X Epatopatie Deficit di Vit. K

Tempo di tromboplastina parziale (PTT) Valori di riferimento: 28 -35’’ • Il tempo, in secondi, necessario alla formazione del coagulo di fibrina quando al plasma citrato si aggiungono ioni calcio • Valuta il meccanismo intrinseco e comune della coagulazione del sangue e può essere alterato in presenza di deficit dei Fattori V, X , VIII, IX, XII Carenza dei Fattori VIII (emofilia A) e X (emofilia B) Epatopatie Deficit di Vit. K

Tempo di trombina Valori di riferimento: fino a 22’ • Il tempo necessario alla formazione del coagulo quando al plasma citrato si aggiunge trombina • Dipende dalla presenza di fibrinogeno, di plasmina e dei prodotti di degradazione della fibrina e del fibrinogeno (FDP)* Ipofibrinogemia e disfibrinogenemia: congenita acquisita Epatopatie Eccesso di eparina FDP*: prodotti di degradazione della fibrina e del fibrinogeno che inibiscono la funzione piastrinica; hanno attività antitrombinica ed interferiscono con la polimerizzazione della fibrina.

Significato dei principali test emocoagulativi Via intrinseca Via estrinseca XII VII XI III IX VIII Tempo di tromboplastina parziale (PTT) Via comune Protrombina Fibrinogeno Tempo di trombina (TT) Fibrina Tempo di protrombina (PT)
Disordini dell’emostasi nella malattia epatica • Il fegato produce la maggior parte dei fattori della coagulazione e sali biliari, che sono essenziali per l’assorbimento della Vit. K • Il fegato elimina dal circolo i fattori della coagulazione attivati Tendenza emorragica Stato di ipercoagulabilità
- Slides: 96