Biochemick vyetovac metody as RNDr Zdenk Fiar CSc

Biochemické vyšetřovací metody as. RNDr. Zdeněk Fišar, CSc. Psychiatrická klinika 1. LF UK

Laboratorní vyšetřovací metody v psychiatrii n n n n n Výchozí postulát: Při duševních poruchách dochází k narušení přenosu signálu v CNS. klasické a speciální biochemické a endokrinní testy imunologické testy elektroencefalografie (EEG) elektrokardiografie (EKG) počítačová tomografie (CT) metody jaderné magnetické rezonance (NMR) genetická vyšetření (mentální retardece, hyperkinetický syndrom, …) falopletysmografie

Metodologické problémy n n V současné době není k dispozici biochemické (ani genetické) vyšetření, na jehož základě by bylo možné jednoznačně diagnostikovat duševní poruchu a případně navrhnout optimální léčbu. Základní metodologický problém tedy spočívá ve skutečnosti, že v oblasti myšlení neexistují dostatečně citlivé a specifické měřící metody. Je to dáno složitostí funkce mozku, kdy i jeho „normální“ funkce zahrnují výrazné odchylky z rovnováhy.

Některé biochemické a neuroendokrinní testy v psychiatrii n n n hladiny psychofarmak hladiny neuromediátorů a jejich metabolitů neuroendokrinní parametry aktivita enzymů podílejících se na syntéze a metabolismu neuromediátorů vlastnosti receptorových systémů zpětné vychytávání uvolněných neuromediátorů

Biologická psychiatrie n n Není dosud jasné, co je primární příčinou vzniku většiny duševních poruch a jaké jsou molekulární mechanismy vedoucí k terapeutickým účinkům používaných léčiv. Dosavadní pozorování svědčí o tom, že při duševních poruchách je porušen normální přenos nervového signálu, a to zvláště v oblasti chemických synapsí
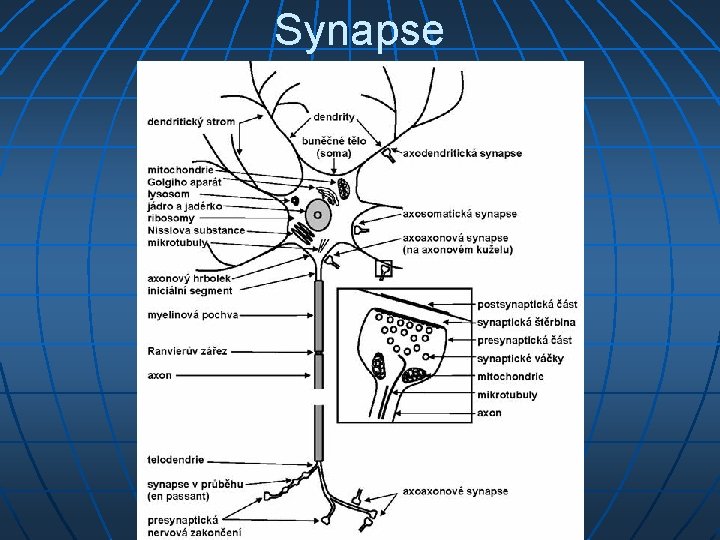
Synapse
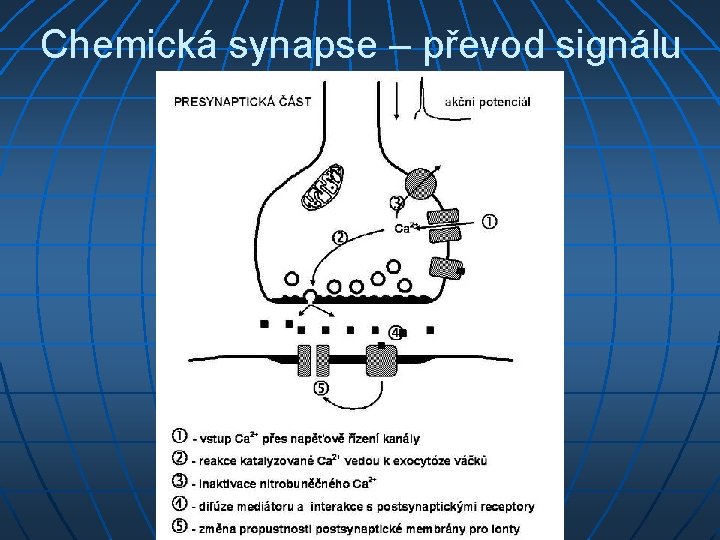
Chemická synapse – převod signálu
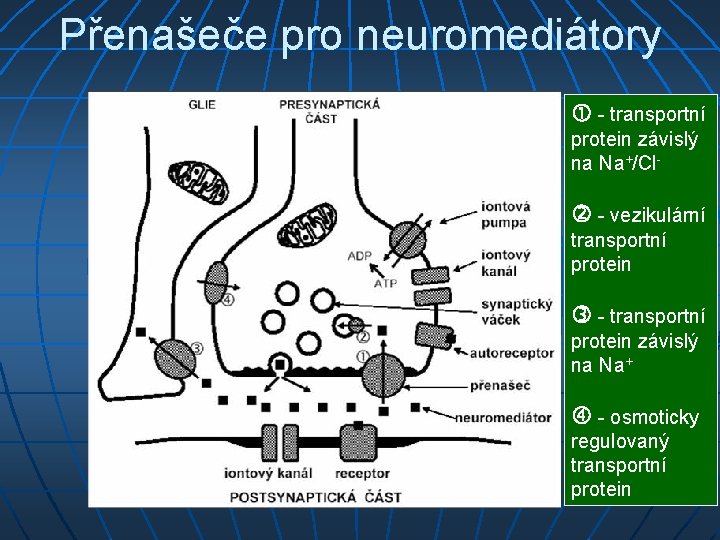
Přenašeče pro neuromediátory - transportní protein závislý na Na+/Cl - vezikulární transportní protein - transportní protein závislý na Na+ - osmoticky regulovaný transportní protein

Důsledky aktivity přenašečů 1. koncentrace neuromediátoru ve štěrbině je snižována rychleji, než při pouhé difúzi, což umožňuje lepší časové rozlišení následných dějů 2. účinky neuromediátoru jsou omezeny na menší plochu, což dovoluje funkci anatomicky blízkých chemicky identických ale funkčně odlišných synapsí 3. neuromediátor může být po přenosu do presynaptického zakončení znovu použit

Kritéria pro identifikaci neuromediátoru 1. výskyt ve vysokých koncentracích v presynaptických nervových zakončeních 2. syntéza v presynaptickém neuronu 3. uvolňování v dostatečném množství z neuronu při depolarizaci membrány a existence mechanismu pro ukončení jeho působení 4. indukce fyziologických účinků odpovídajících normální synaptické transmisi i při exogenní aplikaci 5. existence specifického receptoru pro tento neuromediátor

Klasické neuromediátory Systém cholinergní aminokyselinergní Mediátor acetylcholin GABA asparagová kys. glutamová kys. glycin homocystein monoaminergní katecholaminy dopamin noradrenalin indolaminy tryptamin serotonin jiné odvozené od ak histamin taurin purinergní adenosin ADP AMP ATP Prekurzory cholin+acetylkoenzym A glukóza glutamát glukóza+glutamin; aspartát serin cystein cystin tyrozin DOPA dopamin noradrenalin tryptofan 5 -hydroxytryptofan histidin cysteamin

Receptory n n Receptor je makromolekula specializovaná na přenos informace. Lze jej definovat jako specifické vazebné místo s funkčními vztahy.

Vlastnosti receptorů Receptorový komplex 1. rozpoznávací místo 2. transdukční prvek 3. efektorový systém Regulace receptorů 1. regulace změnou počtu receptorů 2. regulace vlastností receptorů

Rozdělení receptorů podle jejich efektorového systému 1. ligandem řízené iontové kanály 2. receptory spojené s G proteiny 3. receptory s vnitřní guanylátcyklázovou aktivitou 4. receptory s vnitřní tyrozinkinázovou aktivitou

Schéma pro hypotézu druhých poslů první poslové receptory G proteiny efektorové proteiny druzí poslové proteinkinázy třetí poslové biologická odezva genová exprese a jiné procesy

Typy receptorů Mediátorový systém acetylcholinový monoaminový aminokyselinový peptidový purinový Receptorový typ acetylcholinové nikotinové receptory acetycholinové muskarinové receptory 1 -adrenoceptory 2 -adrenoceptory dopaminové receptory serotoninové receptory GABA receptory glutamátové ionotropní receptory glutamátové metabotropní receptory glycinové receptory histaminové receptory opioidní receptory jiné peptidové receptory adenosinové receptory (P 1 purinoceptory) P 2 purinoceptory
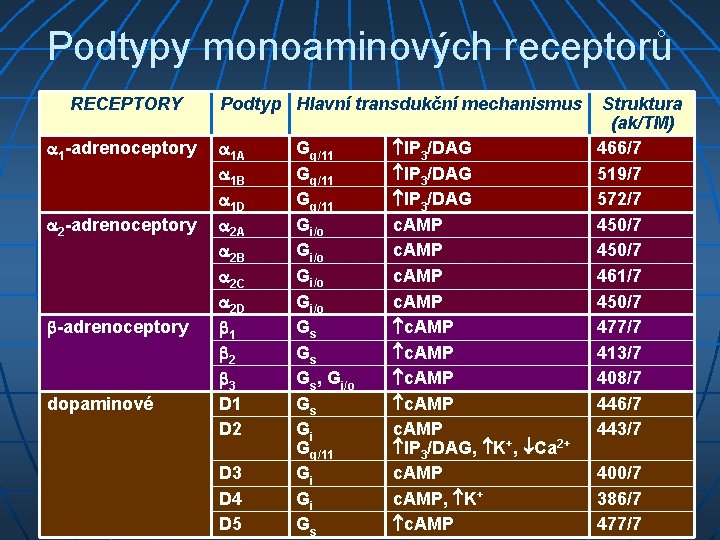
Podtypy monoaminových receptorů RECEPTORY 1 -adrenoceptory 2 -adrenoceptory dopaminové Podtyp Hlavní transdukční mechanismus 1 A 1 B 1 D 2 A 2 B 2 C 2 D 1 2 3 D 1 D 2 D 3 D 4 D 5 Gq/11 Gi/o Gs Gs, Gi/o Gs Gi Gq/11 Gi Gi Gs IP 3/DAG c. AMP c. AMP IP 3/DAG, K+, Ca 2+ c. AMP, K+ c. AMP Struktura (ak/TM) 466/7 519/7 572/7 450/7 461/7 450/7 477/7 413/7 408/7 446/7 443/7 400/7 386/7 477/7
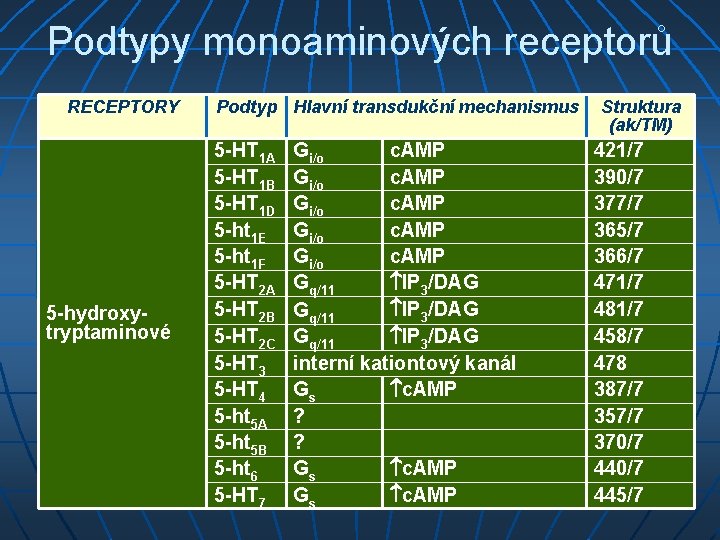
Podtypy monoaminových receptorů RECEPTORY 5 -hydroxytryptaminové Podtyp Hlavní transdukční mechanismus 5 -HT 1 A 5 -HT 1 B 5 -HT 1 D 5 -ht 1 E 5 -ht 1 F 5 -HT 2 A 5 -HT 2 B 5 -HT 2 C 5 -HT 3 5 -HT 4 5 -ht 5 A 5 -ht 5 B 5 -ht 6 5 -HT 7 Gi/o c. AMP Gq/11 IP 3/DAG interní kationtový kanál Gs c. AMP ? ? Gs c. AMP Struktura (ak/TM) 421/7 390/7 377/7 365/7 366/7 471/7 481/7 458/7 478 387/7 357/7 370/7 445/7
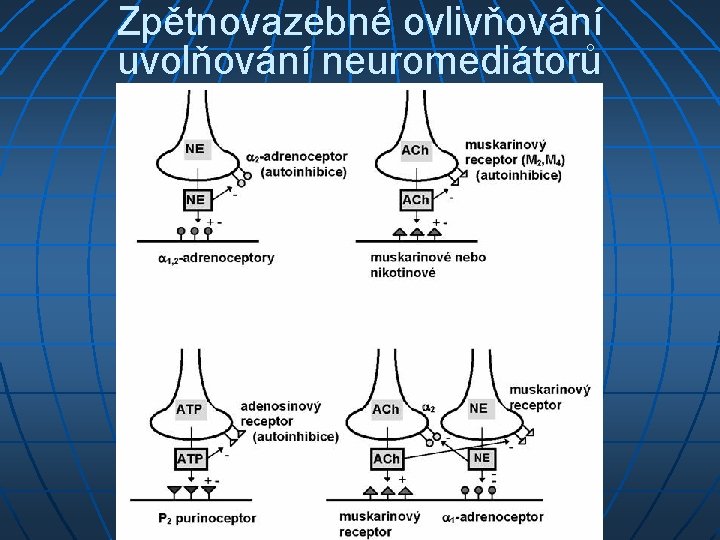
Zpětnovazebné ovlivňování uvolňování neuromediátorů
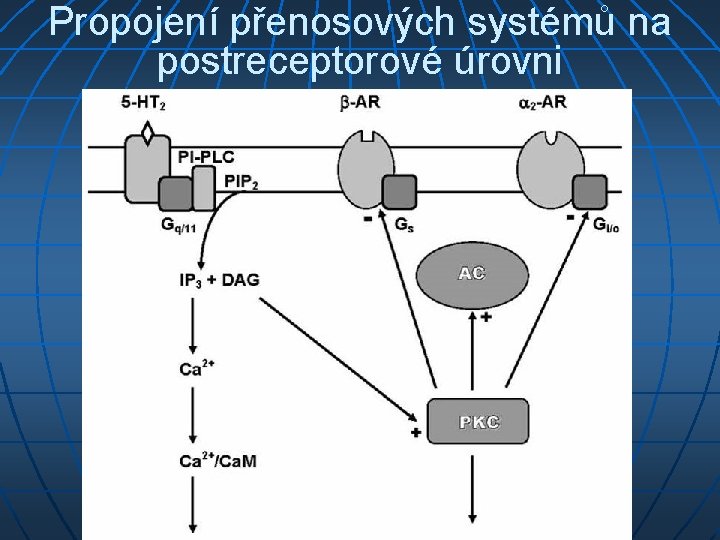
Propojení přenosových systémů na postreceptorové úrovni

Mechanismy účinku antipsychotik konvenční antipsychotika blokáda postsynaptických D 2 receptorů v meso-limbické dráze (potlačení pozitivních symptomů); zvýšené uvolňování DA a blokáda 5 -HT 2 A atypická receptorů v meso-kortikální dráze antipsychotika (potlačení negativních symptomů); vazba na další receptory (účinnost v terapii afektivních symptomů, zlepšení kognitivních funkcí)

Rozdělení antidepresiv podle primárního biochemického účinku inhibitory katabolismu neuromediátorů (IMAO) blokátory reuptake neuromediátorů (SRI/NRI, SSRI, SNRI) agonisté receptorových systémů (5 -HT 1 A) antagonisté receptorových systémů ( 2 -AR, 5 -HT 2) inhibitory či stimulátory jiných složek transdukce signálu (G proteinů, AC, PL, PK, fosfatáz, ATPáz, proteinů závislých na membránových fosfolipidech, transkripčních faktorů, systémů 2. a 3. poslů)

Schizofrenie n n n schizofrenie je specificky lidské onemocnění dosud neznámé etiologie projevující se poruchami myšlení, jednání, vnímání, emocí a vůle jedná se onemocnění heterogenní etiologie („skupina schizofrenií“) předpokládá se multifaktoriální etiologie a mnohočetné patogenetické vlivy

Environmentální modely schizofrenie model vyvolávající faktory psychosociální situace vyžadující akci nebo (s vyvolávajícím rozhodnutí vlivem komplexních složitost, dvojznačnost či nejasnost sociálních informací poskytovaných k vyřešení požadavků) úkolu situace vyžadující akci nebo rozhodnutí přetrvává, aniž byla vyřešena osoba nemá možnost únikové cesty nepsychosociální porodní komplikace (se specifickým nitroděložní virová infekce poškozením mozku citlivost na gluten a jeho funkcí) malformace mozku, atd.

Neurovývojová hypotéza schizofrenie Významná část osob s diagnózou schizofrenie získanou v dospělém věku prodělala poruchu vývoje mozku desítky let před symptomatickou fází onemocnění. Narušení vývoje mozku může způsobit buď: 1. takové poškození mozku, které se v dospělosti vlivem interakcí s dosud neznámými faktory projeví vznikem psychotických symptomů, nebo 2. toto časné poškození CNS vede k ovlivnění dalšího vývoje mozku a vzniku náchylnosti ke schizofrenii v pozdějším věku Tento model může vysvětlit: 1. vysokou pravděpodobnost vzniku klinických projevů onemocnění v pozdní adolescenci nebo časné dospělosti 2. úlohu stresu při vzniku onemocnění a jeho relapsu 3. terapeutickou účinnost antipsychotik

Vývojová neuropatologie vztah ke schizofrenii in vivo: poněkud zvětšené mozkové komory a širší kortikální štěrbiny a rýhy post mortem: rozdíly ve velikosti mozkových komor, v různých oblastech mozkové kůry, v hipokampální formaci (vč. parahipokampálního kortexu) a morfometrické abnormality v různých periventrikulárních subkortikálních jádrech; konzistentní data o chybění gliózy anomální lateralizace: méně vyvinutá normální anatomická asymetrie hemisfér orientace hipokampálních pyramidových abnormality buněk, laminární organizace neuronů cytoarchitektury v neokortexu a limbické kůře, vzájemné vztahy mezi neurony

Východiska klasické dopaminové hypotézy schizofrenie 1. Psychózu lze aktivovat psychostimulancii, která jsou agonisty dopaminu, jako je amfetamin, meskalin, dietylamid kyseliny lysergové (LSD, lysergid); jedná se zřejmě o látky vhodné pro vyvolání modelového psychotického stavu. 2. Společným znakem látek účinných při terapii schizofrenie (neuroleptik, resp. antipsychotik 1. generace) je jejich působení na dopaminergní systém; skoro všechny tyto léky přitom ovlivňují pozitivní příznaky, pravděpodobně tím, že blokují účinky dopaminu a jiných dopaminergních agonistů v určitých oblastech mozku. 3. Neuroleptika zvyšují obrat dopaminu; může se jednat o důsledek blokády postsynaptických DA receptorů, nebo nedostatečného počtu či citlivosti inhibičních DA autoreceptorů na buněčných tělech.

Klasická dopaminová hypotéza schizofrenie • Psychotické symptomy u schizofrenie jsou vztaženy k dopaminergní hyperaktivitě v mozku. Hyperaktivita dopaminergních systémů spojená se schizofrenií je důsledkem zvýšení citlivosti a počtu dopaminových D 2 receptorů. Tato zvýšená aktivita se může týkat jen určité oblasti mozku.

Afektivní poruchy n n Afektivní poruchy se projevují patickou náladou v epizodách trvajících od několika dnů do několika měsíců. Při bipolárním typu onemocnění dochází ke střídání depresivních a manických epizod, unipolární typ zahrnuje pouze epizody depresivní, nebo manické. Těžká podoba postihuje asi 1% populace a je obvykle dobře léčitelná. Anatomické změny v mozku jsou podobné jako u chronické schizofrenie.
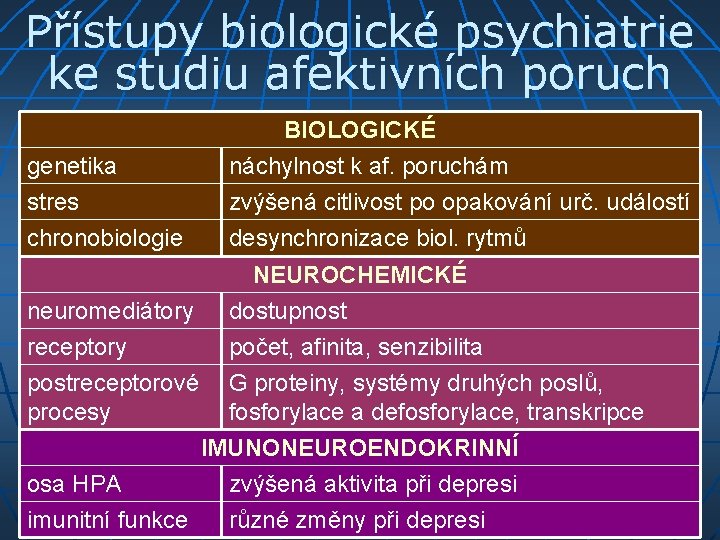
Přístupy biologické psychiatrie ke studiu afektivních poruch genetika stres chronobiologie BIOLOGICKÉ náchylnost k af. poruchám zvýšená citlivost po opakování urč. událostí desynchronizace biol. rytmů NEUROCHEMICKÉ neuromediátory dostupnost receptory počet, afinita, senzibilita postreceptorové G proteiny, systémy druhých poslů, procesy fosforylace a defosforylace, transkripce IMUNONEUROENDOKRINNÍ osa HPA zvýšená aktivita při depresi imunitní funkce různé změny při depresi

Receptorové hypotézy afektivních poruch Klasická noradrenalinová receptorová hypotéza: Depresivní porucha může být spojena se zvýšenou senzitivitou centrálních noradrenergních receptorů. Terapeutické účinky antidepresiv jsou potom vztaženy k adaptivním změnám v senzitivitě adenylátcyklázového systému spojeného s postsynaptickými noradrenergními receptory. Tato hypotéza byla upřesněna tím, že desenzitizace adenylátcyklázy po chronickém podávání antidepresiv je způsobena snížením počtu 1‑adrenoceptorů. Obecná katecholaminová hypotéza: Supersenzitivita určitých katecholaminových receptorů při nízkých hladinách 5 -HT je biochemickým základem deprese. Tato hypotéza je elegantní, ale nelze ji považovat za prokázanou, neboť klinické studie dostatečně nepotvrdily přítomnost takových supersenzitivních receptorů u nemocných. Obecná serotoninová receptorová hypotéza: Deprese je vztažena k těmto abnormalitám serotoninových receptorů: 1. 2. 3. upregulace 5 -HT 2 desenzibilizace 5 -HT 1 A abnormální transdukce signálu po vazbě 5 -HT k receptoru.

Postreceptorové hypotézy afektivních poruch Molekulární a buněčná teorie deprese: Transkripční faktor CREB je možným intrabuněčným cílem dlouhodobé léčby antidepresivy a gen pro mozkový neurotrofní faktor BDNF je možným cílovým genem CREB. Náchylnost k depresi může vzniknout v důsledku poškození neuronů po chronickém stresu, který snižuje expresi BDNF v hippokampu. Přežití neuronů snižuje také dlouhodobé zvýšení hladin glukokortikoidů, hypoglykémie, ischémie, neurotoxiny a některé virové infekce. Dlouhodobé podávání antidepresiv zvyšuje expresi BDNF i jeho receptoru trk. B přes zvýšení funkce 5 -HT nebo NA systému.

Model pro molekulární mechanismus účinků dlouhodobé léčby antidepresivy Antidepresivní terapie (AT) Inhibice reuptake 5 -HT a NA nebo jejich štěpení Krátkodobá AT: Zvýšení mimobuněčných hladin 5 -HT nebo NA Dlouhodobá AT: Snížení funkce a exprese 5 -HT a NA receptorů Zvýšení přenosu v signální dráze c. AMP (zvýšené hladiny adenylátcyklázy a PKA a translokace PKA do buněčného jádra) Zvýšení exprese transkripčního faktoru CREB (c. AMP response element-binding protein); předpokládá se, že CREB je společným postreceptorovým cílem pro antidepresiva. Zvýšená aktivita v signální dráze c. AMP naznačuje, že funkční výstupy 5 -HT a NA jsou upregulovány, i když určité serotoninové a noradrenalinové receptory jsou downregulovány. Exprese BDNF (brain-derived neurotrophic factor) a trk. B je také zvýšena po dlouhodobém podávání antidepresiv ( zvýšené přežití neuronů, jejich funkce a přetváření synapsí) Duman et al. 1997

Některé biochemické a neuroendokrinní testy v psychiatrii n n n hladiny psychofarmak hladiny neuromediátorů a jejich metabolitů neuroendokrinní parametry aktivita enzymů podílejících se na syntéze a metabolismu neuromediátorů vlastnosti receptorových systémů zpětné vychytávání uvolněných neuromediátorů

Měřené vzorky n n n moč krev mozkomíšní mok izolované buňky různé modelové systémy (buněčné a tkáňové kultury, synaptosomy izolované ze zvířecích mozků, umělé membrány)

Hladiny psychofarmak I n n n za metabolismus léčiv, včetně psychofarmak, jsou odpovědné především enzymy ze systému cytochromu P-450 nejvýznamnějším způsobem eliminace je vylučování ledvinami obecně dochází k rozdělení léčiva mezi plazmu, krevní buňky, tkáňový mok a buňky tkání, přičemž část je vázána na bílkoviny, část je kumulována v lipidových dvojvrstvách a část zůstává volná

Hladiny psychofarmak II n n měření hladin psychofarmak v krvi vychází z předpokladu, že tyto koncentrace korelují s koncentracemi v místě působení, tj. v mozku byla určena tzv. terapeutická okna, tj. koncentrační rozmezí, v nichž jsou psychofarmaka obvykle účinná

Hladiny psychofarmak III Účinnost a toxicitu léčiv lze charakterizovat řadou farmakologických parametrů: n n střední účinná dávka (ED 50) vyvolává požadovaný efekt u 50% jedinců střední toxická dávka (TD 50) způsobuje určité toxické příznaky u 50% pokusných zvířat střední smrtná dávka (LD 50) vede k úhynu 50% pokusných zvířat pro rozsah použitelných dávek se používají parametry jako terapeutická šíře (TD 50 – ED 50 nebo LD 50 – ED 50) a terapeutický index (např. LD 50/ED 50, LD 5/ED 95, TD 5/ED 95)

Hladiny psychofarmak IV n clearance je definovaná jako množství plazmy (nebo krve) v ml, které se očistí od sledované látky za jednotku času

Lithium I n n n podává se terapeuticky v akutní manické nebo depresivní epizodě nebo profylakticky při bipolární afektivní poruše aplikuje se perorálně ve formě uhličitanu lithného. Obvyklá denní dávka je kolem 900 mg při profylaktickém podávání by sérová hladina lithia neměla klesnout pod 0, 4 mmol/l, obvykle se pohybuje v rozmezí 0, 6 – 0, 8 mmol/l. Terapeutické hladiny u mánie mohou dosahovat až 1, 2 – 1, 5 mmol/l.

Lithium II Před nasazením lithia: n krevní obraz a diferenciální počet lymfocytů n sedimentace erytrocytů n vyšetření na ionty (Na, K, Ca, Cl, Mg) n vyšetření renálních funkcí (urea, kreatinin, clearance kreatininu, …) n EKG n EEG V průběhu léčby: n koncentrace lithia v plazmě n půlroční kontroly (thyreotropní hormon, urea, kreatinin)

Kontrola užívání psychofarmak n n stanovení fenothiazinových neuroleptik a tricyklických antidepresív odvozených od imipraminu v moči Forrestovou zkouškou, kdy pouhým smísením moči a Forrestova činidla lze z barevné reakce odhadnout užívanou denní dávku léku pro přesnější stanovování hladin psychofarmak se používají hlavně elektrochemické a chromatografické metody a radioimunoanalýza

Hladiny neuromediátorů a jejich metabolitů I n měření hladin neuromediátorů a jejich metabolitů a aktivity enzymů podílejících se na jejich syntéze a katabolismu zůstává užitečnou výzkumnou metodou sledování změn aktivity neuromediátorových systémů v mozku při onemocnění a jeho léčbě

Hladiny neuromediátorů a jejich metabolitů II Sledovány jsou nejčastěji: n kyselina 5‑hydroxyindoloctová (5 HIAA, hlavní metabolit serotoninu) n 3 -metoxy-4 -hydroxyfenylglykol (MHPG, relativně selektivní metabolit noradrenalinu v mozku) n kyselina homovanilová (HVA, hlavní metabolit dopaminu) a další

Neuroendokrinní testy n n neurochemické a neuroendokrinologické přístupy ke studiu duševních poruch se vzhledem k provázanosti obou systémů vzájemně doplňují studována je především osa hypotalamus-hypofýza-kůra nadledvin (HPA) a osa hypotalamushypofýza-štítná žláza

Dexametazonový supresní test n n dexametazonový supresní test (DST) spočívá v perorálním podání dexametazonu v dávce kolem 1 mg ve 23 hodin a měření kortizolémie následující den Byl navržen jako endokrinní test pro diagnózu těžké depresivní epizody, neboť DST není účinný u 25 -45% depresivních pacientů a úspěšná léčba antidepresivy vede k obnově normální odezvy.

Fenfluraminový test n n n fenfluraminový test se používá pro sledování aktivity serotoninergního systému v mozku d‑Fenfluramin zvyšuje hladiny uvolněného 5 -HT v mozku, což vede ke zvýšenému vyplavování prolaktinu z adenohypofýzy. test spočívá v podání 60 mg d‑fenfluraminu s předchozím a následným měřením prolaktinémie. Předpokládá se, že osoby v depresívní epizodě mohou mít vyšší bazální prolaktinémii a menší zvýšení prolaktinu v odpovědi na podání fenfluraminu oproti kontrolám

Vlastnosti receptorů n n n disociační vazebná konstanta (Kd) se používá pro charakterizaci síly vazby ligandu k receptoru (menší hodnoty Kd pro specifická vazebná místa přitom znamenají větší sílu vazby) vazebná kapacita (Bmax) vyjadřuje množství maximálně navázaného ligandu vztažené obvykle na jednotkovou hmotnost membránových proteinů disociační konstanta a vazebná kapacita jsou základní veličiny pro charakterizaci vztahu struktura-funkce při interakcích léčiva se specifickým receptorem

Vlastnosti přenašečů pro neuromediátory n n n maximální rychlost transportu do buňky (Vmax) odráží existenci saturovatelného množství přenašečů zdánlivá Michaelisova konstanta (Km) je definovaná jako hodnota koncentrace transportované látky, při níž dosahuje rychlost transportu do buňky poloviny Vmax; Km charakterizuje afinitu přenašeče k neuromediátoru. řada psychofarmak, především antidepresiv, působí inhibičně na reuptake serotoninu, noradrenalinu nebo dopaminu jak do presynaptických nervových zakončení v mozku, tak do buněk izolovaných z jiných tkání
- Slides: 49