Bindungen Ionen Molekl und Metallbindungen Bindungen In der

Bindungen Ionen-, Molekül- und Metallbindungen

Bindungen § In der Natur kommen meist Verbindungen von zwei oder mehr Elementen vor. § Als Bindung bezeichnet man das Zusammenhalten von zwei oder mehreren Elementen (Atomen). § Es gibt verschiedene Bindungen: – – Ionenbindung Molekülbindung Metallbindung und weitere

Die Oktettregel § Alle Atome haben ein Bestreben, die äusserste Elektronenschale komplett zu füllen. § Weil alle Edelgase die äusserste Schale komplett gefüllt haben, spricht man von der Edelgaskonfiguration oder Oktettregel.

Die Ionenbindung § Für die Bindungen sind ausschliesslich die Elektronen der äussersten Schale von Bedeutung. § Bei der Ionenbindung geben die Metalle Elektronen ab. § Die Nichtmetalle nehmen Elektronen auf.

Die Ionenbindung § Beispiel: Das Natriumatom (Na) in der I Hauptgruppe hat in der äussersten Schale 1 Elektron. Damit Na eine komplett gefüllte äusserste Elektronenschale erreicht, muss es also das eine Elektron loszuwerden.
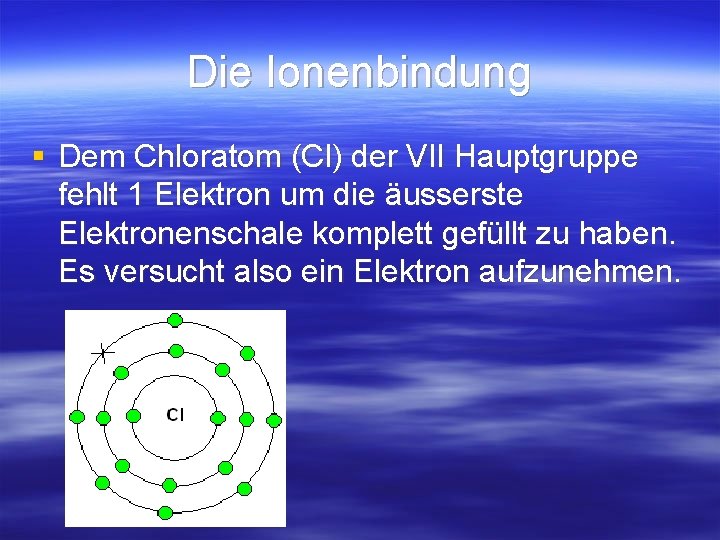
Die Ionenbindung § Dem Chloratom (Cl) der VII Hauptgruppe fehlt 1 Elektron um die äusserste Elektronenschale komplett gefüllt zu haben. Es versucht also ein Elektron aufzunehmen.

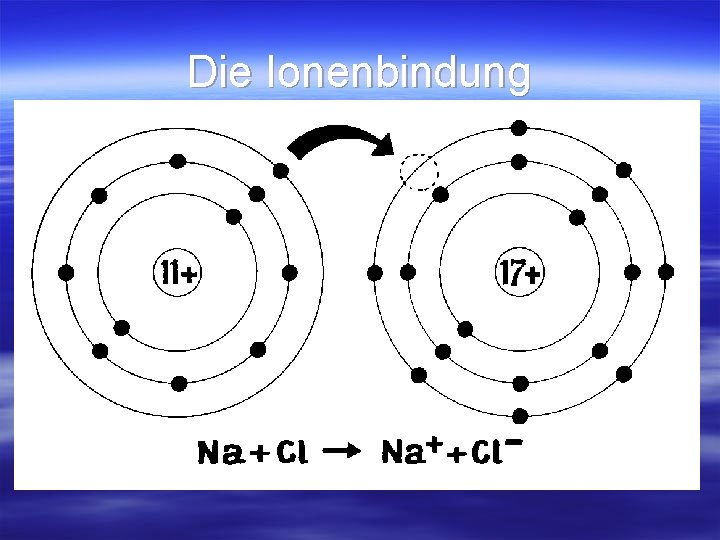
Die Ionenbindung § Wenn nun ein Na und ein Cl zusammen zur Reaktion gebracht werden, geht das Elektron vom Na zum Cl.
Die Ionenbindung

Die Ionenbindung § Da das Na nun ein Elektron mit der Ladung 1 - weniger hat, ist es einfach positiv geladen. (Die positive Ladung der Protonen im Kern überwiegt. ) § Ein geladenes Atom bezeichnet man als Ion. § Das Natriumion Na+ § Das umgekehrte gilt in diesem Fall für das Chloratom, das wegen der einfachen negativen Ladung zum Chlorion wird. Cl-

Die Ionenbindung § § § Theorieblatt „Die Ionenbindung“ Arbeitsblatt „Ionenbildung und Aufbau “ Lösung „Ionenbildung und Aufbau “ Arbeitsblatt „Ionenbindung im Modell 01“ Arbeitsblatt „Ionenbindung im Modell 02“ Lösung „Ionenbindung im Modell 01+02“

Die Molekülbindung § Die meisten bei Zimmertemperatur flüssigen und gasförmigen Stoffen bestehen aus Molekülen. § Da Edelgase keine Verbindungen eingehen bilden sie auch hier die Ausnahme. § Bei den Molekülbindungen lassen sich vorerst keine Ladungen wie bei der Ionenbindung feststellen.

Die Molekülbindung § Theorie zu Ionenbindung und Molekülbindung S. 122 -125 und 128 -129

Die Molekülbindung § Molekülbindung am Beispiel von Wasserstoff und Sauerstoff. Experiment mit Wasserstoff-Sauerstoff-Ballon § Die exotherme Reaktion bei der Wasserstoff (H 2) und Sauerstoff (O 2) miteinander verbunden wird, ist sehr heftig.

Die Wertigkeit § Die Atome haben verschiedene Wertigkeiten. § Das Chloratom kann nur ein Wasserstoffatom an sich binden. § Darum sagt man, das Chloratom sei einwertig. § Ein Sauerstoffatom, das 2 Wasserstoffatome an sich binden kann, ist zweiwertig. § Beispiel H 2 O (Wassermolekül) § Kohlenstoff kann 4 Wasserstoffatome an sich binden und ist darum vierwertig. (CH 4)

Die Wertigkeit § Einzelne Elemente haben verschiedene Wertigkeiten. § Kupfer (Cu) kann zum Beispiel die Wertigkeiten I und II haben. § Wenn ein zweiwertiges Atom mit einem einwertigen Atom verbunden wird, so muss auch das Atomverhältnis 1: 2 sein. § Beispiel Wassermolekül: § Wasserstoff (H) hat die Wertigkeit I § Sauerstoff (O) hat die Wertigkeit II § Darum braucht es doppelt so viele H wie O

Die Reaktionsgleichung § Ist die Wertigkeit der an einer Verbindung beteiligten Atome bekannt, so lässt sich die Reaktion als Reaktionsgleichung darstellen. § Auf beiden Seiten des Reaktionspfeil muss die gleiche Anzahl Atome vorhanden sein. § Beispiel: Reaktion zwischen Wasserstoff (H 2) und Sauerstoff (O 2) § 2 H 2 + O 2 2 H 2 O

Die Reaktionsgleichung § Übungsblatt „Wir üben das Aufstellen von Formeln“ § Lösung „Wir üben das Aufstellen von Formeln“

Die Reaktionsgleichung § Übungsblatt „Wir stellen Reaktionsgleichungen auf“ § Lösung „Wir stellen Reaktionsgleichungen auf“

Die Reaktionsgleichung § Ergänze die Gleichungen so, dass sie stimmen: § Mg + O § Mg + F § Na + S § S+O

Die Reaktionsgleichung § § § Lösungen 2 Mg + O 2 Mg + 2 F 2 Na + S 2 S + O 2 2 Mg. O Mg. F 2 Na 2 S 2 SO

Das Wassermolekül § Versuch: Plexiglasstab wird an einem Wolltuch gerieben und anschliessend an einen Wasserstrahl herangeführt. § Versuchsskizze: § Beobachtung: Der Wasserstrahl bewegt sich zum Plexiglasstab hin. § Auswertung: Im Wasser müssen elektrische Ladungen vorhanden sein, obwohl es bei Wasser um eine Molekülbindung handelt.

Das Wassermolekül § Bei Molekül- und Ionenbindungen bindende Kräfte zwischen den einzelnen Atomen.

Das Wassermolekül

Das Wassermolekül

Das Wassermolekül
- Slides: 25