Biljni hormoni Apikalna dominacija Vrh izdanka izvor auksina

Biljni hormoni
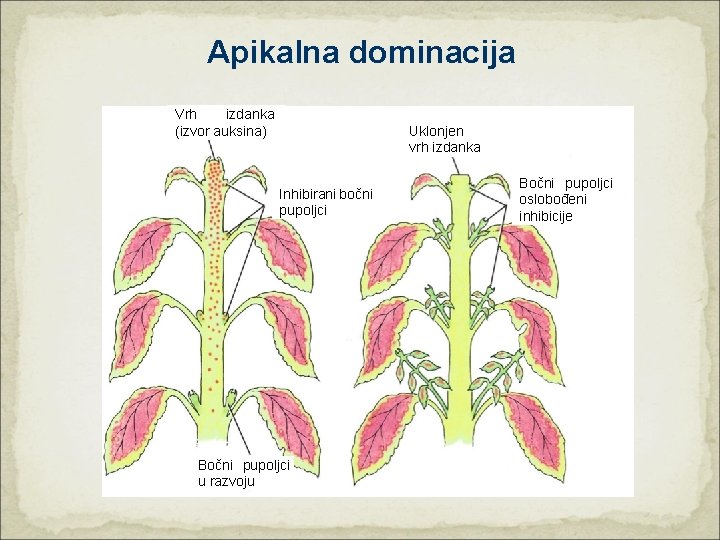
Apikalna dominacija Vrh izdanka (izvor auksina) Uklonjen vrh izdanka Inhibirani bočni pupoljci Bočni pupoljci u razvoju Bočni pupoljci oslobođeni inhibicije

Cilj vežbe: Uočiti apikalnu dominaciju kod intaktnih mladih biljaka graška i kod biljaka tretiranih IAA § Četiri grupe biljaka (10 biljaka u grupi): I - intaktne II - dekapitovane III - dekapitovane sa lanolinom IV - dekapitovane sa lanolinom i auksinom
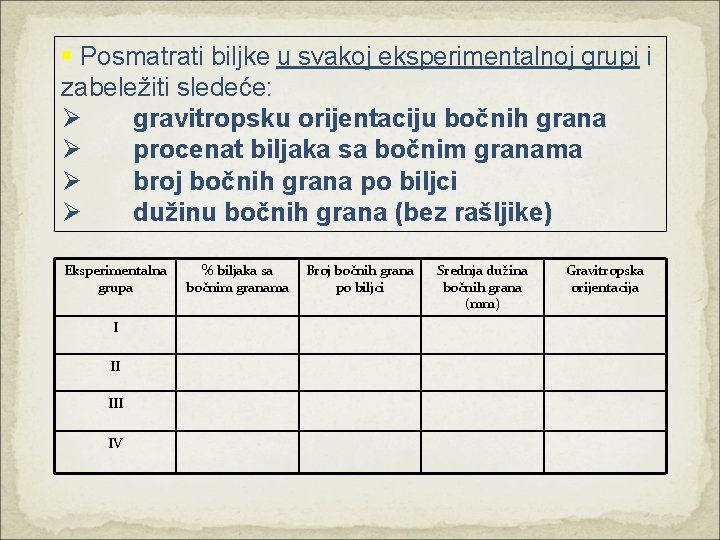
§ Posmatrati biljke u svakoj eksperimentalnoj grupi i zabeležiti sledeće: Ø gravitropsku orijentaciju bočnih grana Ø procenat biljaka sa bočnim granama Ø broj bočnih grana po biljci Ø dužinu bočnih grana (bez rašljike) Eksperimentalna grupa I II IV % biljaka sa bočnim granama Broj bočnih grana po biljci Srednja dužina bočnih grana (mm) Gravitropska orijentacija

Bočne grane u odnosu na stablo mogu rasti : Plagiogravitropno – grana i stablo formiraju ugao manji od 90° Dijagravitropno – grana i stablo formiraju ugao od 90° Ortogravitropno – grana i stablo rastu paralelno (ugao je približno 0°)

Kontrola 10 mg/L IBA 25 mg/L IBA 50 mg/L IBA Rizogeneza Nakon 24 h rastvor IBA zamenjen vodom.
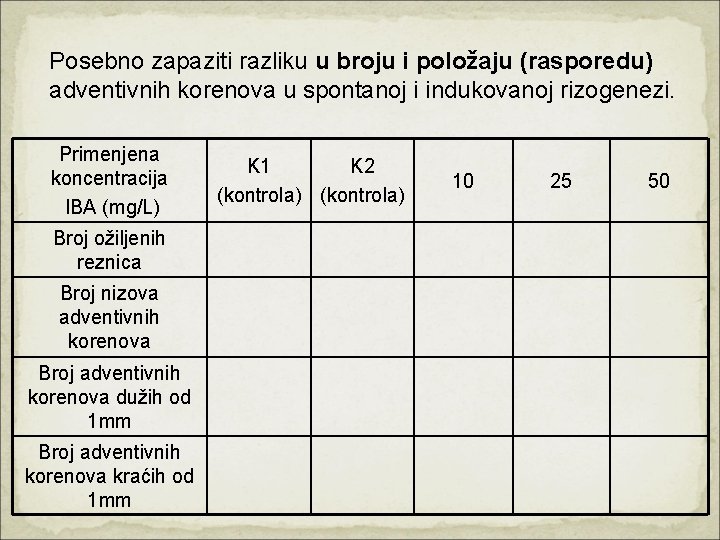
Posebno zapaziti razliku u broju i položaju (rasporedu) adventivnih korenova u spontanoj i indukovanoj rizogenezi. Primenjena koncentracija IBA (mg/L) Broj ožiljenih reznica Broj nizova adventivnih korenova Broj adventivnih korenova dužih od 1 mm Broj adventivnih korenova kraćih od 1 mm K 1 K 2 (kontrola) 10 25 50

GIBERELINI – Test sa patuljastim mutantima graška Koncentracije GA 3 (mg/ml): • 100 • 0. 1 • 10 • 0. 01 • K Internodije
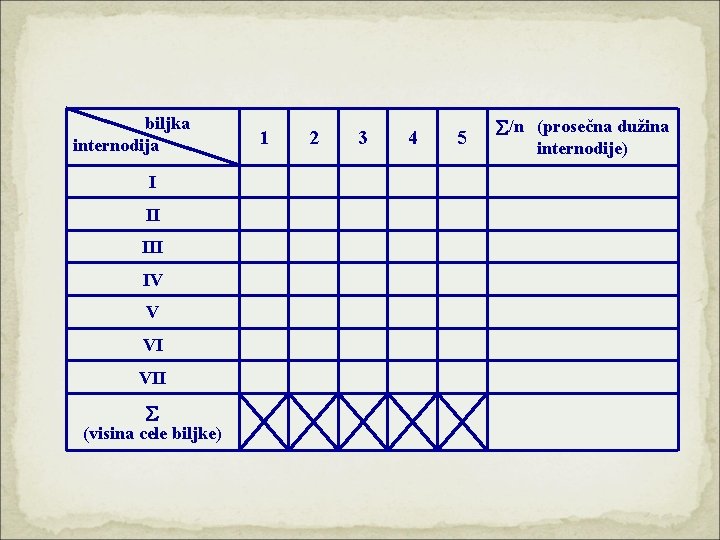
biljka internodija I II IV V VI VII (visina cele biljke) 1 2 3 4 5 /n (prosečna dužina internodije)


Interakcija giberelina i svetlosti u procesu izduživanja hipokotila salate Etiolirane biljke Izdužene internodije Nerazvijeni listovi Prisustvo apikalne kuke Odsustvo hlorofila i antocijanina Etiolman Antagonističko dejstvo svetlosti i giberelina na izduživanje hipokotila salate Mrak Svetlost

Biološki test sa hipokotilom salate • Pripremiti 7 petri kutija i obeležiti ih: Km Ks 10 -2 10 -1 1 10 102 • Napraviti seriju rastvora GA 3: 102; 10; 1; 10 -2 g/ml • U svaku petri kutiju staviti po krug filter papira i sipati po 3 ml odgovarajućeg rastvora GA 3, odnosno vode u kontrolu • U svaku petri šolju staviti 10 proklijalih semena salate • Kontrola u mraku se postavlja u mračnoj komori
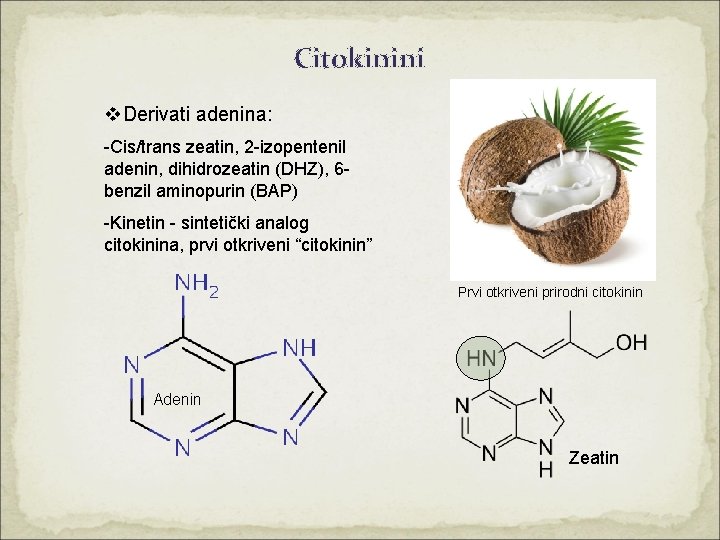
Citokinini v. Derivati adenina: -Cis/trans zeatin, 2 -izopentenil adenin, dihidrozeatin (DHZ), 6 benzil aminopurin (BAP) -Kinetin - sintetički analog citokinina, prvi otkriveni “citokinin” Prvi otkriveni prirodni citokinin Adenin Zeatin

Osnovni fiziološki efekti citokinina: Regulacija ćelijskog ciklusa Antagonisti auksinima u apikalnoj dominaciji Retencija hlorofila i odlaganje starenja listova Indukcija de novo razvoja pupoljaka, stimulacija rastenja mirujućih pupoljaka, stimulacija razvoja adventivnih i aksilarnih pupoljaka

Test retencije hlorofila Usmeravanje transporta i akumulacija asimilata i metabolita – mladi listovi koji sintetišu citokinine privlače hranljive materije iz drugih delova biljke

Odlažu destrukciju kompleksa hlorofila i proteina u tilakoidnim membranama, samim tim i destrukciju samog hlorofila – retencija hlorofila

Cilj • Detektovati uticaj kinetina na retenciju hlorofila u isečcima listova pšenice • Konstruisati standardnu krivu za opseg koncentracija 10 -3– 10 mg/l • Odrediti nepoznatu koncentraciju kinetina

Način rada: • Napraviti razblaženja KIN od početnog štok rastvora koncentracije 1 mg/ml (tj. 1000μg/ml). • Obeležiti petri kutije oznakama koncentracija rastvora kinetina i kontrole (10, 1, 10 -2, 103 i nepoznata koncentracija X). Imajte u vidu da se pri pravljenju razblaženja mora prvo početni rastvor mora razblažiti 10 x tako da se dobije koncentracija od 100 μg/ml, ali se ona ne koristi za postavku eksperimenta, već samo za dalja razblaženja!

• Naliti po 4 ml dobijenih razblaženja rastvora kinetina / vode za kontrolu. • Poređati 10 listova pšenice kao novčiće. Žiletom iseći odsečke veličine 10 mm i pincetom ih postaviti u svaku petri kutiju. • Postavke preneti u mrak, inkubirati na 25°C, tokom 48 h. • Nakon 7 dana, meriti apsorpciju hlorofila na spektrofotometru, a zatim izračunati koncentraciju hlorofila na osnovu formula i nacrtati grafik.
- Slides: 19