Bicarbonatos nicamente los metales alcalinos excepto el Li

Bicarbonatos • Únicamente los metales alcalinos (excepto el Li) forman compuestos sólidos con el ión bicarbonato HCO 3 - , que se descomponen a carbonato cuando se calientan. Na. HCO 3(s) D Na 2 CO 3(s) + H 2 O(l) +CO 2(g) • El ión bicarbonato reacciona con acidos para dar CO 2 y con bases para dar el ión carbonato CO 3 2 - 1

Carbonatos • La mayoría de los carbonatos son insolubles, con excepción del carbonato de amonio y los carbonatos de los metales alcalinos. • El ión carbonato es muy básico en solución acuosa como resultado de la hidrólisis que da el ión bicarbonato y el ión hidróxido. 2

Tetrahaluros de carbono • Todos los tetrahaluros contienen el átomo de carbono tetrahédricamente coordinado a cuatro átomos de halógenos. • El tetracloruro de carbono es un excelente solvente no polar. – Causa cancer • Las fases de los tetrahaluros reflejan el incremento en la fuerza de la fuerzas de dispersión intermoleculares. • 3

Tetrahaluros de carbono Tetrafloruro de carbono Gas sin color Tetracloruro de carbono Líquido denso Tetrabromuro de carbono Solido amarillo pálido Tetrayoduro de carbono Sólido rojo brillante 4

Clorofluorocarbonos • Tomas Midgley, Un químico de la General Motors que en 1928 sintetizó el diclorodiflourometano CCl 2 F 2. En la búsqueda de un refrigerante seguro. • En el tiempo del descubrimiento de la familia de compuestos clorofluorocarbono, estos fueron considerados como lo mejor. – No tóxicos. – Casi completamente no reactivos. • Usados en aire acondicionado, propelentes en aerosoles, agentes desengrasante, anestésicos. 5

Nomenclatura especial para los clorofluorocarbonos • El primer dígito representa el número de átomos de carbono menos 1. Para los CFC de un carbono, el cero se elimina. • El segundo dígito representa el número de átomos de hidrógeno mas uno. • El tercer dígito representa el número de átomos de fluor. • Los isómeros estructurales se distinguen por las letras a, b. Ejem. CFCl 3 (CFC-11); CF 2 Cl 2 (CFC-12) 6

Estabilidad de los Clorofluorocarbonos • Su falta de reactividad se debe – Falta de un camino de descomposición – Fuerza de enlace carbono-flour • Fue hasta 1970, cuando su mejor propiedad, su estabilidad se vio como una amenaza al ambiente – Los compuestos permanecen en la atmósfera por cientos de años. – Algunos de estos compuestos se difunden a la estratosfera donde la luz UV remueve un átomo de cloro, reaccionando con el ozono. 7

Destrucción de la capa de ozono por los clorofluorocarbonos • El cloro reacciona con las moléculas de ozono en una serie de pasos. • El átomo de cloro es libre después para repetir el ciclo varias veces, destruyendo grandes capas de ozono 8

HFCs como alternativa a los CFCs • Los hidrofluorocarbonos (HFC). No tienen el cloro que daña la capa de ozono. • Problemas – Proceso de producción costoso – Las unidades de refrigeración deberán ser alteradas. – Los fluorocarbonos son excelentes gases con efectos de invernadero. 9
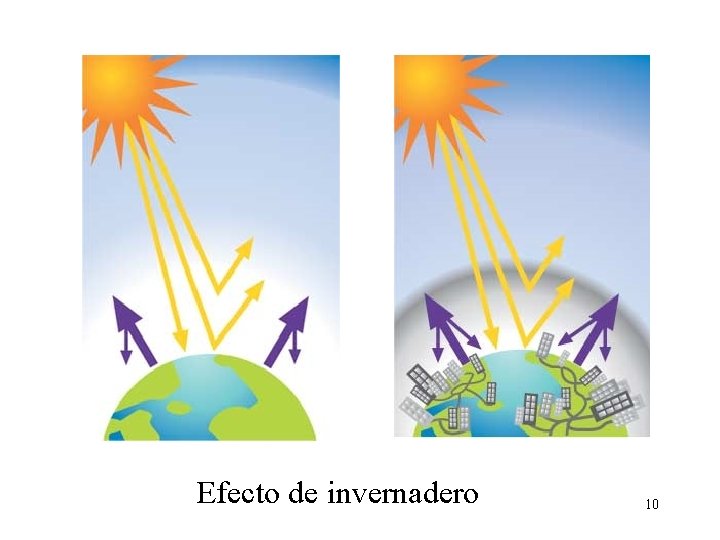
Efecto de invernadero 10

Cianuros • Toxicidad del cianuro de hidrógeno HCN y el ión cianuro, CN. • Se utiliza para producir polimeros de importancia industrial como nylon, melamina y los plásticos acrílicos. • El ión cianuro se usa para extraer la plata y el oro de sus minerales. 11

Preparación de cianuros • El proceso Degussa, involucra la reacción del metano con amoniaco a temperatura alta con platino como catalizador. • Mientras que el proceso Andrussow es similar pero requiere la presencia de oxígeno • El cianuro de hidrógeno es líquido a temperatura ambiente debido a los puentes de hidrógeno entre el hidrógeno y el nitrógeno. 12
- Slides: 12