Biaka w diagnostyce laboratoryjnej Stelmach Justyna Gr A

Białka w diagnostyce laboratoryjnej Stelmach Justyna Gr. A 2 III OAM

Rola białek osocza: �Kontrola dystrybucji płynów przestrzeni pozakomórkowej �Funkcje transportowe �Regulatory enzymów �Białka odpornościowe �Ciśnienie onkotyczne �Funkcja odżywcza

Proteinogram �Albuminy 60 -70% �Alfa-1 globuliny 2 -4% �Alfa-2 globuliny 4 -7% �Beta globuliny 8 -13% �Gamma globuliny 9 -22% Całkowite stężenie białka w osoczu 60 -80 g/l Wydalane z moczem= 20 -80 mg/dobę

�Za krytyczne uznaje się poziomy białka całkowitego poniżej 45 g/l i albuminy poniżej 20 g/l. Przy takich stężeniach ciśnienie onkotyczne jest bardzo niskie, dochodzi do ucieczki wody poza naczynia, powstawania obrzęków i przesięków do jam ciała.

Białka specyficzne: �Albuminy- ciśnienie onkotyczne (80%) �Alfa 1 -antytrypsyna-inhibitor proteaz �Beta 2 -mikroglubulina- podjednostka układu HLA �Ceruloplazmina- białko wiążące miedź i enzym �Białko C-reaktywne (CRP)- wskaźnik stanu zapalnego �Transferyna- białko transportujące żelazo �Ferrytyna- białko transportujące żelazo w tkankach �Haptoglobina- białko wiążące hemoglobinę �SHBG-Glubulina wiążąca hormony płciowe- wiąże testosteron �TBG-Globulina wiążąca hormony tarczycy �Transkobalamina- wiąże wit. B 12

Paraproteiny �immunoglobuliny produkowane przez pojedynczy klon komórek linii limfocytów B (np. plazmocyty) �zazwyczaj występuje w obrębie globulin gamma �paraproteiny pojawiają się najczęściej w przebiegu szpiczaka mnogiego, plazmocytom i choroby Waldemstrom’a (makroglobulinemia-Ig. M) �elektroforeza białek osocza jest podstawowym badaniem wykrywającym paraproteiny ale mocz powinien być także badany �w przebiegu szpiczaka wydzielane są tylko immunoglobuliny zbudowane z łańcuchów lekkich, które są wykrywane w 75% przypadków w moczu jako białko Bence-Jones’a

Synteza i degradacja białek osocza: � Dwie duże pule białek: � albumina-czynnikiem regulującym jej syntezę w wątrobie jest ciśnienie onkotyczne działające poprzez onkoreceptory łożyska naczyniowego � immunoglobuliny-syntetyzowane w limfocytach w wyniku ich aktywacji przez różne antygeny. � Degradacja ATP-niezależna w lizosomach (białka nieuszkodzone, „długo żyjące”). � Degradacja ATP-zależna w cytosolu (białka nieprawidłowe, „krótko żyjące”). � Okres półtrwania białek (czas wymagany do zmniejszenia stężenia białka do 50% wartości początkowej): � czynnik VIII krzepnięcia: kilka godzin � albumina: czternaście dni � immunoglobuliny: dwadzieścia cztery dni � Białka osocza nie gromadzą się w wątrobie, prawie cała pula białek znajduje się w przestrzeni międzykomórkowej, tylko 40% jest w naczyniach, pozostałe 60% w przestrzeni pozanaczyniowej. � Prawidłowy poziom białka całkowitego zależy od równowagi miedzy syntezą a degradacją dwóch, głównych frakcji białkowych: albuminy i immunoglobulin. � Większość białek jest katabolizowana w wątrobie lub komórkach śródbłonka naczyń.

Hipoproteinemia: �Obniżenie poziomu białek w wyniku: a) zwiększonej utraty białek b) zahamowania ich syntezy w wątrobie c) rozcieńczenia przez nadmiar lub zmiany dystrybucji wody pozakomórkowej. �Niedobory immunoglobulin �Zmiany objętości przestrzeni pozakomórkowej: � przewodnienia � spadek ciśnienia krwi �stany zapalne

� Przyczyny: � Zespoły utraty białka: nerkowe (kłębkowe zapalenie nerek, cukrzyca, toczeń rumieniowaty trzewny, zakrzepica żył nerkowych) � jelitowo/żołądkowe (stany zapalne, nowotwory złośliwe, zwężenie, uchyłki, choroba popromienna, niewydolność krążenia, zapalenie krezki) � skórne (rozległe oparzenia, dermatozy) � wysięki (obrzęki, zapalenia płuc, wodobrzusze) � krwotoki � stany ciężkie (urazy, nowotwory, sepsa) � � Zahamowanie syntezy białek w wątrobie: uszkodzenie miąższu wątroby (toksyczne, marskość, zanik miąższu, pierwotny lub wtórny nowotwór) � zaburzenia wchłaniania (zespoły poresekcyjne, biegunki bakteryjne, zakażenia, mukowiscydoza) � niedobory białka w diecie (niedożywienie) �

�Ocena niedoborów białek osocza � Niskie poziomy białka całkowitego i albuminy mogą poza leczeniem ich przyczyny, wymagać uzupełniania ich niedoboru, a szczególnie gdy są poniżej poziomów krytycznych. � Podczas uzupełniania niedoborów należy uwzględnić również wielkość dobową ujemnego bilansu białkowego. Skuteczność tego typu leczenia należy monitorować przez oznaczanie poziomu białka całkowitego i albuminy.

Hiperproteinemie � Prawdziwa hiperproteinemia jest spowodowana znacznym wzrostem produkcji jednej lub wielu klas immunoglobulin. � Zwiększeniu stężenia immunoglobulin często towarzyszy obniżenie poziomu albuminy. � Stężenie białka całkowitego może być w granicach normy lub obniżone, nawet przy znacznej hipergammaglobulinemii (w póżnych stadiach marskości wątroby, w rozwoju zespołu nerczycowego w przebiegu chorób kolagenowych). � Przyczyny hiperproteinemii � Hipergammaglobulinemie: monoklonalne (szpiczak mnogi, makroglobulinemia Waldenströma, choroba ciężkich łańcuchów) � poliklonalne (przewlekłe stany zapalne, choroby autoimmunologiczne) � przewlekłe choroby wątroby (marskość, wirusowe zapalenia, sarkoidoza) � odwodnienia �

Dysproteinemia � to nie prawidłowe proporcje białka we krwi, przy prawidłowym poziomie białka całkowitego

Szybkość opadania krwinek czerwonych (Odczyn Biernackiego, OB). �Test oceny zaburzeń proporcji między stężeniami poszczególnych białek osocza i właściwości erytrocytów. �W próbie krwi pobranej z antykoagulantem (cytrynian sodu) krwinki czerwone opadają w wyniku większego ciężaru właściwego (1. 095 g/l) niż osocze (1. 027 g/l).
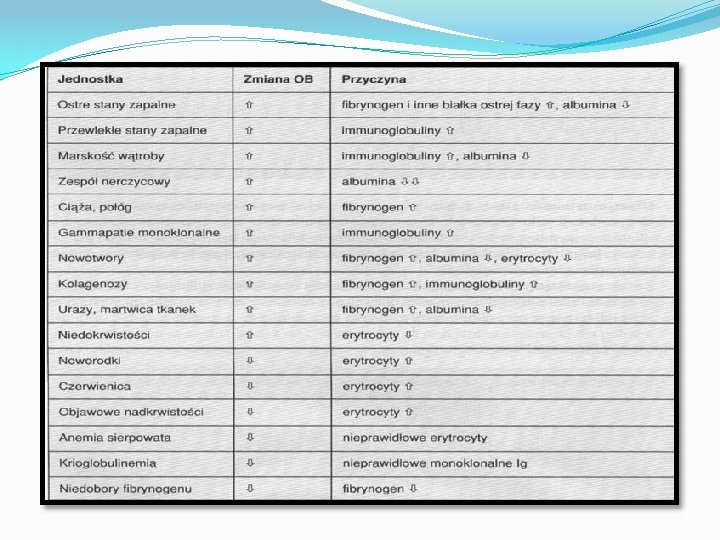

�Szybkość OB. Jest wypadkową składu osocza oraz właściwości erytrocytów. Zwiększenie stężenia fibrynogenu, białek frakcji globulinowych alfa i beta (białka ostrej fazy), oraz spadek poziomu albuminy powodują wzrost OB. �Mała ilość erytrocytów w niedokrwistościach jest przyczyną ich szybszego opadania.
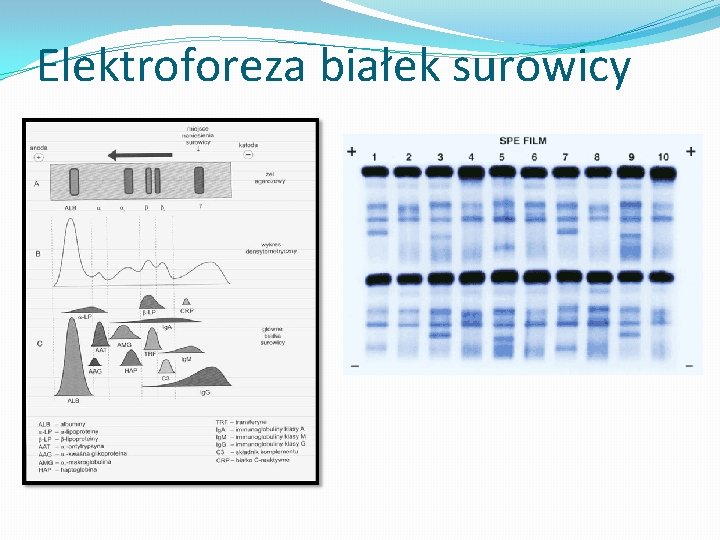
Elektroforeza białek surowicy

Elekroforeza (bibułowa, na agarozie, na octanie celulozy, w żelu skrobiowym i żelu poliakylamidowym) polega na wędrówce oznaczonych ładunkiem elektrycznym cząstek białkowych w roztworze elektrolitu podczas przepływu stałego prądu elektrycznego � szybkość wędrówki zależy od ruchliwości w polu elektrycznym, a ta zależy od wielkości cząstek i wielkości ładunku powierzchniowego � Białka, których zmiana stężeń może wpłynąć na obraz elektroforetyczny surowicy to: a) frakcja albuminowa (53 -68%) b) frakcja α 1 -globulinowa (1 -4%) c) frakcja α 2 - globulinowa (1 -14%) d) frakcja β globulinowa (8 -17% razem z beta 2) e) frakcja gamma-globulinowa (9 -22%)

Immunoelektroforeza białek surowicy ludzkiej � to połączenie rozdziału elektroforetycznego i immunoprecypitacji białek, przy zastosowaniu specyficznych reakcji precypitacji antygen-przeciwciało, jest często wykorzystywana w rozpoznawaniu paraproteinemii. Identyfikacja nieprawidłowych białek po rozdziale elektroforetycznym jest możliwa, jeśli zastosuje się surowice odpornościową. W wyniku reakcji antygen (antygenem jest w tym przypadku rozdzielone elektroforetycznie białko) z przeciwciałami znajdującymi się w surowicy odpornościowej wytwarzają się linie precypitacyjne, które umożliwiają identyfikację nieprawidłowego białka. Charakterystyczne zmiany zawartości jednej lub kilku frakcji białkowych stwierdza się w wielu chorobach.

CHROMATOGRAFIA �(bibułowa, jonowo wymienna, cienkowarstwowa) wykorzystuje różnice szybkości wędrówki składników białkowych w ośrodkach porowatych.

Białka płynu mózgowordzeniowego: mają skład podobny do białek osoczowych � zaliczamy do nich: prealbuminy, α 1 - i 2 - , β-, gamma- globuliny �stężenie białek w płynie mózgowo-rdzeniowym jest ok. 100 razy mniejsze i wynosi 0, 15 -0, 45 g/l

Elektroforeza białek PMR �Cechy charakterystyczne: prealbumina, białko tau (związane z mikrotubulami neuronów, odpowiada za ich stabilizacje oraz wiązanie z neurofilamentami i organellami komórkowymi) Brak fibrynogenu.

Albumina �Syntetyzowana w wątrobie, ok. 15 g/dobę. �Czas połowicznego trwania (T 1/2) 14 dni. �Nieswoisty transporter bilirubiny, hormonów, witamin, wapnia, magnezu, kwasów tłuszczowych, leków oraz substancji wchłoniętych w jelitach i transportowanych do wątroby. �Bisalbuminemia – występowanie dwóch rodzajów albumin o różnym składzie aminokwasowym i różnej mobilności elektroforetycznej.

Immunoglobuliny: �Immunoglobuliny (przeciwciała) mają zdolność swoistego łączenia się z antygenem i są najważniejszymi cząsteczkami układu odpornościowego. �Syntetyzowane przez limfocyty B. �Na podstawie różnic w budowie łańcuchów ciężkich (α, δ, ε, γ, μ) wyróżniamy odpowiednio pięć klas: Ig. A, Ig. D, Ig. E, Ig. G, Ig. M.

Hipogammaglobulinemia � Pierwotna – uwarunkowana genetycznie raczej rzadko spotykana, może dotyczyć wszystkich lub jednej klasy Ig. � Wtórna – związana z chorobą (nowotwory, leczenie cytostatykami, usunięcie śledziony). Bardzo niskie poziomy immunoglobulin związane są najczęściej z ubytkiem limfocytów B.

Hipergammaglobulinemia poliklonalna – jest to prawidłowa odpowiedź organizmu na infekcję bakteryjną lub wirusową. W pierwszym etapie infekcji następuje wzrost stężenia Ig. M, po dwóch tygodniach Ig. G oraz stopniowy zanik Ig. M. � Podwyższony poziom Ig. A jest często związany z infekcjami błon śluzowych (S-Ig. A wytwarzane miejscowo przez komórki plazmatyczne błon śluzowych mają zdolność neutralizowania wirusów i wiekszą efektywność aglutynacji bakterii). � Hipergammaglobulinemia monoklonalna – wzrost immunoglobulin produkowanych przez nadmiernie rozrastającą się linię limfocytów (grupa chorób nowotworowych limfocytów B). � Przyczyny: szpiczaki, makroglobulinemia Waldenströma, chłoniaki i łagodne gammapatie monoklonalne. �

Białka ostrej fazy �Synteza w wątrobie pod wpływem cytokin zapalnych w przebiegu zakażeń bakteryjnych, martwicy tkanek, ostrych i przewlekłych stanów zapalnych, chorób zakaźnych, nowotworów. Część nieswoistej odpowiedzi immunologicznej. �Rola- modulowanie odczynu zapalnego i ochrona tkanek nieobjętych stanem zapalnym przed niszczącym działaniem proteinaz i silnych oksydantów wydzielanych przez fagocyty.

Niewielki ↑: �Choroby nowotworowe �Niedożywienie �Ciąża �Menstruacja �Zespół metaboliczny �Opsoniny, inhibitory proteinaz, chelatory metali, transportery hormonów, białka wiążące hem i hemoglobinę, białka układu krzepnięcia (fibrynogen i antyplazmina III) oraz białka układu dopełniacza.

Ujemne białka ostrej fazy: �Albumina �Transferryna �Prealbumina Dodatnie białka ostrej fazy: �fibrynogen �α 1 - antytrypsyna (AAT) �ceruloplazmina �haptoglobina (HP) �białko C-reaktywne (CRP) �surowicze amyloidowe białko A (SAA) �laktoferryna �białka układu dopełniacza

Białko C-reaktywne Znaczny wzrost obserwowany jest w pierwszej dobie uszkodzenia tkanek (zawał mięśnia sercowego, białaczek, w odrzucie przeszczepów, zakażeniach bakteryjnych). � Prawidłowe stężenie CRP w surowicy jest mniejsze niż 5 mg/l. � hs. CRP - test o wysokiej czułości: 0. 2 mg/l; pozwala na zmierzenie bardzo małych wartości CRP z dużą precyzją w zakresie decyzyjnym. � Wyniki ostatnich badań wskazują, że stężenie CRP posiada znaczenie prognostyczne w chorobie sercowo-naczyniowej. Procesy zapalne odgrywają bardzo ważną rolę w patogenezie miażdżycy, a stopień podwyższenia poziomu CRP, który jest charakterystyczny dla przewlekłego stanu zapalnego, jest czynnikiem oceniającym ryzyko wystąpienia zawału mięśnia sercowego lub udaru mózgu. � Poziom CRP powyżej 2. 1 mg/l jest związany z trzykrotnym zwiększeniem ryzyka wystąpienia zawału mięśnia sercowego oraz dwukrotnym zwiększeniem ryzyka wystąpienia udaru mózgu. �

Metody ilościowego oznaczania białek: �Metoda Lowry’ego �Metoda Bradforda �Metoda mikrobiuretowa �Metoda pomiaru absorbancji w UV �Metoda z kwasem Bis-cynchoninowym (BCA) �Metoda Kiejdahla �Metoda biuretowa �Metoda kolorymetryczna z odczynnikiem Nesslera

Metoda Kiejdahla �Metoda referencyjna, oznaczanie azotu, Zasada: �Zawartość azotu w różnych białkach jest względnie stała i wynosi ok. 16%. �Znając odsetek azotu w badanej próbie, można obliczyć, ile zawiera białka.

Metoda kolorymetryczna z odczynnikiem Nesslera �Żółtozielony roztwór jodku rtęciowo-potasowego przechodzi w czerwony jodek amidooksyrtęciowy. Pomiar absorbancji 490 -510 nm �Zalety: duża specyficzność da wszystkich białek �Wady: duża pracochłonność

Metoda biuretowa Zasada oznaczenia: �Oznaczanie natężenia barwy powstałej w wyniku utworzenia związków kompleksowych białek z jonami miedzi (II) w środowisku zasadowym λ =530 nm �Zalety: Wysoka specyficzność dla wszystkich białek �Wady: niska czułość (10 mg/l). �Materiał: Surowica, mocz (w zaawansowanej nerczycy)

Metoda mikrobiuretowa: Modyfikacja metody biuretowej � Mechanizm podobny, ale zastosowana długość fali 310 nm zwiększa ok 10 x jej czułość � Każdą próbę wykonuje się w dwóch szeregach: biały (B) i niebieski (N) � Szereg biały zawiera roztwór białka + 30% Na. OH, szereg niebieski roztwór białka + Cu. SO 4 w 30% Na. OH �Właściwą absorbancję do obliczeń otrzymuje się z różnicy N-B. Zalety: wysoka specyficzność w stosunku do wszystkich białek. Wady: duże zużycie roztworu białka (dwa szeregi)

Metoda Lowry’ego �Zasada: dwie odrębne reakcje: reakcja aminokwasów z odczynnikiem Folina reakcja biuretowa. �Zalety: bardzo wysoka czułość reakcji (1 mg/l) �Wady: mała specyficzność. �Materiał : Mocz, PMR.

Metoda Bradforda �W metodzie wykorzystuje się zdolność wiązania barwnika błękitu brylantowego - Coomassie Brilliant Blue G-250 (CBB G 250) z grupami aminowymi białek. �λ=595 nm �Zalety: � prostota i szybkość oznaczenia � duża czułość (0, 5 mg/l) �oznaczenia można wykonywać w obecności powszechnie stosowanych buforów, EDTA, związków tiolowych, sacharozy, glicerolu

Metoda pomiaru absorbancji w UV �Wartość wsp. absorpcji zależy od % zawartości aminokwasów aromatycznych i dla białek osocza o stężeniu 1 mg/ml wynosi od 0, 8 do 1, 6 �Obecność kwasów nukleinowych w badanym materiale przeszkadza w oznaczeniu (max absorbcji 260 nm) �Wady: � Mała specyficzność �Metoda nadaje się do oznaczania stężenia oczyszczonego białka (na podstawie znanego wsp. absorpcji)

Metoda z kwasem bis-cynchoninowym (BCA) �W alkalicznym środowisku niektóre składniki białek (tyrozyna, tryptofan, cysteina, cystyna) redukują jony Cu 2+ do Cu 1+ � Cu 1+ tworzą barwny kompleksowy związek z kwasem biscynchoninowym(BCA) �λ=540 – 580 nm

Białka markery

Markery zawału mięśnia secowego �Markery prognostyczne: Hs-CRP- high sensitive-C-Reactive Protein (wysoko czułe białko C-reaktywne) MPO- mieloperoksydaza CD-40 �Markery destabilizacji blaszki miażdżycowej PAPP-A- Pregnancy-Associated Protein-A (ciążowe białko osoczowe A) �Markery niedokrwienia IMA (ACB)- Ischemia Modifed Albumin (Albumin Cobalt Binding) Albumina modyfikowana niedokrwieniem (wiązanie kobaltu przez albuminę)

�Markery martwicy komórkowej Mioglobina (niespecyficzny) H-FABP- Hart-Fatty Acid Binding Protein (sercowe białko wiążące kwasy tłuszczowe) CK-MB Troponiny sercowe (cardiac)- c. Tn. T, c. Tn. I �Marker niewydolności serca Peptydy natriuretyczne (Natriuretic peptides)- ANPprzedsionkowy (atrial) (typ A); BNP- mózgowy (brain) (typ B); NT-pro. BNP

Markery filtracji kłębkowej (nerkowej): �Beta-2 mikroglobulina- jest niskocząsteczkowym białkiem (11. 8 k. Da) obecnym na błonie komórkowej prawie wszystkich komórek jądrzastych (także limfocytów). Beta 2 -M jest małą podjednostką antygenu zgodności tkankowej (HLA). Nerka jest głównym miejscem eliminacji beta-2 -M gdzie jest filtrowana w kłębuszkach i w 99. 9% reabsorbowana w kanalikach proksymalnych. �cystatyna C- jest kationowym polipeptydem o masie cząsteczkowej 13 k. Da. Ponieważ podlega stałej i równomiernej produkcji i ulega całkowitej filtracji w kłębuszkach nerkowych, cystatna-C jest endogennym markerem filtracji (GFR) lepszym niż beta-2 -M i kreatynina.

SHBG �Steroi Hormons Binding Globulin (globulina wiążąca hormony sterydowe)- oznaczenie SHBG jest polecane w przypadku konieczności wyjaśnienia niskiego lub wysokiego stężenia testosteronu, gdy wolny (biologicznie aktywny) testosteron jest w normie
- Slides: 43