Bi ging HA HC I CNG 30 tit

Bài giảng HÓA HỌC ĐẠI CƯƠNG (30 tiết) GV: Th. S. Nguyễn Thị Trâm Châu DD: 0905 628 268 Mail: nguyenthitramchau@yahoo. com Blog: nguyenthitramchaudhcn. wordpress. com
Giới thiệu HÓA HỌC ĐẠI CƯƠNG (30 tiết) NỘI DUNG MÔN HỌC STT Nội dung Số tiết 4 1 Chương 1: Các khái niệm cơ bản 2 Chương 2: Cấu tạo nguyên tử 5 3 Chương 3: Định luật tuần hoàn 3 4 7 5 Chương 4: Cấu tạo phân tử Thi giữa học kỳ 6 Chương 5: Các trạng thái tự nhiên 4 7 Chương 6: Dung dịch 7 1

Tài liệu HÓA HỌC ĐẠI CƯƠNG (30 tiết) Giáo trình chính: Hóa học đại cương- Trung tâm CN Hóa học. Tài liệu tham khảo: [1]. Nguyễn Minh Châu – Hoá đại cương – NXB Giáo dục 2001. [2]. Nguyễn Đức Chuy – Hoá học đại cương – NXB Giáo dục 2002. [3]. Nguyễn Đình Soa – Hoá học đại cương 1 và 2 – NXB Giáo dục 2002. [4]. Lâm Ngọc Thiềm và Trần Hiệp Hải – Bài tập những nguyên lý cơ bản của hoá học – NXB Giáo dục 2002.

Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ NỘI DUNG 1. 1. Các khái niệm cơ bản 1. 2. Các định luật cơ bản 1. 2. 1. Định luật bảo toàn khối lượng 1. 2. 2. Định luật thành phần không đổi 1. 2. 3. Định luật tỷ lệ bội 1. 2. 4. Định luật tỷ lệ thể tích chất khí 1. 2. 5. Định luật đương lượng 1. 2. 6. Phương trình trạng thái khí lý tưởng 1. 2. 7. Xác định khối lượng phân tử và nguyên tử 1. 3. Hướng dẫn cách tính đương lượng

Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ 1. 1. Các khái niệm 1. 1. 1. Nguyên tử, nguyên tố hoá học a. Nguyên tử (1) Khái niệm - Về phương diện cấu tạo: nguyên tử là đơn vị nhỏ nhất của các chất vì các chất đều được tạo thành từ nguyên tử. - Về phương diện hoá học: nguyên tử là tiểu phân nhỏ nhất của một nguyên tố hoá học, không thể chia nhỏ hơn được nữa về mặt hoá học và không bị biến đổi trong các phản ứng hoá học.

Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ (2) Cấu tạo nguyên tử * Gồm: hạt nhân mang điện tích dương và lớp vỏ electron (e) mang điện tích âm. - Hạt nhân ngtử gồm: Hạt proton (p) mang điện dương (+1) và hạt nơtron (n) không mang điện. + Điện tích hạt nhân (Z+) = số p = số e + Khối lượng ngtử: Số khối (A)= p + n = Z + n + STT trong bảng HTTH = Z = p = e

Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ b. Nguyên tố hóa học: là chất được tạo thành từ các nguyên tử có điện tích hạt nhân giống nhau. (Hay: Nguyên tố hhọc là chất mà các nguyên tử của nó có cùng điện tích hạt nhân và cùng chiếm một chỗ trong bảng HTTH). - Kí hiệu đầy đủ ngtử ngtố X: - Với mỗi nguyên tố: proton (hay Z) là cố định, số N có thể thay đổi.
Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ - Đồng vị là: những nguyên tử có điện tích hạt nhân giống nhau (cùng số p, số Z, số e), nhưng có khối lượng khác nhau (khác số N). - VD: Có bao nhiêu proton, nơtron và electron cho 16 8 mỗi ngtố hoá học sau: O 12 6 C 14 6 C

Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ 1. 1. 2. Phân tử, chất hoá học, đơn chất, hợp chất a. Phân tử - Khái niệm: Phân tử là tiểu phân nhỏ nhất của một chất có khả năng tồn tại độc lập, mang đầy đủ bản chất hóa học của chất đó. - Phân tử là tập hợp một nhóm nguyên tử có thể cùng loại hoặc khác loại.

Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ b. Chất hóa học, đơn chất, hợp chất Chất hoá học: là tập hợp các phân tử cùng loại có thành phần và cấu tạo hoá học như nhau. Đơn chất: là chất hoá học mà phân tử của chúng tạo thành từ các nguyên tử của một nguyên tố kết hợp với nhau, như khí H 2 , O 3 , S, Fe, Na, Cl 2 … Hợp chất: là chất hoá học mà phân tử của chúng tạo thành từ những nguyên tử của các nguyên tố khác loại kết hợp với nhau, như CO, CO 2, NH 3, HNO 3, HCl, Ca. CO 3…

Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ 1. 1. 3. Khối lượng nguyên tử, phân tử, nguyên tử gam, phân tử gam a. Khối lượng nguyên tử - Trước đây, người ta thống nhất lấy khối lượng nguyên tử hyđro (đ. v. H) và sau là lấy 1/16 khối lượng nguyên tử oxy làm đơn vị đo (đ. v. O). - Từ 1961 đến nay, người ta thống nhất lấy 1/12 khối lượng của nguyên tử đồng vị C 12 làm đơn vị đo (đ. v. C). * Như vậy: Khối lượng ngtử của ngtố có thể được đo bằng đơn vị đ. v. H, đ. v. O, hay đ. v. C ? (Btập 5)

Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ * Khái niệm: Khối lượng nguyên tử là khối lượng một ngtử của ngtố đo bằng đơn vị cacbon, ký hiệu là A. Ví dụ: Khối lượng ngtử O = b. Khối lượng phân tử: là khối lượng một phân tử của một chất tính bằng đơn vị cacbon, ký hiệu là M. Ví dụ: H 2 O là 18, 0152 đv. C, NH 3 là 17, 0304 đv. C. c. Nguyên tử gam: “ Nguyên tử gam của 1 nguyên tố là lượng tính bằng gam của nguyên tố đó, có số đo bằng khối lượng ngtử của nó. ” - Ví dụ: Một ngtử gam của Fe bằng 55, 847 g; một ngtử gam của O là 15, 9994 g; của Cu là 63, 546 g…

Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ d. Phân tử gam: “Phân tử gam của một chất là lượng tính bằng gam của chất đó, có số đo bằng khối lượng phân tử của nó”. - Vd: Khối lượng ngtử của Cl bằng 35, 453 đv. C có nghĩa là: ngtử Cl có khối lượng gấp 35, 453 lần so với 1/12 khối lượng của nguyên tử 12 C, còn nguyên tử gam của Cl bằng 35, 453 g. • Mol: là đơn vị đo lượng chất, 1 mol bất kỳ đều chứa số tiểu phân như nhau (số Avogadro: N = 6, 02214199. 1023).

Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ - Khối lượng mol phân tử (phtử gam): là khối lượng tính bằng gam của 1 mol phân tử chất đó (g). - Khối lượng mol nguyên tử (ngtử gam): là khối lượng tính bằng gam của 1 mol nguyên tử đó (g). - Tương tự: khối lượng mol ion Ví dụ 1: + 1 mol nguyên tử Cl chứa 6, 022. 1023 ngtử Cl, + khối lượng mol ngtử Cl = 35, 453 g. + Khối lượng ngtử Cl = 35, 453 đ. v. C Ví dụ 2: + Khối lượng phân tử CO 2 bằng 44 đv. C + Khối lượng mol phân tử CO 2 bằng 44 g (Phân tử gam của CO 2 là 44 g). (Bài tập: 7, 8)

Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ 1. 1. 4. Ký hiệu hóa học, công thức, phương trình hóa học a. Kí hiệu hoá học: - Mỗi nguyên tố hóa học được kí hiệu bằng chữ cái đầu hay hai chữ cái trong tên Latinh của nguyên tố đó. - Mỗi kí hiệu hoá học của nguyên tố đồng thời chỉ 1 nguyên tử của nguyên tố đó. b. Công thức: dùng biểu thị các chất (phân tử), ví dụ: hidro (H 2). c. Phương trình hóa học: dùng để biểu thị các phản ứng hóa học bằng công thức hóa học. Ví dụ: 2 NO + 1 O 2 → 2 NO 2 2 (14 + 16)g 32 g 2 (14 +32)g
Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ * Phân loại phản ứng hóa học Phản ứng kết hợp: C + O 2 CO 2 Phản ứng phân hủy: Ca. CO 3 Ca. O + CO 2 Phản ứng thế: Fe + Cu. SO 4 Fe. SO 4 + Cu Phản ứng trao đổi: Ag. NO 3+Na. Cl Ag. Cl+ Na. NO 3 Phản ứng tỏa nhiệt: H 2 + Cl 2 2 HCl, H = -2, 3 k. J Phản ứng thu nhiệt: N 2 + O 2 2 NO, H = +90, 4 k. J Phản ứng một chiều: 2 KCl. O 3 2 KCl + 3 O 2 Phản ứng hai chiều: N 2 + 3 H 2 ↔ 2 NH 3 Phản ứng oxy hóa khử: 2 Fe. Cl 3 + Sn. Cl 2 Fe. Cl 2 + Sn. Cl 4

Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ 1. 2. Các định luật căn bản 1. 2. 1. Định luật bảo toàn khối lượng Nội dung: Tổng khối lượng các sản phẩm thu được đúng bằng tổng khối lượng các chất ban đầu đã tác dụng. 1. 2. 2. Định luật thành phần không đổi Nội dung: Mỗi hợp chất hoá học có thành phần khối lượng không đổi và không phụ thuộc vào các phương pháp điều chế nó. Ví dụ: * H 2 O dù điều chế bằng cách nào khi phân tích thành phần đều cho tỷ lệ: 11, 1% : 88, 9% hay 1 g : 8 g. * Na. Cl: có 39, 34% Na và 60, 66% Cl * Trừ trường hợp các khuyết tật trong mạng tinh thể.

Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ 1. 2. 3. Định luật tỷ lệ bội - Nội dung: Nếu hai nguyên tố kết hợp với nhau tạo thành một số hợp chất thì những lượng khối lượng của một nguyên tố so với cùng một lượng khối lượng của nguyên tố kia sẽ tỷ lệ với nhau như những số nguyên đơn giản. - Ví dụ: Nitơ kết hợp với oxi tạo thành 5 oxit có công thức phân tử lần lượt là: N 2 O, N 2 O 3, NO 2, N 2 O 5, nếu ứng với một đơn vị khối lượng nitơ thì khối lượng của oxy trong các oxit đó lần lượt là: 16/28 : 16/14 : 48/28 : 32/14 : 80/28 = 0, 57 : 1, 14 : 1, 71 : 2, 28 : 2, 85 hay 1 : 2 : 3 : 4 : 5
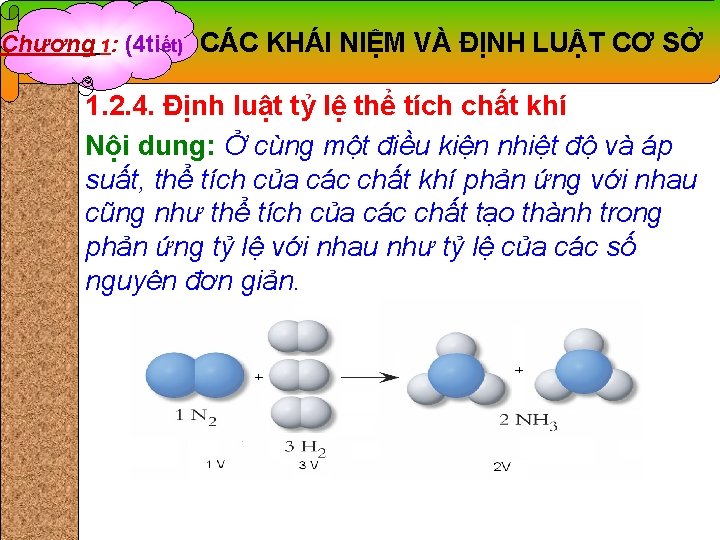
Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ 1. 2. 4. Định luật tỷ lệ thể tích chất khí Nội dung: Ở cùng một điều kiện nhiệt độ và áp suất, thể tích của các chất khí phản ứng với nhau cũng như thể tích của các chất tạo thành trong phản ứng tỷ lệ với nhau như tỷ lệ của các số nguyên đơn giản.

Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ 1. 2. 5. Định luật Avogadro Nội dung: Ở cùng một điều kiện nhiệt độ và áp suất, những thể tích bằng nhau (V 1=V 2) của các khí đều chứa cùng một số phân tử (N 1=N 2). - Ở điều kiện tiêu chuẩn 00 C và 760 mm. Hg một mol khí của bất kỳ một chất nào cũng chiếm một thể tích là 22, 4 lít và có chứa cùng một số phân tử. Số này gọi là hằng số Avogadro, ký hiệu N. N = 6, 022. 1023 (Bài tập 18)

Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ 1. 2. 6. Định luật đuơng lượng a. Định nghĩa: Đương lượng của một nguyên tố là số phần khối lượng của nguyên tố đó kết hợp (hoặc thay thế) vừa đủ với 1, 008 phần khối lượng của hyđro hoặc 8 phần khối lượng của oxy. - Đương lượng của hyđro là ĐH=1, 008; ĐO= 8 b. Nội dung định luật đương lượng: Các nguyên tố hoá học kết hợp với nhau theo những lượng khối lượng tỷ lệ với đương lượng của chúng.

Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ - Nếu gọi m là khối lượng, Đ là đương lượng và A, B là 2 nguyên tố hóa học đã kết hợp với nhau thì định luật đương luợng có thể biểu diễn bằng biểu thức: - Bằng cách biến đổi đơn giản, biểu thức trên có dạng như sau: - Mối liên quan giữa đương lượng của hợp chất và số ion trao đổi được thể hiện trong hệ thức sau:

Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ c. Xác định đương lượng * Xác định đương lượng của axit và bazơ: Đương lượng của acid và bazơ được xác định theo công thức: Với, n: số ion H+ hay OH- bị thay thế trong phân tử acid hay bazơ * Xác định đương lượng của muối/oxit: Đương lượng của muối được xác định theo công thức: Trong đó, n: số ion đã thay thế. z: điện tích ion đã thay thế.

Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ * Xác định đương lượng của chất oxy hóa và chất khử: Để xác định đương lượng chất oxy hóa, chất khử chúng ta sử dụng công thức: -Trong đó, n là số electron mà một phân tử chất khử có thể cho hay một phân tử chất oxy hóa có thể nhận được. * Đương lượng của một nguyên tố A trong hợp chất: ĐA = MA / Số oxh A Ví dụ 1: Đương lượng của Cr trong hợp chất: Cr 2(SO 4)3 là: ĐCr = 55/3 ; Cr. Cl 3 là: ĐCr = 55/3 (Bài tập: 37, 39)

Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ Ví dụ 2: Đương lượng của acid H 2 SO 4 trong 2 pứ sau: H 2 SO 4 + Na. OH Na. HSO 4 + H 2 O (1) Đ = 98/1 = 98 H 2 SO 4 + 2 Na. OH Na 2 SO 4 + 2 H 2 O (2) Đ = 98/2 = 49 Ví dụ 3: Đương lượng của muối trong các pứ: Fe 2(SO 4)3 + 6 Na. OH 2 Fe(OH)3 +Na 2 SO 4 (3) ĐFe 2(SO 4)3 = 400/6 = 66, 66 2 Fe. Cl 3 + Sn. Cl 2 Fe. Cl 2 + Sn. Cl 4 (4)
Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ Bài tập về đương lượng 1. Tính ñöông löôïng töøng acid, bazô trong caùc phaûn öùng: H 3 PO 4 + Na. OH Na. H 2 PO 4 + H 2 O H 3 PO 4 + 3 Na. OH Na 3 PO 4 + 3 H 2 O 2 HCl + Cu(OH)2 Cu. Cl 2 + 2 H 2 O HCl + Cu(OH)2 Cu(OH)Cl + H 2 O 2. Tính đượng lượng của các chất in màu xanh Fe. SO 4 + Ba. Cl 2 Ba. SO 4 + Fe. Cl 2 Al 2 O 3 + 6 HCl 2 Al. Cl 3 + 3 H 2 O CO 2 + Na. OH Na. HCO 3 CO 2 + 2 Na. OH Na 2 CO 3 + H 2 O Al 2 O 3 + 2 Na. OH 2 Na. Al. O 2 + H 2 O 3. Tính đượng lượng của các chất in màu xanh và màu đỏ 2 Fe. Cl 3 + Sn. Cl 2 2 Fe. Cl 2 + Sn. Cl 4 2 KMn. O 4+5 HNO 2+ 3 H 2 SO 4 2 Mn. SO 4 + K 2 SO 4 + 5 HNO 3 + 3 H 2 O K Cr O + 3 H S + 4 H SO Cr (SO ) +3 S + K SO + 7 H O

Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ 1. 2. 7. Phương trình trạng thái khí lý tưởng a. Khí lý tưởng: Chất khí mà phân tử của nó là những quả cầu đàn hồi, không có thể tích riêng và không tương tác với nhau. Phương trình trạng thái khí lý tưởng: Trong đó: P: áp suất của chất khí (atm) V: thể tích (l) m: khối lượng (g) M: phân tử lượng n: số mol khí R: hằng số khí Trang 22

Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ * Công thức tính số nguyên tử, số phân tử: Số nguyên tử = nngtử. N Số phân tử = nphtử. N Ví dụ 1: Tính khối lượng phân tử của chất khí biết rằng ở 250 C và 745 mm. Hg, 304 ml chất khí đó cân nặng 0, 78 g. Ví dụ 2: Tính khối lượng của khí NH 3 chứa trong bình có dung tích 12 lit ở 770 C, áp suất 2, 5 atm. Có bao nhiêu phân tử NH 3 trong khối lượng trên.
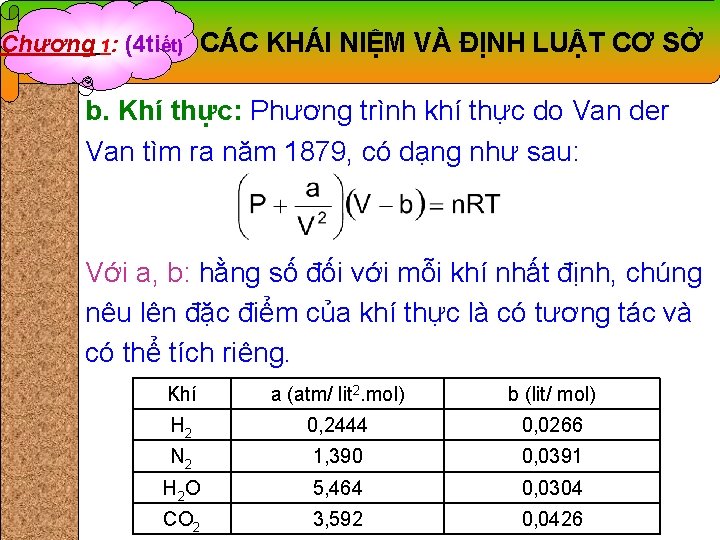
Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ b. Khí thực: Phương trình khí thực do Van der Van tìm ra năm 1879, có dạng như sau: Với a, b: hằng số đối với mỗi khí nhất định, chúng nêu lên đặc điểm của khí thực là có tương tác và có thể tích riêng. Khí a (atm/ lit 2. mol) b (lit/ mol) H 2 0, 2444 0, 0266 N 2 1, 390 0, 0391 H 2 O 5, 464 0, 0304 CO 2 3, 592 0, 0426

Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ Ví dụ: Tính áp suất của một mol khí CO 2 có thể tích 0, 5 lít ở 250 C trong hai trường hợp khí lý tưởng và khí thực. a. Xem là khí lý tưởng: b. Xem là khí thực:

Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ c. Áp suất riêng chất khí và định luật Dalton * Định nghĩa: Áp suất riêng của một chất khí trong một hỗn hợp là áp suất do chất khí đó tạo ra khi nó chiếm thể tích của toàn bộ hỗn hợp khí trong cùng một điều kiện. Pi = Ni. P Trong đó: Pi: áp suất riêng phần của cấu tử i P: áp suất tổng của hỗn hợp Ni: phần mol của cấu tử i * Định luật Dalton: Áp suất chung của hỗn hợp các chất khí không tham gia phản ứng hóa học với nhau bằng tổng áp suất riêng phần của các chất khí tạo nên hỗn hợp.
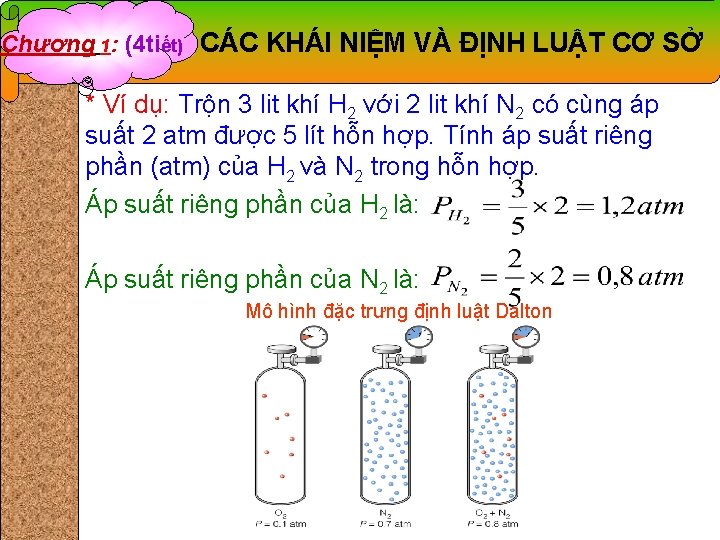
Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ * Ví dụ: Trộn 3 lit khí H 2 với 2 lit khí N 2 có cùng áp suất 2 atm được 5 lít hỗn hợp. Tính áp suất riêng phần (atm) của H 2 và N 2 trong hỗn hợp. Áp suất riêng phần của H 2 là: Áp suất riêng phần của N 2 là: Mô hình đặc trưng định luật Dalton

Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ 1. 2. 8. Xác định khối lượng phân tử và nguyên tử a. Xác định khối lượng phân tử theo tỷ khối của khí và hơi Phạm vi áp dụng: sử dụng cho các chất khí, lỏng, rắn dễ bay hơi. - Với D được gọi là tỷ khối của khí A đối với khí B. b. Xác định khối lượng phân tử từ phương trình Clapeyron – Mendeleve → Phạm vi áp dụng: chất lỏng, chất rắn dễ bay hơi.

Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ c. Xác định khối lượng phân tử chất tan bằng phương pháp nghiệm sôi - Nguyên tắc: Khi hòa tan một chất vào dung môi thì dung dịch thu được sẽ có nhiệt độ sôi cao hơn nhiệt độ sôi của dung môi và nhiệt độ đông đặc thấp hơn nhiệt độ đông đặc của dung môi. Trong đó, k: Hằng số nghiệm sôi (Ks) hoặc nghiệm đông (Kđ) tương ứng của dung môi. m: Lượng chất tan đã dùng trong 1000 g dung môi. ∆t: Độ tăng nhiệt độ sôi hay độ giảm nhiệt độ đông đặc của dung dịch. ∆t sôi = ts - 100 ; ∆t đđ= 0 - tđđ
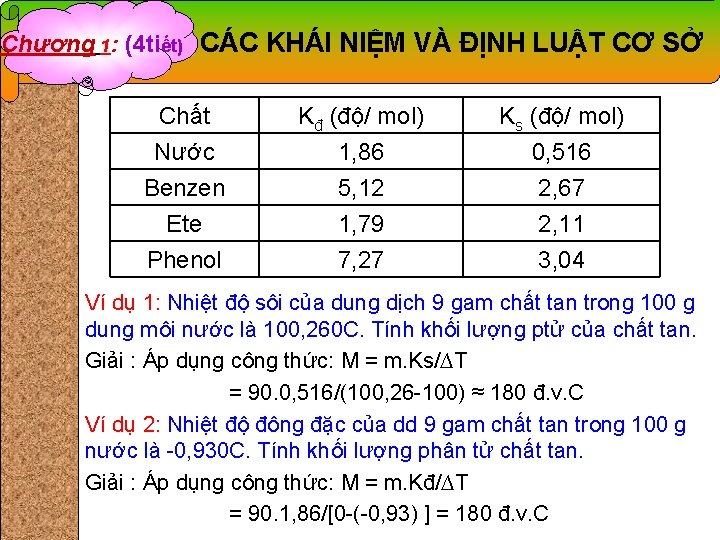
Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ Chất Nước Benzen Ete Kđ (độ/ mol) 1, 86 5, 12 1, 79 Ks (độ/ mol) 0, 516 2, 67 2, 11 Phenol 7, 27 3, 04 Ví dụ 1: Nhiệt độ sôi của dung dịch 9 gam chất tan trong 100 g dung môi nước là 100, 260 C. Tính khối lượng ptử của chất tan. Giải : Áp dụng công thức: M = m. Ks/∆T = 90. 0, 516/(100, 26 -100) ≈ 180 đ. v. C Ví dụ 2: Nhiệt độ đông đặc của dd 9 gam chất tan trong 100 g nước là -0, 930 C. Tính khối lượng phân tử chất tan. Giải : Áp dụng công thức: M = m. Kđ/∆T = 90. 1, 86/[0 -(-0, 93) ] = 180 đ. v. C

Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ d. Xđịnh klượng ptử chất tan bằng áp suất thẩm thấu Nguyên tắc: Bằng thực nghiệm người ta đo được áp suất thẩm thấu của dung dịch thu được khi hòa tan chất tan vào dung môi, từ đó tính được khối lượng phân tử của chất tan theo công thức sau: Với, m: lượng chất tan đã hòa tan vào dung môi (g) V: thể tích dung dịch thu được (l) R: hằng số khí T: nhiệt độ tuyệt đối (K) π: áp suất thẩm thấu của dung dịch (atm)

Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ Ví dụ: Trong 1 lit dung dịch chứa 0, 1 mol một chất tan không điện li ở 00 C. Tại nhiệt độ trên, tính áp suất thẩm thấu của dung dịch. Giải: Áp dụng công thức ta có: Vπ = n. RT Suy ra: π = n. RT/V = 0, 1. 0, 082. 273/1 ≈ 2, 239 atm
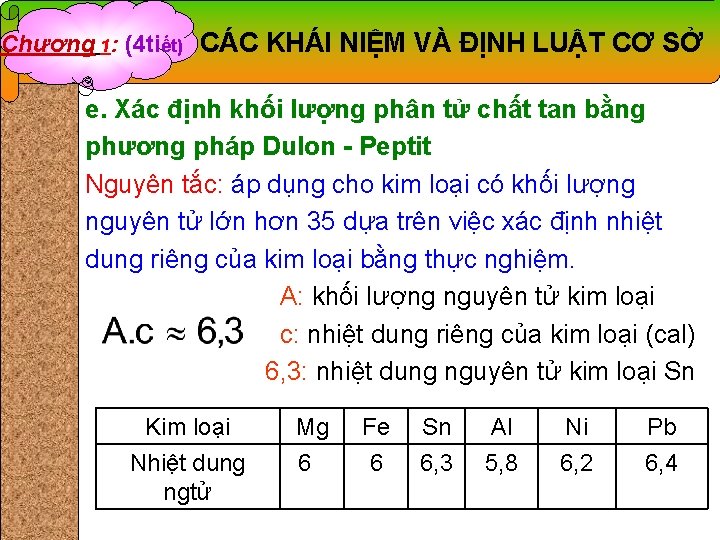
Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ e. Xác định khối lượng phân tử chất tan bằng phương pháp Dulon - Peptit Nguyên tắc: áp dụng cho kim loại có khối lượng nguyên tử lớn hơn 35 dựa trên việc xác định nhiệt dung riêng của kim loại bằng thực nghiệm. A: khối lượng nguyên tử kim loại c: nhiệt dung riêng của kim loại (cal) 6, 3: nhiệt dung nguyên tử kim loại Sn Kim loại Nhiệt dung ngtử Mg 6 Fe 6 Sn 6, 3 Al 5, 8 Ni 6, 2 Pb 6, 4

Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ Ví dụ: Xác định khối lượng nguyên tử của một kim loại có nhiệt dung riêng là 0, 093 cal/g và đương lượng là 32, 7. Giải: Khối lượng gần đúng của kim loại đó là: Hóa trị của kim loại là: Khối lượng nguyên tử chính xác của kim loại sẽ là: Acx =32, 7. 2 = 65, 4 BÀI TẬP VỀ NHÀ Trắc nghiệm: bt 1 -53 trang 297 -310 Tự luận: bt 1 -18 trang 29 -32

Chương 1: (4 tiết) CÁC KHÁI NIỆM VÀ ĐỊNH LUẬT CƠ SỞ
- Slides: 40