BI GING HA HC 11 BI 11 AXIT

BÀI GIẢNG HÓA HỌC 11 BÀI 11: AXIT PHOTPHORIC VÀ MUỐI PHOTPHAT

KIỂM TRA BÀI CŨ - Nêu tính chất hóa học của Photpho? - Viết các phương trình hóa học minh họa? - Gọi tên các chất sản phẩm?

ĐÁP ÁN Tính chất hóa học của photpho: -Tính oxi hóa: + Tác dụng với Kim loại hoạt động 0 -3 2 P + 3 Ca Ca 3 P 2 ( Canxi photphua) -Tính khử: + Tác dụng với khí Oxi 0 Thiếu O 2: 2 P + 3 O 2 0 Dư O 2: 2 P + 5 O 2 +3 2 P 2 O 3 ( điphotpho trioxit) +5 2 P 2 O 5 ( điphotpho pentaoxit)
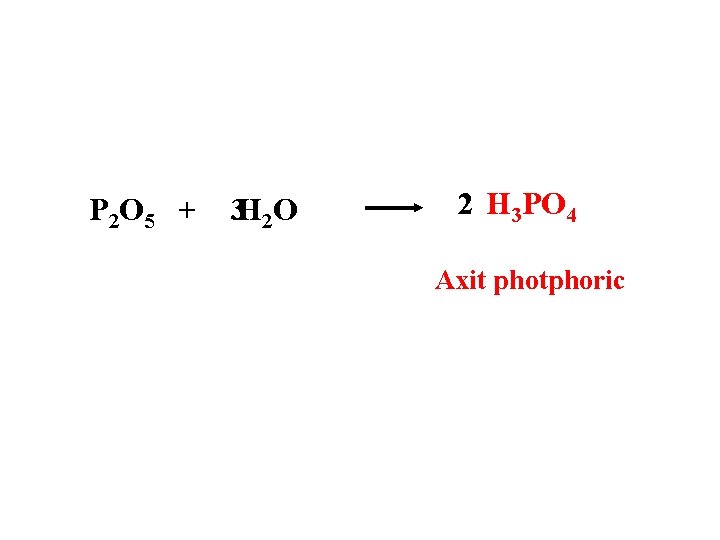
P 2 O 5 + 3 H 2 O 2 H 3 PO 4 Axit photphoric

BÀI 11: AXIT PHOTPHORIC VÀ MUỐI PHOTPHAT A. AXIT PHOTPHORIC I. CẤU TẠO PH N TỬ II. TÍNH CHẤT VẬT LÍ III. TÍNH CHẤT HÓA HỌC IV. ĐIỀU CHẾ V. ỨNG DỤNG B. MUỐI PHOTPHAT I. TÍNH TAN II. NHẬN BIẾT ION PHOTPHAT

BÀI 11: AXIT PHOTPHORIC VÀ MUỐI PHOTPHAT A. AXIT PHOTPHORIC I. CẤU TẠO PH N TỬ - Công thức phân tử: H 3 PO 4 : H : O : - Công thức electron: : - Công thức cấu tạo: H–O +5 H–O–P=O H–O : : H : O: P : : O: : H : O :

BÀI 11: AXIT PHOTPHORIC VÀ MUỐI PHOTPHAT A. AXIT PHOTPHORIC II. TÍNH CHẤT VẬT LÍ Axit photphoric: -Trạng thái: Tinh thể - Màu sắc: Trong suốt Mẫu axit photphoric - Tính tan trong nước: Tan trong nước theo bất kì tỉ lệ nào. - Nhiệt độ nóng chảy: 42, 5 0 C axit photphoric đặc

BÀI 11: AXIT PHOTPHORIC VÀ MUỐI PHOTPHAT A. AXIT PHOTPHORIC III. TÍNH CHẤT HÓA HỌC 1. Trong dung dịch nước, H 3 PO 4 phân li: 3 nấc Nấc 1: H 3 PO 4 H+ + H 2 PO 4 - (ion đihiđrophotphat) Nấc 2: H 2 PO 4 - H+ + HPO 42 – (ion hiđrophotphat) Nấc 3: HPO 4 2 - H+ + PO 43 – (ion photphat) Axit photphoric là axit: 3 nấc có độ mạnh trung bình. Trong dung dịch axit photphoric gồm: H+, H 2 PO 4 -, HPO 42 - , PO 43 – và H 3 PO 4 không phân li. . . . . . .
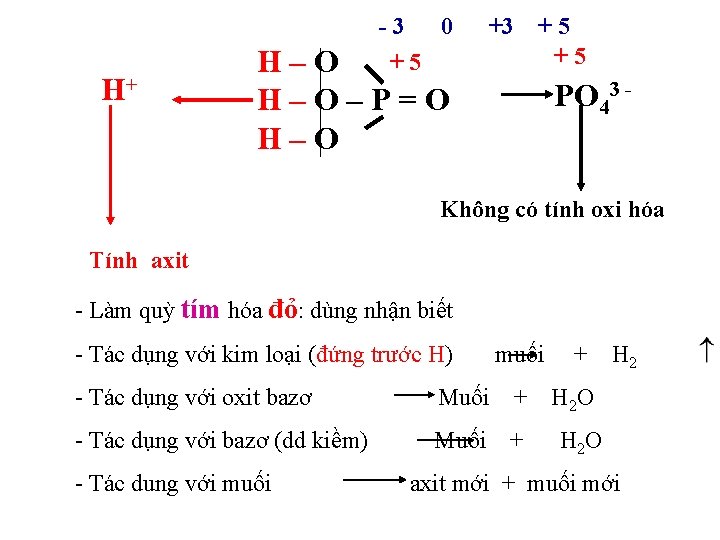
H+ -3 0 +5 +3 H–O–P=O H–O +5 +5 PO 43 - Không có tính oxi hóa Tính axit - Làm quỳ tím hóa đỏ: dùng nhận biết - Tác dụng với kim loại (đứng trước H) muối - Tác dụng với oxit bazơ Muối + - Tác dụng với bazơ (dd kiềm) Muối - Tác dung với muối + + H 2 O axit mới + muối mới

BÀI 11: AXIT PHOTPHORIC VÀ MUỐI PHOTPHAT III. TÍNH CHẤT HÓA HỌC 1. Trong dung dịch nước, H 3 PO 4 phân li: 3 nấc 2. Tính axit a. Làm quỳ tím hóa đỏ: dùng nhận biết b. Tác dụng với kim loại (đứng trước H) muối c. Tác dụng với oxit bazơ Muối + d. Tác dụng với bazơ (dd kiềm) Muối + e. Tác dụng với muối + H 2 O axit mới + muối mới
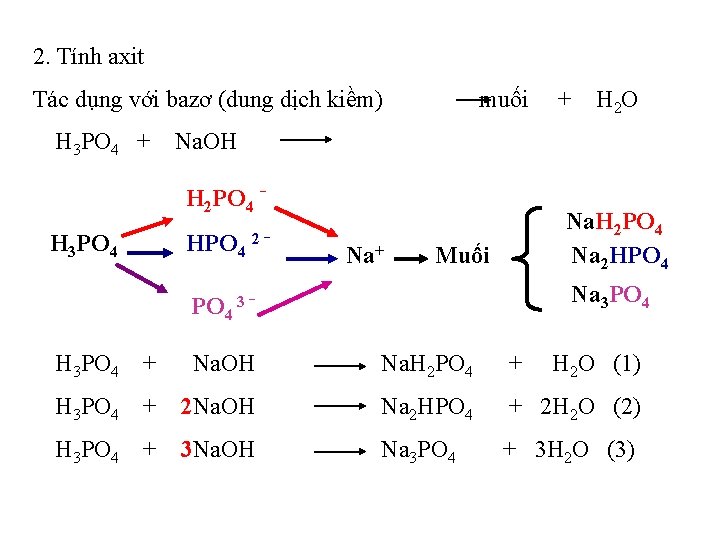
2. Tính axit Tác dụng với bazơ (dung dịch kiềm) H 3 PO 4 + muối H 2 O Na. OH H 2 PO 4 - H 3 PO 4 + HPO 4 2 - Na+ Na. H 2 PO 4 Na 2 HPO 4 Muối Na 3 PO 4 3 H 3 PO 4 + Na. OH Na. H 2 PO 4 + H 2 O (1) H 3 PO 4 + 2 Na. OH Na 2 HPO 4 + 2 H 2 O (2) H 3 PO 4 + 3 Na. OH Na 3 PO 4 + 3 H 2 O (3)
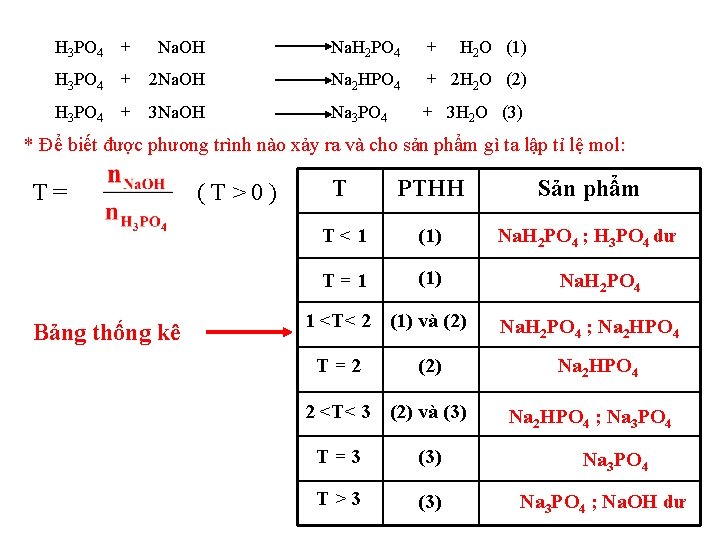
H 3 PO 4 + Na. OH Na. H 2 PO 4 + H 2 O (1) H 3 PO 4 + 2 Na. OH Na 2 HPO 4 + 2 H 2 O (2) H 3 PO 4 + 3 Na. OH Na 3 PO 4 + 3 H 2 O (3) * Để biết được phương trình nào xảy ra và cho sản phẩm gì ta lập tỉ lệ mol: T= Bảng thống kê (T>0) T PTHH Sản phẩm T<1 (1) Na. H 2 PO 4 ; H 3 PO 4 dư T=1 (1) 1 <T< 2 (1) và (2) T=2 (2) 2 <T< 3 (2) và (3) T=3 (3) T>3 (3) Na. H 2 PO 4 ; Na 2 HPO 4 ; Na 3 PO 4 ; Na. OH dư
Ví dụ 1: Cho 0, 1 mol dd H 3 PO 4 tác dụng hoàn toàn với 0, 1 mol dd Na. OH. Muối tạo thành là: A. Na. H 2 PO 4 B. Na 2 HPO 4 C. Na 3 PO 4 D. Na 2 HPO 4 và Na 3 PO 4 Ví dụ 2: Cho 0, 2 mol dd H 3 PO 4 tác dụng hoàn toàn với 0, 3 mol dd Na. OH. Muối tạo thành là: A. Na. H 2 PO 4 B. Na 2 HPO 4 C. Na. H 2 PO 4 và Na 2 HPO 4 D. Na 2 HPO 4 và Na 3 PO 4

BÀI 11: AXIT PHOTPHORIC VÀ MUỐI PHOTPHAT III. TÍNH CHẤT HÓA HỌC Chú ý: H 3 PO 4 không có tính oxi hóa.

BÀI 11: AXIT PHOTPHORIC VÀ MUỐI PHOTPHAT A. AXIT PHOTPHORIC IV. ĐIỀU CHẾ: H 3 PO 4 1. Trong phòng thí nghiệm: +5 5 HNO 3 đặc 0 + +5 H 3 PO 4 P +4 5 NO 2 + H 2 O + 1 5 2. Trong công nghiệp: Phương pháp 1: Phương pháp 2: Ca 3(PO 4)2 + 3 H 2 SO 4 đặc 4 P + 5 O 2 P 2 O 5 + 3 H 2 O 2 H 3 PO 4 + 3 Ca. SO 4 2 P 2 O 5 2 H 3 PO 4

BÀI 11: AXIT PHOTPHORIC VÀ MUỐI PHOTPHAT A. AXIT PHOTPHORIC V. ỨNG DỤNG: Phân Lân H 3 PO 4 Thuốc trừ sâu Dược phẩm

BÀI 11: AXIT PHOTPHORIC VÀ MUỐI PHOTPHAT A. AXIT PHOTPHORIC B. MUỐI PHOTPHAT - Muối photphat là muối của axit - Phân loại: Na. H 2 PO 4 photphoric 3 loại ; Muối đihiđrophotphat Na 2 HPO 4 ; Muối hiđrophotphat Na 3 PO 4 Muối photphat
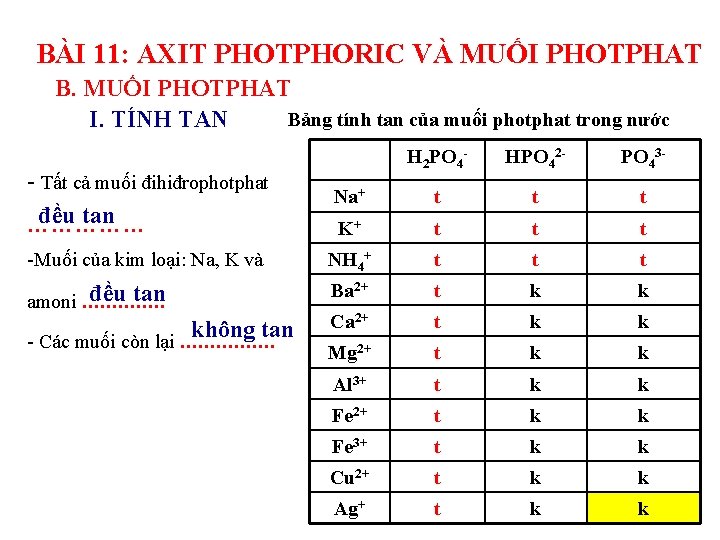
BÀI 11: AXIT PHOTPHORIC VÀ MUỐI PHOTPHAT Bảng tính tan của muối photphat trong nước I. TÍNH TAN H 2 PO 4 - HPO 42 - PO 43 - - Tất cả muối đihiđrophotphat đều tan …………… Na+ t t t K+ t t t -Muối của kim loại: Na, K và NH 4+ t t t đều tan amoni. . . Ba 2+ t k k Ca 2+ t k k Mg 2+ t k k Al 3+ t k k Fe 2+ t k k Fe 3+ t k k Cu 2+ t k k Ag+ t k k không tan - Các muối còn lại. . . .
BÀI 11: AXIT PHOTPHORIC VÀ MUỐI PHOTPHAT B. MUỐI PHOTPHAT II. NHẬN BIẾT ION PHOTPHAT: PO 4 3 - dd Ag. NO 3 - Thuốc thử để nhận biết ion PO 43 – trong dd muối photphat là: . . . . - Hiện tượng: Xuất hiện kết tủa màu vàng ( Ag 3 PO 4 ) 3 Ag. NO 3 + Na 3 PO 4 Ag 3 PO 4 + ( màu vàng ) - PT ion rút gọn: 3 Ag+ + PO 43 - Ag 3 PO 4 3 Na. NO 3
BÀI TẬP Câu 1. H 3 PO 4 không tác dụng được với kim loại nào sau đây? A. Mg, Al B. Zn, Fe C. Al, Fe D. Cu, Ag Câu 2. Cho 0, 2 mol dd H 3 PO 4 tác dụng hoàn toàn với 200 ml dd Na. OH 2 M. Muối tạo thành là: A. Na. H 2 PO 4 B. Na 2 HPO 4 C. Na 3 PO 4 D. Na. H 2 PO 4 và Na 2 HPO 4
BÀI TẬP Câu 3. Cho 100 ml dd H 3 PO 4 2 M tác dụng hoàn toàn với 0, 5 mol dd Na. OH. Muối tạo thành là: A. Na 2 HPO 4 B. C. D. Na 2 HPO 4 và Na 3 PO 4 Na. H 2 PO 4 và Na 2 HPO 4 Câu 4. Cho 3 dd không màu chứa trong từng lọ mất nhãn gồm: Na. NO 3, Na. Cl, Na 3 PO 4. Thuốc thử dùng nhận biết 3 dd trên là: A. Ba. Cl 2 B. Ag. NO 3 C. Ba(OH)2 D. Na. OH

KÍNH CHÀO QUÝ THẦY CÔ CHÚC CÁC EM HỌC TỐT!
- Slides: 22