BI GING HA HC 11 ANKAN HIDROCACBON NO

BÀI GIẢNG HÓA HỌC 11 ANKAN HIDROCACBON NO ANKAN 1

• Giới thiệu chung • Hiđrocacbon no là hiđrocacbon mà trong phân tử các nguyên tử liên kết với nhau chỉ bằng liên kết đơn (liên kết ). • Hiđrocacbon no được chia làm 2 loại: Hiđrocacbon no mạch hở gọi là ankan, công thức chung Cn. H 2 n+2 (n 1) VD : CH 4 , C 2 H 6 ……. • Hiđrocacbon no rất phổ biến trong tự nhiên. Metan có trong khí quyển, trong khí thiên nhiên, khí dầu mỏ. Các ankan từ C 1 – C 10 là thành phần chính của dầu mỏ. Trong thực vật cũng gặp các hiđrocacbon no C 10–C 37. Hiđrocacbon no là nhiên liệu và nguyên liệu quan trọng của nhân loại. HIDROCACBON NO ANKAN 2
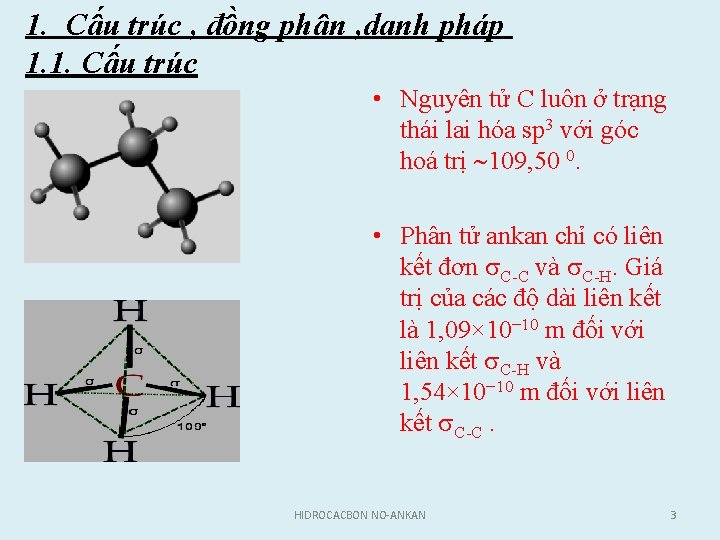
1. Cấu trúc , đồng phân , danh pháp 1. 1. Cấu trúc • Nguyên tử C luôn ở trạng thái lai hóa sp 3 với góc hoá trị 109, 50 0. • Phân tử ankan chỉ có liên kết đơn C C và C H. Giá trị của các độ dài liên kê t là 1, 09× 10− 10 m đối với liên kết C H và 1, 54× 10− 10 m đối với liên kết C C. HIDROCACBON NO-ANKAN 3
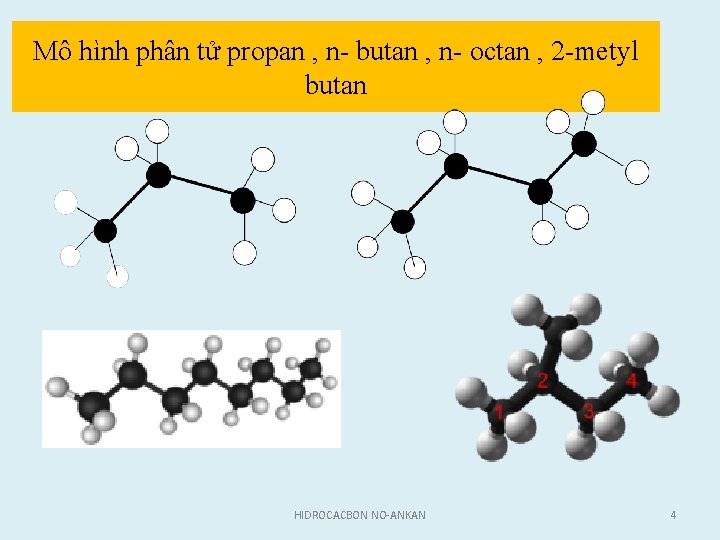
Mô hình phân tử propan , n butan , n octan , 2 metyl butan HIDROCACBON NO-ANKAN 4
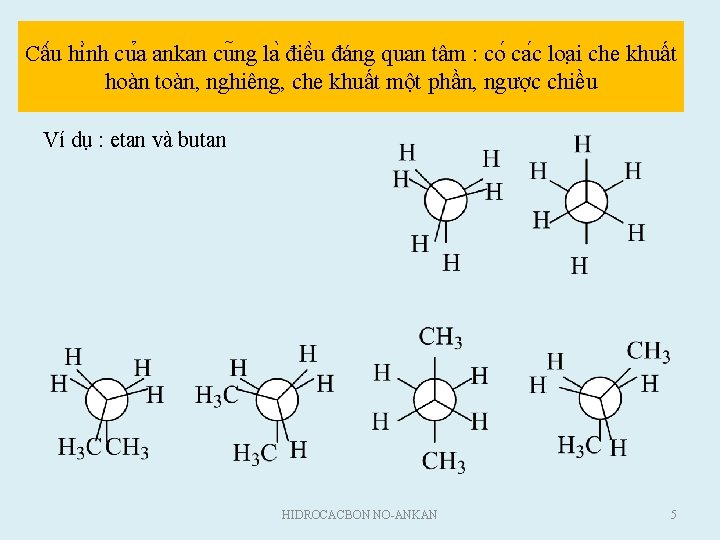
Câ u hi nh cu a ankan cu ng la điê u đáng quan tâm : co ca c loa i che khuất hoàn toàn, nghiêng, che khuất một phần, ngược chiều Ví dụ : etan và butan HIDROCACBON NO ANKAN 5
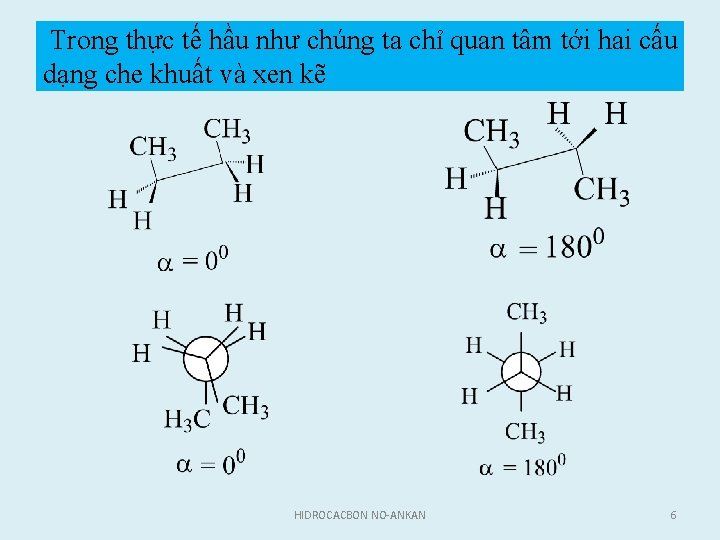
Trong thực tế hầu như chúng ta chỉ quan tâm tới hai cấu dạng che khuất và xen kẽ HIDROCACBON NO-ANKAN 6

1. 2. Đồng phân a. Đồng phân cấu trúc Đó là các đồng phân mạch cacbon , dạng mạch thẳng nhánh từ propan trở đi mới có đồng phân cấu trúc b. Đồng phân cấu dạng: Nguyên nhân hình thành là do khả năng quay xung quanh liên kết c c. Do khả năng quay xung quanh lk C C với các góc khác nhau nên tạo ra vô số các đồng phân , song người ta chỉ chú ý tới 2 cấu dạng : đồng phân che khuất ( có năng lượng cao )và đồng phân xen kẽ ( có năng lượng thấp nhất ). HIDROCACBON NO-ANKAN 7

1. 3. Danh pháp được sử dụng rộng rãi nhất là danh pháp quy định bởi IUPAC (International Union of Pure and Applied Chemistry). • a. Đối với các ankan mạch thẳng : phân tử chỉ có cacbon bậc I và bậc II có công thức chung là CH 3(CH 2)n. CH 3 được gọi là n ankan (n: normal) hoặc ankan mạch thẳng. Đầu tố “n” nếu n>3 + tên gốc HIDROCACBON NO-ANKAN + hậu tố “an” 8
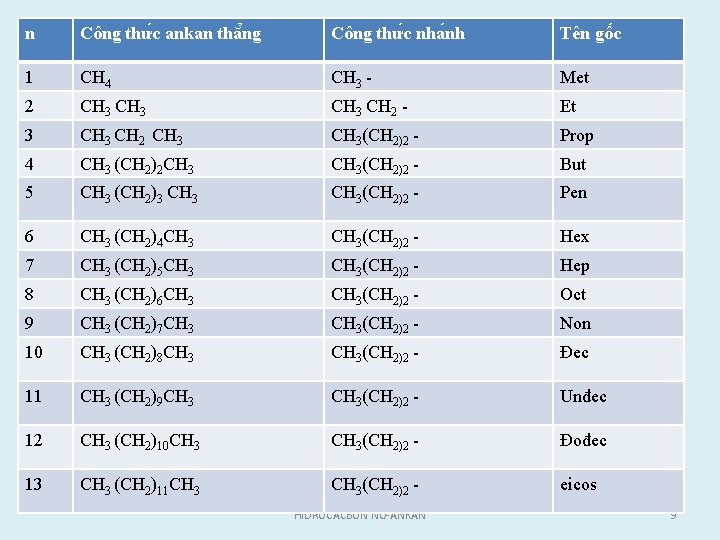
n Công thư c ankan thă ng Công thư c nha nh Tên gô c 1 CH 4 CH 3 Met 2 CH 3 CH 2 Et 3 CH 2 CH 3(CH 2)2 Prop 4 CH 3 (CH 2)2 CH 3(CH 2)2 But 5 CH 3 (CH 2)3 CH 3(CH 2)2 Pen 6 CH 3 (CH 2)4 CH 3(CH 2)2 Hex 7 CH 3 (CH 2)5 CH 3(CH 2)2 Hep 8 CH 3 (CH 2)6 CH 3(CH 2)2 Oct 9 CH 3 (CH 2)7 CH 3(CH 2)2 Non 10 CH 3 (CH 2)8 CH 3(CH 2)2 Đec 11 CH 3 (CH 2)9 CH 3(CH 2)2 Unđec 12 CH 3 (CH 2)10 CH 3(CH 2)2 Đođec 13 CH 3 (CH 2)11 CH 3(CH 2)2 eicos HIDROCACBON NO-ANKAN 9

b. Đối với các ankan phân nhánh : theo danh pháp IUPAC + Mạch cacbon dài nhất và có nhiều nhánh nhất là mạch chính. + Đánh số các nguyên tử C ở mạch chính, sao chỉ số vị trí của nhánh là nhỏ nhất. + Coi mạch chính tương ứng với ankan không phân nhánh có cùng số nguyên tử C. + Đặt chỉ số trước tên nhánh, lần lượt gọi tên nhánh theo thứ tự bảng chữ cái, cuối cùng là tên ankan tương ứng với mạch chính, các nhóm có cùng tên dùng thêm các tiền tố như đi (hai), tri (ba), tetra (bốn), peta (năm)…. + Dùng dấu gạch ngang để nối các chỉ số với tên nhánh, dùng dấu phẩy để phân tách hai chỉ số cạnh nhau. HIDROCACBON NO-ANKAN 10

Sơ đồ tóm tắt tên của 1 ankan mạch nhánh bất kì Sô thư tư nha nh Sô nha nh cu ng loa i Tên nha nh Hâ u tô “yl” Tên ma ch (tên gô c) chi nh (tên gốc) + “an” • Tên gọi của các nhóm ankyl phân nhánh được quy định như sau • Sec : gốc ở vị trí C bậc 2 Ter : gốc ở vị trí C bậc 3 Neo : 3 nhóm metyl ở đầu mạch Iso : 2 nhóm metyl ở đầu mạch HIDROCACBON NO-ANKAN 11
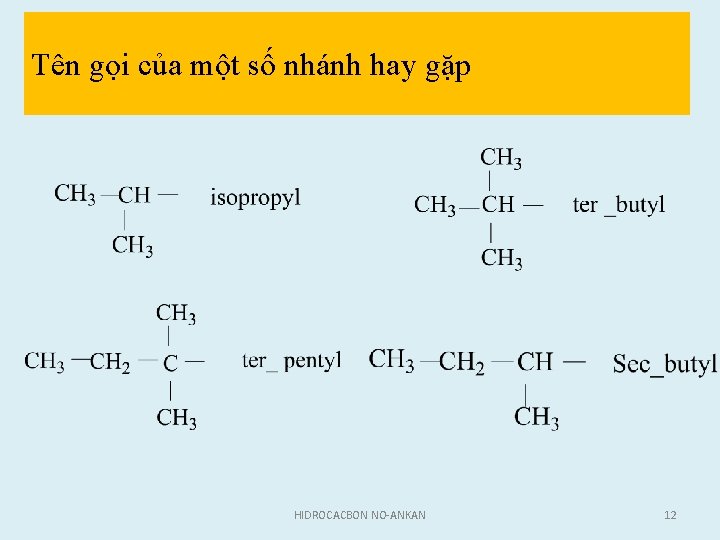
Tên gọi của một số nhánh hay gặp HIDROCACBON NO-ANKAN 12
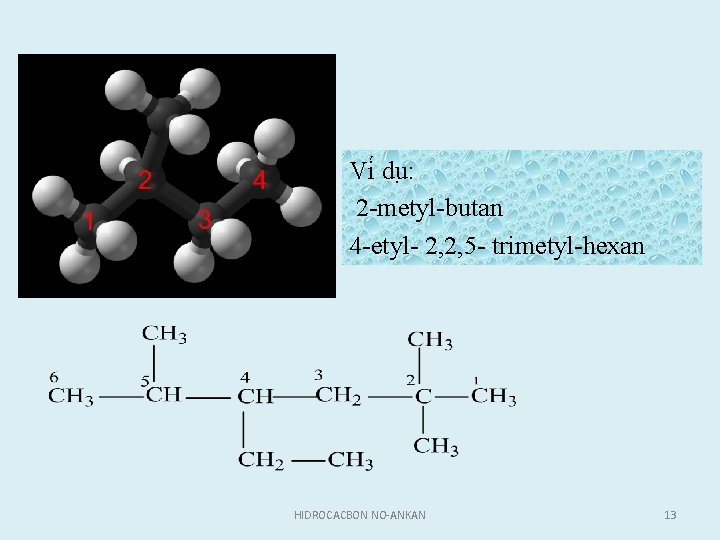
Vi du : 2 metyl butan 4 etyl 2, 2, 5 trimetyl hexan HIDROCACBON NO-ANKAN 13

Chúng ta thử gọi tên chất sau nhé !!! • 3, 3 dimetyl 6 etyl 5 propyl nonan HIDROCACBON NO-ANKAN 14

2. Tính chất vật lý • Nhiệt độ sôi, nhiệt độ nóng chảy của các ankan phụ thuộc vào lực hút Van de Van, hình dạng và kích thước phân tử. Trong cùng dãy đồng đẳng, thông thường nhiệt độ sôi và tỉ khối của các n ankan trong dãy tăng dần. • Dạng tồn tại Từ C 1 →C 4 : Khí Từ C 5 →C 16 : Lỏng Từ C 17 trở lên : Rắn Theo nghiên cứu cụ thể thì trung bình cứ tăng 1 nhóm CH 2 thì nhiệt độ sôi tăng từ 20 30 độ C. Mạch Cacbon càng phân nhánh thì diện tích tiếp xúc giữa các phân tử càng giảm , nhiệt độ nóng chảy tăng nhưng nhiệt độ sôi giảm ứng ( trừ trường hợp sự phân nhánh làm tăng tính đối xứng phân tử thì điểm nóng chảy lại tăng lên ). HIDROCACBON NO-ANKAN 15
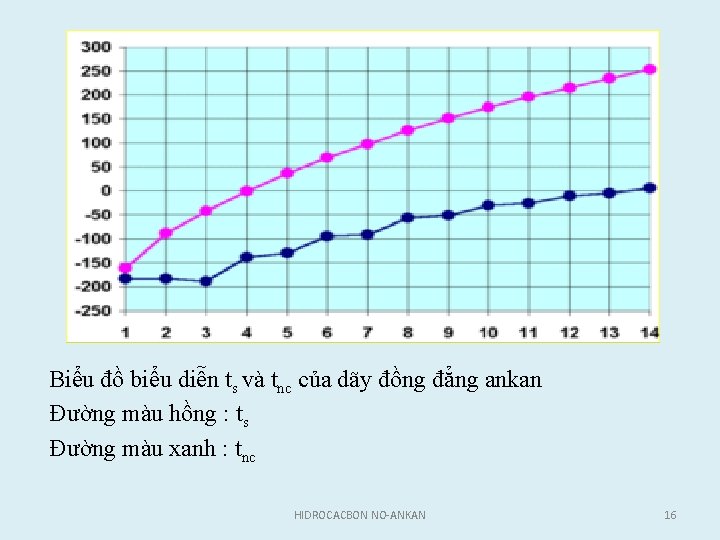
Biểu đồ biểu diễn ts và tnc của dãy đồng đẳng ankan Đường màu hồng : ts Đường màu xanh : tnc HIDROCACBON NO-ANKAN 16

Các ankan giống nhau về tính tan, chúng ko tan trong nước ( vì chúng chỉ có liên kết nên hầu như không phân cực ) , chúng tan tốt trong các dung môi không phân cực , và đa số các dung môi hữu cơ => được gọi là ưa mỡ. Tỷ trọng của các ankan thông thường tăng theo chiều tăng của số nguyên tử cacbon, nhưng vẫn thấp hơn tỷ trọng của nước. Vì thế, các ankan tạo thành lớp trên trong hỗn hợp ankan nước HIDROCACBON NO-ANKAN 17

Phổ của ankan Ankan chi hâ p thu đươ c như ng bươ c so ng ngă n hơn 200 nm • Phổ hồng ngoại • Phổ cộng hưởng từ hạt nhân • Phổ khối lượng: có thể xác định nhanh chóng các ankan trong hỗn hợp nhiều thành phần , phân biệt đồng phân mạch nhánh và thẳng. Phương pháp này hay dùng trong việc nhận biết thành phần dầu mỏ ankan có số khối 43, 57, 71, 85, 99, 113 naphten có dãy vạch 41, 55, 69, 83, 97, 111 ankylbenzen có các vạch 77, 91, 105, 119 HIDROCACBON NO-ANKAN 18

3. Tính chất hóa học • Phân tử ankan chỉ gồm 2 loại liên kết C C và C H là loại liên kết hầu như không phân cực, vì vậy thông thường chúng không có khuynh hướng phân cắt theo cách dị li. Và đương nhiên phân tử ankan chỉ gồm hai loại phản ứng đó là phân cắt liên kết C C và C H • Trong điều kiện có xúc tác và nhiệt độ cao, ankan tham gia nhiều phản ứng như phản ứng thế, phản ứng tách, phản ứng đồng phân hoá và phản ứng oxi hoá…Phản ứng của ankan xảy ra chủ yếu theo con đường phân cắt đồng li, nghĩa là hình thành các gốc tự do. • Chính vì vậy, trong các phản ứng của ankan chất phản ứng có thể tấn công vào liên kết C–H hoặc liên kết C–C theo cơ chế gốc và tạo thành một hỗn hợp các chất đồng phân, đồng đẳng, . . . HIDROCACBON NO-ANKAN 19

3. 1. Phản ứng thế 3. 1. 1. Phản ứng halogen hóa ( theo cơ chế gốc ) Chuỗi cơ chế phản ứng như sau ( xét R CH 3 và Cl 2 ) • 1. Khởi đầu : Chia cắt phân tử clo bằng bức xạ cực tím. Nguyên tử clo có điện tử không bắt cặp và phản ứng như là một gốc tự do. • Cl 2 → 2 Cl* • 2. Lan truyền (2 bước): Nguyên tử hiđrô bị lôi ra khỏi R sau đó gốc mêtyl kéo Cl* từ Cl 2. R CH 3 + Cl* → R – CH 2* + HCl R CH 3* + Cl → R – CH 2 Cl + Cl* • Nếu có đủ Cl 2, các sản phẩm khác chẳng hạn như CH 2 Cl 2 có thể tạo ra. HIDROCACBON NO-ANKAN 20

3. Kết thúc: Tái tổ hợp của hai gốc tự do: • • • Cl* + Cl* → Cl 2 R CH 3* + Cl* → R CH 3 Cl R CH 3* + R CH 3* → R CH 3 – CH 3 R • Cơ chế phản ứng ở trên gọi là cơ chế phản ứng dây chuyền SR , và các ankan khác cũng tuân theo cơ chế trên HIDROCACBON NO-ANKAN 21
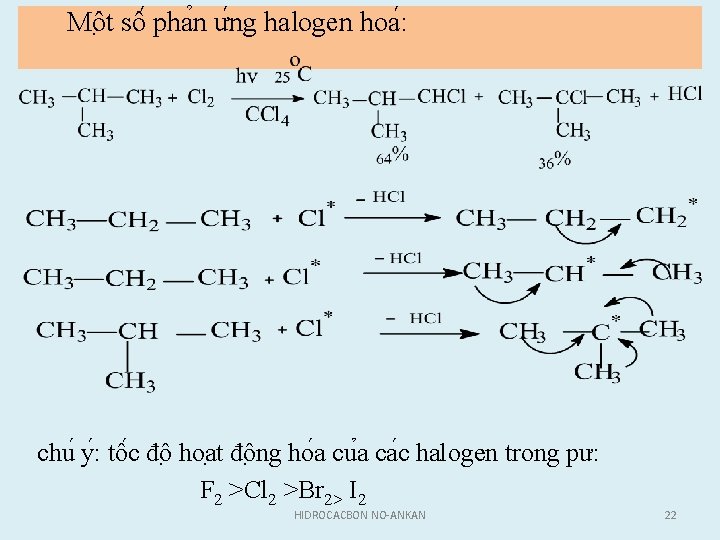
Mô t sô pha n ư ng halogen hoa : chu y : tô c đô hoa t đô ng ho a cu a ca c halogen trong pư: F 2 >Cl 2 >Br 2> I 2 HIDROCACBON NO-ANKAN 22
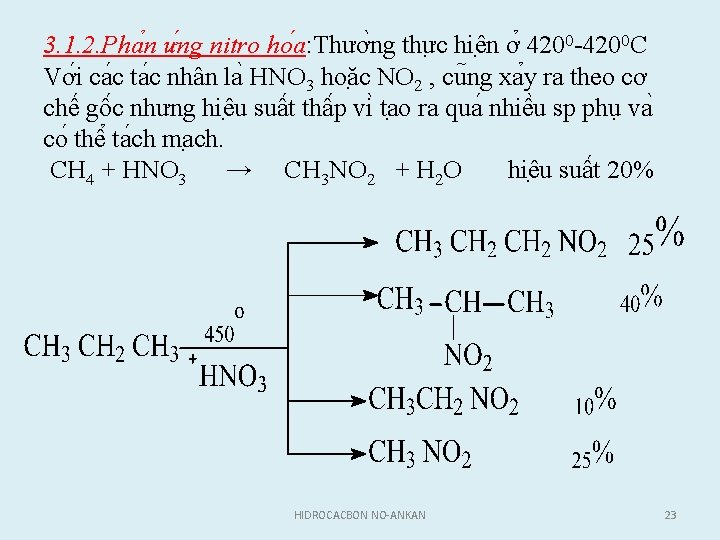
3. 1. 2. Pha n ư ng nitro ho a: Thươ ng thư c hiê n ơ 4200 C Vơ i ca c ta c nhân la HNO 3 hoă c NO 2 , cu ng xa y ra theo cơ chê gô c nhưng hiê u suâ t thâ p vi ta o ra qua nhiê u sp phụ va co thê ta ch ma ch. CH 4 + HNO 3 → CH 3 NO 2 + H 2 O hiê u suâ t 20% HIDROCACBON NO-ANKAN 23
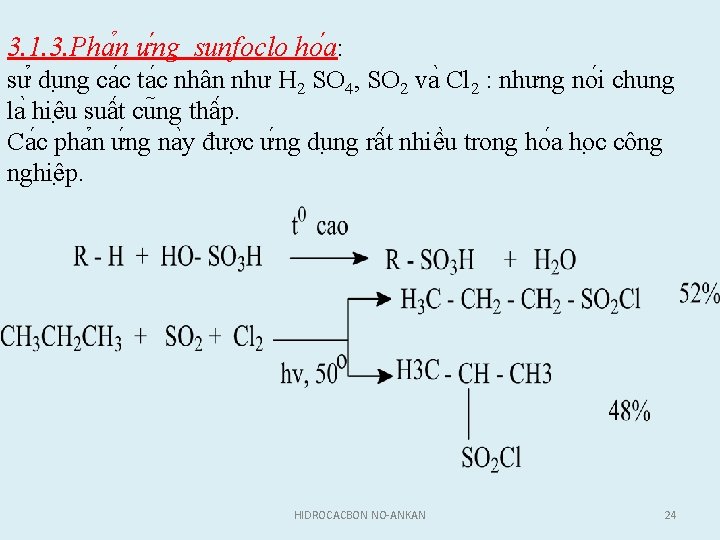
3. 1. 3. Pha n ư ng sunfoclo ho a: sư du ng ca c ta c nhân như H 2 SO 4, SO 2 va Cl 2 : nhưng no i chung la hiê u suâ t cu ng thâ p. Ca c pha n ư ng na y đươ c ư ng du ng râ t nhiê u trong ho a ho c công nghiê p. HIDROCACBON NO-ANKAN 24
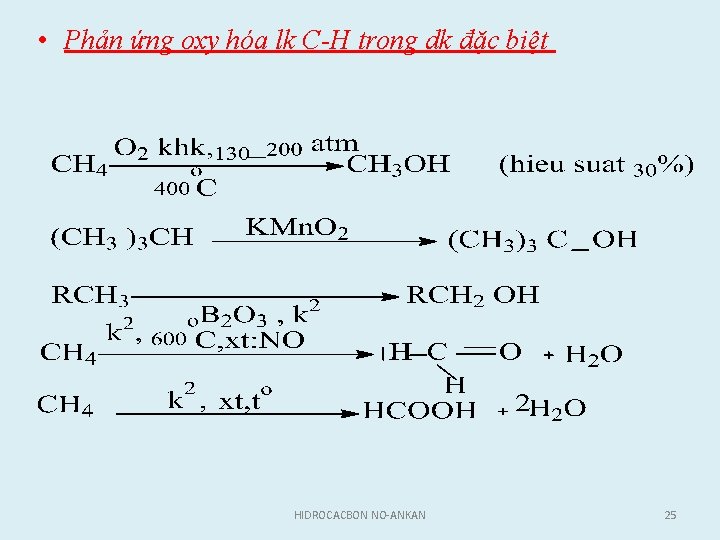
• Phản ứng oxy hóa lk C-H trong dk đặc biệt HIDROCACBON NO-ANKAN 25

3. 2. Pha n ư ng đư t ma ch cacbon v a. Pha n ư ng cha y: Khi bi O 2 dư tâ n công ơ to ca c ankan đê u bi cha y ta o tha nh CO 2 va H 2 O. CH 4 + 2 O 2 → CO 2 + H 2 O ( t 0 cao ) CH 3 –CH 3 + 7 O 2 → 2 CO 2 + 3 H 2 O ( t 0 cao ) v b. Pha n ư ng oxi ho a că t ma ch cacbon: ca c ankan ma ch da i tư 20 30 C thươ ng bi ôxi ho a tha nh hidropeoxit rô i tha nh xeton sau đo ra axit cacboxylic: HIDROCACBON NO-ANKAN 26
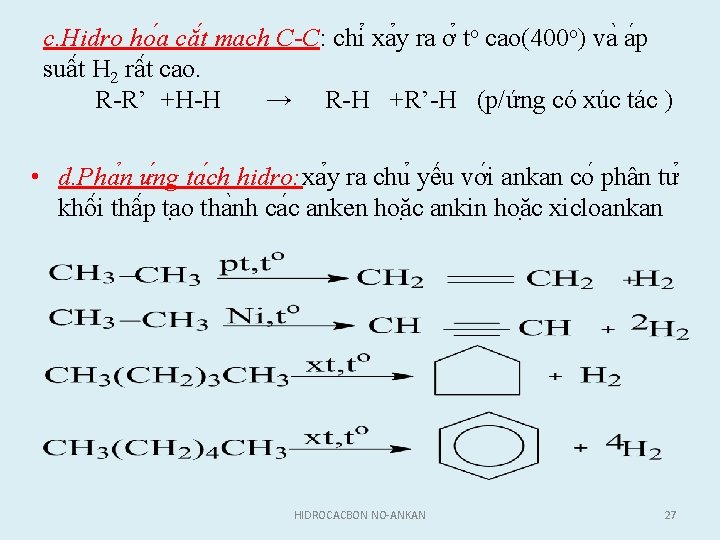
c. Hidro ho a că t ma ch C-C: chi xa y ra ơ to cao(400 o) va a p suâ t H 2 râ t cao. R R’ +H H → R H +R’ H (p/ứng có xúc tác ) • d. Pha n ư ng ta ch hidro: xa y ra chu yê u vơ i ankan co phân tư khô i thâ p ta o tha nh ca c anken hoă c ankin hoă c xicloankan HIDROCACBON NO-ANKAN 27

c. Cracking nhiê t : Khi đun no ng trên 500 o C ca c liên kê t C C tư đư t nhau ra ta o tha nh ca c ankan va ca c anken, tha nh phâ n sa n phâ m phu thuô c va o nhiê t đô va thơ i gian pư. HIDROCACBON NO-ANKAN 28

f. Pha n ư ng đô ng phân ho a: Khi đô t ca c ankan trong nhiê t đô 500 700 o C va mô t sô xu c ta c thi ankan co thê bi đư t ma ch C C nhưng sau đo la i gă n kê t la i vơ i nhau nhưng không theo tri nh tư ban đâ u ta o ca c ankan ma ch nha nh đô ng phân vơ i no. HIDROCACBON NO-ANKAN 29

4. Sản xuất , điều chế • 1. 1. Nguồn gốc tự nhiên • 1. 2. Phương pháp tổng hợp không thay đổi mạch cacbon chất ban đầu • 1. 3. Phương pháp giảm mạch cacbon chất ban đầu • 1. 4. Phương pháp tổng hợp tăng mạch cacbon • 1. 5. Phương pháp tổng hợp metan HIDROCACBON NO-ANKAN 30

4. 1. Nguồn tự nhiên • Ankan là nguyên liệu tự nhiên có từ dầu mỏ , khí thiên nhiên. • Khí thiên nhiên chứa các khí với thành phần không cố định, thường chứa 75% metan, 15% etan, 5% propan, phần còn lại là các ankan cao hơn và nhiều chất khác. Khí thiên nhiên được dùng làm nhiên liệu và trong các quá trình kỹ nghệ HIDROCACBON NO-ANKAN 31
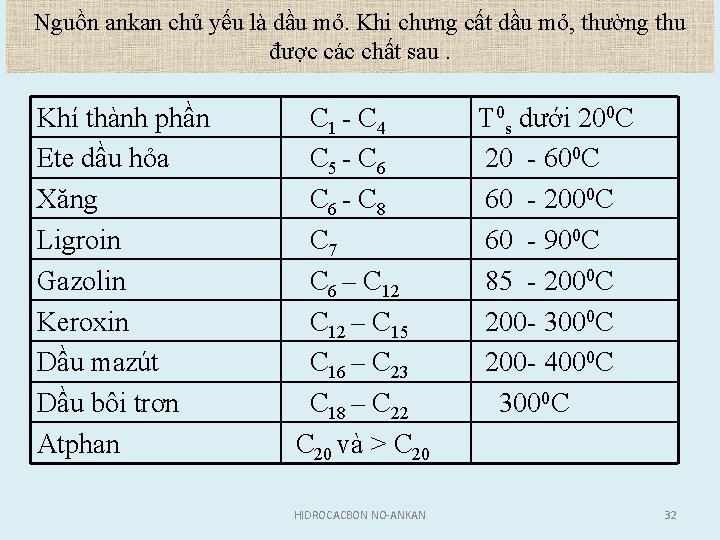
Nguồn ankan chủ yếu là dầu mỏ. Khi chưng cất dầu mỏ, thường thu được các chất sau. Khí thành phần Ete dầu hỏa Xăng Ligroin Gazolin Keroxin Dầu mazút Dầu bôi trơn Atphan C 1 C 4 C 5 C 6 C 8 C 7 C 6 – C 12 – C 15 C 16 – C 23 C 18 – C 22 C 20 và > C 20 HIDROCACBON NO-ANKAN T 0 s dưới 200 C 20 600 C 60 2000 C 60 900 C 85 2000 C 200 3000 C 200 4000 C 32

• Metan và ankan thấp phân tử có thể thu được từ than đá qua các chuyển hóa học nhưng phương pháp chưa hoàn chỉnh • Người ta đã dùng phương pháp hidro hóa than nâu : khi nghiền nhỏ than với dầu nặng , có xúc tác của Fe và H 2ở nhiệt độ cao từ 450 – 5000 C, áp suất 200 – 300 atm, thu được sản phẩm thô. Sau khi chưng cất thu được khí , xăng và sản phẩm dầu nặng. HIDROCACBON NO-ANKAN 33

Chúng ta cũng đã tổng hợp ankan từ oxit cacbon: Cho hỗn hợp CO, H 2 đi qua xúc tác Fe ở nhiệt độ 2000 C và áp suất cao, thu được hỗn hợp ankan gọi là xitin, bao gồm chủ yếu là parafin mạch thẳng và một ít ankan mạch nhánh. HIDROCACBON NO-ANKAN 34
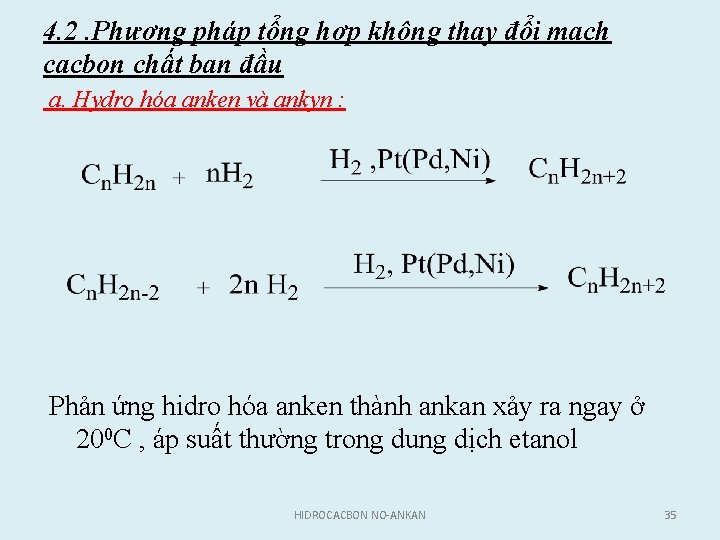
4. 2. Phương pháp tổng hợp không thay đổi mạch cacbon chất ban đầu a. Hydro hóa anken và ankyn : Phản ứng hidro hóa anken thành ankan xảy ra ngay ở 200 C , áp suất thường trong dung dịch etanol HIDROCACBON NO-ANKAN 35

b. Phản ứng khử dẫn xuất halogen chất khử hóa hay dùng là Zn/HCl , hỗn hống Mg trong nước , Li. Al. H 4 , HI c. Thủy phân hợp chất cơ kim : có thể khử hoá gián tiếp một ankyl halogenua bằng cách cho nó tác dụng với kim loại Mg rồi thuỷ phân hợp chất cơ kim trong dung môi ete khan (CH 3 CH 2)2 O để thu lấy ankan: HIDROCACBON NO-ANKAN 36

d. Khử hóa dẫn xuất axit Phản ứng này hay dùng cho điều chế các ankan có mạch lớn. HIDROCACBON NO-ANKAN 37

4. 3. Phản ứng giảm mạch cabon chất ban đầu • Nung muối axit béo với Na. OH hay vôi tôi xút, thu được ankan mới kém một C so với ankan đầu HIDROCACBON NO-ANKAN 38

4. 4. Phản ứng tổng hợp tăng mạch C a. Phản ứng Vuyec : Chú ý trong phản ứng này Hiệu suất phản ứng cao nhất khi 2 gốc C đem ghép giống nhau Nếu dùng 2 dẫn xuất khác nhau thì sẽ thu hỗn hợp các sản phẩm Phản ứng diễn ra trong dung môi hidrocabon chứ ko dùng ete b. Phản ứng điện phân dung dịch muối axit ( phản ứng Kolbe) HIDROCACBON NO-ANKAN 39
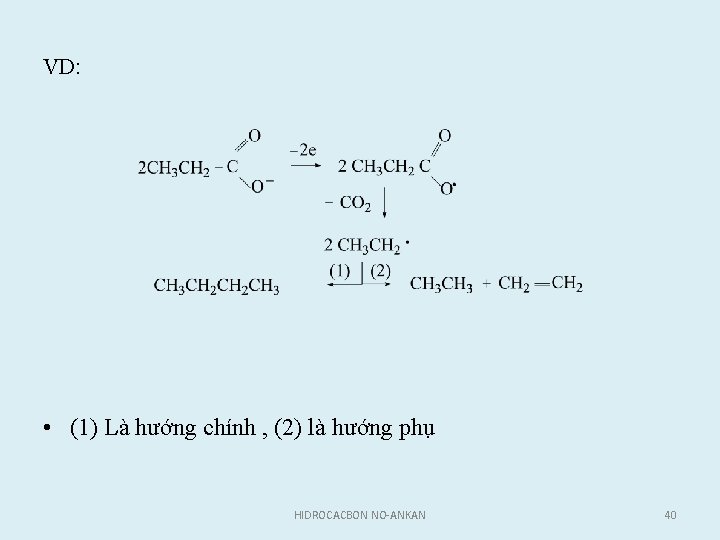
VD: • (1) Là hướng chính , (2) là hướng phụ HIDROCACBON NO-ANKAN 40

c. Phản ứng cộng điancupat liti ( phản ứng E. J. Corey – Herbert House ) • Phản ứng xảy ra theo các giai đoạn sau HIDROCACBON NO-ANKAN 41
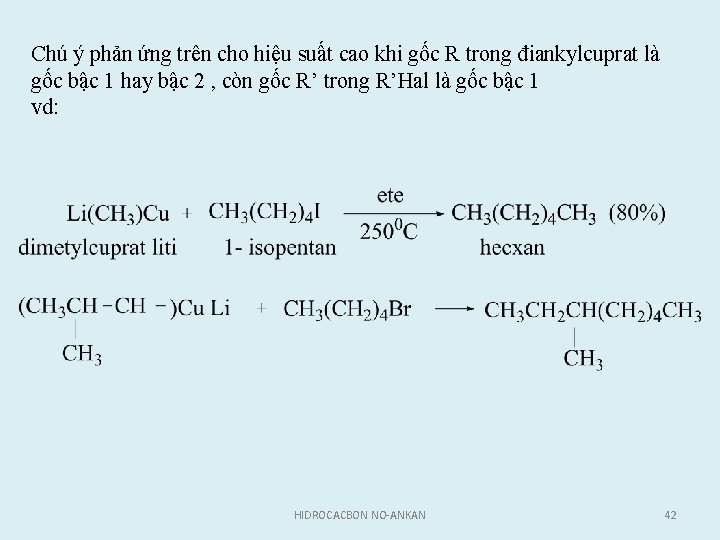
Chú ý phản ứng trên cho hiệu suất cao khi gốc R trong điankylcuprat là gốc bậc 1 hay bậc 2 , còn gốc R’ trong R’Hal là gốc bậc 1 vd: HIDROCACBON NO-ANKAN 42
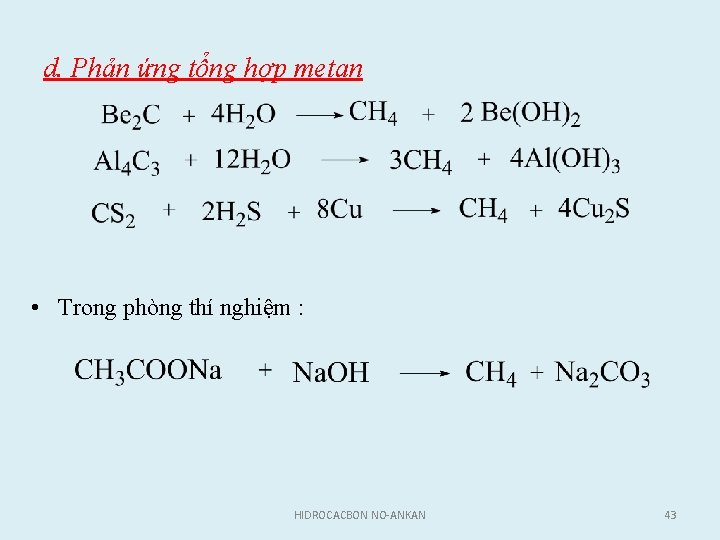
d. Phản ứng tổng hợp metan • Trong phòng thí nghiệm : HIDROCACBON NO-ANKAN 43

5. Ứng dụng 5. 1. Làm nhiên liệu Nhờ khả năng toả nhiệt rất cao khi đốt cháy, ankan được dùng rất rộng rãi làm nhiên liệu. Các ankan khí, nhất là metan dùng để đun nấu, cung cấp hơi nước để sưởi ấm, dùng trong các nhà máy phát điện, cung cấp nhiệt cho nhà máy luyện kim, dùng nung gốm sứ, phân đạm… Khí thiên nhiên hoá lỏng (LNG) và khí mỏ dầu hoá lỏng (LPG) thành phần chủ yếu là propan và butan cung cấp nhiệt năng, điện năng và cơ năng cho các phương tiện giao thông vận tải và các nhu cầu khác. HIDROCACBON NO-ANKAN 44

5. 2. Làm nguyên liệu trong công nghiệp hoá học _Từ các phân đoạn của dầu mỏ, các ankan được sử dụng làm nguồn nguyên liệu đặc biệt quan trọng trong tổng hợp hữu cơ. _Từ metan sản xuất ra các dẫn xuất clo như CH 3 Cl ứng dụng trong tổng hợp hữu cơ, các dẫn xuất còn lại CH 2 Cl 2, CHCl 3 và CCl 4 dùng làm dung môi hữu cơ; CF 2 Cl 2 dùng làm chất sinh hàn. _Từ metan có thể sản xuất được axetilen, fomanđehit, CO và H 2 là các nguồn nguyên liệu quan trọng trong sản axit axetic, chất dẻo. Sản phẩm CO và H 2 được chuyển sang công đoạn tổng hợp metanol và H 2 cung cấp cho công đoạn tổng hợp NH 3. _Cracking ankan dầu mỏ, người ta thu được etilen, propilen…tổng hợp ra etannol, etylenglicol và các chất dẻo quan trọng. HIDROCACBON NO-ANKAN 45

_Refoming các ankan C 6 C 8, người ta thu được các sản phẩm thơm hoá, isome hoá. Đặc biệt các sản phẩm isome có ứng dụng quan trọng trong việc sản xuất xăng sạch. _Oxi hoá cắt mạch các ankan mạch dài, thu được các axit ankanoic được dùng để sản xuất xà phòng. _Các n ankan mạch dài (C 20 C 35) có độ nhớt và nhiệt độ sôi cao được dùng làm dầu gốc để pha chế dầu nhờn hoặc mỡ bôi trơn. _Hỗn hợp ankan rắn (parafin) được dùng làm nến và một số lĩnh vực khác. HIDROCACBON NO-ANKAN 46

3. Một số phản ứng tổng hợp cắt ngắn mạch cacbon a. Phản ứng cracking (phương pháp công nghiệp) Nguyên liệu: Dầu điezen (~C 13 – C 20, t 0 s~ 2000 3500 C) Mazut (> C 20, t 0 s 3500 C) • Cracking nhiệt Nhiệt độ: ~ 550 6000 C Sản phẩm chủ yếu: ankan và anken có mạch cacbon ngắn hơn, H 2 Phản ứng xảy ra theo cơ chế gốc. • Cracking xúc tác Nhiệt độ: ~ 450 5000 C Xúc tác: Nhôm silicat hoặc zeolit Na x[(Al. O 2) x(Si. O 2)y. z H 2 O] (kí hiệu chung cho zeolit là Na. Z) có thể thay Na+ bằng ion K+, NH 4+, Ca 2+, H+. Cơ chế: cacbocation (kèm theo cơ chế gốc) Sản phẩm chủ yếu: + Ankan mạch nhánh (C 1 C 4 : 10 20%) + Xicloankan + Aren HIDROCACBON NO-ANKAN 47

b. Refoming (phương pháp công nghiệp) 1. Nguyên liệu: 2. Xúc tác: Etxăng (ts: ~ 80 1800 C) Axit molipđic, … Pt tẩm trên nhôm silicat 3. Nhiệt độ, áp suất: ~ 5000 C/3 35 atm 4. Sản phẩm chủ yếu: Aren (~ 7%) Anken mạch C 5 – C 7 (~20%) Anken (~2%) HIDROCACBON NO ANKAN 48
- Slides: 48