BI GING HA HC 10 KHI QUT NHM

BÀI GIẢNG HÓA HỌC 10 KHÁI QUÁT NHÓM HALOGEN

KHÁI QUÁT NHÓM HALOGEN I. Nhóm halogen trong BTH các nguyên tố : II. Cấu hình electron nguyên tử và cấu tạo phân tử của các nguyên tố trong nhóm halogen : III. Khái quát về tính chất của các halogen : 1. Tính chất vật lí : 2. Tính chất hóa học : Bài tập củng cố :
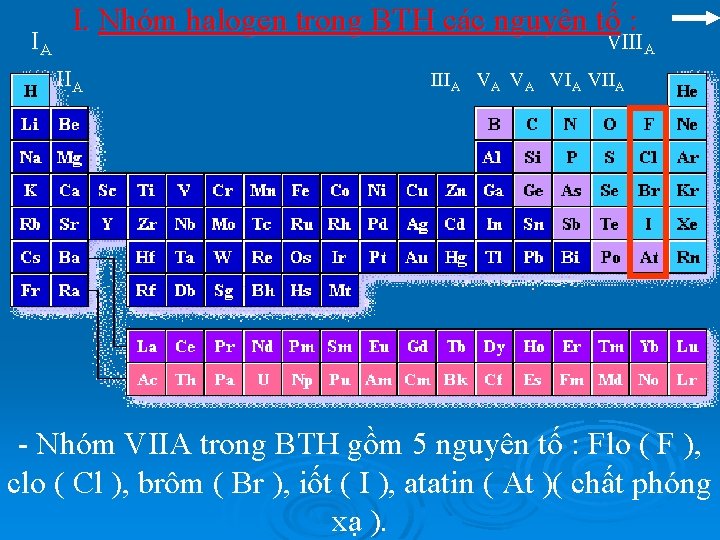
IA I. Nhóm halogen trong BTH các nguyên tố : VIIIA VA VA VIIA - Nhóm VIIA trong BTH gồm 5 nguyên tố : Flo ( F ), clo ( Cl ), brôm ( Br ), iốt ( I ), atatin ( At )( chất phóng xạ ).
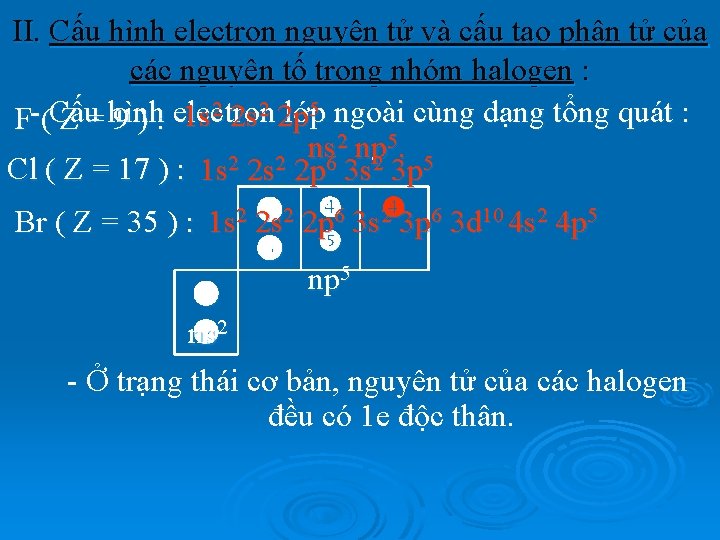
II. Cấu hình electron nguyên tử và cấu tạo phân tử của các nguyên tố trong nhóm halogen : 5 ngoài cùng dạng tổng quát : lớp 1 s 2 2 p F-(Cấu Z = hình 9 ) : electron 2 np 5. ns. 2 5 2 2 6 Cl ( Z = 17 ) : 1 s 2 s 2 p 3 s 3 p 6 2 6 10 2 5 2 2 1 s 2 s 2 p 3 s 3 p 3 d 4 s 4 p Br ( Z = 35 ) : 5 np 2 ns - Ở trạng thái cơ bản, nguyên tử của các halogen đều có 1 e độc thân.
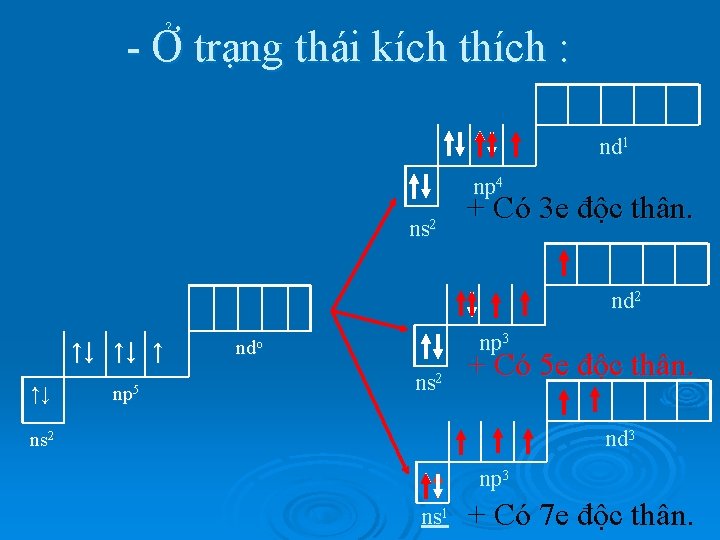
- Ở trạng thái kích thích : nd 1 np 4 ns 2 + Có 3 e độc thân. nd 2 ↑↓ ↑↓ ↑ ↑↓ np 5 np 3 ndo ns 2 + Có 5 e độc thân. nd 3 ns 2 np 3 ns 1 + Có 7 e độc thân.

X + X Công thức cấu tạo : X -Dạng đơn chất, nguyên tử nguyên tố nhóm halogen tồn tại ở dạng phân tử gồm hai nguyên tử : X 2 ( F 2, Cl 2, Br 2, I 2 ) Chú ý : Năng lượng liên kết X – X của phân tử X 2 không lớn ( 151 đến 243 kj/mol) nên các phân tử halogen tương đối dễ tách thành hai nguyên tử hoạt động hoá học mạnh.
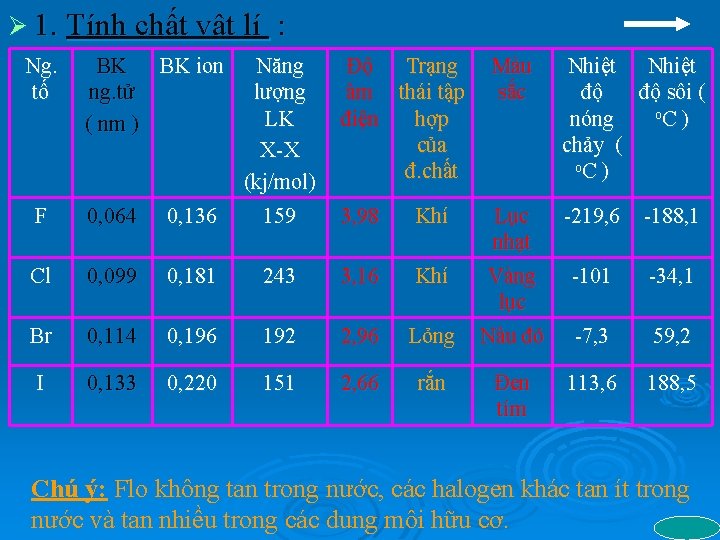
Ø 1. Tính chất vật lí Ng. tố BK BK ion ng. tử ( nm ) : F 0, 064 0, 136 Năng lượng LK X-X (kj/mol) 159 Độ Trạng âm thái tập điện hợp của đ. chất Cl 0, 099 0, 181 243 3, 16 Khí Br 0, 114 0, 196 192 2, 96 Lỏng I 0, 133 0, 220 151 2, 66 rắn 3, 98 Khí Màu sắc Nhiệt độ độ sôi ( o. C ) nóng chảy ( o. C ) Lục -219, 6 nhạt Vàng -101 lục Nâu đỏ -7, 3 Đen tím 113, 6 -188, 1 -34, 1 59, 2 188, 5 Chú ý: Flo không tan trong nước, các halogen khác tan ít trong nước và tan nhiều trong các dung môi hữu cơ.

Ø 2. Tính chất hóa học : - Nguyên tử halogen X có 7 e lớp ngoài cùng nên dể nhận thêm 1 e để trở thành X-. X + 1 e → X– … ns 2 np 5 … ns 2 np 6 → là phi kim điển hình → tính OXH mạnh → có soh đặc trưng là -1 trong hợp chất kim loại và hiđrô. + Tác dụng với Hiđrô : → khí hiđrôhalogenua 2 O dd HX X 2 + H 2 → 2 HX↑ H→ khí hiđrôhalogennua axit halogenhiđric • Tính axit : HF HCl HBr HI Tính axit tăng dần.

+ Tác dụng với kim loại : → muối halogenua 2 M + n. X 2 → 2 MXn n : là hóa trị cao của M • Đa số các muối halogen đều tan, trừ các muối sau không tan và có màu sắc đặc trưng : Ag. Cl↓trắng, Ag. Br ↓vàng nhạt, Ag. I ↓vàng đậm. - Tính OXh của nhóm halogen giảm dần từ Flo đến Iốt. ( F > Cl > Br > I ). - Trong hợp chất, ngoài soh -1 các nguyên tố còn có - Hãy xác định số OXH của clo trong các hợp soh +1, +3, +1 +5, Flo +1 +7 -2 ( trừ -2 ). +1 +5 -2 +1 +3 chất sau: HCl. O, HCl. O 2, HCl. O 3, HCl. O 4 Axit hipoclorơ Axit cloric Axit pecloric

Câu 1 : Phát biểu nào sau đây là không đúng : 1. Trong tất cả các hợp chất, thì soh của các ng. tố nhóm halogen là -1. 2. Trong tất cả các hợp chất của các muối halogenua đều tan và có màu sắc đặc trưng. 3. Tính axit được sắp xếp như sau : HF > HCl > HBr > HI. 4. Cấu hình electron lớp ngoài cùng của nhóm halogen là : ns 2 np 5. a. 2, 3, 4. b. 4. c. 1, 2, 3. d. 1, 2, 3, 4. c. 1, 2, 3. Câu 2 : Đặc điểm nào dưới đây không phải là đặc điểm chung của các nguyên tố halogen ( Flo đến Iôt ) ? a. Nguyên tử có khả năng thu thêm 1 e. b. Lớp e ngoài cùng của ng. tử có 7 e. c. Có soh -1 trong mọi hợp chất. d. Tạo ra hợp chất LKCHT có cực với H 2. Câu 3 : Đặc điểm nào dưới đây là đặc điểm chung của đơn chất halogen ? a. ở điều kiện thường là chất khí. b. Tác dụng mạnh với nước. c. Có tính OXH mạnh. d. vừa có tính OXH, vừa có tính khử. Câu 4 : Sự biến thiên tính chất vật lí của halogen từ Flo đến Iốt ? a. Trạng thái tập hợp từ khí → lỏng → rắn. b. Màu sắc đậm dần. c. Nhiệt độ sôi, nhiệt độ nóng chảy tăng dần. d. cả a, d. b, cảc. a, b, c.
- Slides: 10