BI 30 LU HUNH Ngi son L Hong

BÀI 30 LƯU HUỲNH Người soạn: Lê Hoàng Thủy Tiên

I. Vị trí – cấu hình electron nguyên tử - Cấu hình electron: 1 s 22 p 63 s 23 p 4 - Số hiệu nguyên tử: 16 - Nhóm: VIA - Chu kì: 3

II. Tính chất vật lý Lưu huỳnh là chất rắn, màu vàng, không tan trong nước nhưng tan trong dung môi hữu cơ.

II. Tính chất vật lý Hai dạng thù hình Lưu huỳnh tà phương (Sα) Lưu huỳnh đơn tà (Sβ)
II. Tính chất vật lý Sự biến đổi cấu tạo phân tử và tính chất vật lý theo nhiệt độ Nhiệt độ <113 o. C 119 o. C 187 o. C > 445 o. C Trạng thái Màu sắc Cấu tạo phân tử

II. Tính chất vật lý Sự biến đổi cấu tạo phân tử và tính chất vật lý theo nhiệt độ

II. Tính chất vật lý Sự biến đổi cấu tạo phân tử và tính chất vật lý theo nhiệt độ Nhiệt độ Trạng thái Màu sắc <113 o. C Rắn Vàng 119 o. C Lỏng Vàng 187 o. C Quánh nhớt Nâu đỏ > 445 o. C Hơi Da cam Cấu tạo phân tử
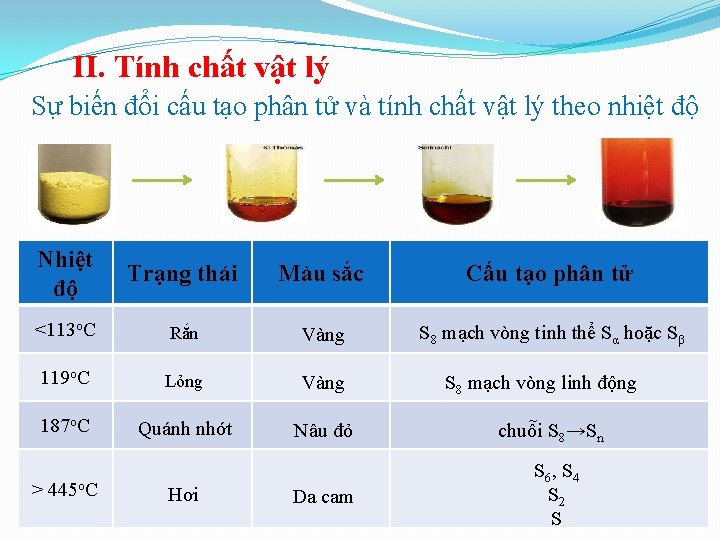
II. Tính chất vật lý Sự biến đổi cấu tạo phân tử và tính chất vật lý theo nhiệt độ Nhiệt độ Trạng thái Màu sắc Cấu tạo phân tử <113 o. C Rắn Vàng S 8 mạch vòng tinh thể Sα hoặc Sβ 119 o. C Lỏng Vàng 187 o. C Quánh nhớt Nâu đỏ chuỗi S 8→Sn Da cam S 6 , S 4 S 2 S > 445 o. C Hơi S 8 mạch vòng linh động

II. Tính chất hóa học Nhận xét: Lưu huỳnh có các số oxi hóa -2 tính oxi hóa 0 S 0 tính khử +4, +6 S Nêu các hợp chất có chứa lưu huỳnh. + Kim Tính loại số oxi hóa Muối sunfua của S trong+ các H 2 hợp chất đó ? ? ? Hidro sunfua + Phi kim

II. Tính chất hóa học 1. Tác dụng với kim loại (trừ Pt, Au, …) Nhiệt độ cao: (Sắt II sunfua) (Nhôm sunfua) Nhiệt độ thường: (Thủy ngân II sunfua) => Phản ứng này dùng để thu hồi thủy ngân trong PTN.

II. Tính chất hóa học 1. Tác dụng với kim loại Al + S →

II. Tính chất hóa học 2. Tác dụng với hidro (Hidro sunfua)

II. Tính chất hóa học 3. Tác dụng với phi kim (trừ N 2, I 2, …)

IV. Ứng dụng - Trạng thái tự nhiên – Điều chế 1. Ứng dụng Lưu huỳnh

2. Trạng thái tự nhiên - Có nhiều ở dạng đơn chất, tạo thành những mỏ lớn trong vỏ trái đất. -Có ở dạng hợp chất như muối sunfat, sunfua, quặng pirit sắt Fe. S 2, … Quặng pirit sắt
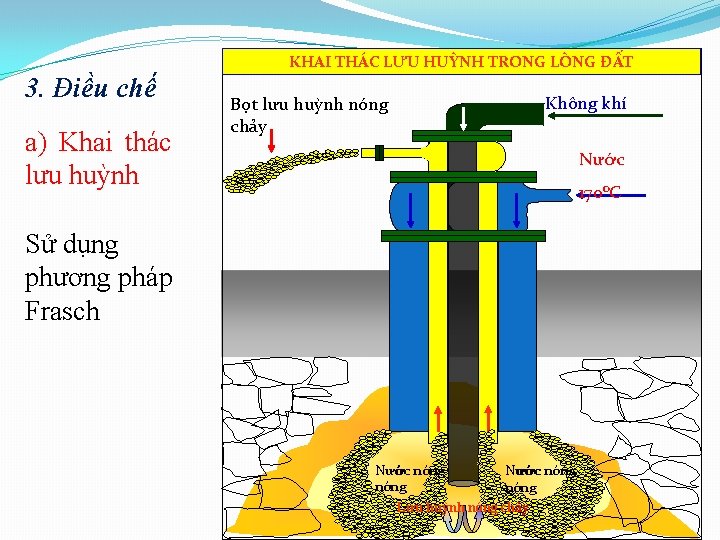
KHAI THÁC LƯU HUỲNH TRONG LÒNG ĐẤT 3. Điều chế a) Khai thác lưu huỳnh Không khí Bọt lưu huỳnh nóng chảy Nước 170 o. C Sử dụng phương pháp Frasch Nước nóng Lưu huỳnh nóng chảy

2. Điều chế b) Sản xuất lưu huỳnh từ các hợp chất - Đốt H 2 S trong điều kiện thiếu không khí -2 2 H 2 S + O 2 0 2 S + 2 H 2 O - Dùng H 2 S khử SO 2: +4 2 H 2 S + SO 2 0 3 S + H 2 O Thu hồi 90% lượng lưu huỳnh có trong các khí thải độc hại SO 2 và H 2 S. Bảo vệ môi trường.

CỦNG CỐ 1) Cho các chất sau: Fe, Cu, H 2 SO 4 loãng, O 2, F 2, Au. Số chất trong dãy tác dụng được với lưu huỳnh là? A. 3 C C. 5 B. 4 Fe Cu + + H 2 + S S S O 2 to to → to + 3 F 2 Fe. S Cu. S H 2 S SO 2 SF 6 D. 6

CỦNG CỐ 2) Xác định vai trò của lưu huỳnh trong các phản ứng sau +6 0 S + 6 HNO 3 → H 2 SO 4 + 6 NO 2 + 2 H 2 O (tính khử) -2 0 3 S + 2 Al → Al 2 S 3 (tính oxi hóa) 0 +6 +4 S + 2 H 2 SO 4 đ → 3 SO 2 + 2 H 2 O (thể hiện tính khử và tính oxi hóa)
- Slides: 19