Bi 30 LU HUNH Bi 30 LU HUNH

Bài 30: LƯU HUỲNH

Bài 30: LƯU HUỲNH I/ VỊ TRÍ, CẤU HÌNH ELECTRON NGUYÊN TỬ II/ TRẠNG THÁI TỰ NHIÊN VÀ TÍNH CHẤT VẬT LÍ III/ TÍNH CHẤT HOÁ HỌC IV/ ỨNG DỤNG VÀ SẢN XUẤT
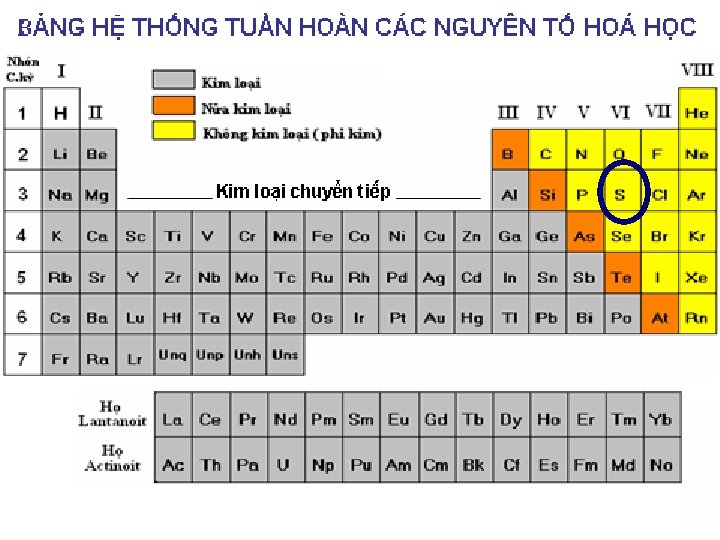
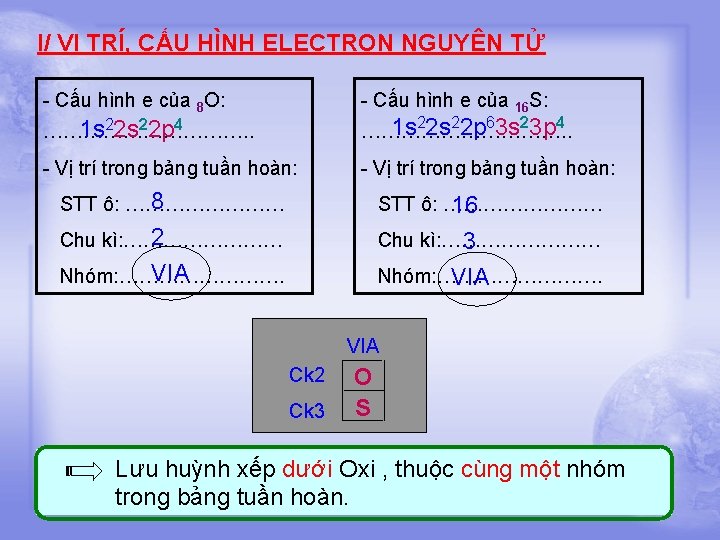
I/ VỊ TRÍ, CẤU HÌNH ELECTRON NGUYÊN TỬ - Cấu hình e của 8 O: - Cấu hình e của 16 S: 1 s 22 p 4 ……………. . 1 s 2 s 2 p 3 s 3 p ……………. . - Vị trí trong bảng tuần hoàn: 8 STT ô: …………………… 16 2 Chu kì: …………………… 3 VIA Nhóm: ……………………. VIA 2 2 6 2 4 VIA Ck 2 Ck 3 O S Lưu huỳnh xếp dưới Oxi , thuộc cùng một nhóm trong bảng tuần hoàn.

Bài 30: LƯU HUỲNH I/ VỊ TRÍ, CẤU HÌNH ELECTRON NGUYÊN TỬ II/ TRẠNG THÁI TỰ NHIÊN VÀ TÍNH CHẤT VẬT LÍ III/ TÍNH CHẤT HOÁ HỌC IV/ ỨNG DỤNG VÀ SẢN XUẤT

II. Trạng thái tự nhiên và tính chất vật lý

Lưu huỳnh trong tự nhiên
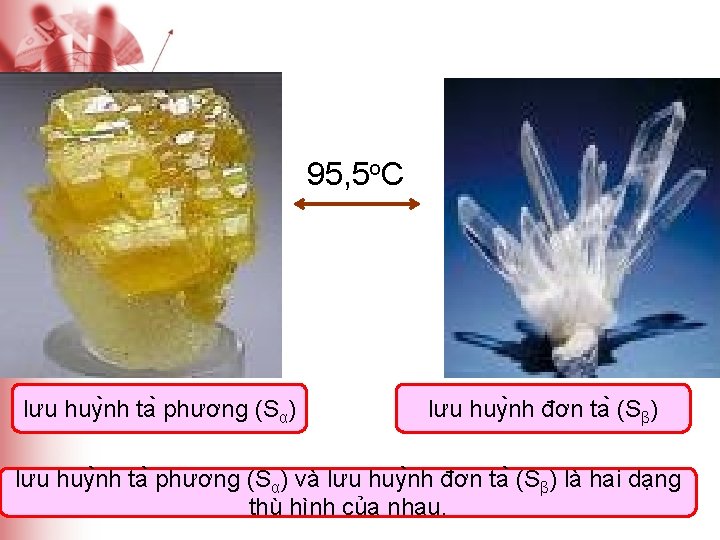
95, 5 o. C lưu huy nh ta phương (Sα) lưu huy nh đơn ta (Sβ) lưu huy nh ta phương (Sα) và lưu huy nh đơn ta (Sβ) là hai dạng thù hình của nhau.
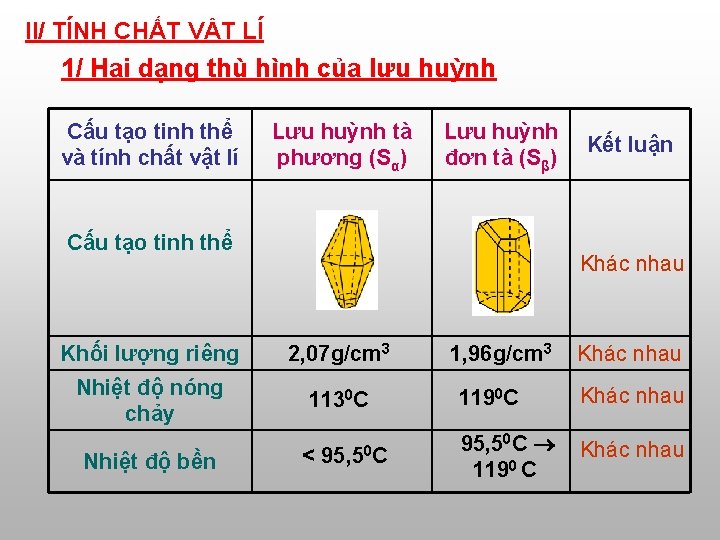
II/ TÍNH CHẤT VẬT LÍ 1/ Hai dạng thù hình của lưu huỳnh Cấu tạo tinh thể và tính chất vật lí Lưu huỳnh tà phương (Sα) Lưu huỳnh đơn tà (Sβ) Cấu tạo tinh thể Khác nhau Khối lượng riêng 2, 07 g/cm 3 Nhiệt độ nóng chảy 1130 C Nhiệt độ bền Kết luận < 95, 50 C 1, 96 g/cm 3 Khác nhau 1190 C Khác nhau 95, 50 C 1190 C Khác nhau

95, 5 o. C lưu huy nh ta phương (Sα) lưu huy nh đơn ta (Sβ) => Chúng khác nhau về cấu tạo tinh thể và một số đại lượng vật lý, nhưng tính chất hóa học giống nhau

II. Trạng thái tự nhiên và tính chất vật lý: 2. Ảnh hưởng của nhiệt độ đối với cấu tạo của phân tử S Vậy khi nung nóng lưu hùynh ở nhiệt độ cao có xảy ra sự biến đổi gì không?

II/ TÍNH CHẤT VẬT LÍ 2/ Ảnh hưởng của nhiệt độ đến tính chất vật lí Quan sát thí nghiệm sau, ghi nhận sự biến đổi màu sắc và trạng thái của lưu huỳnh trong quá trình nóng chảy ?

II/ TÍNH CHẤT VẬT LÍ 2/ Ảnh hưởng của nhiệt độ đến tính chất vật lí

II. Trạng thái tự nhiên và tính chất vật lý: 2. Ảnh hưởng của nhiệt độ đối với cấu tạo của phân tử S 200 C 1190 C 1870 C 4450 C
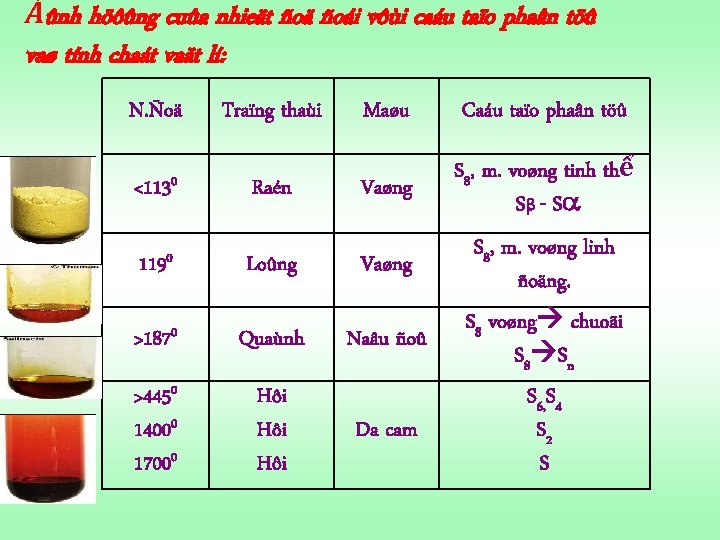
Ảûnh höôûng cuûa nhieät ñoä ñoái vôùi caáu taïo phaân töû vaø tính chaát vaät lí: N. Ñoä <1130 Traïng thaùi Raén Maøu Caáu taïo phaân töû Vaøng S 8, m. voøng tinh thể S - S 1190 Loûng Vaøng >1870 Quaùnh Naâu ñoû >4450 14000 17000 Hôi Hôi Da cam S 8, m. voøng linh ñoäng. S 8 voøng chuoãi S 8 Sn S 6, S 4 S 2 S
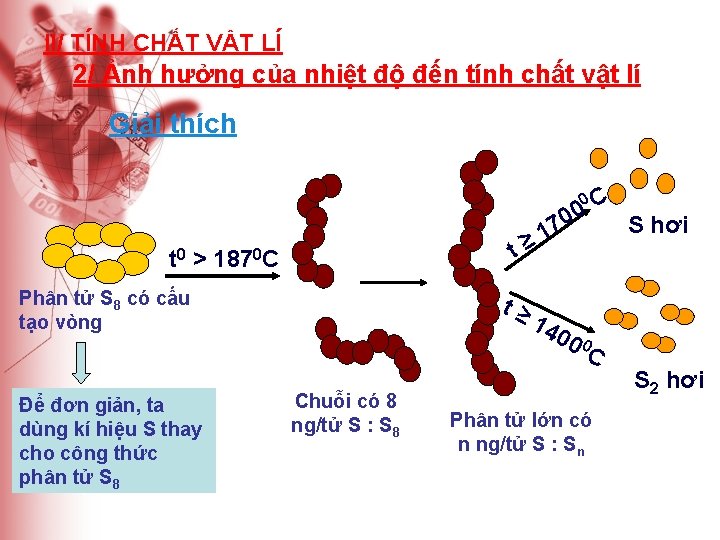
II/ TÍNH CHẤT VẬT LÍ 2/ Ảnh hưởng của nhiệt độ đến tính chất vật lí Giải thích t t 0 > 1870 C Phân tử S 8 có cấu tạo vòng Để đơn giản, ta dùng kí hiệu S thay cho công thức phân tử S 8 7 1 ≥ t≥ Chuỗi có 8 ng/tử S : S 8 14 0 C 0 0 S hơi 00 0 C S 2 hơi Phân tử lớn có n ng/tử S : Sn

Bài 30: LƯU HUỲNH I/ VỊ TRÍ, CẤU HÌNH ELECTRON NGUYÊN TỬ II/ TRẠNG THÁI TỰ NHIÊN VÀ TÍNH CHẤT VẬT LÍ III/ TÍNH CHẤT HOÁ HỌC IV/ ỨNG DỤNG VÀ SẢN XUẤT
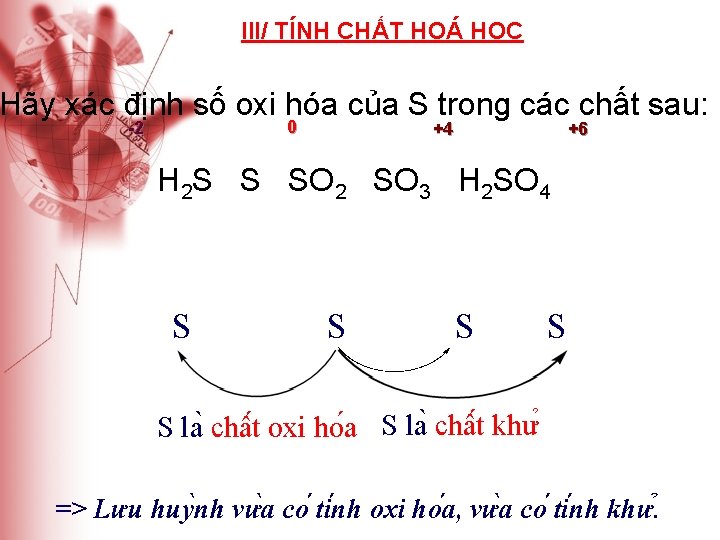
III/ TÍNH CHẤT HOÁ HỌC Hãy xác định số oxi hóa của S trong các chất sau: 0 -2 +4 +6 H 2 S S SO 2 SO 3 H 2 SO 4 S S S la châ t oxi ho a S la châ t khư => Lưu huy nh vư a co ti nh oxi ho a, vư a co ti nh khư.

III/ TÍNH CHẤT HOÁ HỌC 1. TÁC DỤNG VỚI KIM LOẠI Lưu huỳnh tác dụng với kim loại ( trừ : Au, Pt, Ag) S tác dụng với Fe :


III/ TÍNH CHẤT HOÁ HỌC 1. TÁC DỤNG VỚI KIM LOẠI a. Lưu huỳnh tác dụng với kim loại ( trừ : Au, Pt, Ag) -2 b. o to Fe + Al + Hg + S o Fe. S to S Sắt (II) Sunfua -2 Al 2 S 3 Nhôm Sunfua -2 t 0 thường Hg. S Thuỷ ngân Sunfua => Dùng S để thu hồi thủy ngân rơi vãi

III/ TÍNH CHẤT HOÁ HỌC 2. TÁC DỤNG VỚI HIDRO
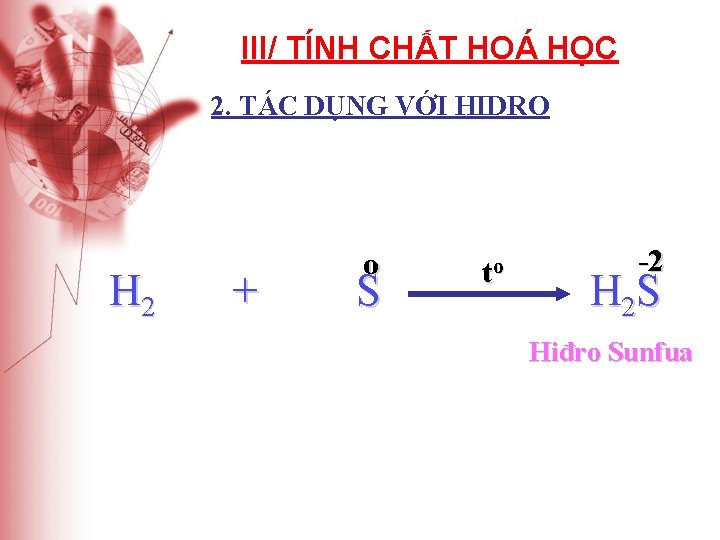
III/ TÍNH CHẤT HOÁ HỌC 2. TÁC DỤNG VỚI HIDRO H 2 + o S to -2 H 2 S Hiđro Sunfua
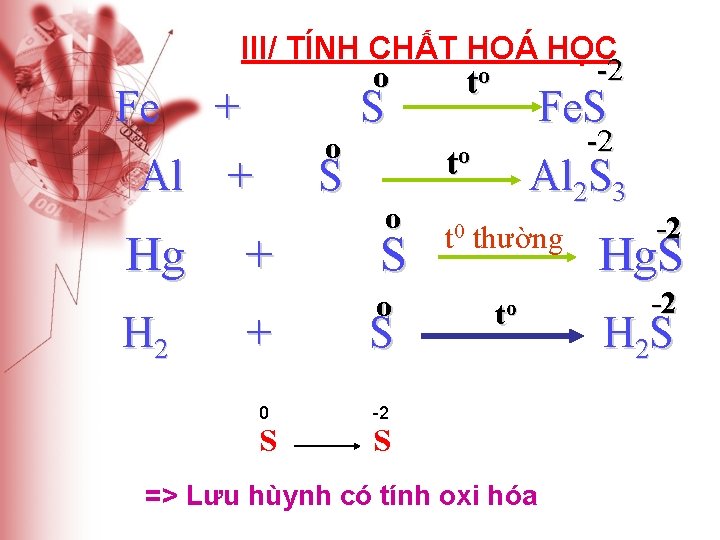
Fe + III/ TÍNH CHẤT HOÁ HỌC -2 o o t o Al + Hg H 2 S + + 0 S S Fe. S -2 to o Al 2 S 3 S t 0 thường o to S -2 S => Lưu hùynh có tính oxi hóa -2 Hg. S -2 H 2 S

III/ TÍNH CHẤT HOÁ HỌC 3. TÁC DỤNG VỚI PHI KIM
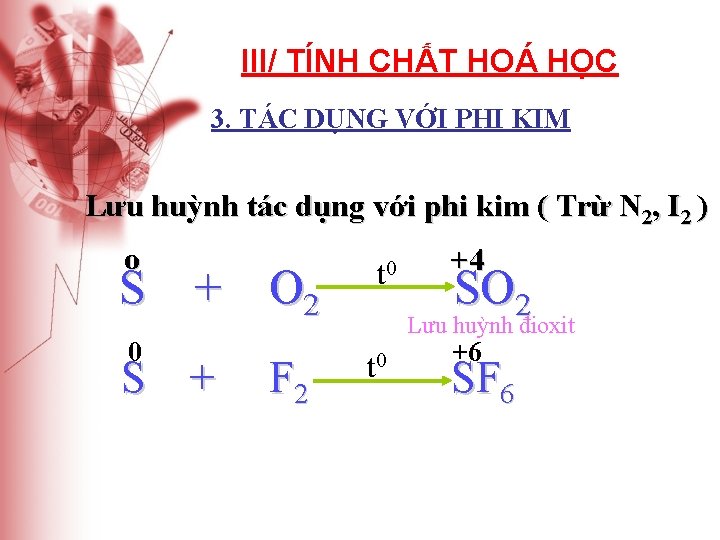
III/ TÍNH CHẤT HOÁ HỌC 3. TÁC DỤNG VỚI PHI KIM Lưu huỳnh tác dụng với phi kim ( Trừ N 2, I 2 ) o S + O 2 0 S + F 2 t 0 +4 SO 2 Lưu huỳnh đioxit t 0 +6 SF 6
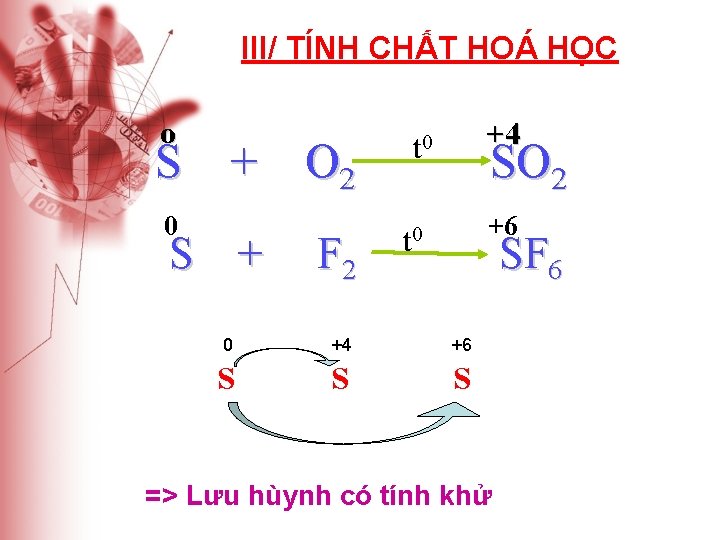
III/ TÍNH CHẤT HOÁ HỌC o S + O 2 0 S + F 2 +4 t 0 SO 2 +6 t 0 SF 6 0 +4 +6 S S S => Lưu hùynh có tính khử

v Khi cho S tác dụng với các nguyên tố có độ âm điện nhỏ hơn thì S thể hiện tính : Oxi hóa v Khi cho có độ âm điện+6 lớn hơn 0 các nguyên tố+4 -2 S tác dụng với thì S thể hiện tính : Khử S S S la châ t oxi ho a S la châ t khư => Lưu huy nh vư a co ti nh oxi ho a, vư a co ti nh khư.

Bài 30: LƯU HUỲNH I/ VỊ TRÍ, CẤU HÌNH ELECTRON NGUYÊN TỬ II/ TRẠNG THÁI TỰ NHIÊN VÀ TÍNH CHẤT VẬT LÍ III/ TÍNH CHẤT HOÁ HỌC IV/ ỨNG DỤNG VÀ SẢN XUẤT

IV/ ỨNG DỤNG

IV/ ỨNG DỤNG

III. Ứng dụng của lưu huỳnh Các ứng dụng: 90% 10% - Sản xuất H 2 SO 4 -Tẩy bộtsu giấy Lưu trắng hoá cao -Chế tạo diêm -Sản xuất chất dẻo Ebonit -Chế mỡ chữa bệnh ngoài da -Sản xuất thuốc trừ sâu. . v. v

IV/ ỨNG DỤNG VÀ SẢN XUẤT
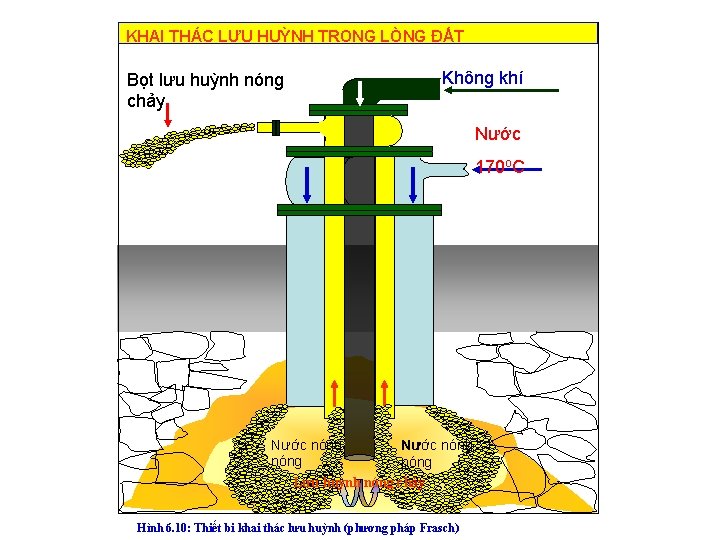
KHAI THÁC LƯU HUỲNH TRONG LÒNG ĐẤT Bọt lưu huỳnh nóng chảy Không khí Nước 170 o. C Nước nóng Lưu huỳnh nóng chảy Hình 6. 10: Thiết bi khai thác lưu huỳnh (phương pháp Frasch)

V/ TRẠNG THÁI TỰ NHIÊN VÀ SẢN XUẤT LƯU HUỲNH TỪ HỢP CHẤT Đốt H 2 S trong điều kiện thiếu không khí 2 H 2 S O 2 2 S 2 H 2 O 3 S 2 H 2 O Dùng H 2 S khử SO 2 2 H 2 S SO 2
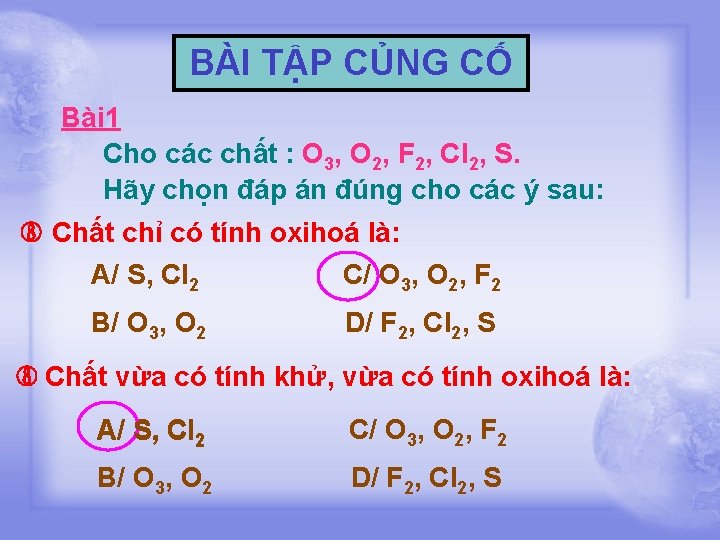
BÀI TẬP CỦNG CỐ Bài 1 Cho các chất : O 3, O 2, F 2, Cl 2, S. Hãy chọn đáp án đúng cho các ý sau: Chất chỉ có tính oxihoá là: A/ S, Cl 2 C/ O 3, O 2, F 2 B/ O 3, O 2 D/ F 2, Cl 2, S Chất vừa có tính khử, vừa có tính oxihoá là: A/ S, Cl 2 C/ O 3, O 2, F 2 B/ O 3, O 2 D/ F 2, Cl 2, S
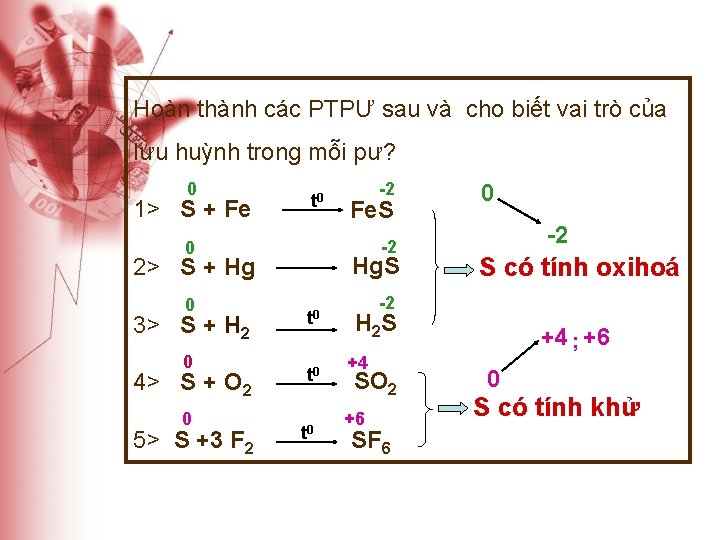
Hoàn thành các PTPƯ sau và cho biết vai trò của lưu huỳnh trong mỗi pư? 0 1> S + Fe t 0 Hg. S 2> S + Hg 3> S + H 2 0 4> S + O 2 0 5> S +3 F 2 Fe. S -2 0 0 -2 t 0 t 0 0 -2 S có tính oxihoá -2 H 2 S +4 SO 2 +6 SF 6 +4 ; +6 0 S có tính khử

- Slides: 38