Bi 24 TNH CHT CA OXI TIT 2
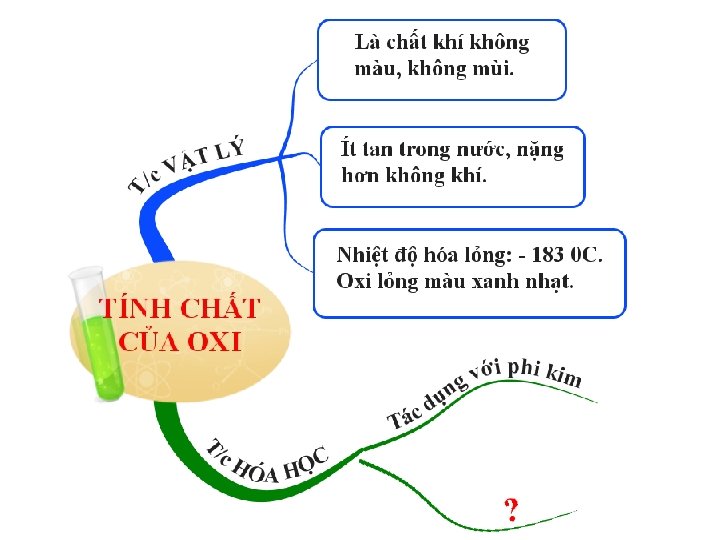
Bài 24: TÍNH CHẤT CỦA OXI (TIẾT 2) I. Tính chất vật lí II. Tính chất hóa học: 1. Tác dụng với phi kim a. Với lưu huỳnh: b. Với photpho: 2. Tác dụng với kim loại Thí nghiệm: Sắt tác dụng với oxi Cách tiến hành 1. Lấy đoạn dây sắt nhỏ đã cuộn một đầu thành hình lò xo bên trong có 1 đoạn gỗ diêm, đưa vào lọ chứa khí oxi. Có thấy dấu hiệu của phản ứng hóa học không? 2. Đốt cho sắt và đoạn gỗ diêm nóng đỏ rồi đưa nhanh vào lọ chứa khí oxi. Nhận xét các hiện tượng xảy ra. Hiện tượng Giải thích
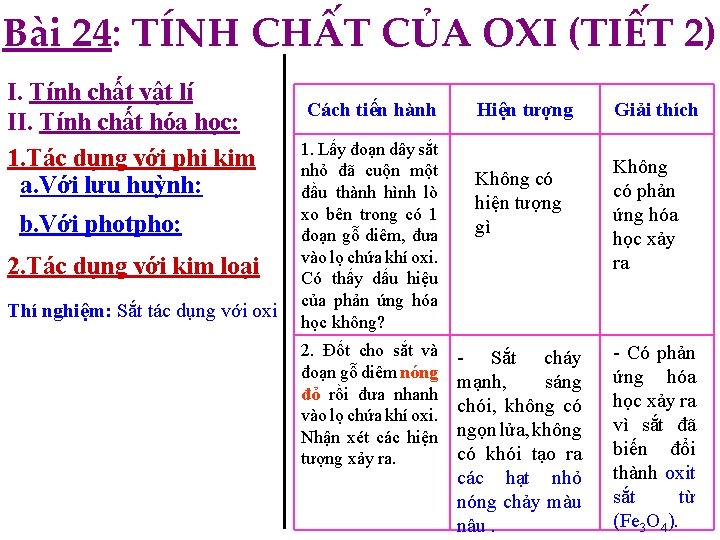
Bài 24: TÍNH CHẤT CỦA OXI (TIẾT 2) I. Tính chất vật lí II. Tính chất hóa học: 1. Tác dụng với phi kim a. Với lưu huỳnh: b. Với photpho: 2. Tác dụng với kim loại Thí nghiệm: Sắt tác dụng với oxi Cách tiến hành 1. Lấy đoạn dây sắt nhỏ đã cuộn một đầu thành hình lò xo bên trong có 1 đoạn gỗ diêm, đưa vào lọ chứa khí oxi. Có thấy dấu hiệu của phản ứng hóa học không? 2. Đốt cho sắt và đoạn gỗ diêm nóng đỏ rồi đưa nhanh vào lọ chứa khí oxi. Nhận xét các hiện tượng xảy ra. Hiện tượng Không có hiện tượng gì - Sắt cháy mạnh, sáng chói, không có ngọn lửa, không có khói tạo ra các hạt nhỏ nóng chảy màu nâu. Giải thích Không có phản ứng hóa học xảy ra - Có phản ứng hóa học xảy ra vì sắt đã biến đổi thành oxit sắt từ (Fe 3 O 4).
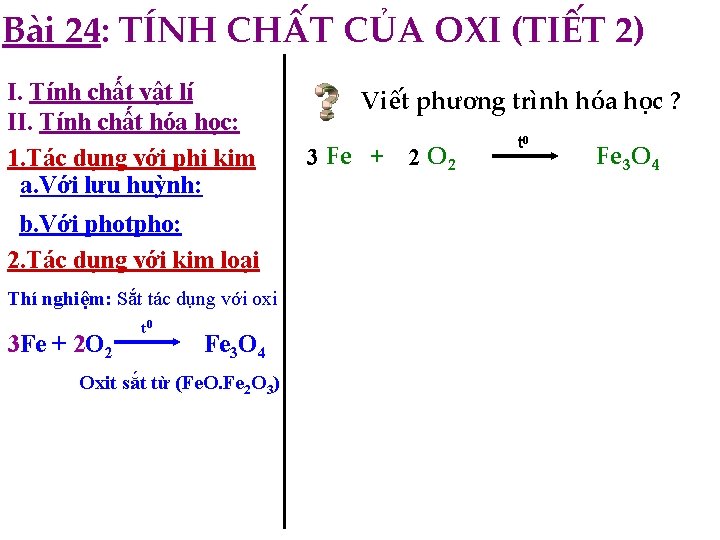
Bài 24: TÍNH CHẤT CỦA OXI (TIẾT 2) I. Tính chất vật lí II. Tính chất hóa học: 1. Tác dụng với phi kim a. Với lưu huỳnh: b. Với photpho: 2. Tác dụng với kim loại Thí nghiệm: Sắt tác dụng với oxi 3 Fe + 2 O 2 t 0 Fe 3 O 4 Oxit sắt từ (Fe. O. Fe 2 O 3) Viết phương trình hóa học ? 3 Fe + 2 O 2 t 0 Fe 3 O 4

Bài 24: TÍNH CHẤT CỦA OXI (TIẾT 2) I. Tính chất vật lí II. Tính chất hóa học: 1. Tác dụng với phi kim a. Với lưu huỳnh: Ví dụ 1: Viết phương trình hóa học cho các phản ứng đốt cháy các kim loại sau ? a. Kim loại canxi (Ca) tạo thành canxi oxit. (Ca. O) b. Kim loại nhôm (Al) tạo thành Nhôm Thí nghiệm: Sắt tác dụng với oxit. (Al 2 O 3) t 0 c. Kim loại magie (Mg) tạo thành magie 3 Fe + 2 O 2 Fe 3 O 4 oxit. (Mg. O) b. Với photpho: 2. Tác dụng với kim loại Oxit sắt từ (Fe. O. Fe 2 O 3) Lời giải 2 Ca + O 2 4 Al + 3 O 2 2 Mg + O 2 to to to 2 Ca. O 2 Al 2 O 3 2 Mg. O

Bài 24: TÍNH CHẤT CỦA OXI (TIẾT 2) I. Tính chất vật lí II. Tính chất hóa học: 1. Tác dụng với phi kim a. Với lưu huỳnh: Khí metan có ở đâu? b. Với photpho: 2. Tác dụng với kim loại Thí nghiệm: Sắt tác dụng với oxi 3 Fe + 2 O 2 t 0 Khí bùn ao Khí hầm biogas Khí mỏ dầu Khí gây nổ mỏ than Fe 3 O 4 Oxit sắt từ (Fe. O. Fe 2 O 3) 2. Tác dụng với hợp chất Khí metan cháy trong không khí

Bài 24: TÍNH CHẤT CỦA OXI (TIẾT 2) I. Tính chất vật lí II. Tính chất hóa học: 1. Tác dụng với phi kim a. Với lưu huỳnh: b. Với photpho: 2. Tác dụng với kim loại Thí nghiệm: Sắt tác dụng với oxi 3 Fe + 2 O 2 t 0 Fe 3 O 4 Oxit sắt từ (Fe. O. Fe 2 O 3) 2. Tác dụng với hợp chất Khí metan cháy trong không khí * Quan sát: * Nhận xét: Khí metan cháy trong không khí tỏa nhiều nhiệt Clip

Bài 24: TÍNH CHẤT CỦA OXI (TIẾT 2) I. Tính chất vật lí II. Tính chất hóa học: 1. Tác dụng với phi kim a. Với lưu huỳnh: b. Với photpho: 2. Tác dụng với kim loại Thí nghiệm: Sắt tác dụng với oxi 3 Fe + 2 O 2 Fe 3 O 4 Oxit sắt từ (Fe. O. Fe 2 O 3) 2. Tác dụng với hợp chất Khí metan cháy trong không khí Phương trình phản ứng: o t CH CO 2 (k) + 2 H 2 O(h) 4 (k) + 2 O 2 (k). . . . .

Bài 24: TÍNH CHẤT CỦA OXI (TIẾT 2) I. Tính chất vật lí II. Tính chất hóa học: 1. Tác dụng với phi kim a. Với lưu huỳnh: b. Với photpho: 2. Tác dụng với kim loại Thí nghiệm: Sắt tác dụng với oxi 3 Fe + 2 O 2 t 0 Fe 3 O 4 Oxit sắt từ (Fe. O. Fe 2 O 3) 2. Tác dụng với hợp chất Khí metan cháy trong không khí CH 4 + 2 O 2 to CO 2 + 2 H 2 O Bài tập 1 Dùng từ hoặc cụm từ thích hợp trong khung để điền vào chỗ trống trong các câu sau: kim loại; phi kim; rất hoạt động; hợp chất; phi kim rất hoạt động; hóa trị II. Khí oxi là một đơn chất phi kim rất hoạt động. . . (1). . . . , đặc biệt ở nhiệt độ cao, dễ dàng tham gia phản ứng hóa học với nhiều kim loại. . . (2). . . . , hợp chất Trong các. (3). . . . . , . . . (4). . . . phi kim hóa trị II hợp chất oxi có. . (5). . .

Bài 24: TÍNH CHẤT CỦA OXI (TIẾT 2) I. Tính chất vật lí II. Tính chất hóa học: 1. Tác dụng với phi kim 2. Tác dụng với kim loại Thí nghiệm: Sắt tác dụng với oxi to 3 Fe + 2 O Fe O 2 3 4 3. Tác dụng với hợp chất o t CH 4 + 2 O 2 CO 2 + 2 H 2 O KL: Khí oxi là một đơn chất phi kim rất hoạt động , đặc biệt ở nhiệt độ cao, dễ dàng tham gia phản ứng hóa học với nhiều phi kim, kim loại, hợp chất. Trong các hợp chất oxi có hóa trị II.

VUI ĐỂ HỌC 60 50 40 30 20 10 ĐỘI A 1 2 3 4 5 6 60 50 40 30 20 10 ĐỘI B
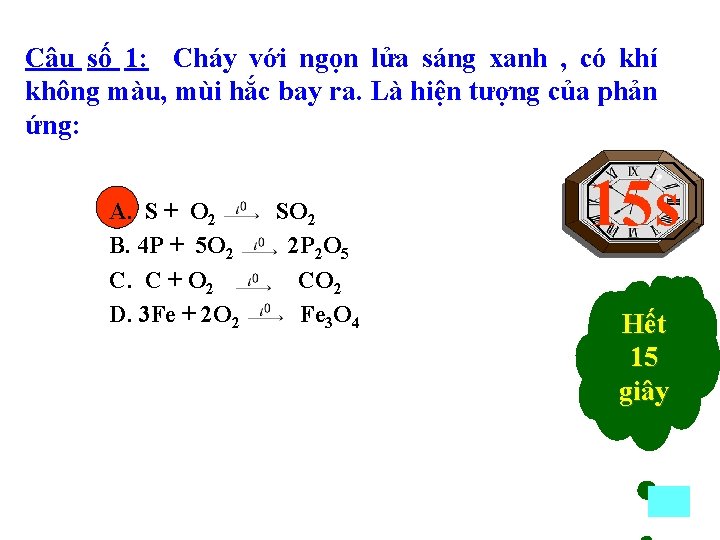
Câu số 1: Cháy với ngọn lửa sáng xanh , có khí không màu, mùi hắc bay ra. Là hiện tượng của phản ứng: A. S + O 2 B. 4 P + 5 O 2 C. C + O 2 D. 3 Fe + 2 O 2 SO 2 2 P 2 O 5 CO 2 Fe 3 O 4 15 s 14 s 13 s 12 s 11 s 10 s 09 s 08 s 07 s 06 s 05 s 04 s 03 s 02 s 01 s 15 Hết giây 15 bắt giây đầu

Câu số 3: Cháy với ngọn lửa sáng chói, tạo khói trắng dày đặc bám vào thành bình. Là hiện tượng của phản ứng: A. 3 Fe + 2 O 2 Fe 3 O 4 B. CH 4 + 2 O 2 CO 2+ 2 H 2 O C. C + O 2 D. 4 P + 5 O 2 CO 2 2 P 2 O 5 15 s 14 s 13 s 12 s 11 s 10 s 09 s 08 s 07 s 06 s 05 s 04 s 03 s 02 s 01 s 15 Hết giây 15 bắt giây đầu

Câu số 4: Cần bao nhiêu gam oxi để đốt cháy hết 2 mol lưu huỳnh ? A. 16 gam B. 32 gam C. 64 gam C D. 48 gam 15 s 14 s 13 s 12 s 11 s 10 s 09 s 08 s 07 s 06 s 05 s 04 s 03 s 02 s 01 s 15 Hết giây 15 bắt giây đầu

Câu số 6: Cháy mạnh, sáng chói, tạo ra các hạt nóng chảy màu nâu. Là hiện tượng của phản ứng : A. CH 4 + 2 O 2 CO 2+ 2 H 2 O B. 3 Fe + 2 O 2 C. C + O 2 CO 2 D. S + O 2 SO 2 Fe 3 O 4 14 s 13 s 12 s 11 s 10 s 09 s 08 s 07 s 06 s 05 s 04 s 03 s 02 s 01 s 15 Hết giây 15 bắt giây đầu

Câu 2: Đốt cháy hoàn toàn 9. 6, g một kim loại R có hóa trị II trong khí oxi dư, người ta thu được 16 g oxit (RO). Khối lượng oxi cần dùng là: 15 s 14 s 13 s 12 s 11 s 10 s 09 s 08 s 07 s 06 s 05 s 04 s 03 s 02 s 01 s A. 4, 8 g B. 4 g C C. 6, 4 g 15 giây bắt đầu Hết 15 giây

Câu 5: Cho 5, 6 g sắt tác dụng với axit clohidric (HCl), có phương trình hóa học: Fe + 2 HCl Fe. Cl 2 + H 2 Số mol axit clohidric cần dùng là: A. 0, 1 mol BB. 0, 2 mol C. 0, 05 mol 15 s 14 s 13 s 12 s 11 s 10 s 09 s 08 s 07 s 06 s 05 s 04 s 03 s 02 s 01 s 15 Hết giây 15 bắt giây đầu
Bài tập vận dụng

Bài tập vận dụng Bài tập 1: Đốt cháy hoàn toàn 6, 4 g bột lưu huỳnh trong không khí thu được lưu huỳnh đioxit ( SO 2). a. Tính khối lượng chất tạo thành ? b. Tính thể tích khí oxi tham gia phản ứng ở đktc ? Bài tập 2: Đốt cháy 12, 4 g photpho trong bình chứa 19, 2 g khí oxi tạo thành điphotpho pentaoxit P 2 O 5 là chất rắn màu trắng. a. Chất nào dư và khối lượng chất dư là bao nhiêu? b. Tính khối lượng chất tạo thành?

Bài tập 1: Đốt cháy hoàn toàn 6, 4 g bột lưu huỳnh trong không khí thu được lưu huỳnh đioxit ( SO 2). a. Tính khối lượng chất tạo thành ? b. Tính thể tích khí oxi tham gia phản ứng ở đktc ? ( Biết S= 32, 0= 16) Tóm tắt Bi ết: Tìm: m. S = 6, 4 g a. m SO = ? g 2 b. VO 2 = ? l ( đktc)
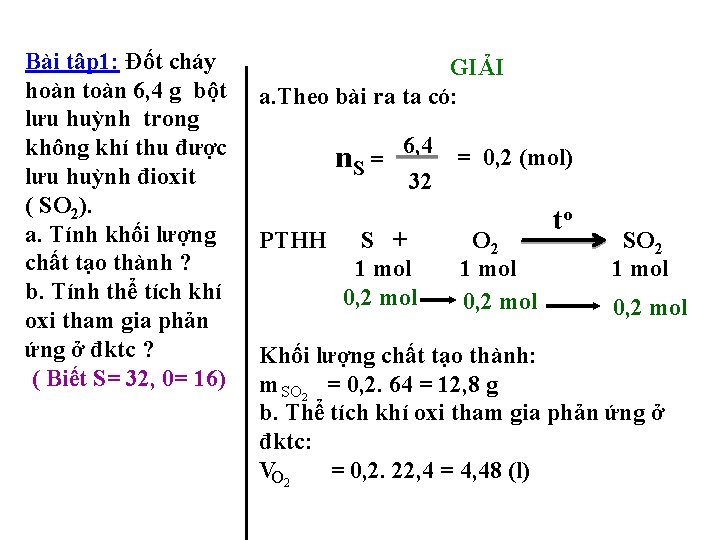
Bài tập 1: Đốt cháy hoàn toàn 6, 4 g bột lưu huỳnh trong không khí thu được lưu huỳnh đioxit ( SO 2). a. Tính khối lượng chất tạo thành ? b. Tính thể tích khí oxi tham gia phản ứng ở đktc ? ( Biết S= 32, 0= 16) GIẢI a. Theo bài ra ta có: n. S = PTHH 6, 4 32 S + 1 mol 0, 2 mol = 0, 2 (mol) O 2 1 mol 0, 2 mol to SO 2 1 mol 0, 2 mol Khối lượng chất tạo thành: m SO 2 = 0, 2. 64 = 12, 8 g b. Thể tích khí oxi tham gia phản ứng ở đktc: VO 2 = 0, 2. 22, 4 = 4, 48 (l)
Tóm tắt Bài tập 2: Đốt cháy 12, 4 g photpho trong bình chứa 19, 2 g khí oxi tạo thành điphotpho pentaoxit P 2 O 5 là chất rắn màu trắng. a. Chất nào dư và khối lượng chất dư là bao nhiêu? b. Tính khối lượng chất tạo thành? ( Biết P = 31, 0 = 16 ) Bi ết: m. P = 12, 4 g m O 2 = 19, 2 g a. Chất nào dư ? m dư = ? g Tìm: b. m P 2 O 5 = ? g
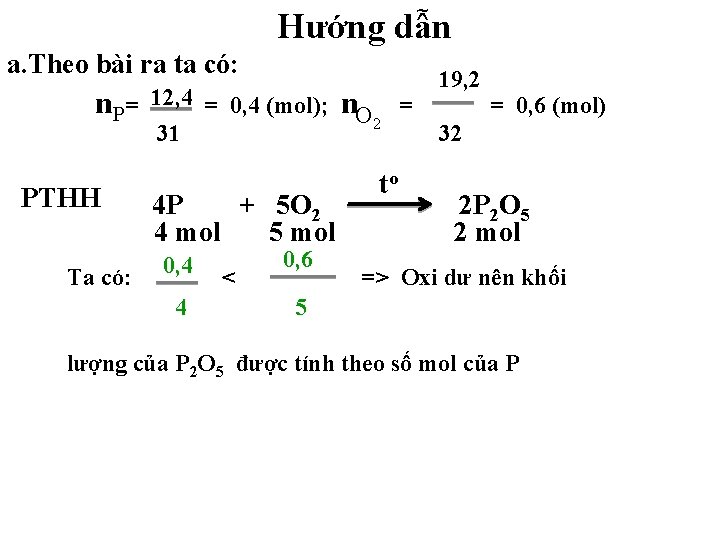
Hướng dẫn a. Theo bài ra ta có: n P= PTHH Ta có: 12, 4 = 0, 4 (mol); 31 4 P + 5 O 2 4 mol 5 mol 0, 4 4 < 0, 6 n. O 2 to = 19, 2 = 0, 6 (mol) 32 2 P 2 O 5 2 mol => Oxi dư nên khối 5 lượng của P 2 O 5 được tính theo số mol của P

PTHH: 4 P to + 5 O 2 2 P 2 O 5 4 mol 5 mol 2 mol 0, 4 mol 0, 5 mol 0, 2 mol Số mol chất dư: n. O dư = 0, 6 – 0, 5 = 0, 1 (mol) Khối lượng chất dư: m O dư = 0, 1. 32 = 3, 2 (g) Chất tạo thành là P 2 O 5 m P O = 0, 2. 142 = 28, 4 (g) 2 2 2 5

- Học bài : + Tính chất vật lí của oxi + Tính chất hóa học của oxi - Làm bài tập 2, 3, 4, 5, 6 / 84 / sgk

CẢM ƠN QUÝ THẦY CÔ GIÁO VÀ CÁC EM HỌC SINH
- Slides: 26