Bezpenost prce v mikrobiologick laboratoi Ochrana pl rukavice

Bezpečnost práce v mikrobiologické laboratoři • Ochrana – plášť, rukavice – převlékat, plášť jen v laboratoři! • • Nejíst, nepít, nekouřit Hlídat zdravotní stav – těhotenství, alergie… Hygiena – MO mohou být patogenní Úrazy ihned hlásit, i malé – ústa vykloktat 1% KMn. O 4 – oči vypláchnout vodou a pak borovou vodou – nesbírat rozbité sklo rukou

Bezpečnost práce v mikrobiologické laboratoři • Čistota a sterilita – pracovní prostory, nástroje… – úklid před započetím práce – kontaminované předměty otřít 0, 1% Ajatinem – úklid po skončení práce • Odpadní kultury před likvidací usmrtit (autokláv, chemicky…)

Základy mikrobiologické práce • • • Sterilita Kultivační metody Mikroskopování Chemické analýzy Biochemické analýzy Genetické analýzy

Sterilní práce • • Při mikrobiologické práci je třeba zbavit se všech nežádoucích MO, které by mohly narušit průběh pokusu Sterilovat je třeba vše potřebné: – – – média laboratorní sklo pracovní plochu nástroje vzduch

Metody sterilace • • • Vlhké teplo Suché teplo Chemické látky Filtrace Plamen Záření

Vlhké teplo • • • Velice účinné proti MO Obvykle za zvýšeného tlaku Zařízení = autokláv Teplota, tlak a čas různé 80 -120°C, 0, 1 -0, 2 MPa, 15 -120 minut

Suché teplo • • Méně účinné než vlhké teplo = je třeba delší čas (2 hodiny a déle) Pro sterilaci objektů, které nesmějí nebo nemohou zvlhnout – chemikálie, suché pracovní nástroje…

Chemické látky • • Rozmanité látky s mikrobicidním účinkem mají různá použití Savo – hrubá sterilace povrchů Ajatin – důkladná sterilace povrchů Ethanol – sterilace pracovních nástrojů a povrchů

Filtrace • • Pro tekutiny (plyny a kapaliny) citlivé na zvýšenou teplotu Jemný filtr s póry řádově menšími než velikost bakteriálních buněk Pozor na protržení Flowbox (laminární box) = zařízení foukající filtrovaný vzduch do uzavřeného prostoru

foukání sterilního vzduchu

Plamen • • • Velmi účinný Jednoduché použití Použitelný pro věci s vysokou tepelnou odolností – kovové nástroje (kličky, pinzety…) • • Pro sterilaci vzduchu v jeho okolí Pozor na požár!

Záření • • • Různá účinnost podle vlnové délky Může vyvolávat fotochemické reakce UV – nerovné povrchy – vzduch – germicidní lampa = UV 260 -270 nm • Gama záření – vysoce ionizující – pro sterilaci půd a speciálních médií

Média • • Většina mikrobiologických metod vyžaduje kultivaci MO Živná média – přirozená (mléko, krev, listí…) – syntetická (definované živiny) – polosyntetická (některé živiny přesně definované, jiné přirozené) • Podle skupenství – tekutá – pevná (ztužená)

Média • Podle bohatosti – bohatá (všechny živiny v nadbytku) – limitovaná (některá živina v nedostatku) • Podle selektivity – obecná (pro kultivaci velké skupiny organismů) – selektivní (pro kultivaci jen omezené skupiny MO)

Složení médií • Zdroj uhlíku – sacharidy (glukóza), aminokyseliny, peptidy, lipidy, organické látky… • Zdroj dusíku – organický (aminokyseliny…) – anorganický (amoniak, dusičnany…) • Další minerální látky – fosfor, síra, biogenní kovy (železo, měď, zinek…)

Složení médií • Selektivní činidla – antibiotika • Speciální látky pro auxotrofy – aminokyseliny, vitamíny… • • Voda Vhodné p. H – pufr • • Vhodná iontová síla Ztužovadlo

Bohatá média • • • Pepton, Trypton = bílkovinný hydrolyzát (zdroj C i N) Kvasničný extrakt (yeast extract) = zdroj minerálů, lipidů, N, C … přírodní živiny – maso, krev, listí…

Selektivní média • Negativní selekce – přídavek látek, které brzdí růst jiných mikroorganismů – antibiotika – barviva • Pozitivní selekce – živiny využitelné jen menšinou organismů (neobvyklé) – zdroj uhlíku (uhlovodíky, polysacharidy, CO 2…) – zdroj dusíku (dusičnany, plynný dusík…) – ostatní

Selektivita médií • Negativní selektivita = nežádoucí MO jsou inhibovány vhodným způsobem – – inhibiční látka (antibiotika, toxiny) osmotická hladina extrémnější podmínky (p. H, teplota) …
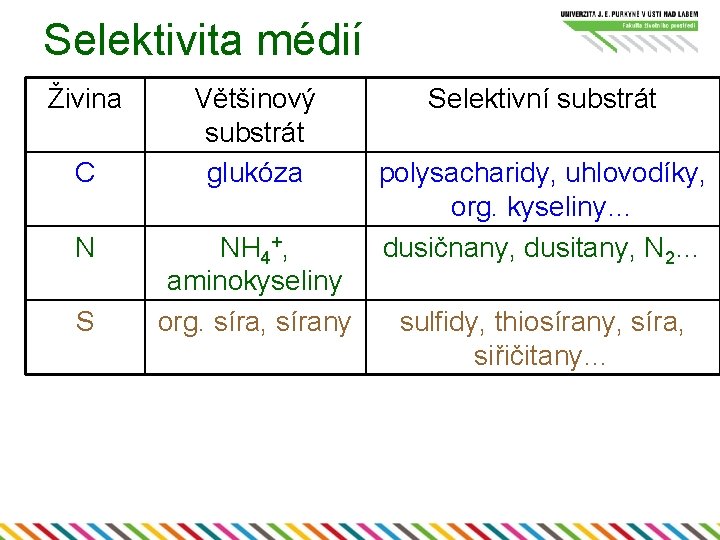
Selektivita médií Živina C N S Většinový substrát glukóza NH 4+, aminokyseliny org. síra, sírany Selektivní substrát polysacharidy, uhlovodíky, org. kyseliny… dusičnany, dusitany, N 2… sulfidy, thiosírany, síra, siřičitany…

Ztužování • • Nejčastěji přídavek 1 -2% agaru do tekutého média Agar = polysacharid (polygalaktóza) – – z mořských řas taje při 96°C tuhne při 40°C většina MO ho neumí využít jako živinu

Ztužená média • Misky • Zkumavky (šikmý agar)

Sterilace médií • • Živná média je nutno zbavit všech nežádoucích MO = sterilace autoklávování – mokré teplo pod tlakem – obvykle 100 -120°C, 0, 1 -0, 2 MPa, 15 -120 min • • filtrování – pro média citlivá na teplo přídavek mikrobicidních látek – antibiotika, ethanol…

Sterilace pevných médií • • • Agar tuhne při 40°C Sterilace v autoklávu Rozlití do cílových nádob při vhodné teplotě (50 -70°C)

Metody kvantifikace MO • • MO jsou malé, přímé počítání je obtížné Počítání pod mikroskopem – na speciálních sklíčkách s počítací komůrkou – obvykle po obarvení • • • Spektrofotometricky – rozptyl světla Kultivačně – jen životaschopné Biochemicky – podle chemických látek (bílkoviny, DNA, lipidy) – metabolickou činností (respirace…)

Bürkerova komůrka • • • Mikroskopické sklíčko s oddělenými komůrkami o přesném objemu Spočítá se průměrný počet buněk ve čtverci a přepočte se na celkovou koncentraci Bakterie je vhodné obarvit

Bürkerova komůrka
Bürkerova komůrka

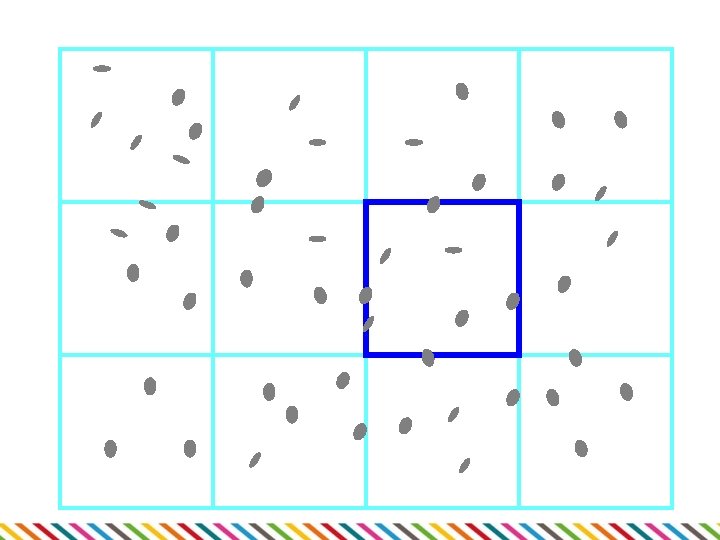
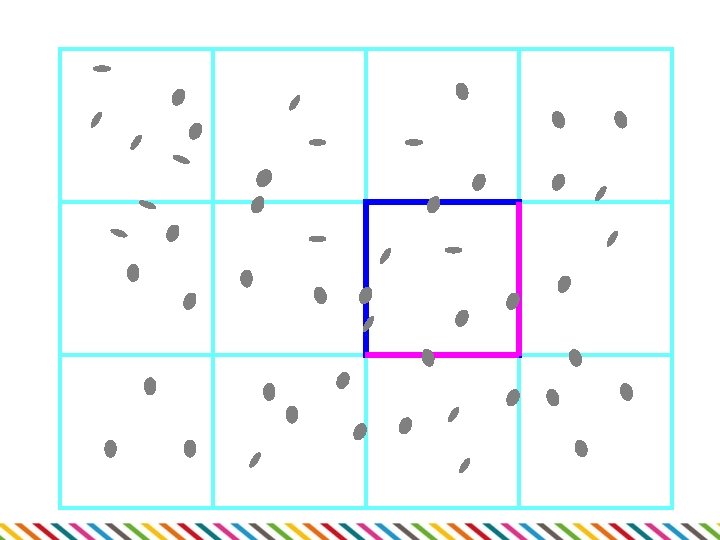
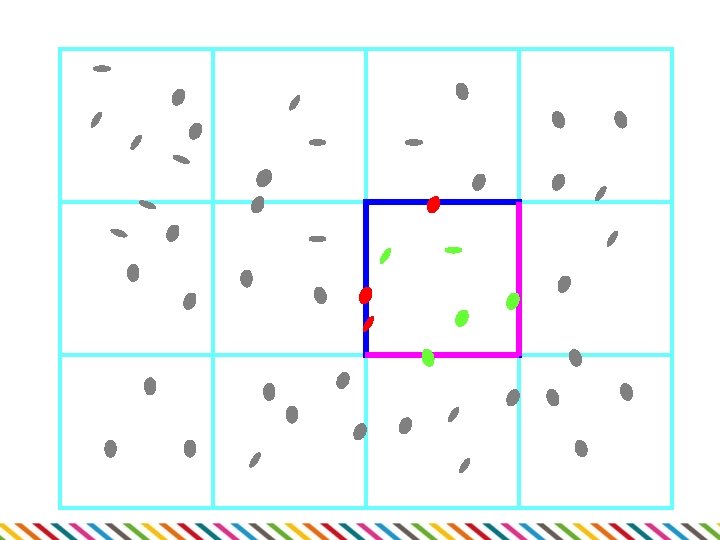
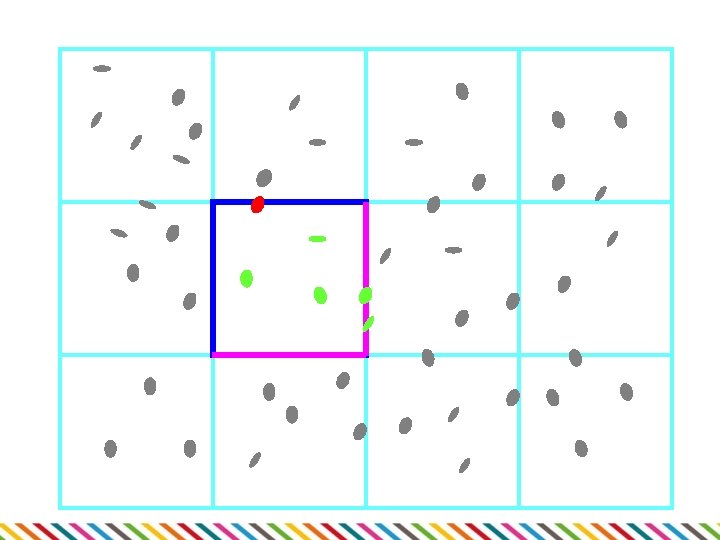

Spektrofotometrické stanovení • • Pro suspenze mikroorganismů Část světla se rozptýlí v kyvetě – vyšší hustota = větší rozptyl • Měření prošlého světla, výpočet absorbance • • • Spektrofotometr Obvyklé vlnové délky 500 -700 nm Lineární jen do A=1, pak nutno ředit
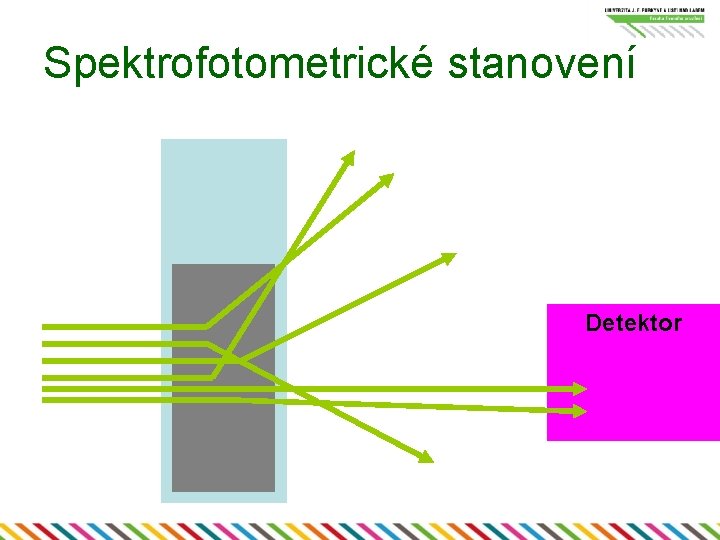
Spektrofotometrické stanovení Detektor

Kultivační stanovení • • Buněčná suspenze se zředí a rozetře na agarové médium Z každé životaschopné buňky vyroste jedna viditelná kolonie Kolonie se sečtou a přepočítají na původní objem Tzv. Colony Forming Units (CFU) – Kolonie tvořící jednotky (KTJ) • Použitím selektivního média je možné stanovit jen vybrané skupiny MO

Biochemická stanovení • Obsah některých látek přibližně koreluje s množstvím MO – obsah dusíku – obsah bílkovin – vybrané lipidy • Je vždy nutná kalibrace pro dané stanovení

Izolace MO • • V prostředí jsou MO přítomné ve společenstvech Izolace je založena na ředění a kultivaci – z jednoho MO jedna kolonie !!!!! Předpokládá se, že dnešními metodami je kultivovatelných jen několik procent všech mikrobiálních druhů!!!!

Metody identifikace MO • Morfologické – tvar těla a orgánů • Metabolické – produkce či přeměna některých látek • • Imunologické Biochemické – identifikační molekuly (mastné kyseliny, sacharidy…) • Genetické – sekvence DNA / RNA – zastoupení bazí

Morfologické znaky • • Málo přesné Význam hlavně u eukaryot (plísně, prvoci) – tvar mycelia – způsob dělení – fruktifikační orgány • U bakterií málo používané – hodně druhů a málo tvarů – tvar buněk (koky, tyčinky…) – grampozitivita

Metabolické metody • Hlavně u prokaryot (eukaryota mají velmi unifikovaný metabolismus) – produkce či využití látek – auxotrofie – anaerobní růst • U kvasinek testování kvasných schopností – zda vůbec – které sacharidy • Produkce extracelulárních enzymů

Imunologické metody • • • Reakce s protilátkami Hlavně u patogenních MO U některých druhů MO dělení na tzv. sérotypy (sérovary)

Biochemické metody • • • Různé látky mají různou strukturou a zastoupení u různých skupin MO Spektrum = procentuální zastoupení jednotlivých složek směsi identifikačních látek Markery = látky vyskytující se jen u určité skupiny organismů – např. ergosterol u hub • Fingerprint = otisk palce – metoda, která umožňuje jednoznačnou identifikaci MO dle skupiny látek

Profily mastných kyselin • Složení membránových mastných kyselin závisí na: – taxonomické skupině – teplotě – složení média • Za konstantních podmínek je možné profily MK použít k identifikaci

Profily mastných kyselin 1. Kultivace MO za definovaných podmínek • • chudé médium konstantní teplota 2. Izolace lipidů 3. Rozklad lipidů 4. Esterifikace MK • =zvýšení těkavosti 5. Analýza na plynovém chromatografu

Společenstva 1. Extrakce fosfolipidů z přírodního materiálu (půda, listí…) 2. Rozklad fosfolipidů 3. Chromatografické měření spektra • zastoupení jednotlivých MK odpovídá přítomnosti určitých skupin MO – houby, bakterie, G+, G-, mykorhizní houby… – např. suma 10 Me 16: 0, 10 Me 17: 0, 10 Me 18: 0 odpovídá zastoupení aktinomycet

Pyrolýza • • • Fingerprint metoda pro identifikaci druhu (kmene) popř. společenstva Zahřátí kultury MO na cca 1000°C rozklad organických látek Analýza kapalinovou chromatografií

Genetické metody • • • Nejperspektivnější Rychlý rozvoj Zohledňují fylogenetické vztahy možnost zařazení do taxonomického systému Možnost izolace úseků DNA specifických pro určité taxonomické skupiny MO (bakterie, houby, G+…) Obvykle fingerprint metody
- Slides: 48