Bevacizumab y ranibizumab para degeneracin macular Presentacin de

Bevacizumab y ranibizumab para degeneración macular Presentación de la experiencia de Brasil II Encuentro de Acceso, Monitoreo y Regulación Económica del Mercado de Medicamentos Organización Pan Americana de la Salud (OPS/OMS) Ministerio de Salud y Acción Social de Argentina 6 de noviembre de 2018

Historia y antecedentes La degeneración macular relacionada con la edad (DMRE) • Daño o fallo de la mácula - visión de colores y distinción de detalles • Lesión a la mácula causa pérdida progresiva de la visión central (perjudica la lectura y actividades más refinadas) • El principal factor de riesgo es el envejecimiento • Causa importante de ceguera • Se clasifica en sequía (79% de los casos) y húmeda • La forma seca no es tratable • La forma húmeda - el mecanismo más probable de lesión implica la neovascularización y el proceso inflamatorio • Factor de crecimiento del endotelio vascular (VEGF) - neovascularización, aumento de la permeabilidad vascular, proceso inflamatorio. • Medicamentos que inhiben el VEGF - principal conducto terapéutico

Historia y antecedentes Inhibidores de la angiogénesis en la DMRE Medicamentos que inhiben el factor de crecimiento del endotelio vascular Hay tres medicamentos registrados para DMRE - pegaptanib sódico, ranibizumab y aflibercepte - están disponibles como inyección intravítrea (intraocular) Sin embargo, en 2004 investigadores de la Universidad de Miami (Rosenfeld y colaboradores), tras la aprobación de la FDA para cáncer de colon y recto, evaluaron el medicamento por vía intravenosa en 18 pacientes con DMRE húmeda observando una mejora de la enfermedad. El uso por vía intravenosa aumentaba el riesgo de infarto y accidente vascular cerebral y aún de alto costo Se evalúa la utilización intraocular con dosis menores (1, 25 mg / 0, 05 m. L) obteniéndose buenos resultados (dos relatos de caso)

Historia y antecedentes Las dosis menores disminuyen el riesgo de eventos cardiovasculares y principalmente el costo de tratamiento en relación a ranibizumab. Ampliación del acceso Se comprobó la no inferioridad de bevacizumab en relación a ranibizumab (estudios controlados aleatorizados de buena calidad metodológica). Sin embargo, la empresa productora del medicamento no lo registra para la DMRE El medicamento se ha utilizado como offlabel

Contexto político y legal en Brasil (Leyes 8. 080 / 90 y 12. 401 / 2011) Sistema único de salud (SUS) (universal) Conjunto de acciones y servicios de salud prestados por el poder público en las esferas federal, estadual y municipal y de forma complementaria por la iniciativa privada; Acciones y servicios de salud están garantizados por la formulación y ejecución de políticas sociales y económicas; Es parte del campo de actuación del SUS la oferta de asistencia terapéutica integral, inclusive farmacéutica; La oferta de medicamentos y productos de interés para la salud se dará preferentemente de acuerdo con Guías de Práctica Clínica para la enfermedad o agravio a la salud a ser tratado; Las tecnologías sanitarias que componen estas Guías serán evaluadas en cuanto a eficacia, seguridad, efectividad y costo-efectividad para las diferentes fases evolutivas de la enfermedad o del agravio a la salud de que trata el protocolo;

Contexto político y legal (Leyes 8. 080 / 90 y 12. 401 / 2011) • La decisión sobre la financiación de tecnologías sanitárias (cobertura) es prerrogativa del Ministerio de Salud con asesoramiento de Conitec • Conitec evalúa tecnologías en salud y emite recomendaciones sobre la eficacia, seguridad, efectividad y costo-efectividad en relación a las conductas ya incorporadas al SUS. • Paralelamente la oferta de servicios de salud es libre a la iniciativa privada (mercado regulado por la Agencia Nacional de Salud - ANS).

Situación de los medicamentos en Brasil Bevacizumab - aprobado para uso como antineoplásico, no está aprobado para el uso en degeneración macular (registrado en 2005). Brasil sólo un producto registrado. Estados Unidos (FDA) (biosimilación - bevacizumab-awwb) y Europa (EMA) (bevacizumab) - también aprobados para su uso como antineoplásico. Forma farmacéutica - solución para dilución para infusión intravenosa (25 mg / ml) - 4 m. L y 16 m. L Precio fábrica (CMED) - frasco ampolla con 4 m. L (25 mg / ml) - R$ 1. 339, 76 (US $ 340) a R$ 1. 674, 70 (US $ 425) (dependiendo del estado de la federación) Ranibizumab - aprobado para el tratamiento de la degeneración macular neovascular (exudativa o neovascular) relacionada a la edad (DMRE) (registro en 2007). Sólo un producto registrado en Brasil. No hay biosimilares registrados en los Estados Unidos o Europa. Forma farmacéutica - solución o jeringa rellenada para inyección intraocular (10 mg / ml) - 0, 165 ó 0, 23 m. L Precio fábrica (CMED) - R $ 3. 139, 76 (US $ 798) a R $ 3. 924, 69 (US $ 997).

Tratamiento de la degeneración macular neovascular (exudativa o húmeda) en Brasil por el sistema público de salud (SUS) Aún no se hace la oferta de medicamentos biológicos Historia de las acciones del Ministerio de Salud Evaluación de las tecnologías Aspectos legales del uso offlabel de bevacizumabe Elaboración de Guía de Práctica Clinica para DMRE Elaboración de Guía para el uso de bevacizumabe Elaboración de un plan de farmacovigilancia

Evaluación de las tecnlogías 1. Evaluación de ranibizumab a pedido de la empresa productora Sumisión y evaluación en 2012 Indicación pleiteada: degeneración macular neovascular (exudativa o húmeda) relacionada con la edad. Comparación: con placebo y bevacizumab Desfechos clínicos evaluados: agudeza visual, seguridade Estudio económico: costo-utilidade Impacto presupuestario.

Resultados de eficacia: Desfecho: agudeza visual (ranibizumab vs bevacizumab): Estudio CATT 1 (EE. UU. , n = 1. 107) - estudio de no inferioridad. Desfecho primario: cambio en la agudeza visual. Estudio de buena calidad metodológica. Dosis: 0, 5 mg de ranibizumab (0, 05 m. L de inyección intraocular) y 1, 25 mg bevacizumab (0, 05 m. L de inyección intraocular) 1. CATT - Comparison of Age-related Macular Degeneration Treatments Trials (CATT) Research Group, Martin DF, Maguire MG, Fine SL, Ying GS, Jaffe GJ, Grunwald JE, Toth C, Redford M, Ferris FL 3 rd. Ranibizumab and bevacizumab for treatment of neovascular age-related macular degeneration: two-year results. Ophthalmology. 2012 Jul; 119(7): 1388 -98. doi: 10. 1016/j. ophtha. 2012. 03. 053. Epub 2012 May 1. Pub. Med PMID: 22555112; Pub. Med Central PMCID: PMC 3389193.

Resultados de seguridad: Ranibizumab vs. bevacizumab: Estudio CATT 1 Mortalidad no fue diferente Aumento en la frecuencia de eventos adversos sistémicos graves (RR 1, 30, IC 95% 1, 07 a 1, 57, p = 0, 009) Estudio IVAN 2 (n = 610) No hubo diferencia en la proporción de eventos adversos sistémicos graves (OR 1, 35, IC 95% 0, 80 -2, 27, p = 0, 25). Menor tendencia a ranibizumab. 1. CATT - Comparison of Age-related Macular Degeneration Treatments Trials (CATT) Research Group, Martin DF, Maguire MG, Fine SL, Ying GS, Jaffe GJ, Grunwald JE, Toth C, Redford M, Ferris FL 3 rd. Ranibizumab and bevacizumab for treatment of neovascular age-related macular degeneration: two-year results. Ophthalmology. 2012 Jul; 119(7): 1388 -98. doi: 10. 1016/j. ophtha. 2012. 03. 053. Epub 2012 May 1. Pub. Med PMID: 22555112; Pub. Med Central PMCID: PMC 3389193. 2. IVAN Study Investigators, Chakravarthy U, Harding SP, Rogers CA, Downes SM, Lotery AJ, Wordsworth S, Reeves BC. Ranibizumab versus bevacizumab to treat neovascular age-related macular degeneration: one-year findings from the IVAN randomized trial. Ophthalmology. 2012 Jul; 119(7): 1399 -411. doi: 10. 1016/j. ophtha. 2012. 04. 015. Epub 2012 May 11. Erratum in: Ophthalmology. 2012 Aug; 119(8): 1508. Ophthalmology. 2013 Sep; 120(9): 1719. Pub. Med PMID: 22578446.
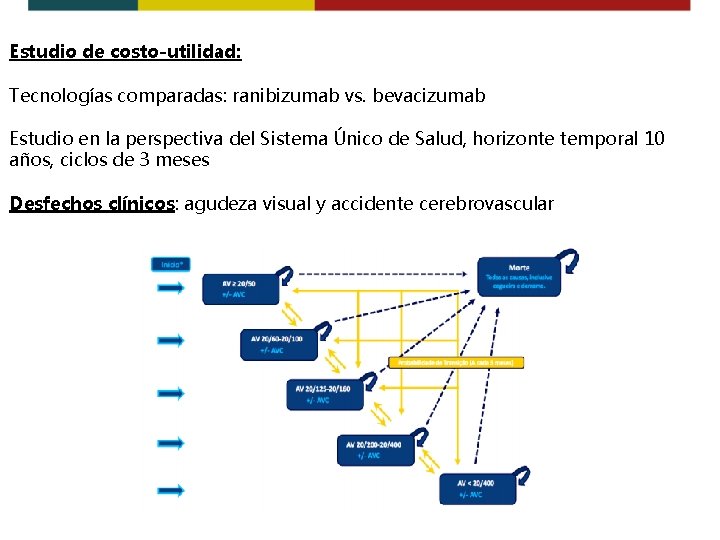
Estudio de costo-utilidad: Tecnologías comparadas: ranibizumab vs. bevacizumab Estudio en la perspectiva del Sistema Único de Salud, horizonte temporal 10 años, ciclos de 3 meses Desfechos clínicos: agudeza visual y accidente cerebrovascular

Estudio de costo-utilidad: Estructura de costes: Cálculo del coste del tratamiento por dosis No considerando el fraccionamiento de dosis: bevacizumab ampolla de 4 m. L (R$ 964, 98 - US$ 247) y ranibizumab ampolla de 0, 23 m. L (R$ 777, 00 - US$ 200). Efectividad incremental = sin diferencia Costo incremental = favorece ranibizumab Ranibizumab es dominante Considerando el fraccionamiento de dosis: 1 ampolla de bevacizumab (4 m. L) = 40 dosis 1 ampolla de ranibizumab (0, 23 m. L) = 2 dosis Efectividad incremental = sin diferencia Costo incremental = favorece bevacizumabe Bevacizumab es dominante

Impacto presupuestario El impacto presupuestario, en el escenario en cinco años y considerando el fraccionamiento de 4 dosis por frasco de 0, 3 ml de ranibizumab y de 40 dosis por vial de 4 ml de bevacizumab, fue de R$ 300. 949. 504, 64 para el ranibizumab y R$ 50. 236. 922, 63 para bevacizumab. No se consideraron los costes de aplicación y seguimiento, ya que son similares a los dos medicamentos Se recomienda la cobertura de bevacizumab 2ª sumisión en 2015 - reducción de precio y propuesta para aumento de volumen de la forma farmacéutica (4 dosis). Sin embargo, el precio por dosis permanecía un 50% mayor que para bevacizumab (1 frasco = 40 dosis). La recomendación se mantuvo negativa. Otros estudios publicados GEFAL (Francia) y MANTA (Austria) - refuerzan la no inferioridad

2. Aspectos legales de uso offlabel de bevacizumabe CONITEC solicita a la ANVISA autorización de uso off-label del bevacizumab en el marco del SUS para viabilizar el suministro del medicamento para tratamiento de la DMRE, con base en el art. 21 del Decreto nº 8. 077, de 14/08/2013, que establece: Art. 21. Mediante solicitud de la Comisión Nacional de Incorporación de Tecnologías en el SUS - Conitec, Anvisa podrá emitir autorización de uso para el suministro, por el SUS, de medicamentos o de productos registrados en los casos en que la indicación de uso pretendida sea distinta de aquella aprobada en el registro, siempre que demostradas por Conitec las evidencias científicas sobre la eficacia, exactitud, la efectividad y la seguridad del medicamento o del producto para el uso pretendido en la solicitud. La Comisión Científica en Vigilancia Sanitaria - CCVISA analizó el mérito de la solicitud, dando lugar a la Resolución de la Junta Directiva de la ANVISA - RDC nº 111, de 06/09/2016, que autorizó el uso excepcional, en carácter temporal, En el tratamiento de la DMRE, permitiendo al Ministerio de Salud dar curso a la elaboración de la Guía de Práctica Clínica de la DMAE y la Guía de Uso del medicamento. El tratamiento, cuando está disponible, será autorizado en un número reducido de Centros Especializados, que serán habilitados por el Ministerio de Salud, una vez comprobada la capacidad de los mismos para realizar el fraccionamiento del producto

Directiva de la ANVISA - RDC nº 111, de 06/09/2016 El uso de bevacizumab está condicionado: I - A la utilización de acuerdo con la Guía de Práctica Clínica para DMRE, del Ministerio de Salud (MS); II - A la utilización de acuerdo con el Protocolo de Uso del Medicamento, del MS. III - A la administración del medicamento exclusivamente en los establecimientos de atención especializada en oftalmología, habilitados por el MS, y regularizados ante la Vigilancia Sanitaria de la Secretaría de Estadual o Municipal de Salud; IV - Al cumplimiento, en lo que sea aplicable, de las buenas prácticas de manipulación y fraccionamiento, conforme a la Resolución de la Junta Directiva - RDC nº 67, de 8 de octubre de 2007 y Resolución del Directorio Colegiado - RDC nº 80, del 11 de mayo de 2007 y sus modificaciones; y V - A la firma, por parte del paciente o responsable, del consentimiento libre y esclarecido, con las principales informaciones sobre el procedimiento y el uso

3. Elaboração de Guías de Práctica Clínica 3. Elaboración de Guía de Práctica Clínica Participación de dos Secretarías del Ministerio de Salud - Secretaría de Ciencia, Tecnología e Insumos Estratégicos (SCTIE) y Secretaría de Atención a la Salud (SAS). Subcomisión de Protocolos (SCTIE) acciona grupo elaborador - revisión sistemática y organización de las líneas de cuidado (consulta a expertos). • Establece criterios de inclusión y exclusión (criterios diagnósticos) • Algoritmo de tratamiento (dosis adecuadas) • Monitoreo de la eficacia y la seguridad Paralelamente se organiza el Guía de uso del bevacizumab • El tratamiento debe ser conducido en servicios de oftalmología con estructura adecuada. • El medicamento debe ser fraccionado en área controlada, destinada a la preparación de antineoplásicos inyectables. • Medidas para minimizar los riesgos de pérdida de estabilidad y esterilidad después del fraccionamiento (RDC n ° 67 Anvisa - Buenas Prácticas de Manipulación).

• Los sujetos tratados deben ser monitorizados por exámenes clínicos para evaluar la eficacia del tratamiento y el perfil de seguridad (local y sistémico). • Tiempo máximo de utilización, número de dosis por frasco, rango de temperatura, acciones para minimización de riesgos, informaciones pacientes y profesionales de salud Secretaría de Atención a la Salud (SAS) • Determinación del valor de resarcimiento del procedimiento de aplicación de la dosis fraccionada • Determinación del promedio de fraccionamiento viable para atender a todas las unidades de la federación • Organización de los servicios especializados en oftalmología

4. Farmacovigilância Las notificaciones de reacciones adversas por el uso de bevacizumab son obligatorias La notificación es responsabilidad del: I - Profesional de salud que ejecutó el procedimiento; II - Establecimiento de atención especializada en oftalmología donde se realizó el procedimiento; III - Establecimiento de salud que haya atendido la ocurrencia, posterior al procedimiento; IV - Titular del registro del medicamento. La empresa somete a Anvisa: I - Plan de Minimización de Riesgo (PMR) para el medicamento II - Informe Periódico de Farmacovigilancia (RPF), con el relato de todas las ocurrencias que llegaron a su conocimiento, entregado semestralmente durante el período de validez de la autorización de uso excepcional.

4. Farmacovigilância La autorización de uso excepcional tendrá validez por 3 (tres) años y podrá ser renovada por períodos iguales y sucesivos. La renovación se dará a partir de nueva solicitud del MS y con base en la reevaluación de evidencias técnicas, científicas y de farmacovigilancia, 6 (seis) meses antes de la extinción de la autorización de uso excepcional concedida. En cualquier momento, incluso dentro del plazo establecido en el caput, la autorización de uso excepcional podrá ser modificada, suspendida o revocada, por razones técnicas y científicas o sobre la base de la información procedente de la farmacovigilancia. Para subsidiar el proceso de revalorización, Anvisa podrá solicitar, en cualquier momento, informaciones sobre el uso del medicamento al MS ya la empresa.

¡ Gracias !
- Slides: 22