Bases de qumica general Trminos importantes Materia Todo

Bases de química general

Términos importantes Materia : Todo aquello que tiene una masa y ocupa un lugar en el espacio. Masa: Cantidad de materia en un objeto. Sustancia: Es la clase de materia de la que están formados los cuerpos

Términos importantes Sustancia pura: Sustancia que no se puede descomponer en otras mediante procedimientos físicos. Elemento: Sustancia pura compuesta por un solo tipo de átomo. Compuesto: Sustancia formada por dos o más tipos de átomos unidos químicamente (moléculas). Posible separar sus componentes por métodos químicos

Términos importantes Mezcla: Resultado de la combinación de varias sustancias puras. Posible su separación mediante procedimientos físicos (destilación, evaporación, suspensión y filtración) y mecánicos (decantación, e imantación). ◦ Mezcla homogéneas: Componentes no visibles (pe. Soluciones) ◦ Mezcla heterogéneas: Componentes visibles
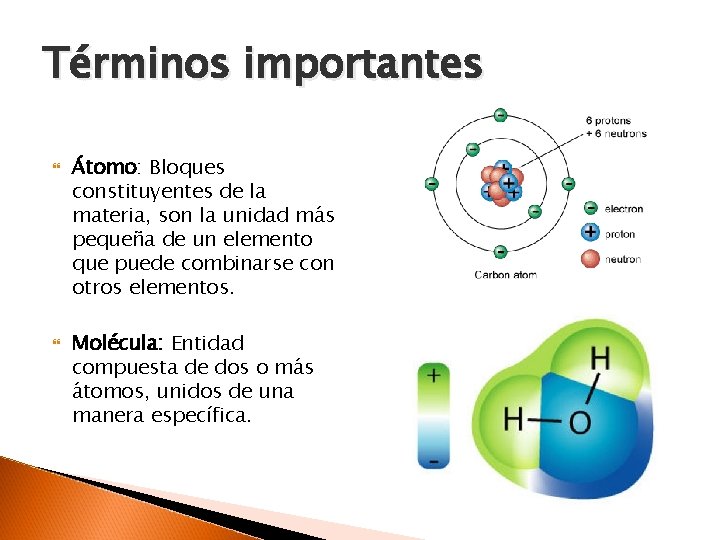
Términos importantes Átomo: Bloques constituyentes de la materia, son la unidad más pequeña de un elemento que puede combinarse con otros elementos. Molécula: Entidad compuesta de dos o más átomos, unidos de una manera específica.

Materia La química es el estudio de la composición, estructura, propiedades y cambios de la materia. La composición de la materia se relaciona con el tipo de elementos que contiene. La estructura de la materia se relaciona con la forma en que se organizan sus átomos.
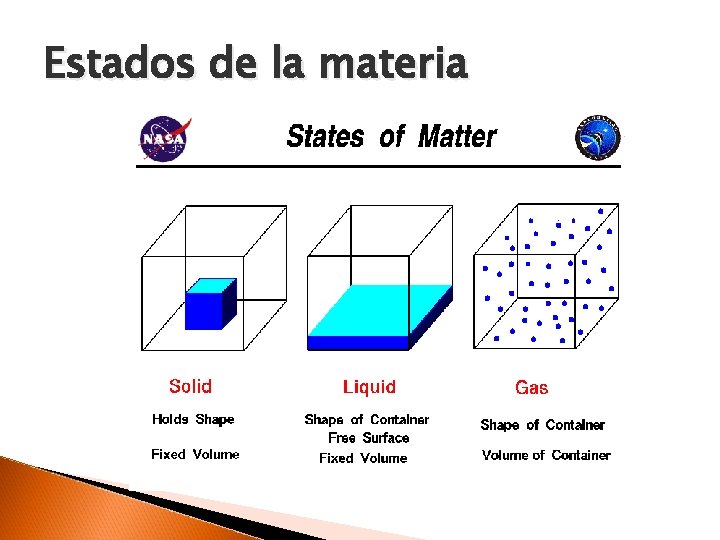
Estados de la materia
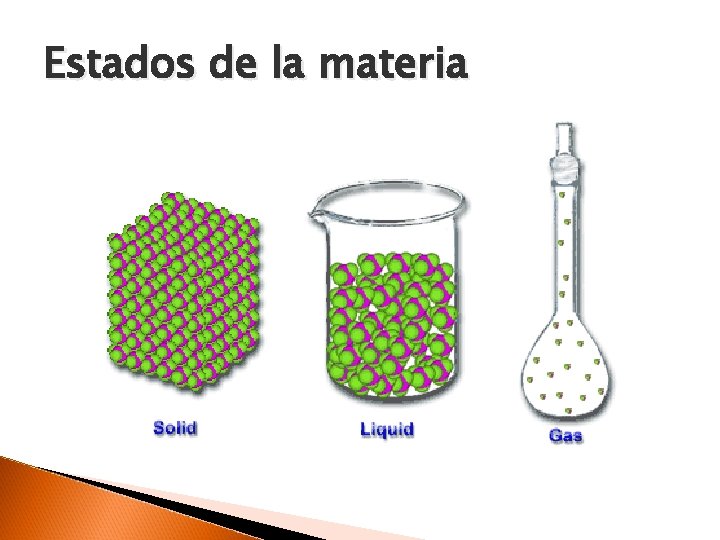
Estados de la materia

Medidas Sistema internacional (SI) ◦ ◦ ◦ Longitud: Metro (m) Masa: Kilogramo (Kg) Tiempo: Segundo (s) Temperatura: Kelvin (K) Cantidad de sustancia (mol) Medidas derivadas ◦ Volumen: Espacio ocupado por un cuerpo (m 3) ◦ Densidad: Masa/volumen (Kg/m 3)
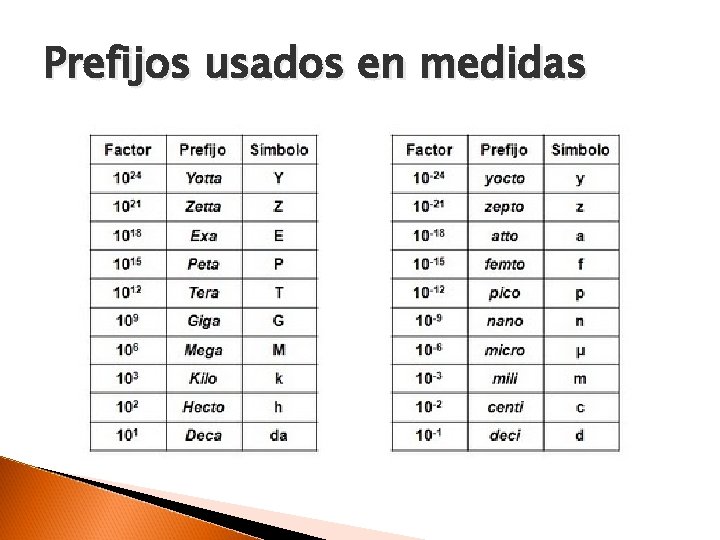
Prefijos usados en medidas
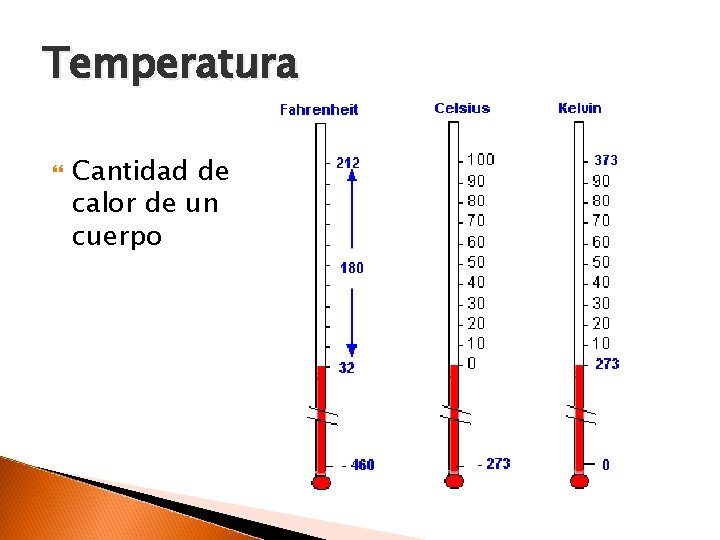
Temperatura Cantidad de calor de un cuerpo

Temperatura Interrelación de las unidades de medida ◦ K= °C + 273. 15 ◦ °C = (5/9)(°F-32) ◦ °F = (9/5)(°C) +32 ◦ Ej: 120°C→K ◦ 120°C→°F K=120°C + 273. 15 = 393. 15°C °F=(9/5)(120°C) + 32 = 248°C

Factores de conversión Si una mujer tiene una masa de 65 Kg, cual es su masa en gramos, y en libras? 1 lb=454 g 65 Kg X 1000 g/1 Kg = 65000 g 65 Kg X 1000 g/1 Kg X 1 lb/454 g=143, 2 lb

Factores de conversión ¿Cuantas pulgadas mide una varilla de 8 m? (1 pulg=2. 54 cm) 1 m=100 cm 8 m X 100 cm/1 m X 1 pulg/2. 54 cm= 315 pulg

Factores de conversión ¿Cuál es la masa en gramos de dos pulgadas cúbicas (2 pulg 3) de oro, el cual tiene una densidad de 19. 3 g/cm 3. (2. 54 cm/1 pulg) 3 = 16. 39 cm 3/1 pulg 3 2 pulg 3 X 16. 39 cm 3/1 pulg 3 X 19. 3 g/cm 3= 633 g
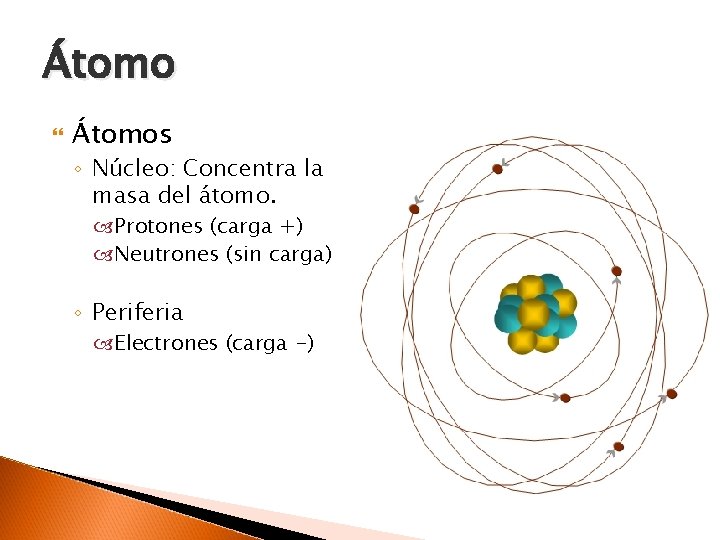
Átomo Átomos ◦ Núcleo: Concentra la masa del átomo. Protones (carga +) Neutrones (sin carga) ◦ Periferia Electrones (carga -)
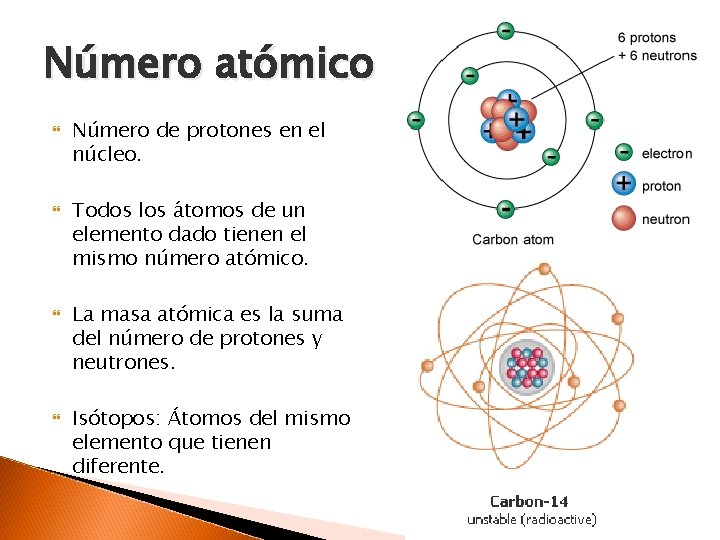
Número atómico Número de protones en el núcleo. Todos los átomos de un elemento dado tienen el mismo número atómico. La masa atómica es la suma del número de protones y neutrones. Isótopos: Átomos del mismo elemento que tienen diferente.

La tabla periódica de los elementos clasifica, organiza y distribuye los distintos elementos químicos, conforme a sus propiedades y características. Los elementos con propiedades similares se sitúan en columnas verticales (Grupo periódico).
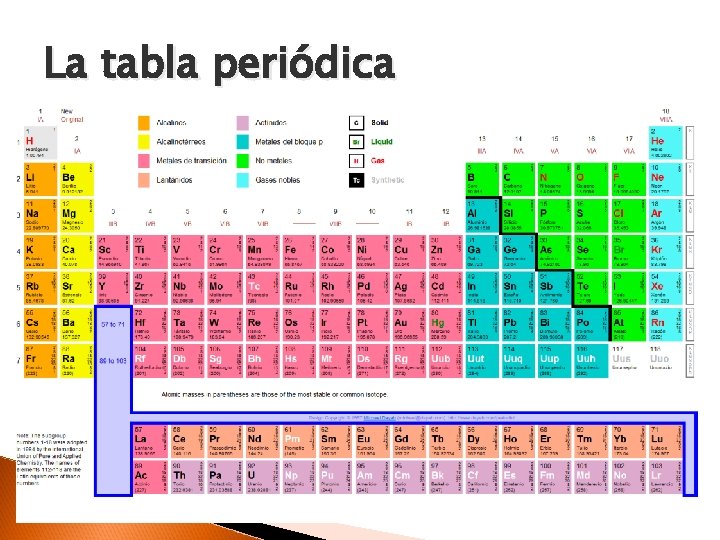
La tabla periódica

Moléculas Los átomos se combinan por enlaces químicos para formar moléculas. Tipos de enlace ◦ Enlace iónico: Unión que resulta de la presencia de fuerzas de atracción electrostática entre los iones de distinto signo. ◦ Enlace covalente: Unión que resulta cuando dos átomos comparten uno o más pares electrónicos.
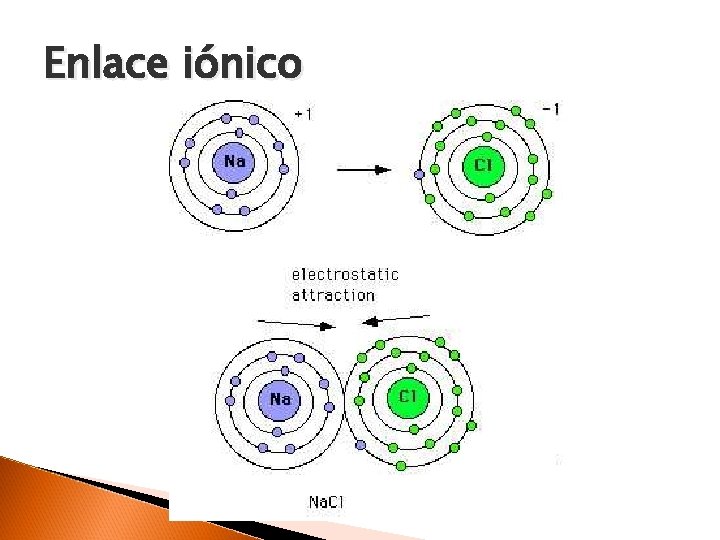
Enlace iónico
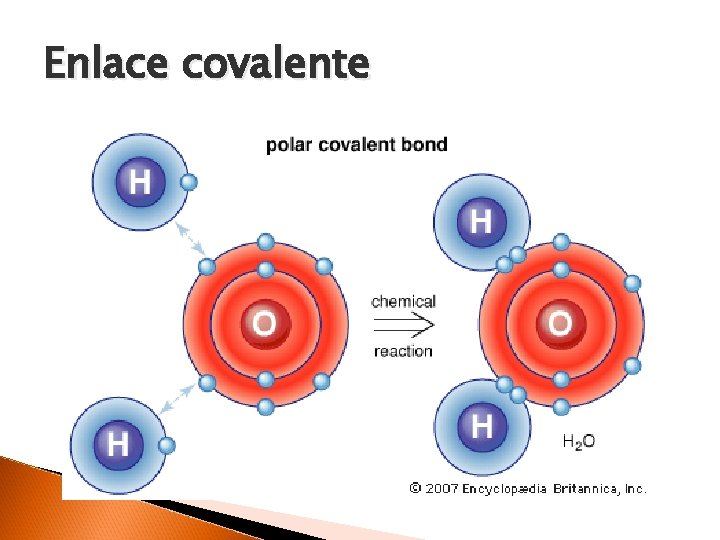
Enlace covalente
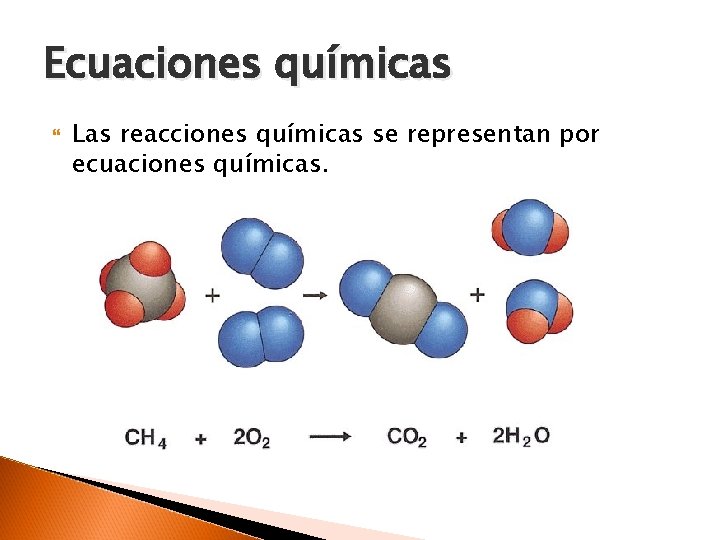
Ecuaciones químicas Las reacciones químicas se representan por ecuaciones químicas.

Ley de la conservación de la masa La masa total de los productos es la misma que la masa total de los reactivos. El mismo número de átomos de cada tipo están presentes antes y después de la reacción. 2 H 2 +O 2 → 2 H 2 O CH 4 + 2 O 2 → CO 2 + 2 H 2 O

Balanceo de las ecuaciones Na + H 2 O → Na. OH + H 2 2 Na + 2 H 2 O → 2 Na. OH + H 2 C 2 H 4 + O 2 → CO 2 + H 2 O C 2 H 4 + 3 O 2 → 2 CO 2 + 2 H 2 O Al + HCl → Al. Cl 3 + H 2 2 Al + 6 HCl → 2 Al. Cl 3 + 3 H 2

Escala de masa atómica Unidad de masa atómica: Unidad utilizada para la medición de la masa de los átomos y moléculas. 1 u. m. a = 1. 66054 X 10 -24 g Elemento Masa atómica (u. m. a) Hidrógeno (H) 1. 00794 Oxígeno (O) 15. 9994 Nitrógeno (N) 14. 00674 Sodio (Na) 22. 989770 Plata (Ag) 107. 8682

Peso molecular Es la suma de los pesos atómicos de cada átomo en su formula química. ¿Acido sulfúrico H 2 SO 4? (H=1, S=32, O=16) H= 1 X 2 = 2 u. m. a S= 32 X 1 = 32 u. m. a O= 16 X 4 = 64 u. m. a H 2 SO 4 = 2 + 32 + 64 = 98 u. m. a

Peso molecular Calcular el peso molecular de la A) Sacarosa, C 12 H 22 O 11 B) Nitrato de calcio, Ca(NO 3)2 C=12, H=1, O=16, Ca=40, N=14 Rta. C 12 H 22 O 11 = 342 uma Ca(NO 3)2 = 164 uma

Mol Cantidad de materia que contiene tantos objetos (átomos, moléculas, etc. ) como el número de átomos en exactamente 12 g de carbono. Número de Avogadro: 6. 02 X 1023 1 mol de C = 6. 02 X 1023 átomos de C 1 mol de H 2 O = 6. 02 X 1023 moléculas de H 2 O

Masa molar La masa en gramos de una mol de atomos (o moléculas) de algún elemento (o compuesto). La masa de un solo átomo de un elemento (en amu) es numéricamente igual a la masa (en gramos) de 1 mol de atomos de ese elemento. 1 átomo de C pesa 12 amu→ 1 mol de C pesa 12 g. 1átomo de Mg pesa 24 amu→ 1 mol de Mg pesa 24 g. 1 molécula de H 2 O pesa 18 amu → 1 mol de H 2 O pesa 18 g

Masa molar Calcular el número de moles de glucosa, C 6 H 12 O 6, en 5. 380 g de esa sustancia. Rta. 0, 03 mol de C 6 H 12 O 6 ¿Cuantas moles de Na. HCO 3, hay en 508 g de esa sustancia? Rta. 6, 05 mol de Na. HCO 3 C=12, H=1, O=16, Na=23.

Masa molar Calcular la masa, en gramos, de 0. 433 moles de nitrato de calcio, Ca(NO 3)2 Rta. 71. 1 g de Ca(NO 3)2 ¿Cuál es la masa en gramos de 6. 33 moles de Na. HCO 3? Rta. 532 g de Na. HCO 3 Ca=40, C=12, H=1, O=16, Na=23, N=14.

Soluciones Mezclas homogéneas de dos o más sustancias ◦ Solvente: Componente presente en mayor cantidad. ◦ Solutos: Componentes disueltos en el solvente.
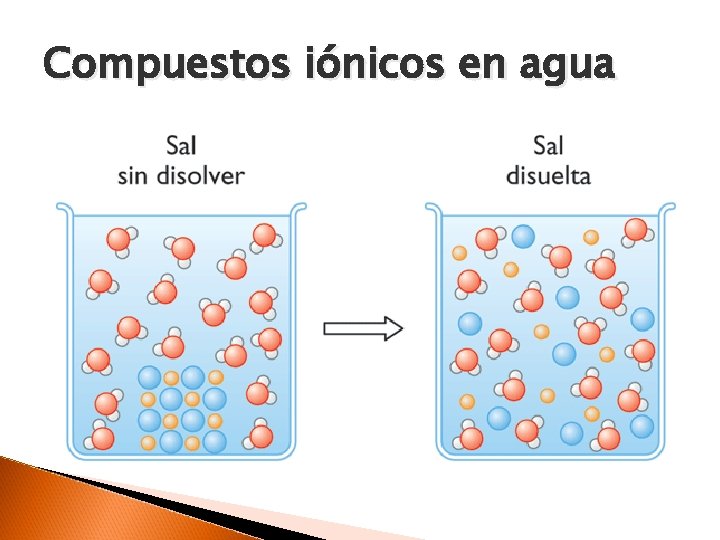
Compuestos iónicos en agua
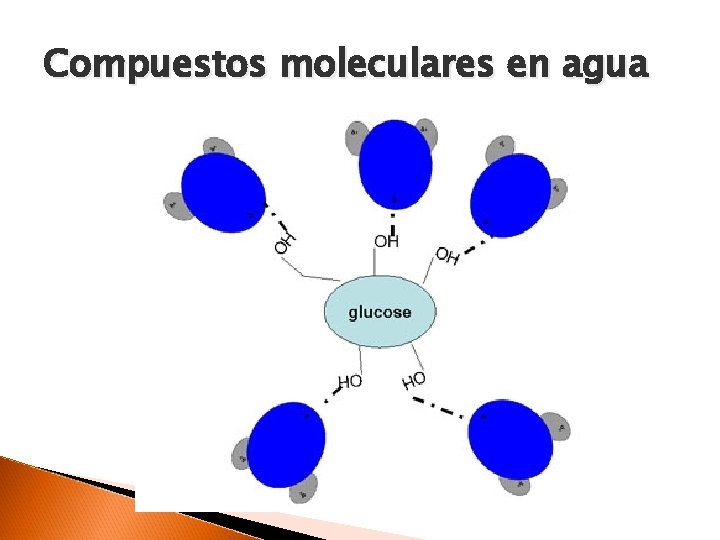
Compuestos moleculares en agua

Electrolitos Sustancias que en soluciones acuosas contienen iones y de esa forma conducen electricidad (Ej. Sal).

Solución saturada Una solución saturada es la que contiene el máximo nivel de soluto que puede disolverse en un volumen de disolvente dado. Una solución sobresaturada contiene más soluto del que puede ser disuelto en el disolvente. Una solución insaturada es aquella que tiene capacidad para disolver más soluto.

Solución saturada
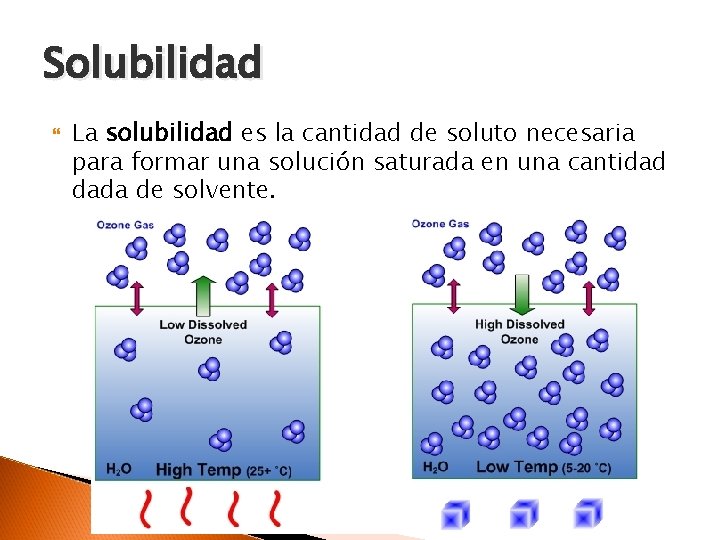
Solubilidad La solubilidad es la cantidad de soluto necesaria para formar una solución saturada en una cantidad dada de solvente.

Medidas de la concentración de soluto

Concentración Una solución es realizada por la disolución de 13. 5 g de glucosa, C 6 H 12 O 6, en 0. 100 Kg de agua. ¿Cuál es el porcentaje en masa de soluto en esta solución? (dens. H 2 O=1 g/m. L) Rta. 11. 9% Calculé el porcentaje en masa de Na. Cl en una solución que contiene 1. 50 g de Na. Cl en 50. 0 g de agua. Rta. 2. 91%

Concentración Una solución es realizada por la disolución de 4. 35 g de glucosa, C 6 H 12 O 6, en 25 m. L de agua. Calcular la molalidad de glucosa en la solución (C=12, O=16, H=1, dens. H 2 O=1 g/m. L). Rta. 0. 964 molal Calculé la molaridad de una solución hecha por la disolución de 23. 4 g de sulfato de sodio, Na 2 SO 4, en suficiente agua para formar una solución de 125 m. L (Na=23, S=32, O=16). Rta. 1. 32 Molar

Concentración ¿Cuantos gramos de Na 2 SO 4 hay en 15 m. L de una solución 0. 50 M? (Na=23, S=32, O=16) Rta. 1. 1 g ¿Cuántos mililitros de solución Na 2 SO 4 0. 50 M se necesitan para suplir 0. 038 moles de esta sal? Rta. 76 m. L

Agua
Agua
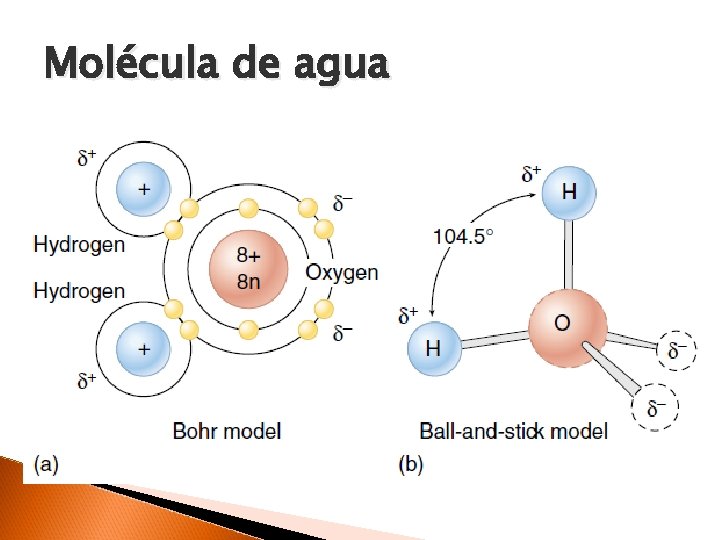
Molécula de agua
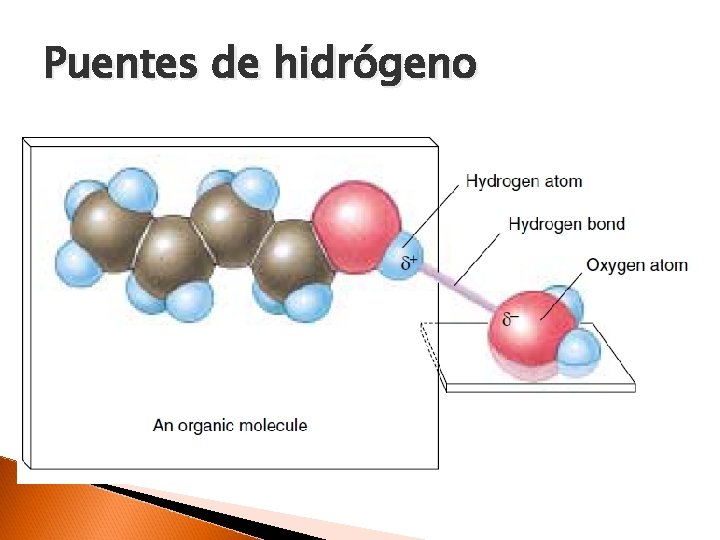
Puentes de hidrógeno

Puentes de hidrógeno Interacciones débiles generadas por la polaridad de moléculas que contienen enlaces entre O-H, N-H, y F-H. Duran 10 -11 segundos. El efecto acumulativo de muchos puentes de hidrógeno, puede ser enorme. Tiene de 5 a 10% de la fuerza de un enlace covalente. El agua genera una gran cantidad de puentes de hidrogeno entre sus moléculas y con moléculas de otros compuestos.

Propiedades del agua generadas por los puentes de hidrógeno Cohesión Alto calor específico Alto calor de vaporización Baja densidad del agua Alta polaridad

H 2 O: Cohesión Atracción entre moléculas de agua

H 2 O: Cohesión Genera la alta tensión superficial del agua
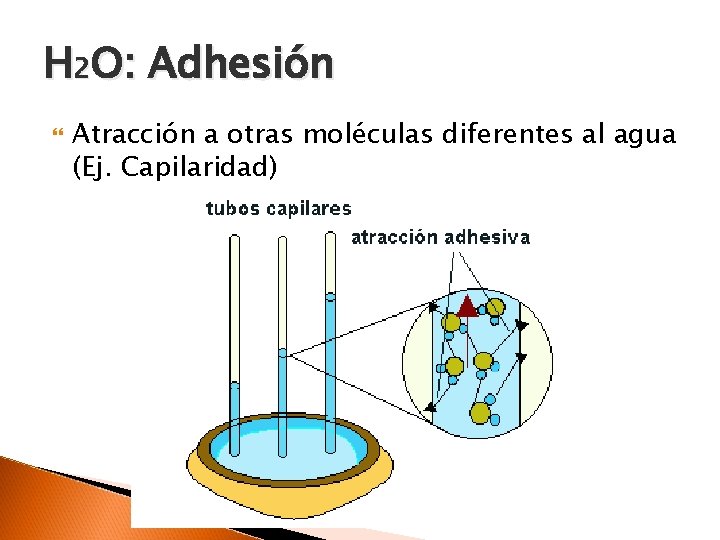
H 2 O: Adhesión Atracción a otras moléculas diferentes al agua (Ej. Capilaridad)
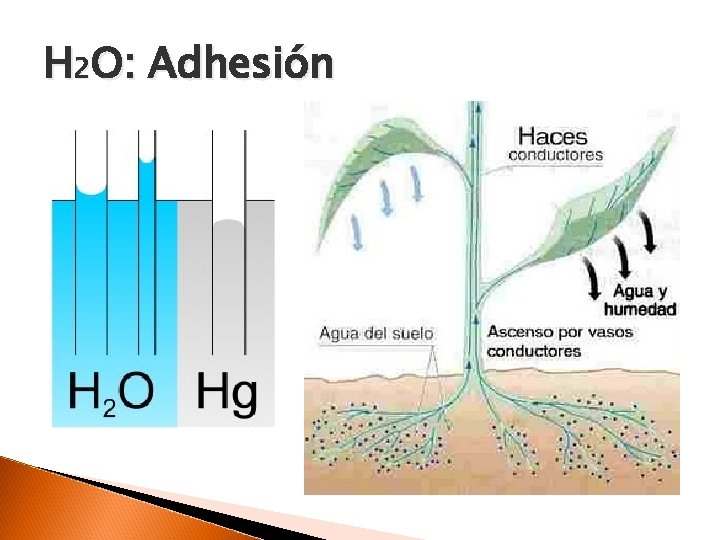
H 2 O: Adhesión

H 2 O: Alto calor específico Calor específico: Cantidad de calor que debe ser absorbida o perdida por 1 g de sustancia para cambiar su temperatura en 1°C. Entre mayor polaridad, mayor calor específico. De 0 a 100°C, solo se rompe el 20% de los puentes de hidrógeno. Alta retención de calor.
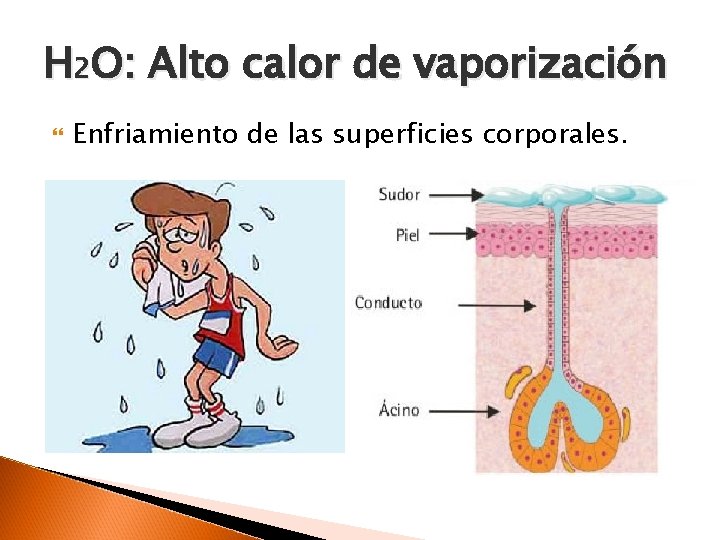
H 2 O: Alto calor de vaporización Enfriamiento de las superficies corporales.
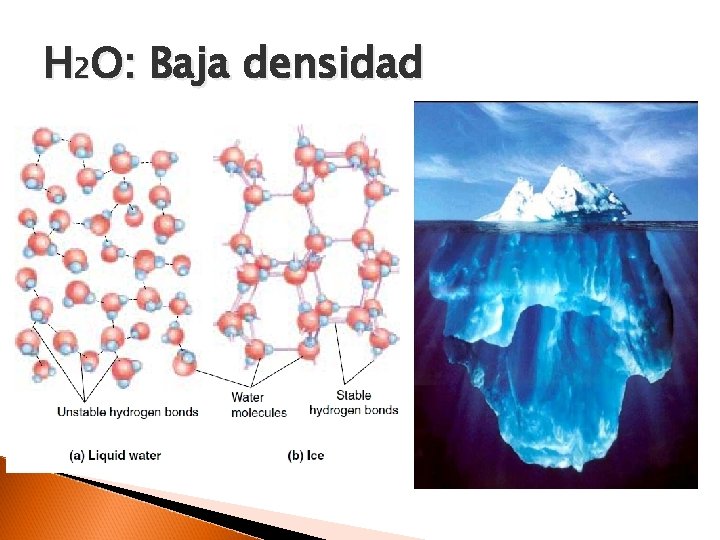
H 2 O: Baja densidad
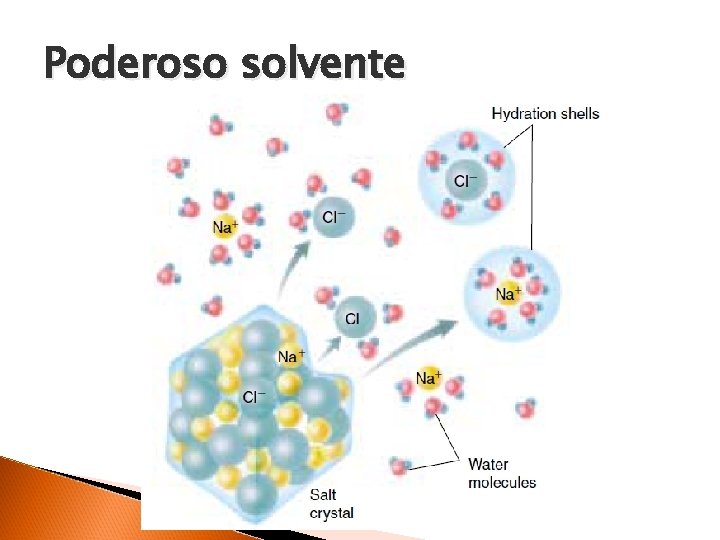
Poderoso solvente

Ionización del agua Algunas veces los enlaces covalentes del agua, se rompen espontáneamente. Sucede en 1 de cada 550 millones de moléculas de H 2 O → OH- + H+ A 25°C, 1 L de H 2 O tiene 10 -7 moles de iones H+ y 10 -7 moles de iones OH-.
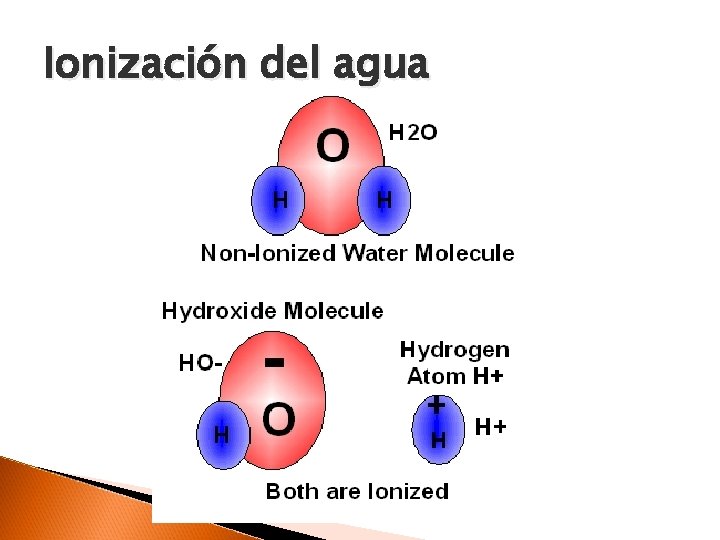
Ionización del agua
![p. H p. H=-log[H+] En el agua que tiene 10 -7 moles H+, p. p. H p. H=-log[H+] En el agua que tiene 10 -7 moles H+, p.](http://slidetodoc.com/presentation_image/44f2df4b1ea60a998e02637f6f305658/image-60.jpg)
p. H p. H=-log[H+] En el agua que tiene 10 -7 moles H+, p. H=-log[10 -7]=7 p. H 7 es el p. H neutro, donde hay una concentración igual de OH- y H+. El p. H fisiológico es cercano a 7.
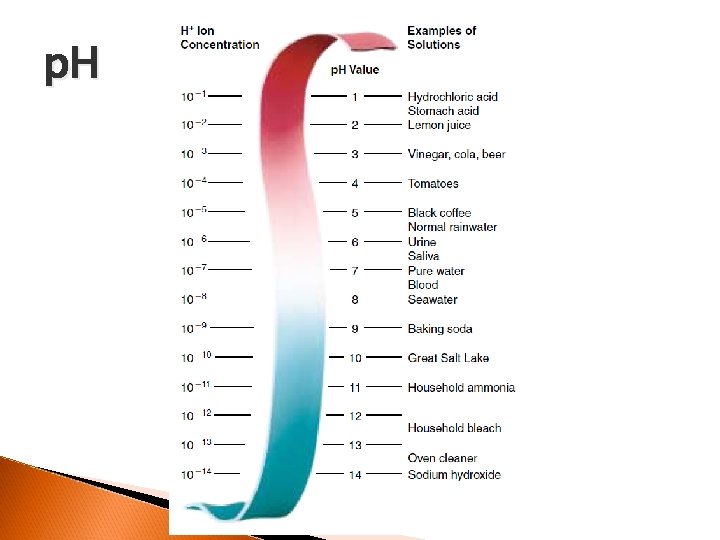
p. H

Acidos Sustancias que son capaces de disolverse en agua, donando iones hidrogeno, y por lo tanto aumentando la concentración de H+. HCl → H+ + CL- H 2 SO 4 → H+ + HSO 4 → H+ + SO 42 - Soluciones ácidas tienen un p. H inferior a 7

Bases Son sustancias capaces de disolverse en agua, que aceptan (reaccionan con) iones H+. Los iones OH- son básicos porque ellos reaccionan con iones H+ para formar agua OH- + H+ → H 2 O Na. OH → Na+ + OHNH 3 + H 20 → NH 4+ + OH- Soluciones básicas tiene p. H mayor a 7.
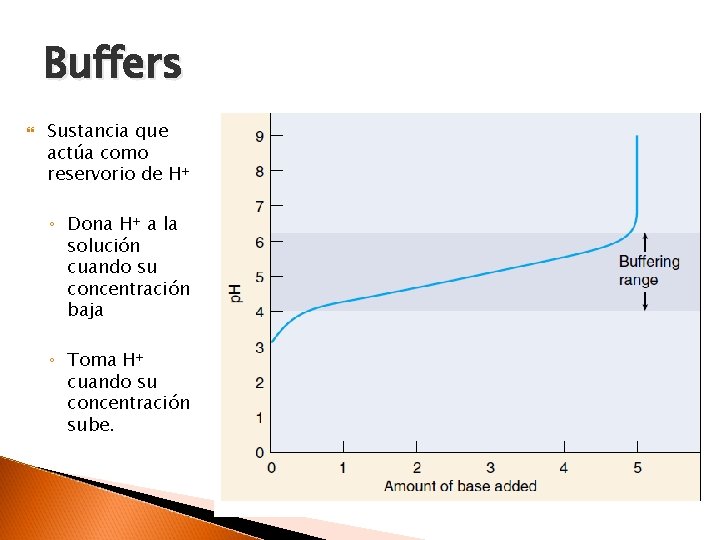
Buffers Sustancia que actúa como reservorio de H+ ◦ Dona H+ a la solución cuando su concentración baja ◦ Toma H+ cuando su concentración sube.
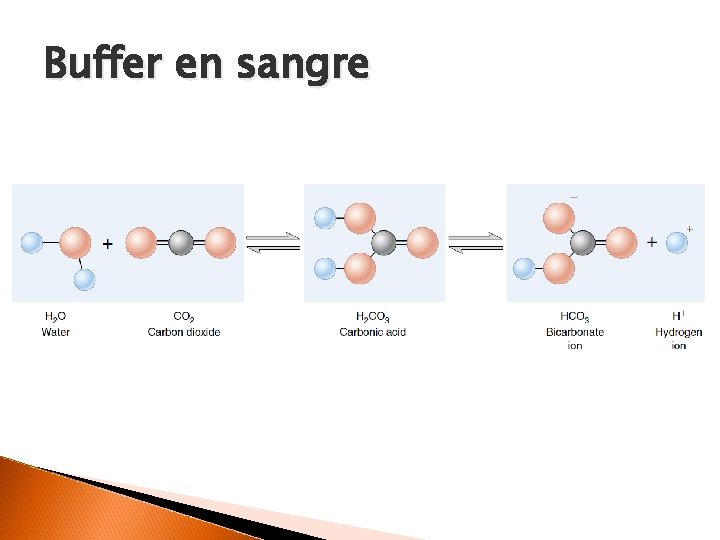
Buffer en sangre
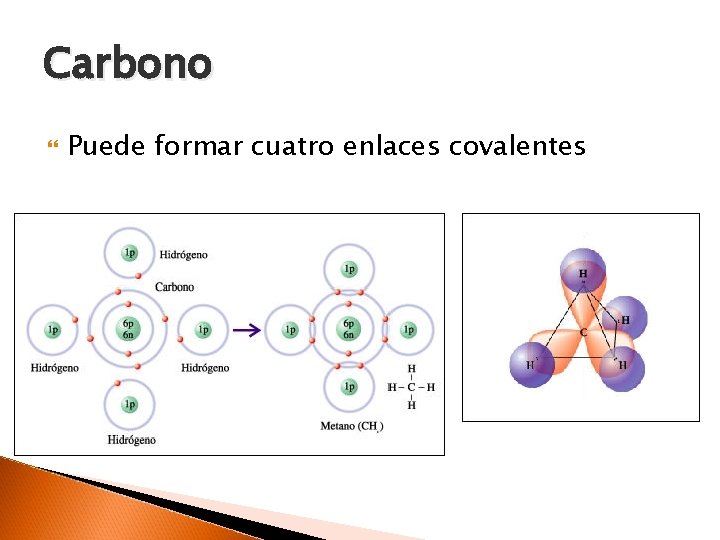
Carbono Puede formar cuatro enlaces covalentes
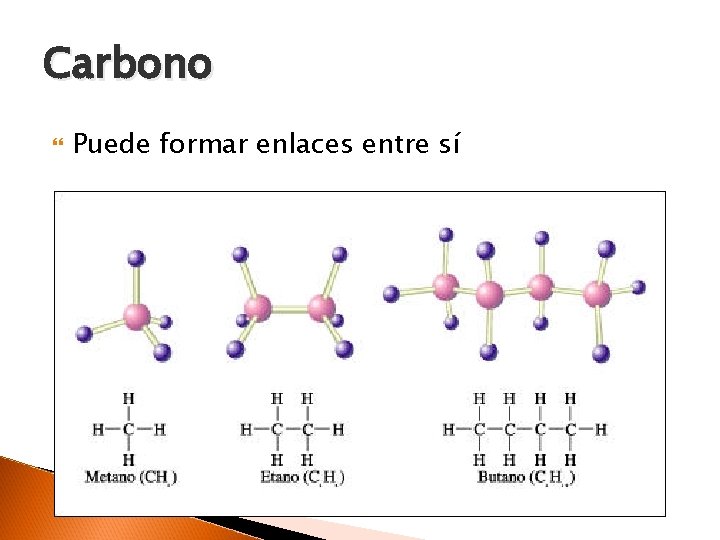
Carbono Puede formar enlaces entre sí
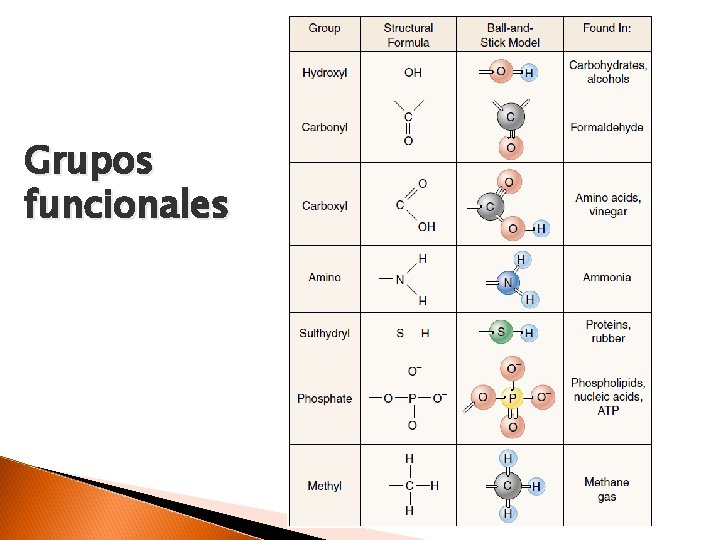
Grupos funcionales
- Slides: 68