BASAAL PLUS insulinetherapie bij diabetes mellitus type 2

BASAAL PLUS insulinetherapie bij diabetes mellitus type 2 De volgende stap als basale insuline + orale medicatie niet meer voldoende is

Inhoud • ‘Glycemic memory’ – UKPDS – DCCT/EDIC – ADVANCE en ACCORD • ADA/EASD consensus statement – Het basaal PLUS concept • Klinische studie met het basaal PLUS concept – De OPAL studie
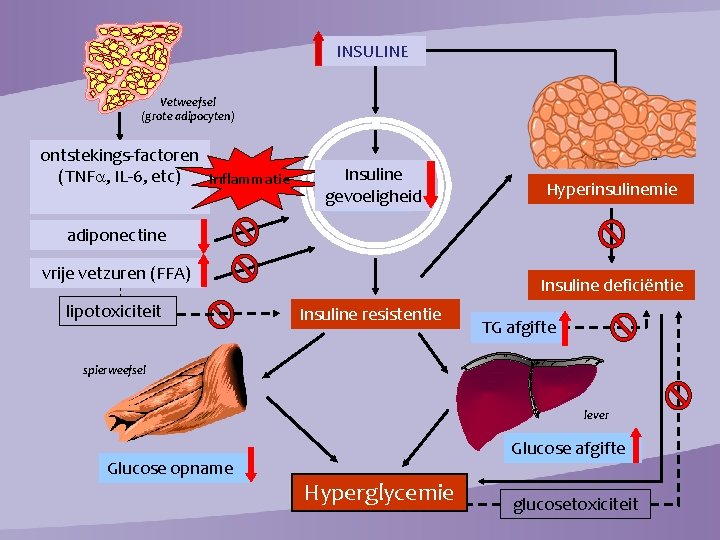
INSULINE Vetweefsel (grote adipocyten) ontstekings-factoren (TNF , IL-6, etc) inflammatie pancreas Insuline gevoeligheid effect Hyperinsulinemie adiponectine vrije vetzuren (FFA) lipotoxiciteit Insuline deficiëntie Insuline resistentie TG afgifte spierweefsel lever Glucose opname Glucose afgifte Hyperglycemie glucosetoxiciteit
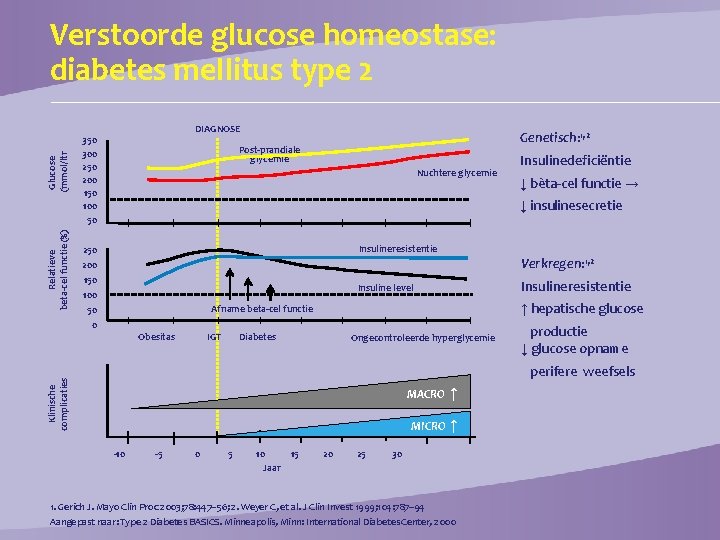
DIAGNOSE 350 300 250 200 150 100 50 Genetisch: 1, 2 Post-prandiale glycemie Nuchtere glycemie Insulinedeficiëntie ↓ bèta-cel functie → ↓ insulinesecretie Insulineresistentie 250 200 150 100 50 0 Verkregen: 1, 2 Insulineresistentie Insuline level ↑ hepatische glucose Afname beta-cel functie Obesitas IGT Diabetes Ongecontroleerde hyperglycemie productie ↓ glucose opname perifere weefsels Klinische complicaties Relatieve beta-cel functie (%) Glucose (mmol/ltr Verstoorde glucose homeostase: diabetes mellitus type 2 -10 -5 0 5 10 Jaar 15 20 25 MACRO ↑ MICRO ↑ 30 1. Gerich J. Mayo Clin Proc 2003; 78: 447– 56; 2. Weyer C, et al. J Clin Invest 1999; 104: 787– 94 Aangepast naar: Type 2 Diabetes BASICS. Minneapolis, Minn: International Diabetes Center, 2000
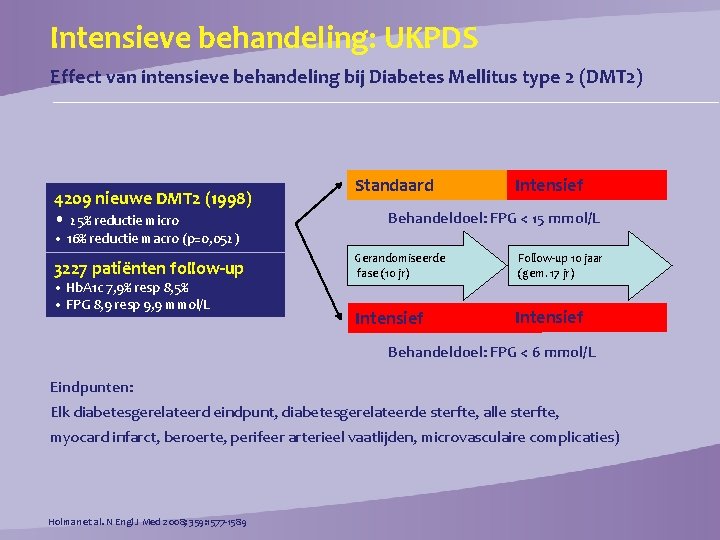
Intensieve behandeling: UKPDS Effect van intensieve behandeling bij Diabetes Mellitus type 2 (DMT 2) 4209 nieuwe DMT 2 (1998) • 25% reductie micro Standaard Intensief Behandeldoel: FPG < 15 mmol/L • 16% reductie macro (p=0, 052) 3227 patiënten follow-up • Hb. A 1 c 7, 9% resp 8, 5% • FPG 8, 9 resp 9, 9 mmol/L Gerandomiseerde fase (10 jr) Follow-up 10 jaar (gem. 17 jr) Intensief Behandeldoel: FPG < 6 mmol/L Eindpunten: Elk diabetesgerelateerd eindpunt, diabetesgerelateerde sterfte, alle sterfte, myocard infarct, beroerte, perifeer arterieel vaatlijden, microvasculaire complicaties) Holman et al. N Engl J Med 2008; 359: 1577 -1589
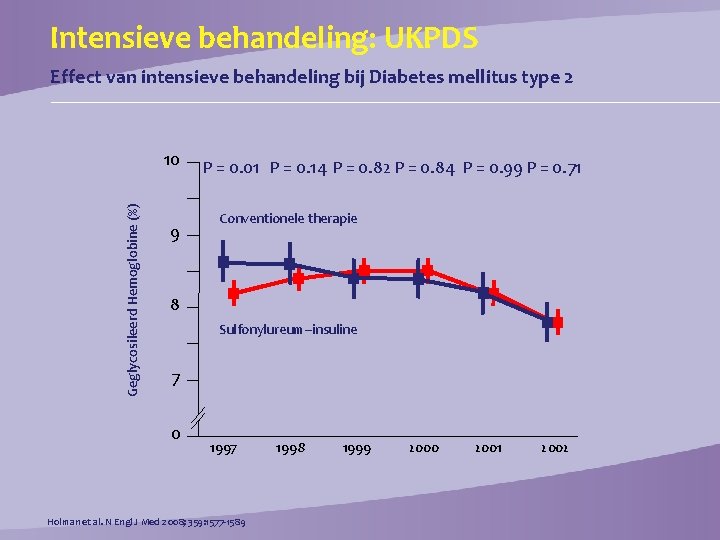
Intensieve behandeling: UKPDS Effect van intensieve behandeling bij Diabetes mellitus type 2 Geglycosileerd Hemoglobine (%) 10 9 P = 0. 01 P = 0. 14 P = 0. 82 P = 0. 84 P = 0. 99 P = 0. 71 Conventionele therapie 8 Sulfonylureum–insuline 7 0 1997 Holman et al. N Engl J Med 2008; 359: 1577 -1589 1998 1999 2000 2001 2002
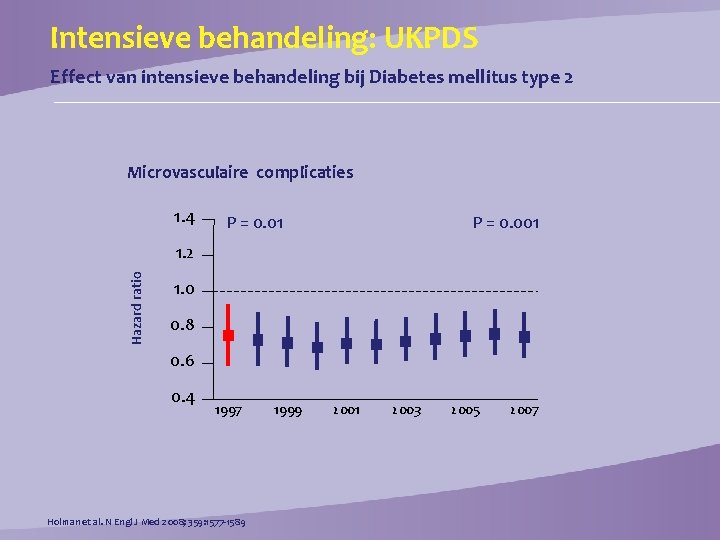
Intensieve behandeling: UKPDS Effect van intensieve behandeling bij Diabetes mellitus type 2 Microvasculaire complicaties 1. 4 P = 0. 01 P = 0. 001 Hazard ratio 1. 2 1. 0 0. 8 0. 6 0. 4 1997 Holman et al. N Engl J Med 2008; 359: 1577 -1589 1999 2001 2003 2005 2007
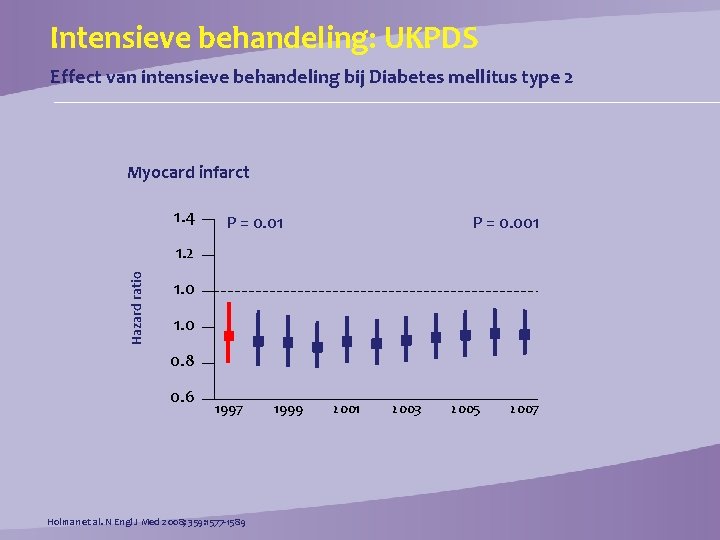
Intensieve behandeling: UKPDS Effect van intensieve behandeling bij Diabetes mellitus type 2 Myocard infarct 1. 4 P = 0. 01 P = 0. 001 Hazard ratio 1. 2 1. 0 0. 8 0. 6 1997 Holman et al. N Engl J Med 2008; 359: 1577 -1589 1999 2001 2003 2005 2007
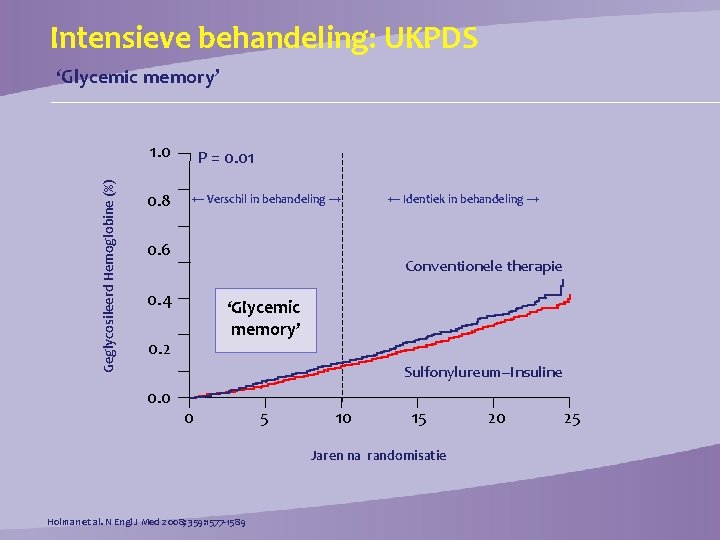
Intensieve behandeling: UKPDS ‘Glycemic memory’ Geglycosileerd Hemoglobine (%) 1. 0 0. 8 P = 0. 01 ← Verschil in behandeling → 0. 6 ← Identiek in behandeling → Conventionele therapie 0. 4 ‘Glycemic memory’ 0. 2 Sulfonylureum–Insuline 0. 0 0 5 10 15 Jaren na randomisatie Holman et al. N Engl J Med 2008; 359: 1577 -1589 20 25

Intensieve behandeling: ADVANCE ‘Glycemic memory’ • Macrovasculaire events in voorgeschiedenis – NEE relatieve risicoreductie 14% (CI [4 – 23]) – JA relatieve risicoreductie 4% (CI [– 10 – 16]) • Microvasculaire events in voorgeschiedenis: – NEE relatieve risicoreductie 11% (CI [2 – 19]) – JA relatieve risicoreductie 4% (CI [– 16 – 21]) Patel et al. N Engl J Med 2008; 358: 2560 -2572
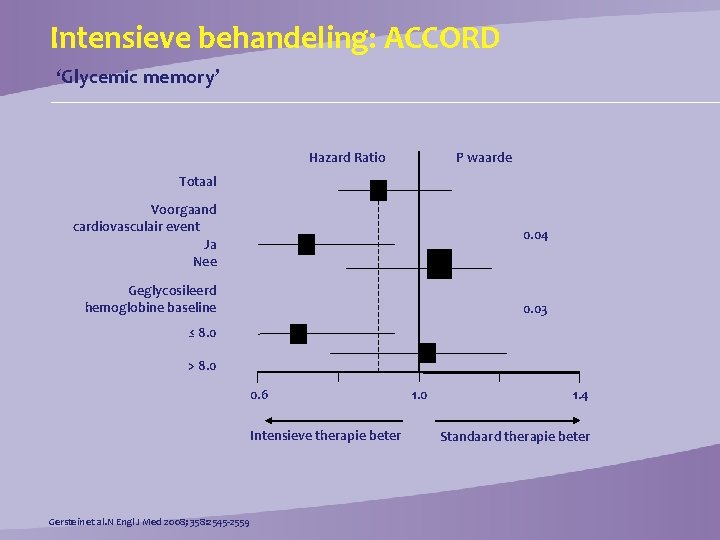
Intensieve behandeling: ACCORD ‘Glycemic memory’ Hazard Ratio P waarde Totaal Voorgaand cardiovasculair event Ja Nee 0. 04 Geglycosileerd hemoglobine baseline 0. 03 ≤ 8. 0 > 8. 0 0. 6 Intensieve therapie beter Gerstein et al. N Engl J Med 2008; 358: 2545 -2559 1. 0 1. 4 Standaard therapie beter
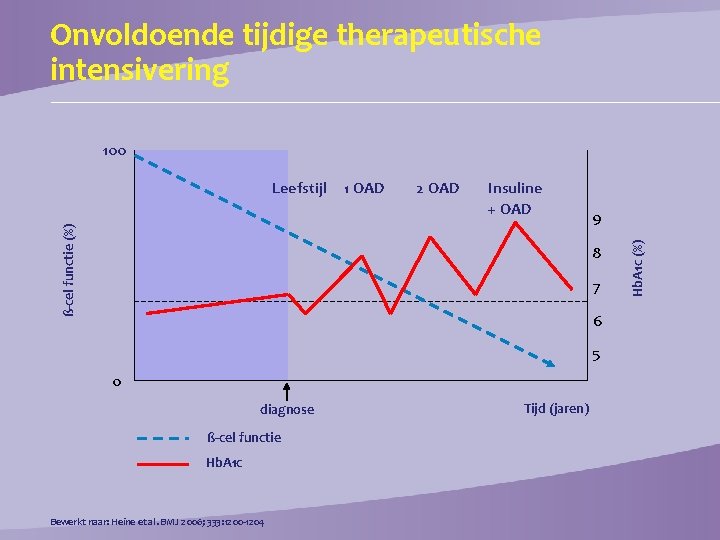
Onvoldoende tijdige therapeutische intensivering 100 2 OAD Insuline + OAD 9 8 7 6 5 0 diagnose ß-cel functie Hb. A 1 c Bewerkt naar: Heine et al. BMJ 2006; 333: 1200 -1204 Tijd (jaren) Hb. A 1 c (%) 1 OAD ß-cel functie (%) Leefstijl
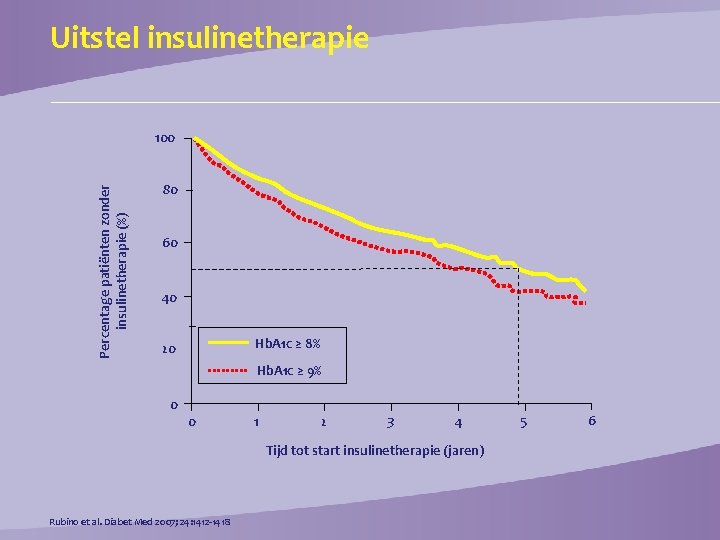
Uitstel insulinetherapie Percentage patiënten zonder insulinetherapie (%) 100 80 60 40 Hb. A 1 c ≥ 8% 20 Hb. A 1 c ≥ 9% 0 0 1 2 3 4 Tijd tot start insulinetherapie (jaren) Rubino et al. Diabet Med 2007; 24: 1412 -1418 5 6

Inhoud • ‘Glycemic memory’ – UKPDS – DCCT/EDIC – ADVANCE en ACCORD • ADA/EASD consensus statement – Het basaal PLUS concept • Klinische studie met het basaal PLUS concept – De OPAL studie Patel et al. N Engl J Med 2008; 358: 2560 -2572

ADA/EASD consensus statement Pleidooi voor vroeg inzetten insulinetherapie • Lower levels of glycaemia at the time of initial therapy are associated with lower A 1 C levels over time and decreased longterm complications • Early addition of insulin therapy in patients who do not meet target goals Nathan DM, et al. Diabetologia 2009; 52: 17 -30.
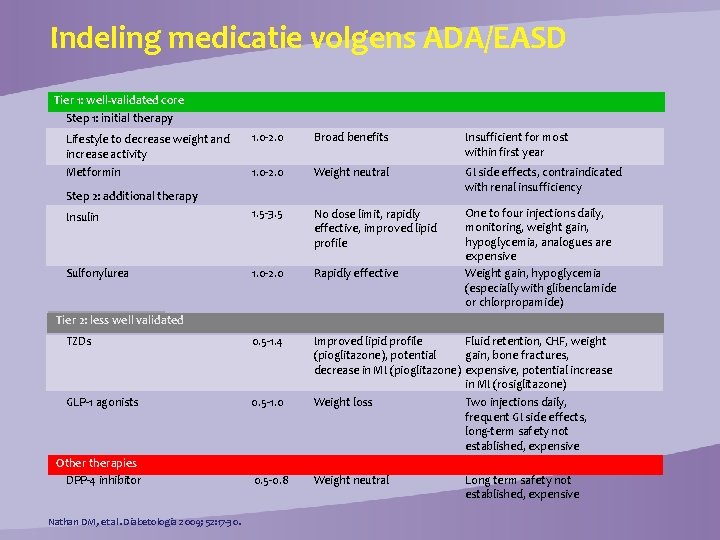
Indeling medicatie volgens ADA/EASD Tier 1: well-validated core Step 1: initial therapy Lifestyle to decrease weight and increase activity 1. 0 -2. 0 Broad benefits Insufficient for most within first year Metformin 1. 0 -2. 0 Weight neutral GI side effects, contraindicated with renal insufficiency Insulin 1. 5 -3. 5 No dose limit, rapidly effective, improved lipid profile Sulfonylurea 1. 0 -2. 0 Rapidly effective One to four injections daily, monitoring, weight gain, hypoglycemia, analogues are expensive Weight gain, hypoglycemia (especially with glibenclamide or chlorpropamide) TZDs 0. 5 -1. 4 Improved lipid profile Fluid retention, CHF, weight (pioglitazone), potential gain, bone fractures, decrease in MI (pioglitazone) expensive, potential increase in MI (rosiglitazone) GLP-1 agonists 0. 5 -1. 0 Weight loss Two injections daily, frequent GI side effects, long-term safety not established, expensive Otherapies DPP-4 inhibitor 0. 5 -0. 8 Weight neutral Long term safety not established, expensive Step 2: additional therapy Tier 2: less well validated Nathan DM, et al. Diabetologia 2009; 52: 17 -30.
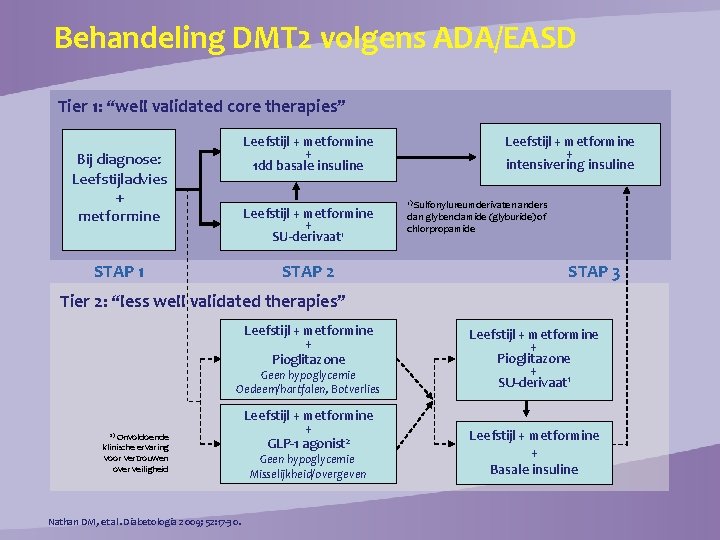
Behandeling DMT 2 volgens ADA/EASD Tier 1: “well validated core therapies” Leefstijl + metformine + intensivering insuline Leefstijl + metformine + 1 dd basale insuline Bij diagnose: Leefstijladvies + metformine Leefstijl + metformine + SU-derivaat 1 STAP 2 Sulfonylureumderivaten anders dan glybenclamide (glyburide) of chlorpropamide 1) STAP 3 Tier 2: “less well validated therapies” Leefstijl + metformine + Pioglitazone Geen hypoglycemie Oedeem/hartfalen, Botverlies 2) Onvoldoende klinische ervaring voor vertrouwen over veiligheid Nathan DM, et al. Diabetologia 2009; 52: 17 -30. Leefstijl + metformine + GLP-1 agonist 2 Geen hypoglycemie Misselijkheid/overgeven Leefstijl + metformine + Pioglitazone + SU-derivaat 1 Leefstijl + metformine + Basale insuline
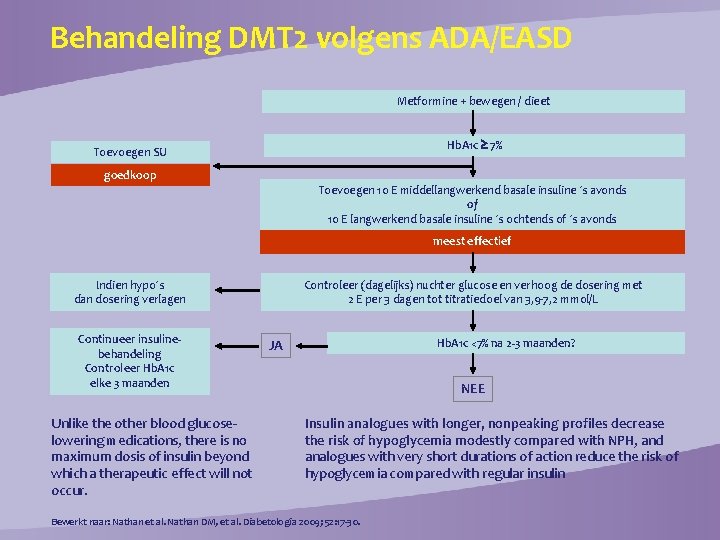
Behandeling DMT 2 volgens ADA/EASD Metformine + bewegen / dieet Hb. A 1 c 7% Toevoegen SU goedkoop Toevoegen 10 E middellangwerkend basale insuline ´s avonds of 10 E langwerkend basale insuline ´s ochtends of ´s avonds meest effectief Indien hypo´s dan dosering verlagen Continueer insulinebehandeling Controleer Hb. A 1 c elke 3 maanden Unlike the other blood glucoselowering medications, there is no maximum dosis of insulin beyond which a therapeutic effect will not occur. Controleer (dagelijks) nuchter glucose en verhoog de dosering met 2 E per 3 dagen tot titratiedoel van 3, 9 -7, 2 mmol/L Hb. A 1 c <7% na 2 -3 maanden? JA NEE Insulin analogues with longer, nonpeaking profiles decrease the risk of hypoglycemia modestly compared with NPH, and analogues with very short durations of action reduce the risk of hypoglycemia compared with regular insulin Bewerkt naar: Nathan et al. Nathan DM, et al. Diabetologia 2009; 52: 17 -30.
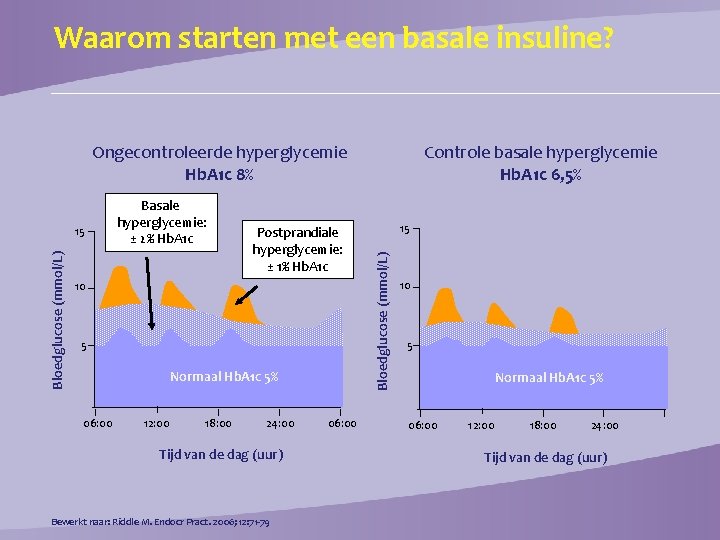
Waarom starten met een basale insuline? Ongecontroleerde hyperglycemie Hb. A 1 c 8% Postprandiale hyperglycemie: ± 1% Hb. A 1 c 10 5 Normaal Hb. A 1 c 5% 06: 00 12: 00 18: 00 24: 00 Tijd van de dag (uur) Bewerkt naar: Riddle M. Endocr Pract. 2006; 12: 71 -79 06: 00 15 Bloedglucose (mmol/L) 15 Basale hyperglycemie: ± 2% Hb. A 1 c Controle basale hyperglycemie Hb. A 1 c 6, 5% 10 5 Normaal Hb. A 1 c 5% 06: 00 12: 00 18: 00 24: 00 Tijd van de dag (uur)
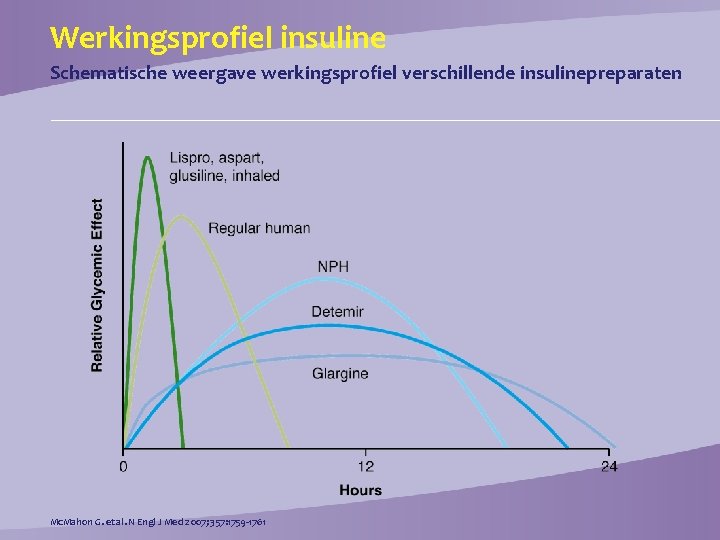
Werkingsprofiel insuline Schematische weergave werkingsprofiel verschillende insulinepreparaten Mc. Mahon G. et al. N Engl J Med 2007; 357: 1759 -1761
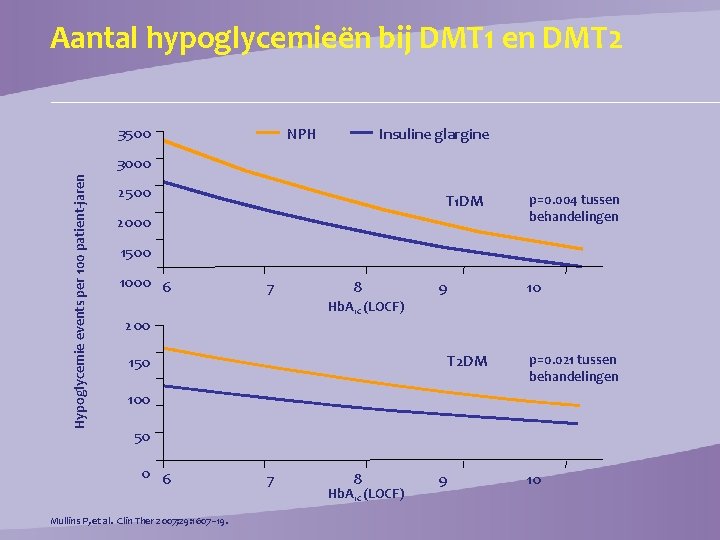
Aantal hypoglycemieën bij DMT 1 en DMT 2 3500 NPH Insuline glargine Hypoglycemie events per 100 patient-jaren 3000 2500 T 1 DM 2000 p=0. 004 tussen behandelingen 1500 1000 6 7 8 9 10 Hb. A 1 c (LOCF) 200 T 2 DM 150 p=0. 021 tussen behandelingen 100 50 0 6 Mullins P, et al. Clin Ther 2007; 29: 1607− 19. 7 8 Hb. A 1 c (LOCF) 9 10
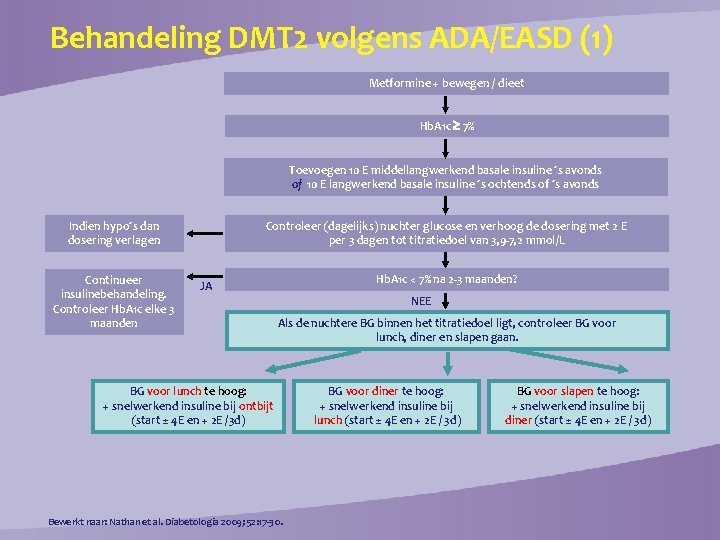
Behandeling DMT 2 volgens ADA/EASD (1) Metformine + bewegen / dieet Hb. A 1 c 7% Toevoegen 10 E middellangwerkend basale insuline ´s avonds of 10 E langwerkend basale insuline ´s ochtends of ´s avonds Indien hypo´s dan dosering verlagen Continueer insulinebehandeling. Controleer Hb. A 1 c elke 3 maanden Controleer (dagelijks) nuchter glucose en verhoog de dosering met 2 E per 3 dagen tot titratiedoel van 3, 9 -7, 2 mmol/L Hb. A 1 c < 7% na 2 -3 maanden? JA NEE Als de nuchtere BG binnen het titratiedoel ligt, controleer BG voor lunch, diner en slapen gaan. BG voor lunch te hoog: + snelwerkend insuline bij ontbijt (start ± 4 E en + 2 E /3 d) Bewerkt naar: Nathan et al. Diabetologia 2009; 52: 17 -30. BG voor diner te hoog: + snelwerkend insuline bij lunch (start ± 4 E en + 2 E / 3 d) BG voor slapen te hoog: + snelwerkend insuline bij diner (start ± 4 E en + 2 E / 3 d)
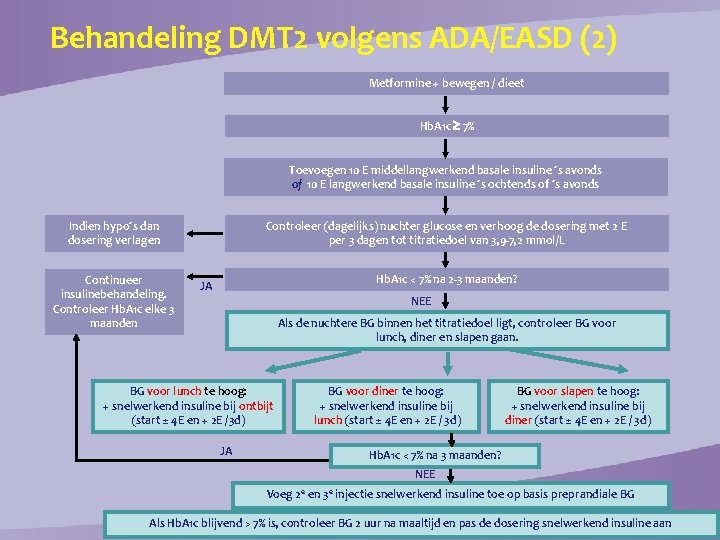
Behandeling DMT 2 volgens ADA/EASD (2) Metformine + bewegen / dieet Hb. A 1 c 7% Toevoegen 10 E middellangwerkend basale insuline ´s avonds of 10 E langwerkend basale insuline ´s ochtends of ´s avonds Indien hypo´s dan dosering verlagen Continueer insulinebehandeling. Controleer Hb. A 1 c elke 3 maanden Controleer (dagelijks) nuchter glucose en verhoog de dosering met 2 E per 3 dagen tot titratiedoel van 3, 9 -7, 2 mmol/L Hb. A 1 c < 7% na 2 -3 maanden? JA NEE Als de nuchtere BG binnen het titratiedoel ligt, controleer BG voor lunch, diner en slapen gaan. BG voor lunch te hoog: + snelwerkend insuline bij ontbijt (start ± 4 E en + 2 E /3 d) JA BG voor diner te hoog: + snelwerkend insuline bij lunch (start ± 4 E en + 2 E / 3 d) BG voor slapen te hoog: + snelwerkend insuline bij diner (start ± 4 E en + 2 E / 3 d) Hb. A 1 c < 7% na 3 maanden? NEE Voeg 2 e en 3 e injectie snelwerkend insuline toe op basis preprandiale BG Als Hb. A 1 c blijvend > 7% is, controleer BG 2 uur na maaltijd en pas de dosering snelwerkend insuline aan
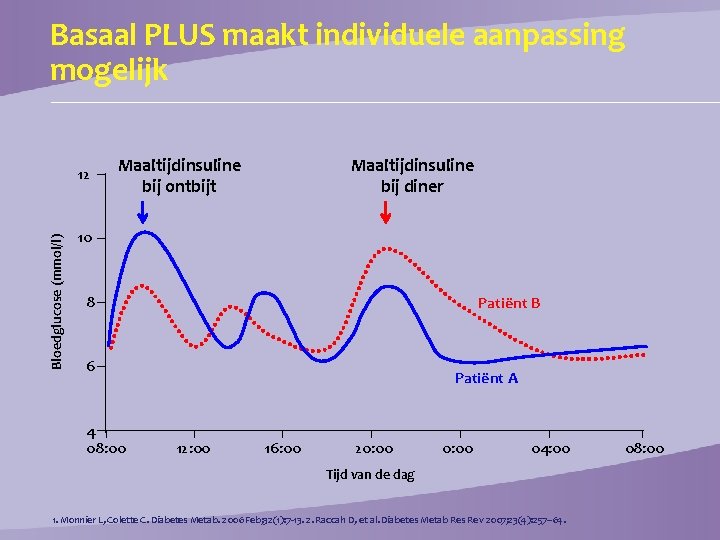
Basaal PLUS maakt individuele aanpassing mogelijk Bloedglucose (mmol/l) 12 Maaltijdinsuline bij ontbijt Maaltijdinsuline bij diner 10 8 Patiënt B 6 4 08: 00 Patiënt A 12: 00 16: 00 20: 00 04: 00 Tijd van de dag 1. Monnier L, Colette C. Diabetes Metab. 2006 Feb; 32(1): 7 -13. 2. Raccah D, et al. Diabetes Metab Res Rev 2007; 23(4): 257– 64. 08: 00
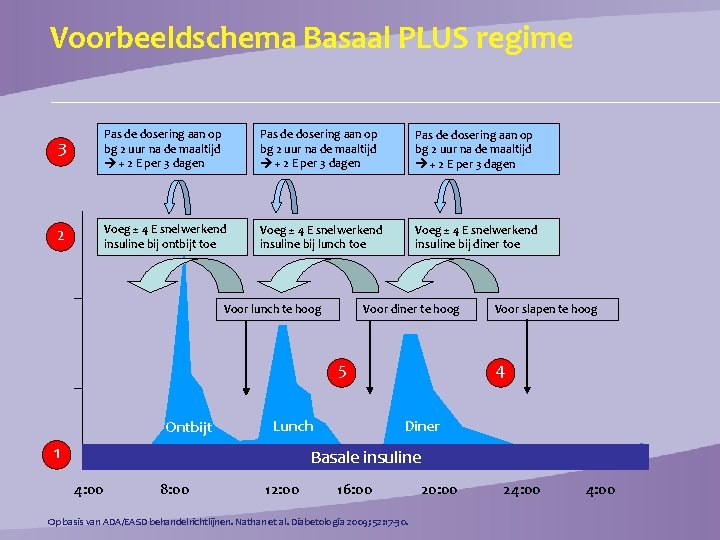
Voorbeeldschema Basaal PLUS regime 3 Pas de dosering aan op bg 2 uur na de maaltijd + 2 E per 3 dagen 2 Voeg ± 4 E snelwerkend insuline bij ontbijt toe Voeg ± 4 E snelwerkend insuline bij lunch toe Voeg ± 4 E snelwerkend insuline bij diner toe Voor lunch te hoog Voor diner te hoog 4 5 Ontbijt Lunch 1 Voor slapen te hoog Diner Basale insuline 4: 00 8: 00 12: 00 16: 00 Op basis van ADA/EASD behandelrichtlijnen. Nathan et al. Diabetologia 2009; 52: 17 -30. 20: 00 24: 00

Basaal PLUS regime Wanneer moet de eerste maaltijdinsuline worden ingezet? • Een maaltijdinsuline dient te worden toegevoegd indien: – NBG onder controle (4 -7 mmol/L), maar Hb. A 1 c >7% – NBG onder controle, maar PPBG consequent te hoog – Onacceptabel vaak of ernstige hypoglycemieën gedurende titratie basale insuline • Voeg 1 injectie maaltijdinsuline toe (4 IE) – Start met de grootste maaltijd NBG = nuchter bloedglucose PPBG = post-prandiaal bloedglucose 1. Nathan DM, et al. Diabetes Care 2006; 29: 1963– 72. 2. Nathan DM, et al. Diabetes Care 2008; 31: 173– 5. 3. Raccah D, et al. Diabetes Metab Res Rev 2007; 23: 257− 64.

Inhoud • ‘Glycemic memory’ – UKPDS – DCCT/EDIC – ADVANCE en ACCORD • ADA/EASD consensus statement – Het basaal PLUS concept • Klinische studie met het basaal PLUS concept – De OPAL studie

Basaal PLUS behandeling bij DMT 2 De OPAL studie Insuline glargine 1 dd + 1 x insuline glulisine bij grootste maaltijd (N=154) 393 DMT 2 met: • LANTUS (27 -30 U/day) • OAD (metformine ± SU) • Hb. A 1 c 7, 3% • FPG 6, 8 mmol/L Follow-up 24 weken Insuline glargine 1 dd + 1 x insuline glulisine bij ontbijt (N=162) • • • Doel: Hb. A 1 c ≤ 6, 5% FBG ≤ 5, 5 mmol/L 2 hr PPBG ≤ 7, 5 mmol/L Primaire parameter: • Afname in Hb. A 1 c percentage ten opzichte van baseline (non-inferiority ) Lankisch et al. Diabetes, Obesity and Metabolism 2008; 10: 1178 -1185
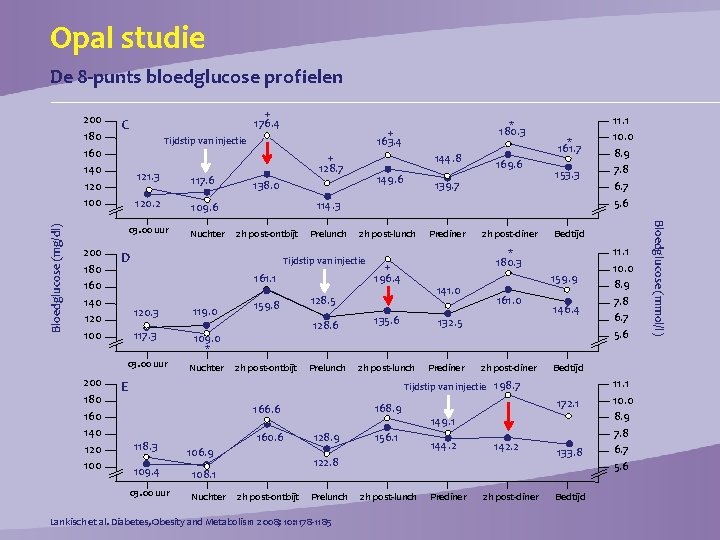
Opal studie De 8 -punts bloedglucose profielen 200 180 160 140 120 100 + 176. 4 C + 163. 4 Tijdstip van injectie 121. 3 117. 6 120. 2 109. 6 03. 00 uur Nuchter 144. 8 + 128. 7 149. 6 138. 0 2 h post-ontbijt Prelunch 161. 1 117. 3 109. 0 * 03. 00 uur Nuchter 139. 7 2 h post-lunch Tijdstip van injectie 120. 3 169. 6 159. 8 2 h post-ontbijt Prediner 2 h post-diner 128. 5 128. 6 135. 6 Prelunch 2 h post-lunch 161. 0 132. 5 Prediner 2 h post-diner 168. 9 166. 6 03. 00 uur 160. 6 106. 9 156. 1 2 h post-ontbijt Prelunch Lankisch et al. Diabetes, Obesity and Metabolism 2008; 10: 1178 -1185 2 h post-lunch 146. 4 172. 1 149. 1 144. 2 142. 2 Prediner 2 h post-diner 11. 1 10. 0 8. 9 7. 8 6. 7 5. 6 Bedtijd 198. 7 122. 8 108. 1 Nuchter 128. 9 11. 1 10. 0 8. 9 7. 8 6. 7 5. 6 Bedtijd 159. 9 141. 0 Tijdstip van injectie 109. 4 153. 3 * 180. 3 + 196. 4 E 118. 3 * 161. 7 114. 3 D 119. 0 * 180. 3 133. 8 Bedtijd 11. 1 10. 0 8. 9 7. 8 6. 7 5. 6 Bloedglucose (mmol/l) Bloedglucose (mg/dl) 200 180 160 140 120 100
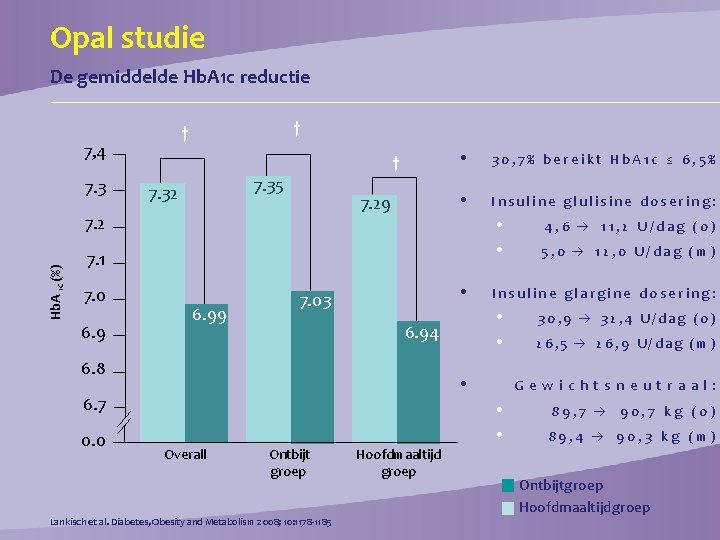
Opal studie De gemiddelde Hb. A 1 c reductie 7, 4 7. 3 † † † 7. 35 7. 32 7. 29 Hb. A 1 c (%) 7. 2 • 30, 7% bereikt Hb. A 1 c ≤ 6, 5% • Insuline glulisine dosering: • • 7. 1 7. 0 6. 99 • 7. 03 6. 8 • 6. 7 0. 0 Ontbijt groep Lankisch et al. Diabetes, Obesity and Metabolism 2008; 10: 1178 -1185 Hoofdmaaltijd groep 30, 9 32, 4 U/dag (o) 26, 5 26, 9 U/dag (m) G e w i c h t s n e u t r a a l : • • Overall 5, 0 12, 0 U/dag (m) Insuline glargine dosering: • • 6. 94 4, 6 11, 2 U/dag (o) 89, 7 90, 7 kg (o) 89, 4 90, 3 kg (m) Ontbijtgroep Hoofdmaaltijdgroep
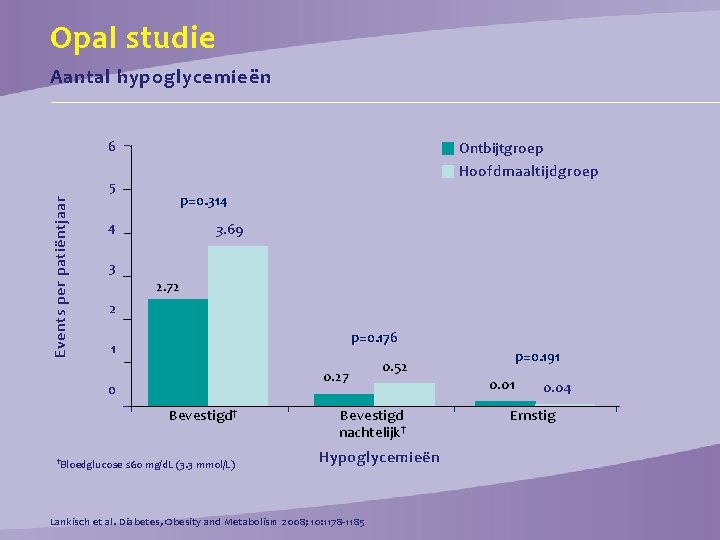
Opal studie Aantal hypoglycemieën 6 Events per patiëntjaar 5 Ontbijtgroep Hoofdmaaltijdgroep p=0. 314 4 3. 69 3 2. 72 2 p=0. 176 1 0. 27 0 Bevestigd † †Bloedglucose ≤ 60 mg/d. L (3. 3 mmol/L) 0. 52 Bevestigd nachtelijk † Hypoglycemieën Lankisch et al. Diabetes, Obesity and Metabolism 2008; 10: 1178 -1185 p=0. 191 0. 04 Ernstig

Basaal PLUS regime Samenvatting 1. Optimaliseer de dosering basale insuline 2. Bepaal de grootste maaltijd van de dag 3. Voeg 1 injectie maaltijdinsuline toe bij die grootste maaltijd 4. Staak het gelijktijdig gebruik van SU-derivaten (en andere producten die de insulineproductie stimuleren) 5. Titreer de dosis maaltijdinsuline om het behandeldoel te bereiken 6. Voeg, indien nodig, een tweede of derde maaltijdinsuline toe
- Slides: 32