Balano de Massa e Energia Professor Digenes Ganghis

Balanço de Massa e Energia Professor: Diógenes Ganghis

Conteúdo Programático & Bibliografia ð Balanço Material – Balanços totais; – Balanços parciais; – Balanços com reação química; ð Estequiometria Industrial - Reynaldo Gomide ð Engenharia Química Princípios e Cálculos David M. Himmeblau. ð Balanço de Energia – Trocadores de Calor – Processos com reações químicas ð Equilíbrio Líquido Vapor – Lei de Antoine – Lei de Raoult – Lei de Henry ð Processos de Combustão ð Compostos de Enxofre ð Indústrias do Petróleo e Petroquímicas. ð Sais minerais 2

Processos Industriais ð Complicados problemas industriais são resolvidos pela aplicação dos princípios da química, da física e da físico-química, e de sua aplicação depende o SUCESSO da solução obtida. ð As técnicas de aplicação dos princípios básicos para resolver problemas de processo, e de operações unitárias, constituem, em seu conjunto, a ESTEQUIOMETRIA INDUSTRIAL. ð A variedade de princípios colocados à disposição para resolução dos problemas de estequiometria industrial é muito grande, eles se dividem em: – – balanços materiais; balanços de energia; reações de equilíbrio; equações de velocidade de equilíbrio. 3
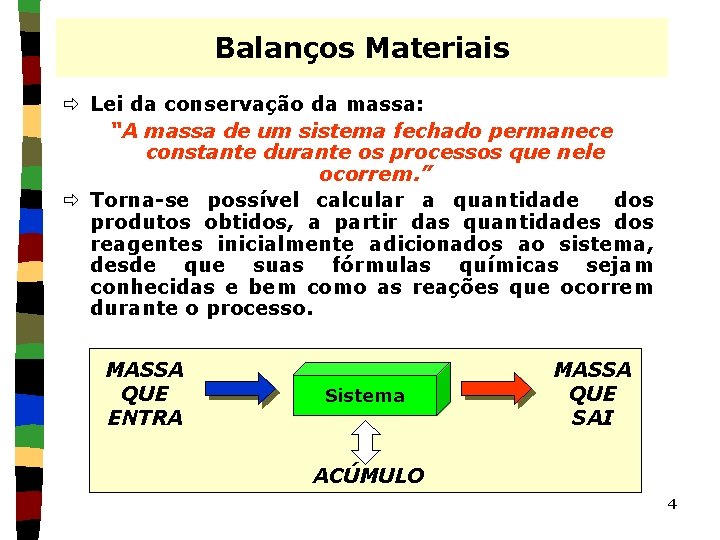
Balanços Materiais ð Lei da conservação da massa: “A massa de um sistema fechado permanece constante durante os processos que nele ocorrem. ” ð Torna-se possível calcular a quantidade dos produtos obtidos, a partir das quantidades dos reagentes inicialmente adicionados ao sistema, desde que suas fórmulas químicas sejam conhecidas e bem como as reações que ocorrem durante o processo. MASSA QUE ENTRA Sistema MASSA QUE SAI ACÚMULO 4

A Técnica dos Balanços Materiais ð Imaginar o o que está ocorrendo no sistema, CONHECER O PROCESSO, é o primeiro passo para a resolução de um problema. ð Esquematizar o processos num FLUXOGRAMA simplificado, onde ilustre apenas as correntes que intervém no casos específico. Todos os os dados importantes disponíveis deverão ser colocados diretamente no fluxograma, dentre eles: vazões, composições, pressão, temperatura. ð ESTUDAR O FLUXOGRAMA E OS DADOS de modo a relacionar mentalmente as diversas correntes do processo e as quantidades das diversas substâncias que compõe estas correntes. 5
A Técnica dos Balanços Materiais ð Escolher a BASE DE CÁLCULO apropriada e indicá-la com clareza e destaque. – Base de cálculo é a quantidade arbitrária de reagentes ou produtos em relação à qual se referem todos os cálculos efetuados. ð Selecionar o SISTEMA em torno do qual serão feitos os balanços. ð Realizar os balanços, obtendo em resultado um número suficiente de equações que permita resolver o sistema, ou seja, o Nº DE EQUAÇÕES SEJA IGUAL AO Nº DE INCÓGNITAS. 6
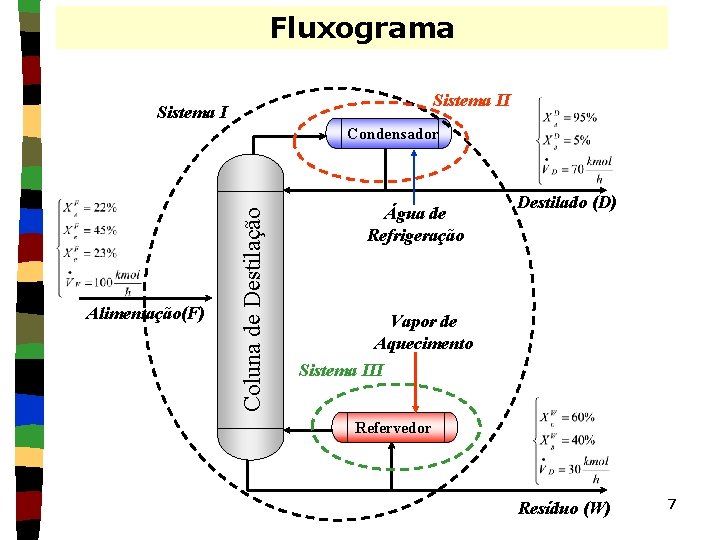
Fluxograma Sistema II Sistema I Alimentação(F) Coluna de Destilação Condensador Água de Refrigeração Destilado (D) Vapor de Aquecimento Sistema III Refervedor Resíduo (W) 7

Tanque de Armazenamento ð Um tanque de armazenamento de água quente destinada a lavar lama de carbonato, numa instalação de recuperação de soda do processo sulfato para produção de celulose, recebe água de várias fontes. Num dia de operação, 240 m 3 de condensado da fábrica são enviados para este tanque, 80 m 3 de água quente contendo pequena quantidade de hidróxido de cálcio e soda cáustica vêm do lavador de lama e 130 m³ são provenientes do filtro rotativo. Durante esse mesmo período, 300 m³ são retirados para usos diversos, 5 m³ e são perdidos por evaporação e 1 m³ por vazamentos. A capacidade do tanque é de 500 m³ e, no início do dia, está com líquido até a sua metade. Quanta água haverá no tanque no fim do dia? 8
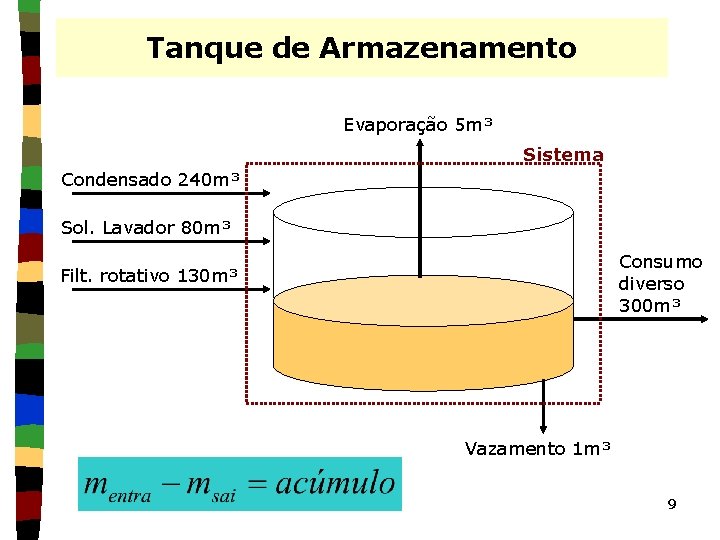
Tanque de Armazenamento Evaporação 5 m³ Sistema Condensado 240 m³ Sol. Lavador 80 m³ Consumo diverso 300 m³ Filt. rotativo 130 m³ Vazamento 1 m³ 9
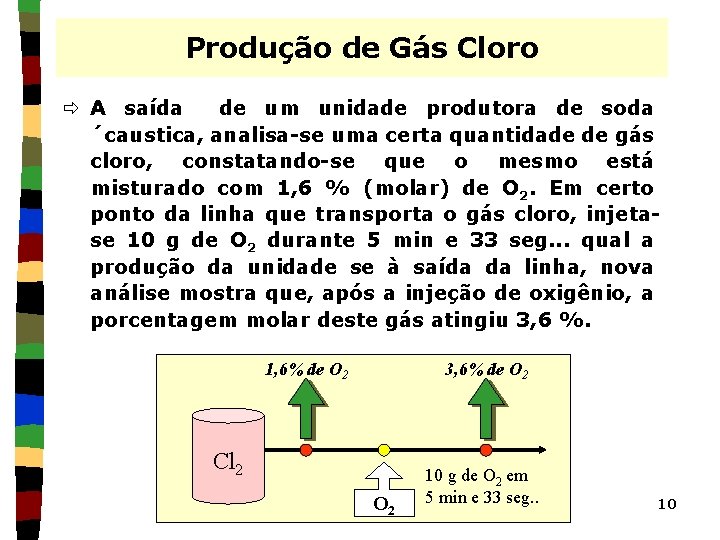
Produção de Gás Cloro ð A saída de um unidade produtora de soda ´caustica, analisa-se uma certa quantidade de gás cloro, constatando-se que o mesmo está misturado com 1, 6 % (molar) de O 2. Em certo ponto da linha que transporta o gás cloro, injetase 10 g de O 2 durante 5 min e 33 seg. . . qual a produção da unidade se à saída da linha, nova análise mostra que, após a injeção de oxigênio, a porcentagem molar deste gás atingiu 3, 6 %. 1, 6% de O 2 3, 6% de O 2 Cl 2 O 2 10 g de O 2 em 5 min e 33 seg. . 10
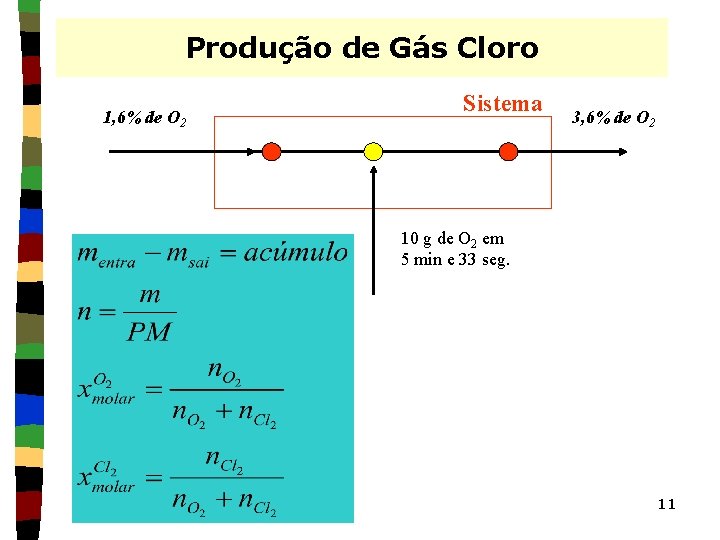
Produção de Gás Cloro 1, 6% de O 2 Sistema 3, 6% de O 2 10 g de O 2 em 5 min e 33 seg. 11

Licor Ácido ð O licor ácido resultante de um processo de nitração contém 23% de ácido nítrico e 57% de ácido sulfúrico. Este licor deve ser concentrado para conter 27% de ácido nítrico e 605 de ácido sulfúrico, em peso, pela adição de H 2 SO 4 a 93% e H 2 NO 3 a 90%. Calcular o peso do licor inicial e dos ácidos concentrados que devem ser misturados para obter 1000 kg de mistura final concentrada. 12
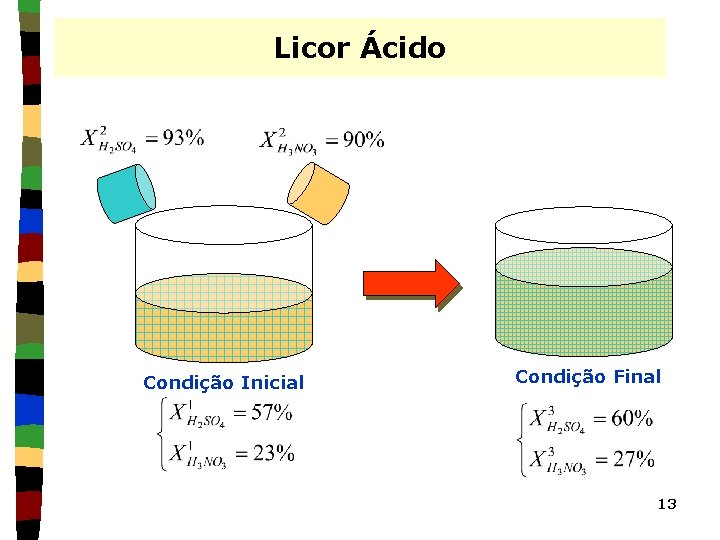
Licor Ácido Condição Inicial Condição Final 13
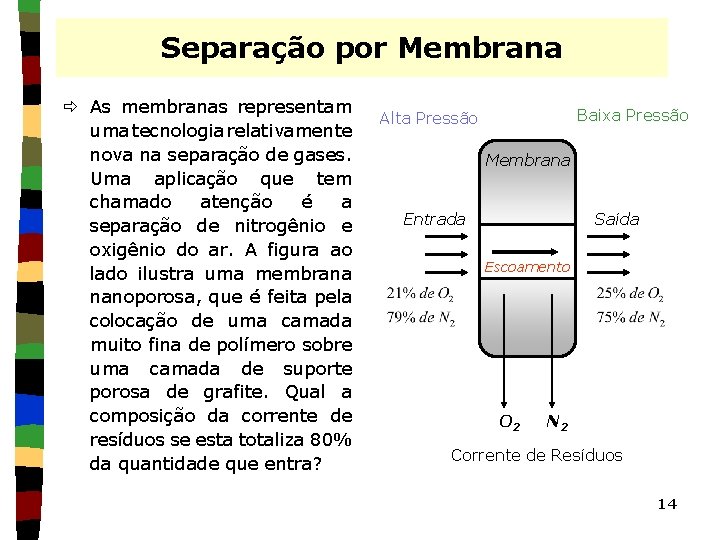
Separação por Membrana ð As membranas representam uma tecnologia relativamente nova na separação de gases. Uma aplicação que tem chamado atenção é a separação de nitrogênio e oxigênio do ar. A figura ao lado ilustra uma membrana nanoporosa, que é feita pela colocação de uma camada muito fina de polímero sobre uma camada de suporte porosa de grafite. Qual a composição da corrente de resíduos se esta totaliza 80% da quantidade que entra? Baixa Pressão Alta Pressão Membrana Entrada Saída Escoamento O 2 N 2 Corrente de Resíduos 14
- Slides: 14