Bagian ilmu kimia yang mempelajari hubungan massa zat


Bagian ilmu kimia yang mempelajari hubungan massa zat -zat kimia, rumus kimia dengan reaksi kimia (mempelajari aspek-aspek kuantitatif dari zat-zat kimia di dalam reaksi kimia)

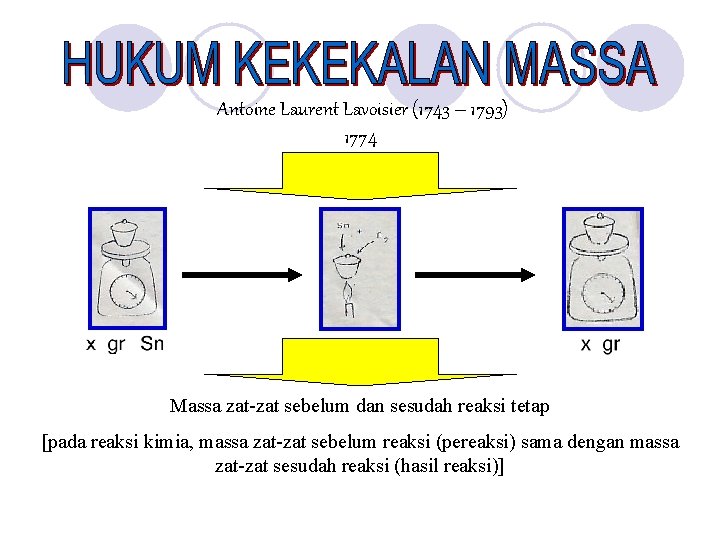
Antoine Laurent Lavoisier (1743 – 1793) 1774 Massa zat-zat sebelum dan sesudah reaksi tetap [pada reaksi kimia, massa zat-zat sebelum reaksi (pereaksi) sama dengan massa zat-zat sesudah reaksi (hasil reaksi)]
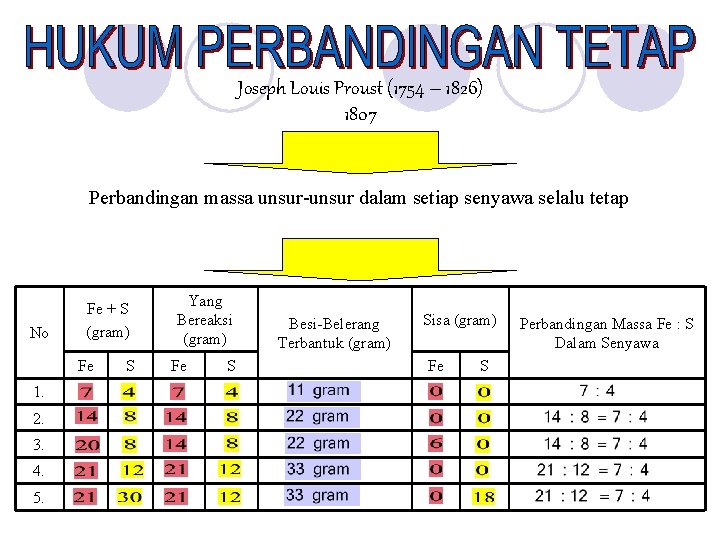
Joseph Louis Proust (1754 – 1826) 1807 Perbandingan massa unsur-unsur dalam setiap senyawa selalu tetap No Fe + S (gram) Fe 1. 2. 3. 4. 5. S Yang Bereaksi (gram) Fe S Besi-Belerang Terbantuk (gram) Sisa (gram) Fe S Perbandingan Massa Fe : S Dalam Senyawa

John Dalton Bila 2 unsur atau lebih bisa membentuk 2 senyawa atau lebih, dan salah satu unsur yang dikandung tiap senyawa massanya sama, maka massa unsur yang kedua pada tiap senyawa akan berbanding sebagai bilangan bulat dan sederhana Senyawa Karbon Oksigen CO 42, 8% 57, 2% CO 2 27, 3% 72, 7% OI : OII Karbon : Oksigen

Joseph Louis Gay-Lussac (1778 – 1850) 1809 Volume gas-gas yang terlibat dalam suatu reaksi kimia, jika diukur pada suhu dan tekanan yang sama berbanding sebagai bilangan bulat dan sederhana

KEBERATAN DALTON ATAS TEORI GAY LUSSAC Gas mempunyai partikel yang dapat bergerak bebas dan mempunyai tekanan dan volume tertentu Jika volume diperkecil (pada P tetap), maka kerapatan partikel bertambah besar, tetapi jumlahnya sama Gas-gas yang volumenya sama jika diukur pada suhu dan tekanan yang sama mengandung atom-atom yang sama banyaknya

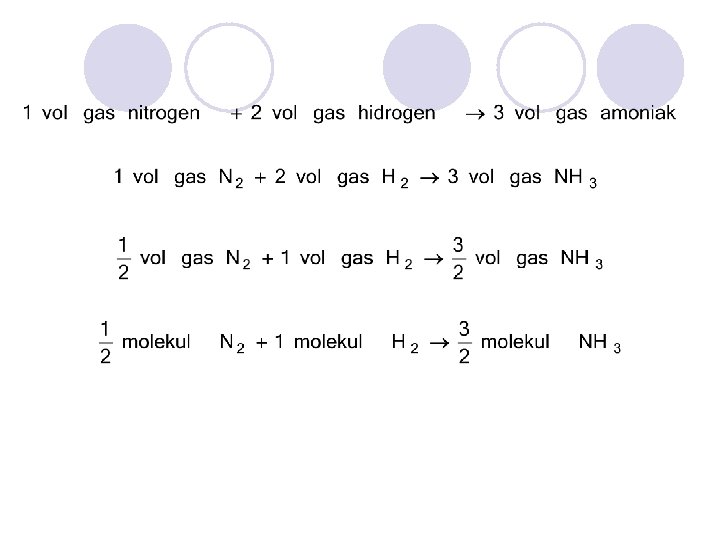
Pada suhu dan tekanan yang sama, semua gas yang volumenya sama mempunyai jumlah molekul yang sama Amadeo Avogadro (1776 – 1856) 1811 Unsur-unsur gas terdapat sebagai molekul-molekul diatomik

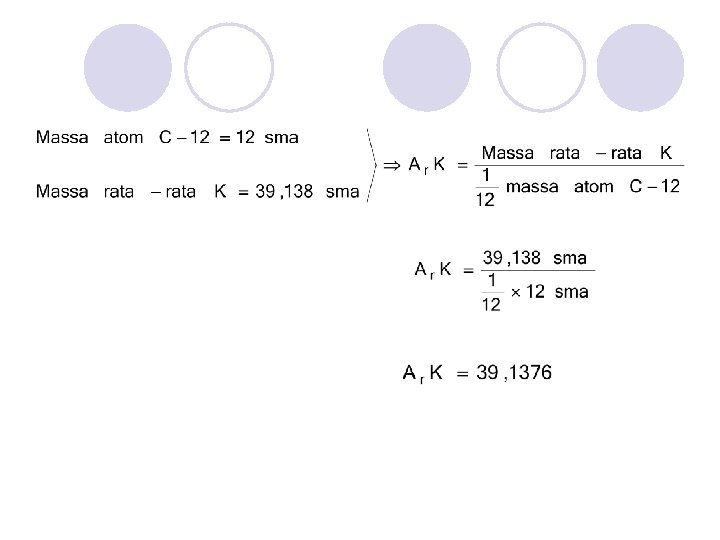
Angka yang menunjukkan perbandingan massa antara satu atom unsur dengan sebuah atom standar IUPAC (Internasional Union of Pure and Applied Chemestry) Atom standar : C-12 Massa 1 atom C-12 = 12 sma 1 sma = 1, 66 × 10 -24 gram

SPEKTROSKOPI MASSA Kalium (K) Bermassa atom relatif 39 sma dengan jumlah 93, 12% Bermassa atom relatif 41 sma dengan jumlah 6, 88%

Angka yang menunjukkan perbandingan massa antara satu molekul senyawa dengan sebuah atom standar Massa molekul relatif dihitung dari jumlah seluruh massa atom relatif yang menyusun senyawa itu
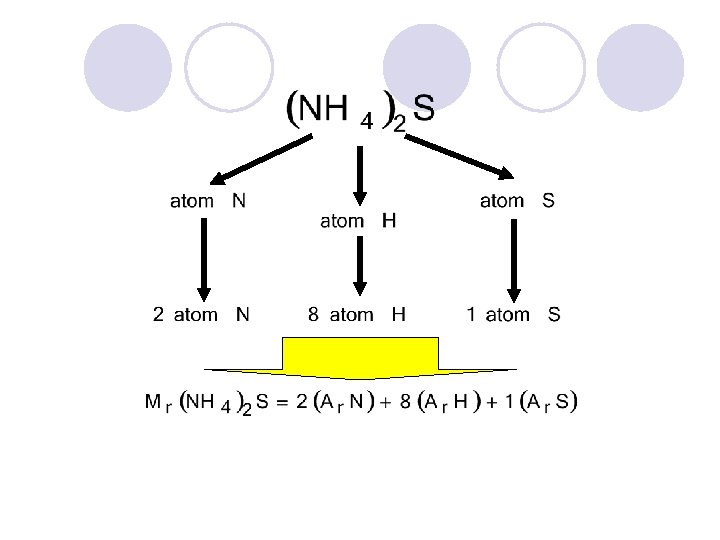

SATUAN JUMLAH ZAT
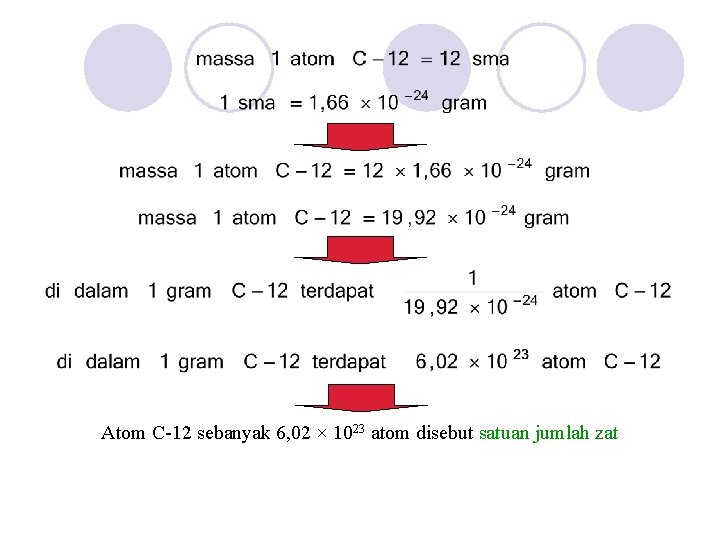
Atom C-12 sebanyak 6, 02 × 1023 atom disebut satuan jumlah zat
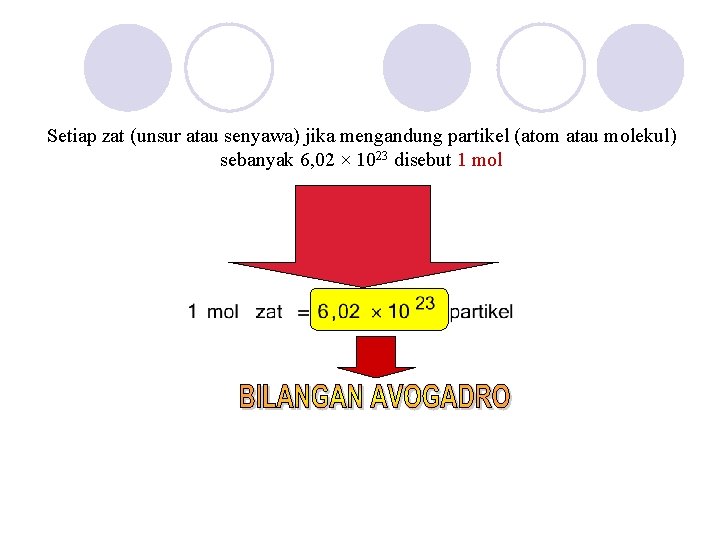
Setiap zat (unsur atau senyawa) jika mengandung partikel (atom atau molekul) sebanyak 6, 02 × 1023 disebut 1 mol
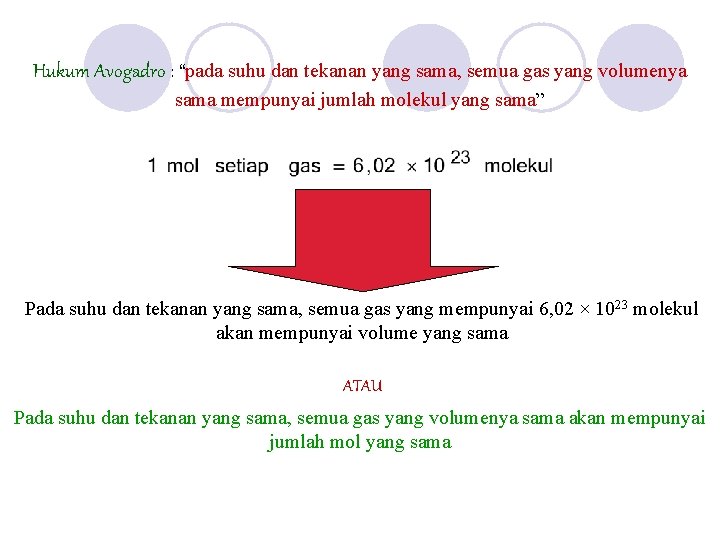
Hukum Avogadro : “pada suhu dan tekanan yang sama, semua gas yang volumenya sama mempunyai jumlah molekul yang sama” Pada suhu dan tekanan yang sama, semua gas yang mempunyai 6, 02 × 1023 molekul akan mempunyai volume yang sama ATAU Pada suhu dan tekanan yang sama, semua gas yang volumenya sama akan mempunyai jumlah mol yang sama
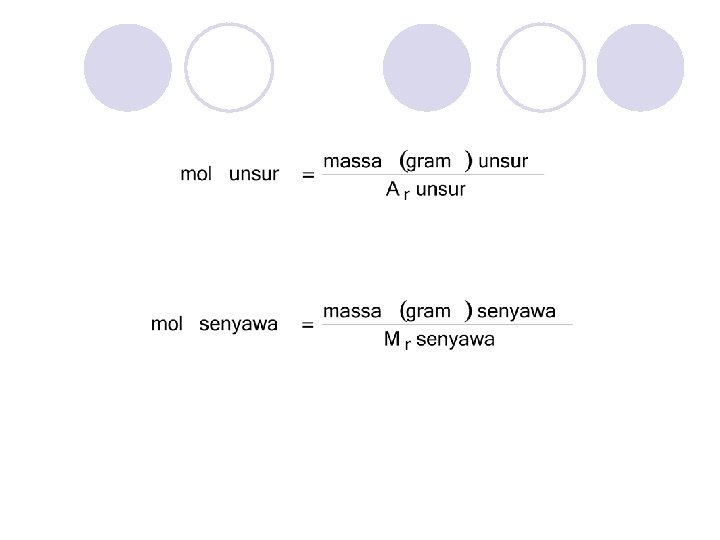

VOLUME 1 MOL GAS Pada keadaan standar (STP) 1 mol setiap gas mempunyai volume sebesar 22, 4 liter
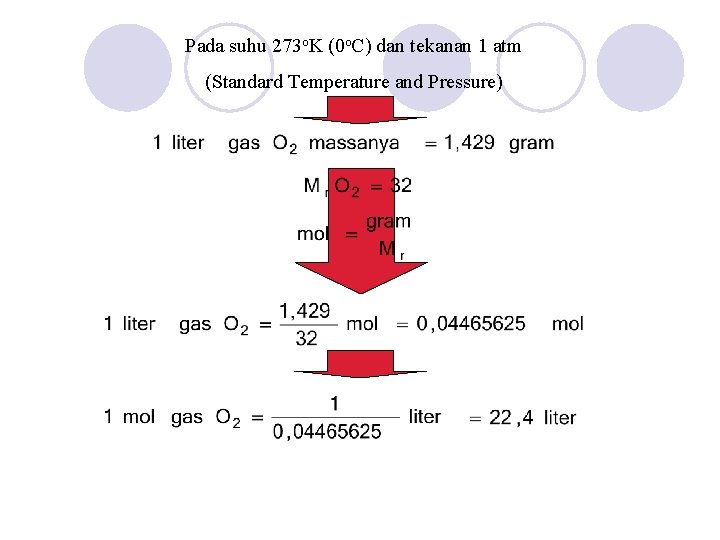
Pada suhu 273 o. K (0 o. C) dan tekanan 1 atm (Standard Temperature and Pressure)
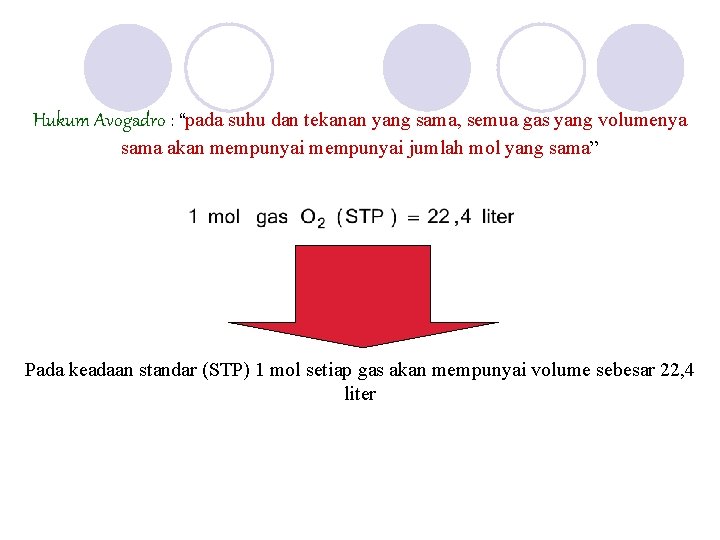
Hukum Avogadro : “pada suhu dan tekanan yang sama, semua gas yang volumenya sama akan mempunyai jumlah mol yang sama” Pada keadaan standar (STP) 1 mol setiap gas akan mempunyai volume sebesar 22, 4 liter
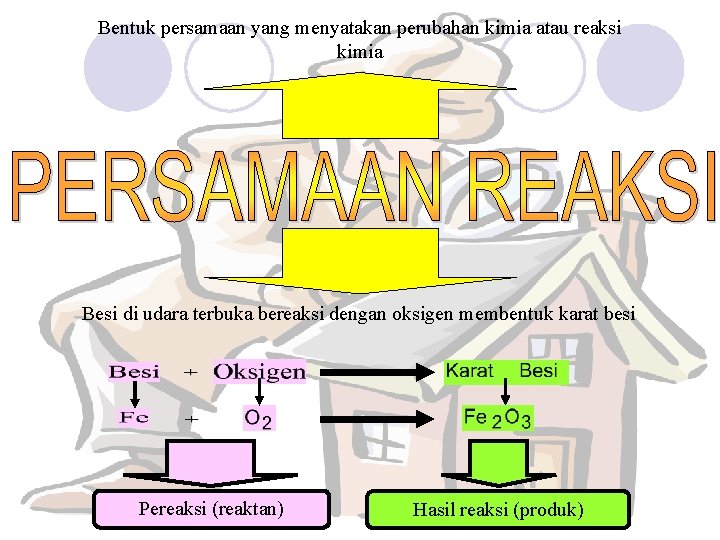
Bentuk persamaan yang menyatakan perubahan kimia atau reaksi kimia Besi di udara terbuka bereaksi dengan oksigen membentuk karat besi Pereaksi (reaktan) Hasil reaksi (produk)

Penulisan persamaan reaksi biasa juga dilengkapi dengan menuliskan wujud zat-zat pereaksi maupun zat-zat hasil reaksi Padat : (s) atau (p) Cair : (l) atau (c) Gas : (g) Larutan dalam air: (aq)
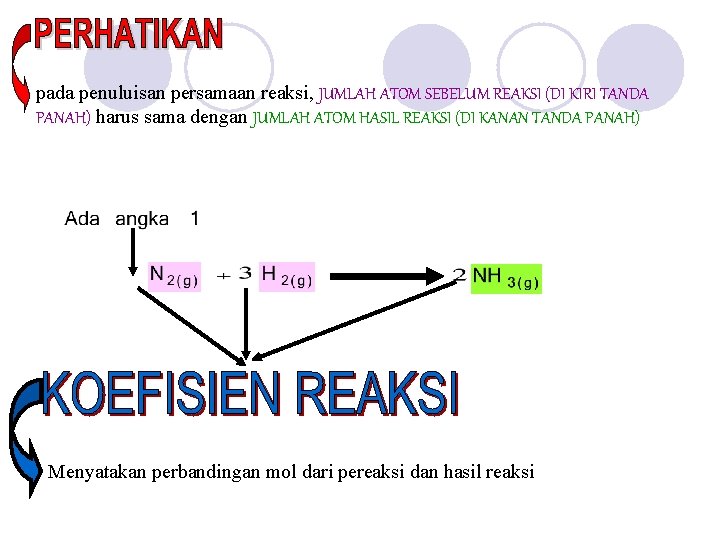
pada penuluisan persamaan reaksi, JUMLAH ATOM SEBELUM REAKSI (DI KIRI TANDA PANAH) harus sama dengan JUMLAH ATOM HASIL REAKSI (DI KANAN TANDA PANAH) Menyatakan perbandingan mol dari pereaksi dan hasil reaksi

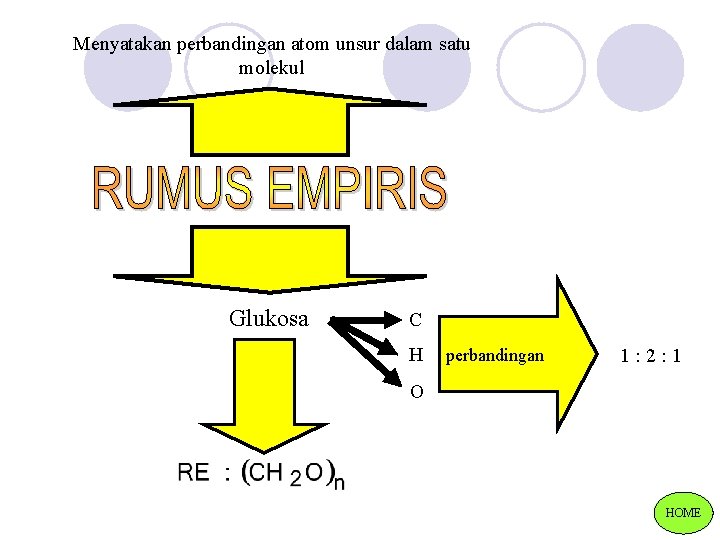
Menyatakan perbandingan atom unsur dalam satu molekul Glukosa C H perbandingan 1: 2: 1 O HOME

Menyatakan baik jenis maupun jumlah atom yang terdapat dalam satu molekul penelitian HOME
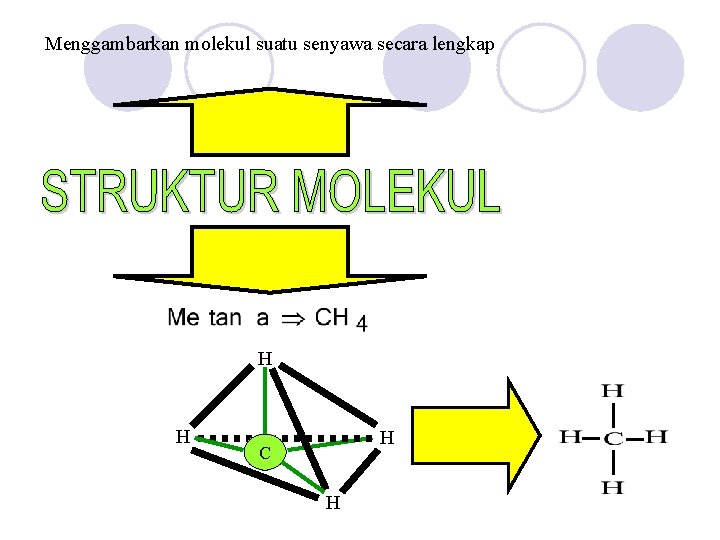
Menggambarkan molekul suatu senyawa secara lengkap H H H C H
- Slides: 30