BAB VII TERMOKIMIA Sifat sifat energi dan jenis

BAB VII TERMOKIMIA Sifat –sifat energi dan jenis energi Perubahan energi dalam reaksi kimia Kalorimeter Hukum Hess Entalpi Reaksi

ENERGI GERAK/KINETIK

ENERGI NUKLIR

ENERGI KIMIA

ENERGI KIMIA

Energi kimia

Energi Kimia Energi kimia yang terdapat dalam bahan bakar atau makanan yang berasal dari energi potensial atom-atom penyusun bahan bakar atau makanan tersebut yang tertata dalam bentuk molekulnya. Energi kimia yang tersimpan ini dapat dilepas dengan cara melakukan pembakaran atau metabolisme.

ENERGI Kesanggupan melakukan kerja KERJA Usaha yg dilakukan untuk memindahkan benda sejauh jarak d dg gaya F → W= F. d Kerja yg dilakukan oleh gaya sebesar 1 N sepanjang jarak 1 m � 1 Nm = 1 kgm 2 dt-2 = 1 J 1 kalori = 4, 184 J
PANAS Jumlah energi yg dipunyai benda →sifat ekstensif Panas Temperatur Satuan Panas : Kalori 1 kalori = jlh panas yg dibutuhkan untuk menaikkan suhu air 1 g sebesar 1°C Menurut Black “ Panas dapat mengalir dari benda yg lebih panas ke benda yang kurang panas tapi jumlah panas total konstan (sebelum dan sesudah proses)” Derajat kepanasan suatu benda→ sifat intensif

Kalorimeter Mengukur panas yang dilepaskan atau diserap oleh sistem pada tekanan kontan (qp) Suatu bejana yg terisolasi yg dilengkapi pengaduk dan termometer Penyekat berfungsi sebagai penghalang terjadinya aliran panas dari atau sekeliling sistem Mula-mula kalorimeter diisi dengan air, dikocok dan tentukan suhunya. Masukan zat lain , aduk sampai homogen dan tentukan lagi suhunya Pada suhu seimbang didapatkan • Qyang dilepas dari sistem = Q yg diterima lingkungan • Sistem = reaksi • Lingkungan = air + bomb (chamber/kalorimeter) • Q kalorimeter ditentukan dari harga air kalorimeter → kapasitas kalorimeter untuk menyerap atau melapas energi yg disetarakan dengan berat air

Perhitungan untuk kalorimeter q = m. c. T q: kalor, panas m: massa Kalor/ panas jenis spesifik (c) adalah jumlah panas yang diperlukan temperatur 1 gram zat sebesar 1 K untuk merubah q = C. T Kapasitas kalor molar (C) adalah jumlah panas yang diperlukan untuk merubah temperatur 1 mol zat sebesar 1 K

Bom Kalorimeter yg digunakan untuk menghitung perubahan energi yg terjadi dalam reaksi pembakaran Caranya : Zat dibakar dengan gas O 2 berlebihan dalam suatu chamber (bom= bejana yang berdinding tebal) Bom dicelupkan kedalam air dan tentukan suhu kalorimeter sebelum dan sesudah pencelupan bom

Latihan Sebanyak 250 g air dipanaskan dalam kalorimeter. Berapa panas yang diperlukan untuk merubah suhu air dari 22 C ke 98 C ? Panas spesifik air adalah 4, 18 J/g. C Diketahui: massa sampel (m) = 250 g perubahan suhu ( T) = 98 C – 22 C = 76 C Ditanya Jawab rumus: : Kalor/ panas yang diserap oleh air (q) : Kalor/ panas yang diserap oleh air dihitung dengan menggunakan q = m. c. T = 250 g. 4, 184 J/g C. (98 C – 22 C) = 7, 9 104 J Jadi 250 g air membutuhkan kalor/panas sebesar 7, 9 104 J untuk merubah suhu dari 22 C menjadi 98 C

Latihan Sebanyak 100 g besi dimasukkan kedalam air mendidih sehingga suhu menjadi 100 C. Kemudian besi dari 100 C ini dimasukkan kedalam kalorimeter yang harga airnya = 20 g, yang mengandung air 300. 0 g air dari 25 C. Temperatur air naik menjadi 27. 60 C. Tentukan panas spesifik besi, bila ρ air = 1 kal/g C Diketahui: massa sampel (m) = 100 g perubahan suhu ( T) = 27. 60 C – 25 C = 2. 6 C Ditanya : panas spesifik besi = ρ besi Jawab : panas yang dipindahkan dari besi ke kalorimeter q = m. c. T = (100 g) x(100 -27. 6) C x (ρbesi kal/g. C) = 7240 ρbesi kal Panas yg diambil dari kalorimeter adalah = (300 g) x(27. 6 -25) C x (1 kal/g. C) + (20 g) nx(27. 6 -25) C x (1 kal/g. C) = 832 kal Persamaan 832 kal = 7240 ρbesi kal ρbesi = 0. 115 kal/g C

Latihan Sebanyak 1, 000 g sampel etanol dibakar dalam kalorimeter bom yang berisi air sebanyak 3000 g. Temperatur air meningkat dari 24, 284 C menjadi 26, 225 C. Kapasitas panas kalorimeter adalah 2, 71 k. J/ C. Berapa jumlah panas yang dihasilkan dari pembakaran etanol. Diketahui: massa air dalam kalorimeter (m) = 3000 g peubahan suhu ( T) = 26, 225 C– 24, 284 C = 1, 941 C C =2, 71 k. J/ C Ditanya : Kalor/ panas yang dihasilkan dari pembakaran etanol (q) Jawab etanol dihitung dengan menggunakan rumus: q 1 = m. c. T • Kalor/ panas yang diserap oleh air q 2 = C. T • Kalor/ panas yang dihasilkan dari pembakaran etanol (q total) dihitung dengan menjumlahkan panas yang diserap air dan kalorimeter

Panas yang dilepas dari reaksi etanol ke air q = m. c. T = 3000 g. 4, 184 J/g C. (1, 941 C) = 24, 36 103 J = 24, 36 k. J Panas dari reaksi etanol ke kalorimeter q = C. T = 2, 71 k. J/ C. (1, 941 C) = 5, 26 k. J Panas total dari reaksi 1, 000 g etanol adalah 24, 36 k. J + 5, 26 k. J = 29, 62 k. J Jadi panas yang dihasilkan dari pembakaran 1, 000 g etanol adalah 29, 62 k. J

Konsep Energi SISTEM : Bahagian tertentu dari alam semesta yang merupakan pusat perhatian yang diteliti Lingkungan : Segala sesuatu yang berada diluar Sistem/tempat melakukan pengamatan Eksotermik : proses pelepasan energi sebagai kalor LINGKUNGAN SISTEM Materi dan energi Endotermik : proses yang menyerap energi sebagai kalor Antara sistem dan lingkungan dapat terjadi pertukaran energi dan materi

Wsistem < 0 (-) : bila sistem melakukan kerja Wsistem > 0 (+): bila sistem dikenai kerja Q < 0 (-): bila energi dilepas sistem (eksotermis) Q > 0 (+): bila energi diserap sistem (endotermis) W (+) : pemampatan gas dalam silinder aki mobil dicas W (-) : gas memuai dalam silinder kalor (q), energi yang dipindahkan melalui Batas-batas sistem, akibat adanya perbedaan temperatur antara sistem dengan lingkungan Q (-) Q (+) sistem W (+) W (-)

Hukum Termodinamika I Kombinasi antara materi dan energi di alam semesta adalah tetap Lebih dikenal sebagai hukum kekekalan energi: Energi tidak dapat diciptakan atau dimusnahkan melalui reaksi kimia atau perubahan fisika. Euniv = Esis + Eling = 0 Dapat dikatakan bahwa perubahan energi internal sistem sebanding dengan jumlah panas yang diperoleh atau hilang dari sistem dan kerja yang dilakukan ke atau oleh sistem Esis = q + w

“ Energi dalam sistem besarnya tetap kecuali jika diubah dengan melakukan kerja atau pemanasan “
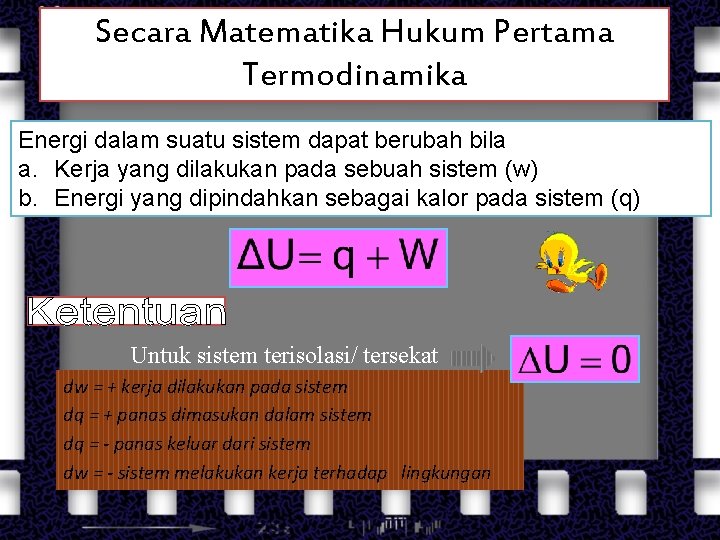
Secara Matematika Hukum Pertama Termodinamika Energi dalam suatu sistem dapat berubah bila a. Kerja yang dilakukan pada sebuah sistem (w) b. Energi yang dipindahkan sebagai kalor pada sistem (q) Untuk sistem terisolasi/ tersekat dw = + kerja dilakukan pada sistem dq = + panas dimasukan dalam sistem dq = - panas keluar dari sistem dw = - sistem melakukan kerja terhadap lingkungan
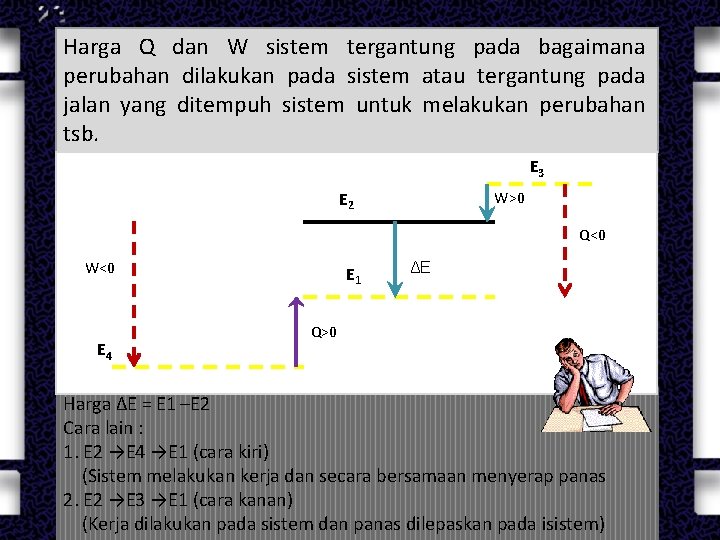
Harga Q dan W sistem tergantung pada bagaimana perubahan dilakukan pada sistem atau tergantung pada jalan yang ditempuh sistem untuk melakukan perubahan tsb. E 3 E 2 W>0 Q<0 W<0 E 4 E 1 ΔE Q>0 Harga ΔE = E 1 –E 2 Cara lain : 1. E 2 →E 4 →E 1 (cara kiri) (Sistem melakukan kerja dan secara bersamaan menyerap panas 2. E 2 →E 3 →E 1 (cara kanan) (Kerja dilakukan pada sistem dan panas dilepaskan pada isistem)

Entalpi Hampir semua reaksi kimia dan perubahan fisika terjadi pada temperatur konstan. Jumlah panas yang ditransfer kedalam atau keluar sistem saat terjadi reaksi kimia atau perubahan fisika pada temperatur konstan, qp didefenisikan sebagai perubahan entalpi H dari proses. Perubahan entalpi sebanding dengan panas (qp) yang bertambah atau hilang oleh sistem saat terjadi proses pada temperatur konstan. H = qp

Penentuan Entalpi Reaksi H = Hakhir - Hawal atau contoh: H = Hproduk - Hreaktan 2 H 2(g) + O 2(g) 2 H 2 O(g) H = -483, 6 k. J • H negatif, menunjukan hasil reaksi melepaskan panas (eksotermik) • Reaksi ini menghasilkan energi 483, 6 kilo Joule saat 2 mol H 2 bereaksi dengan 1 mol O 2 menghasilkan 2 mol H 2 O.

Diagram Energi Sifat-sifat Entalpi: 1. Entalpi adalah sifat ekstensif (terukur berdasarkan banyak materi yang diukur. Besar H tergantung pada jumlah reaktan yang dipakai. 2. Reaksi kimia yang sama tapi dengan arah yang berlawanan memiliki besar entalpi yang sama tapi dengan tanda yang berlawanan 3. Perubahan entalpi suatu reaksi tergantung pada keadaan reaktan dan produk (g, l atau s)

Keadaan Entalpi Suatu Sistem Jika entalpi sistem lebih besar pada akhir reaksi, maka sistem menyerap panas dari lingkungan (reaksi endotermik) Hfinal > Hinitial dan DH positif (+DH) Jika entalpi sistem lebih rendah pada akhir reaksi, maka sistem memberikan panas pada lingkungan (reaksi eksotermik) Hfinal < Hinitial dan DH negatif (-DH)

Latihan Dari reaksi pembakaran metana berikut, berapa energi yang dilepas jika sebanyak 4, 5 g metana dibakar pada tekanan konstan ? CH 4(g) + 2 O 2(g) CO 2(g) + 2 H 2 O(g) H = -802 k. J Jawab: Tanda negatif (eksotermik) menunjukan sebanyak 225, 5 k. J energi dilepaskan oleh sistem ke lingkungan.

Hukum HESS “Perubahan entalpi dari suatu reaksi adalah selalu sama, meski reaksi tersebut berlangsung satu tahap atau lebih” H 0 rx dari suatu reaksi yang terdiri atas beberapa tahapan reaksi merupakan jumlah dari perubahan entalpi seluruh tahapan Data sejumlah perubahan entalpi reaksi dapat digunakan untuk menentukan H 0 rx reaksi yang lain

Latihan (1) (2) Perubahan entalpi suatu reaksi dihitung dengan menjumlahkan perubahan entalpi tahapan reaksinya. Tahapan reaksi dapat dirubah arah reaksinya disesuaikan dengan reaksi akhir. H 0 C(s) + O 2 CO 2(g) CO + O 2(g) -393, 5 k. J -(-283, 0 k. J)
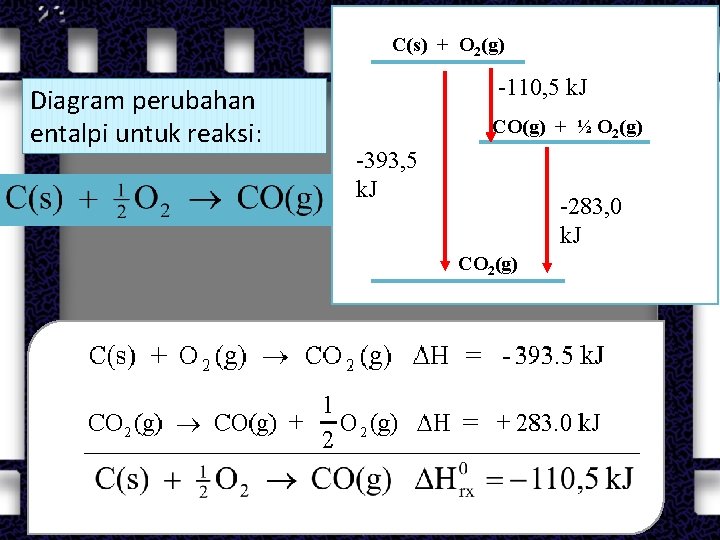
C(s) + O 2(g) Diagram perubahan entalpi untuk reaksi: -110, 5 k. J CO(g) + ½ O 2(g) -393, 5 k. J -283, 0 k. J CO 2(g)
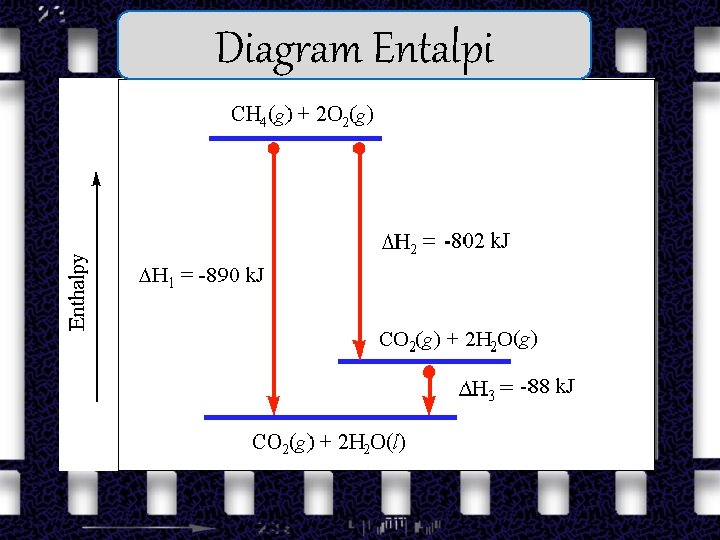
Diagram Entalpi

Perubahan entalpi standar, merupakan perubahan entalpi yang dihasilkan dari reaksi perubahan sejumlah mol reaktan menjadi sejumlah mol produk, dalam keadaan standar. • Keadaan standar senyawa dalam fase cair atau padat adalah keadaan senyawa cair atau padat tersebut dalam bentuk murni • Keadaan standar fase gas adalah pada tekanan satu atmosfir • Keadaan standar larutan adalah pada konsentrasi satu molar Entalpi pembentukan standar adalah perubahan entalpi untuk reaksi pembentukan satu mol senyawa dari unsur-unsurnya, biasa disebut juga sebagai panas pembentukan standar. menunjukan tekanan standar pada 1 atmosfir • Nilai negatif (-) menunjukan reaksi pembentukan terjadi secara eksoterm • Nilai positif (+) menunjukan reaksi pembentukan terjadi secara endoterm

Menentukan Entalpi Reaksi dari Entalpi Pembentukan Contoh: Tentukan H 0 rx reaksi berikut pada suhu 298 K Penyelesaian

Menentukan Entalpi Reaksi dari Energi Ikatan Jumlah energi yang diperlukan untuk memutus satu mol ikatan kovalen senyawa dalam keadaan gas untuk menghasilkan produk pada kondisi temperatur dan tekanan konstan. Contoh: Tentukan entalpi reaksi berikut dengan menggunakan data energi ikatan. Semua reaktan merupakan senyawa kovalen berikatan tunggal Br 2(g) + 3 F 2(g) 2 Br. F 3(g)
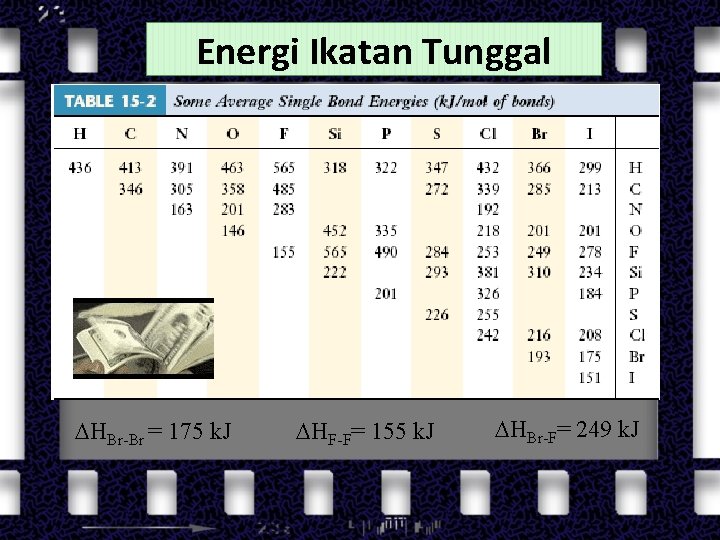
Energi Ikatan Tunggal HBr-Br = 175 k. J HF-F= 155 k. J HBr-F= 249 k. J

Penjelasan dan Penyelesaian Br 2(g) + 3 F 2(g) HBr-Br = 175 k. J HF-F= 155 k. J 2 Br. F 3(g) HBr-F= 249 k. J Setiap 1 molekul Br. F 3 memiliki 3 ikatan Br F, maka 2 mol Br. F 3 memiliki 6 mol ikatan Br - F Setiap 1 molekul F 2 memiliki 1 ikatan F F, maka 3 mol F 2 memiliki 6 mol ikatan F- F Setiap 1 molekul Br 2 memiliki 1 ikatan Br Br, maka 1 mol F 2 memiliki 1 mol ikatan Br - Br = 175 + 3(155) - 6(249) = -854 k. J per mol reaksi
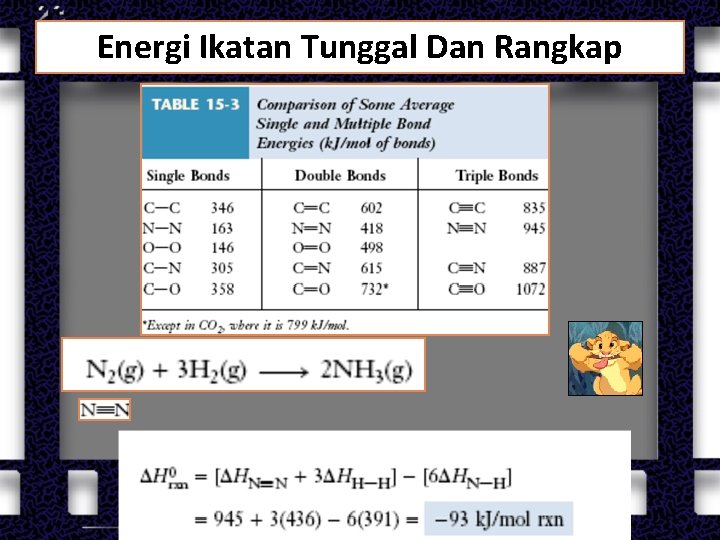
Energi Ikatan Tunggal Dan Rangkap
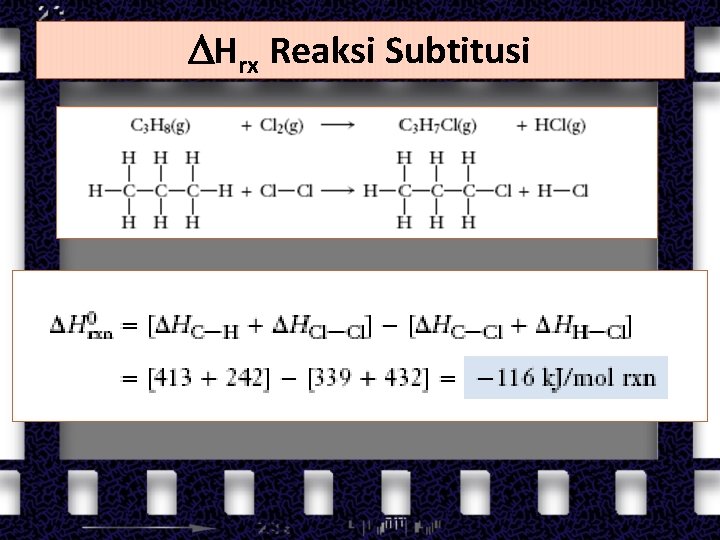
Hrx Reaksi Subtitusi

Perubahan Energi Dalam Energi dalam, E dari suatu senyawa merupakan semua energi yang dimiliki dalam senyawa tersebut, seperti energi kinetik, energi tarik dan tolak antar partikel subatom dll. E = Eakhir – Eawal = Eproduk - Ereaktan = q +w E = q - P V karena w = - P V maka; Pada gas ideal; P V = ( n)RT Pada volume konstan; E = qv E = q + w • q positif, panas diserap sistem dari lingkungan • q negatif, panas dilepas sistem ke lingkungan • w positif, kerja dilakukan terhadap sistem • w negatif, kerja dilakukan oleh sistem

Hubungan H dengan E Defenisi dasar entalpi: H = E + PV H = E + P V pada T dan P konstan Karena E = q + w maka, H = q + w + P V pada T dan P konstan Pada tekanan konstan; w = - P V H = q + (- P V) + P V H = qp Untuk gas ideal; H = E + ( n) RT
- Slides: 41