Bab 3 Stoikiometri Secara Mikro atom molekul Secara

Bab 3 Stoikiometri
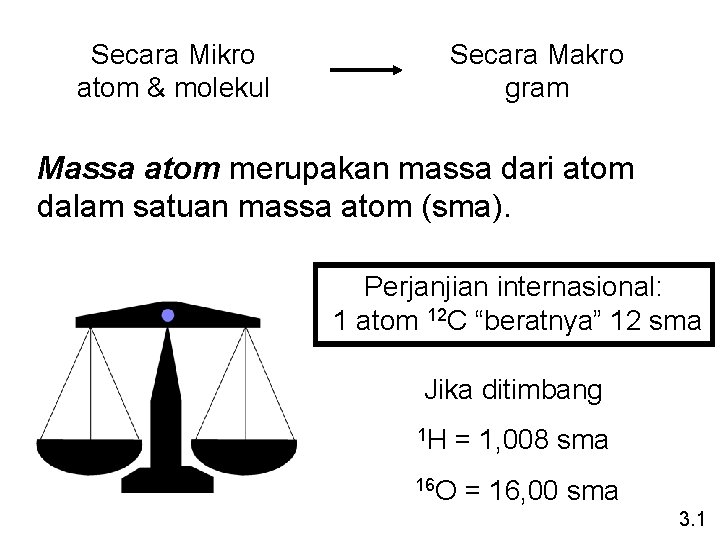
Secara Mikro atom & molekul Secara Makro gram Massa atom merupakan massa dari atom dalam satuan massa atom (sma). Perjanjian internasional: 1 atom 12 C “beratnya” 12 sma Jika ditimbang 1 H = 1, 008 sma 16 O = 16, 00 sma 3. 1
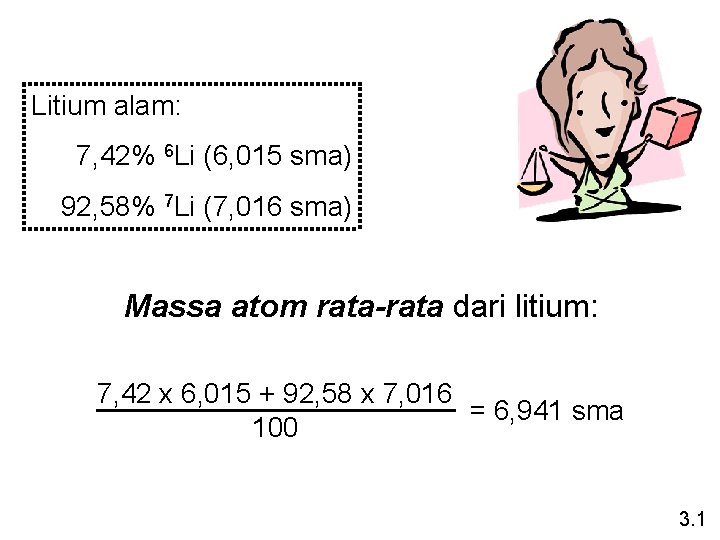
Litium alam: 7, 42% 6 Li (6, 015 sma) 92, 58% 7 Li (7, 016 sma) Massa atom rata-rata dari litium: 7, 42 x 6, 015 + 92, 58 x 7, 016 = 6, 941 sma 100 3. 1
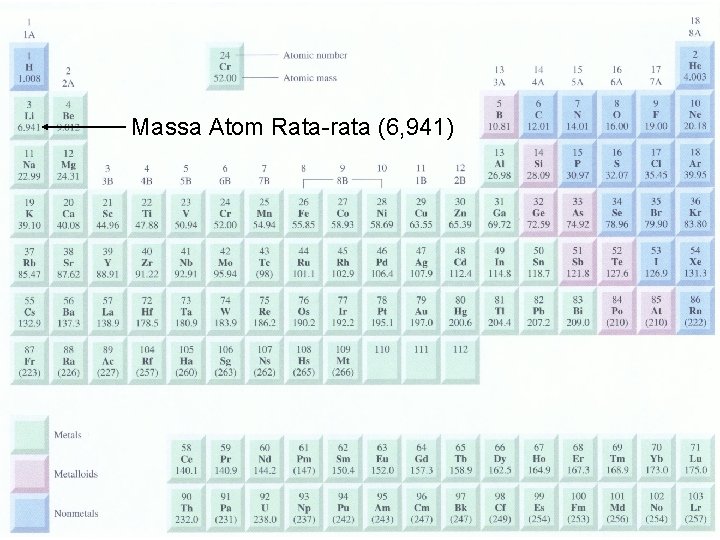
Massa Atom Rata-rata (6, 941)

Mol adalah banyaknya suatu zat yang mengandung entitas dasar (atom, molekul, atau partikel lain) sebanyak jumlah atom yang terdapat dalam 12 gram karbon-12. 1 mol = NA = 6, 0221367 x 1023 Bilangan Avogadro (NA) 3. 2
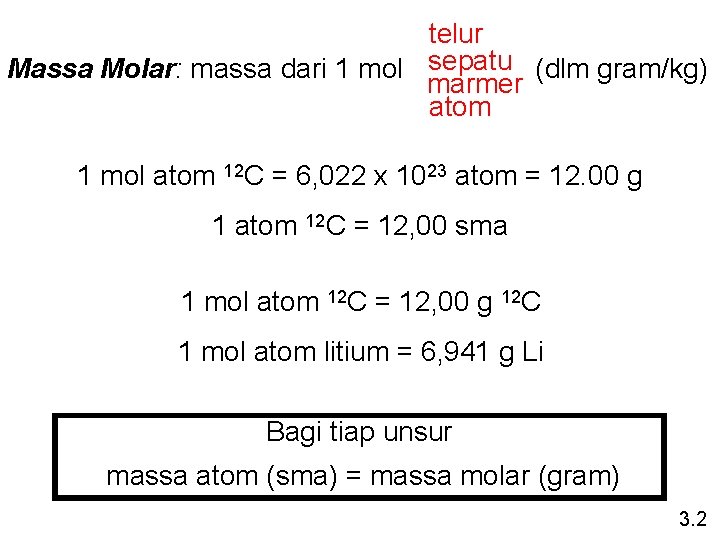
telur Massa Molar: massa dari 1 mol sepatu (dlm gram/kg) marmer atom 1 mol atom 12 C = 6, 022 x 1023 atom = 12. 00 g 1 atom 12 C = 12, 00 sma 1 mol atom 12 C = 12, 00 g 12 C 1 mol atom litium = 6, 941 g Li Bagi tiap unsur massa atom (sma) = massa molar (gram) 3. 2

Satu mol dari: S C Hg Cu Fe 3. 2
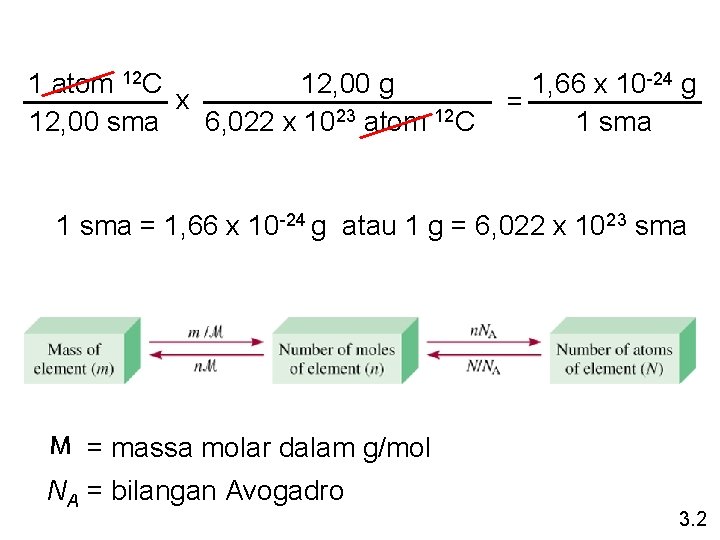
1 atom 12 C 12, 00 g x 12, 00 sma 6, 022 x 1023 atom 12 C 1, 66 x 10 -24 g = 1 sma = 1, 66 x 10 -24 g atau 1 g = 6, 022 x 1023 sma M = massa molar dalam g/mol NA = bilangan Avogadro 3. 2

Apakah Anda Sudah Mengerti Massa Molar? berapa jumlah atom pada 0, 551 g potasium (K) ? 1 mol K = 39, 10 g K 1 mol K = 6, 022 x 1023 atom K 1 mol K 6, 022 x 1023 atom K 0, 551 g K x x = 1 mol K 39, 10 g K 8, 49 x 1021 atom K 3. 2
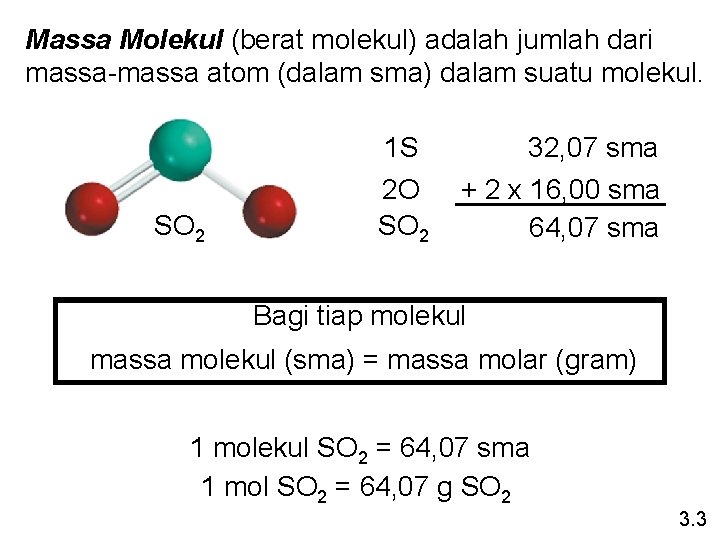
Massa Molekul (berat molekul) adalah jumlah dari massa-massa atom (dalam sma) dalam suatu molekul. 1 S SO 2 2 O SO 2 32, 07 sma + 2 x 16, 00 sma 64, 07 sma Bagi tiap molekul massa molekul (sma) = massa molar (gram) 1 molekul SO 2 = 64, 07 sma 1 mol SO 2 = 64, 07 g SO 2 3. 3
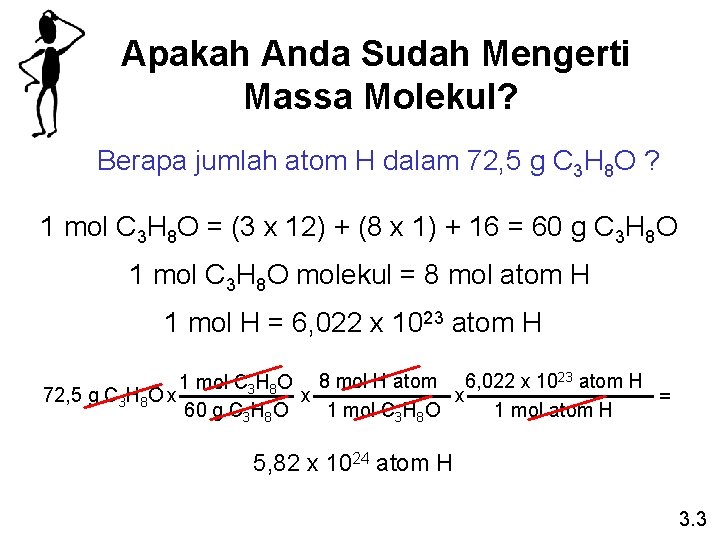
Apakah Anda Sudah Mengerti Massa Molekul? Berapa jumlah atom H dalam 72, 5 g C 3 H 8 O ? 1 mol C 3 H 8 O = (3 x 12) + (8 x 1) + 16 = 60 g C 3 H 8 O 1 mol C 3 H 8 O molekul = 8 mol atom H 1 mol H = 6, 022 x 1023 atom H 1 mol C 3 H 8 O 8 mol H atom 6, 022 x 1023 atom H 72, 5 g C 3 H 8 O x x x = 1 mol C 3 H 8 O 1 mol atom H 60 g C 3 H 8 O 5, 82 x 1024 atom H 3. 3
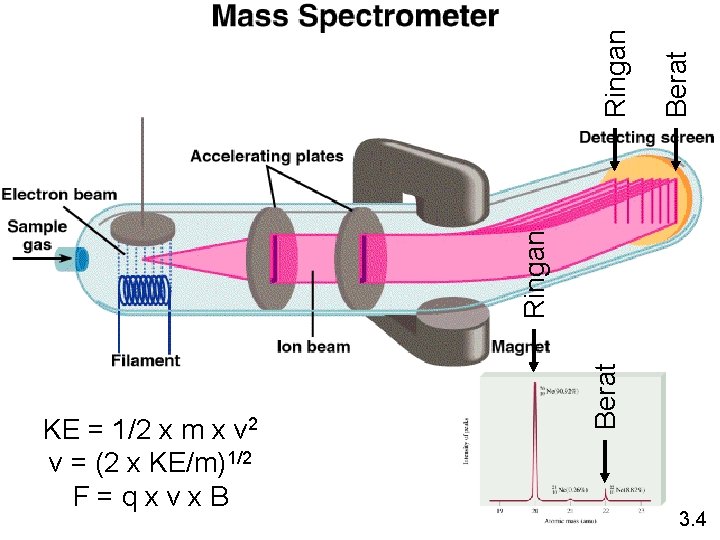
Berat Ringan KE = 1/2 x m x v 2 v = (2 x KE/m)1/2 F=qxvx. B 3. 4
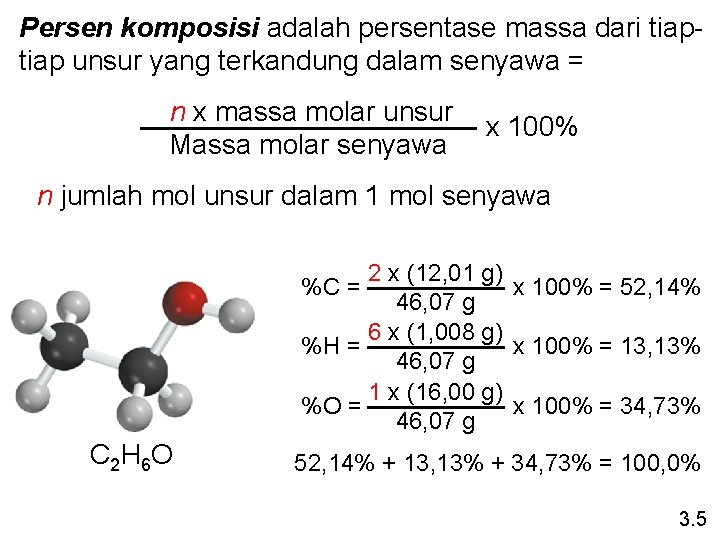
Persen komposisi adalah persentase massa dari tiap unsur yang terkandung dalam senyawa = n x massa molar unsur Massa molar senyawa x 100% n jumlah mol unsur dalam 1 mol senyawa 2 x (12, 01 g) x 100% = 52, 14% 46, 07 g 6 x (1, 008 g) %H = x 100% = 13, 13% 46, 07 g 1 x (16, 00 g) %O = x 100% = 34, 73% 46, 07 g %C = C 2 H 6 O 52, 14% + 13, 13% + 34, 73% = 100, 0% 3. 5
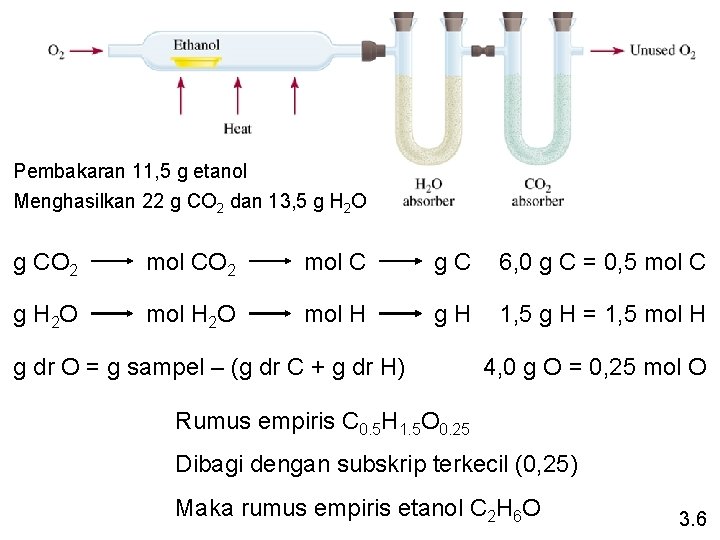
Pembakaran 11, 5 g etanol Menghasilkan 22 g CO 2 dan 13, 5 g H 2 O g CO 2 mol C g. C 6, 0 g C = 0, 5 mol C g H 2 O mol H g. H 1, 5 g H = 1, 5 mol H g dr O = g sampel – (g dr C + g dr H) 4, 0 g O = 0, 25 mol O Rumus empiris C 0. 5 H 1. 5 O 0. 25 Dibagi dengan subskrip terkecil (0, 25) Maka rumus empiris etanol C 2 H 6 O 3. 6
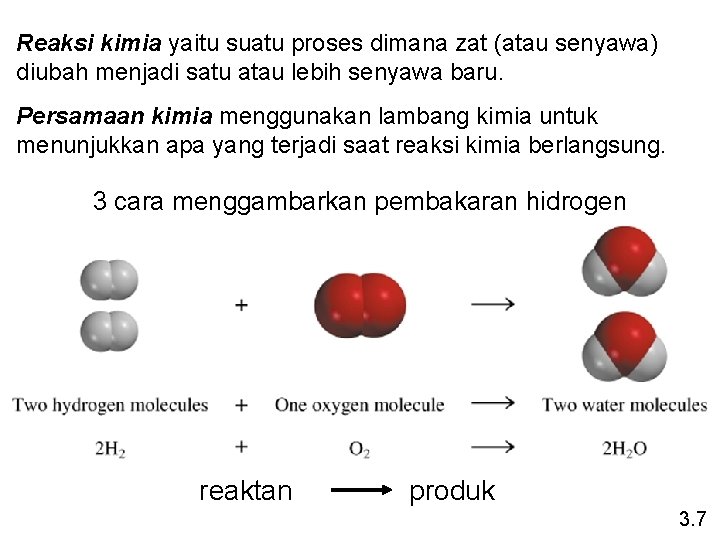
Reaksi kimia yaitu suatu proses dimana zat (atau senyawa) diubah menjadi satu atau lebih senyawa baru. Persamaan kimia menggunakan lambang kimia untuk menunjukkan apa yang terjadi saat reaksi kimia berlangsung. 3 cara menggambarkan pembakaran hidrogen reaktan produk 3. 7
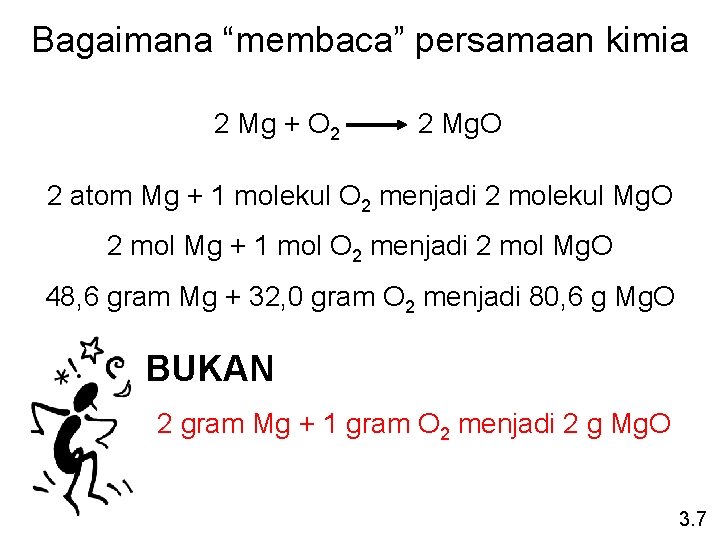
Bagaimana “membaca” persamaan kimia 2 Mg + O 2 2 Mg. O 2 atom Mg + 1 molekul O 2 menjadi 2 molekul Mg. O 2 mol Mg + 1 mol O 2 menjadi 2 mol Mg. O 48, 6 gram Mg + 32, 0 gram O 2 menjadi 80, 6 g Mg. O BUKAN 2 gram Mg + 1 gram O 2 menjadi 2 g Mg. O 3. 7

Menyetarakan Persamaan Kimia 1. Identifikasi semua reaktan dan produk kemudian tulis rumus molekul yang benar masing-masing pada sisi kiri dan kanan dari persamaan. Etana bereaksi dg oksigen membentuk karbon dioksida dan air C 2 H 6 + O 2 CO 2 + H 2 O 2. Ubah koefisien (angka di depan rumus molekul) tetapi jangan ubah subskripnya (angka dalam rumus molekul). 2 C 2 H 6 BUKAN C 4 H 12 3. 7

Menyetarakan Persamaan Kimia 3. Pertama-tama, carilah unsur yang muncul hanya sekali pada tiap sisi persamaan dengan jumlah atom yang sama pada tiap sisi. C 2 H 6 + O 2 2 karbon di kiri C 2 H 6 + O 2 6 hidrogen di kiri C 2 H 6 + O 2 CO 2 + H 2 O mulai dari C atau H bukan O 1 karbon di kanan kalikan CO 2 dengan 2 2 CO 2 + H 2 O 2 hidrogen di kanan 2 CO 2 + 3 H 2 O kalikan H 2 O dengan 3 3. 7

Menyetarakan Persamaan Kimia 4. Periksa persamaan yang disetarakan tersebut untuk memastikan jumlah total tiap jenis atom pada kedua sisi persamaan adalah sama. C 2 H 6 + O 2 2 oksigen di kiri 2 CO 2 + 3 H 2 O Kalikan O 2 dg 7 2 4 oksigen + 3 oksigen = 7 oksigen (3 x 1) di kanan (2 x 2) C 2 H 6 + 7 O 2 2 2 CO 2 + 3 H 2 O 2 C 2 H 6 + 7 O 2 4 CO 2 + 6 H 2 O hilangkan pecahan, Kalikan kedua sisi dg 2 3. 7
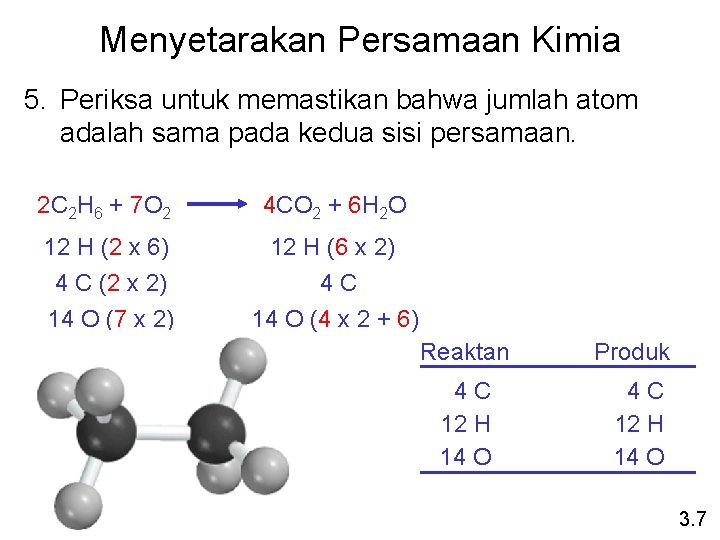
Menyetarakan Persamaan Kimia 5. Periksa untuk memastikan bahwa jumlah atom adalah sama pada kedua sisi persamaan. 2 C 2 H 6 + 7 O 2 4 CO 2 + 6 H 2 O 12 H (2 x 6) 4 C (2 x 2) 12 H (6 x 2) 4 C 14 O (7 x 2) 14 O (4 x 2 + 6) Reaktan Produk 4 C 12 H 14 O 3. 7
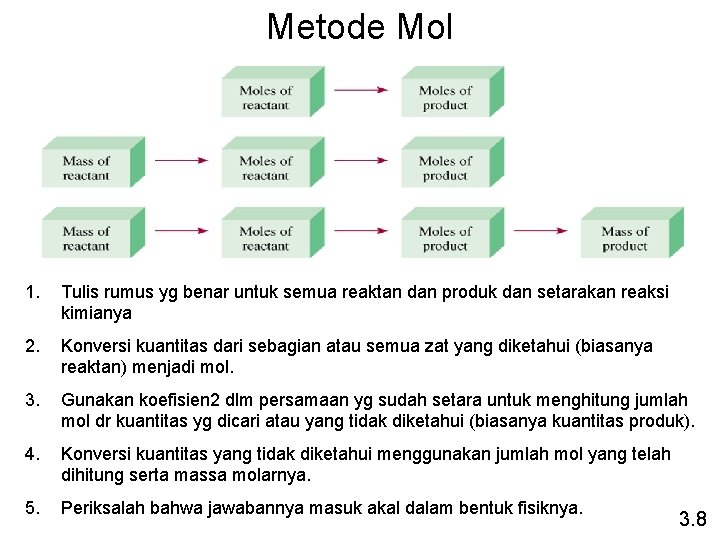
Metode Mol 1. Tulis rumus yg benar untuk semua reaktan dan produk dan setarakan reaksi kimianya 2. Konversi kuantitas dari sebagian atau semua zat yang diketahui (biasanya reaktan) menjadi mol. 3. Gunakan koefisien 2 dlm persamaan yg sudah setara untuk menghitung jumlah mol dr kuantitas yg dicari atau yang tidak diketahui (biasanya kuantitas produk). 4. Konversi kuantitas yang tidak diketahui menggunakan jumlah mol yang telah dihitung serta massa molarnya. 5. Periksalah bahwa jawabannya masuk akal dalam bentuk fisiknya. 3. 8
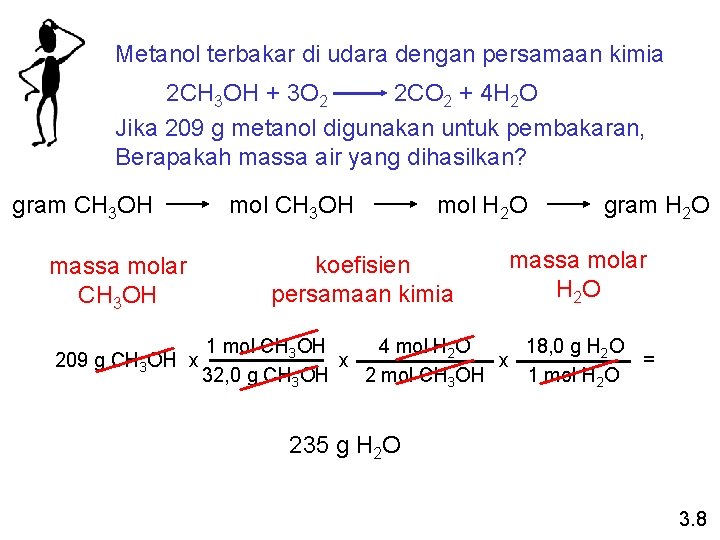
Metanol terbakar di udara dengan persamaan kimia 2 CH 3 OH + 3 O 2 2 CO 2 + 4 H 2 O Jika 209 g metanol digunakan untuk pembakaran, Berapakah massa air yang dihasilkan? gram CH 3 OH massa molar CH 3 OH 209 g CH 3 OH x mol CH 3 OH mol H 2 O koefisien persamaan kimia gram H 2 O massa molar H 2 O 4 mol H 2 O 18, 0 g H 2 O 1 mol CH 3 OH = x x 32, 0 g CH 3 OH 1 mol H 2 O 2 mol CH 3 OH 235 g H 2 O 3. 8
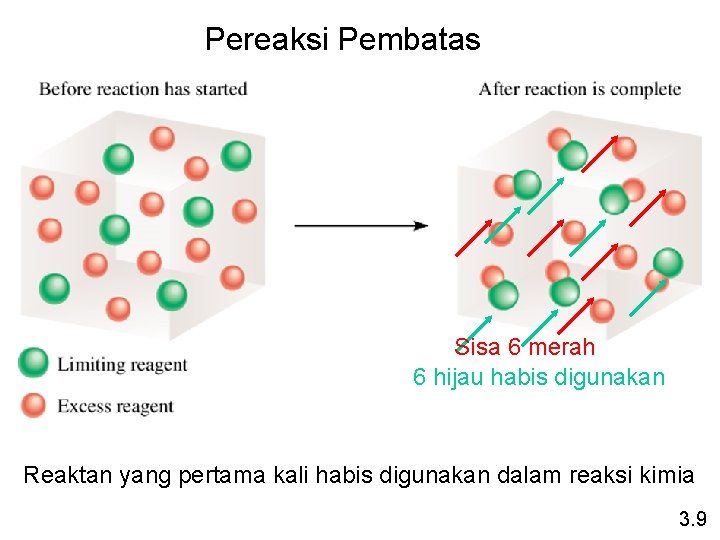
Pereaksi Pembatas Sisa 6 merah 6 hijau habis digunakan Reaktan yang pertama kali habis digunakan dalam reaksi kimia 3. 9

Apakah Anda Mengerti Pereaksi Pembatas? Dlm suatu proses, 124 g Al bereaksi dg 601 g Fe 2 O 3 2 Al + Fe 2 O 3 Al 2 O 3 + 2 Fe Hitung massa Al 2 O 3 yang terbentuk. g Al g Fe 2 O 3 124 g Al x mol Al dibthkan mol Fe 2 O 3 1 mol Al 27. 0 g Al x 124 g Al ATAU dibthkan Al 1 mol Fe 2 O 3 2 mol Al dibthkan Fe 2 O 3 dibthkan g Al 160 g Fe 2 O 3 = x 1 mol Fe 2 O 3 367 g Fe 2 O 3 membthkan 367 g Fe 2 O 3 Menghasilkan Fe 2 O 3 (601 g) shg Al adalah pereaksi pembatas 3. 9
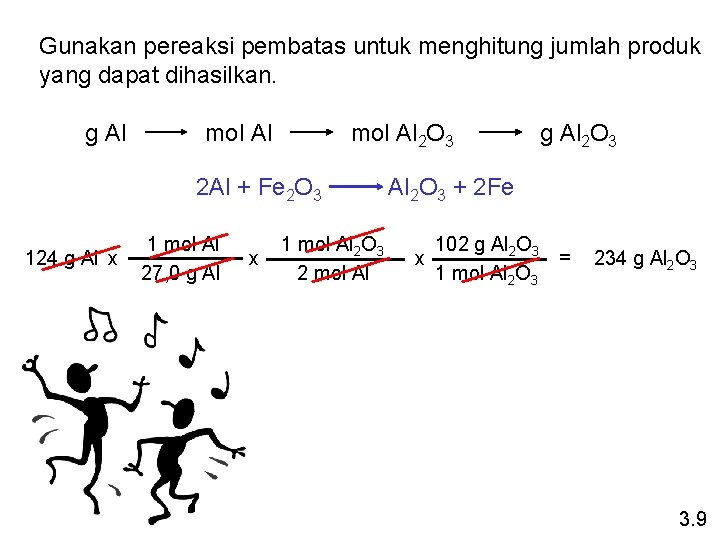
Gunakan pereaksi pembatas untuk menghitung jumlah produk yang dapat dihasilkan. g Al mol Al 2 O 3 2 Al + Fe 2 O 3 124 g Al x 1 mol Al 27, 0 g Al x 1 mol Al 2 O 3 2 mol Al g Al 2 O 3 + 2 Fe 102 g Al 2 O 3 x 1 mol Al 2 O 3 = 234 g Al 2 O 3 3. 9

Hasil Teoritis yaitu jumlah produk yang akan terbentuk jika seluruh pereaksi pembatas terpakai pada reaksi. Hasil Sebenarnya merupakan jumlah produk sebenarnya yang dihasilkan. % Hasil = Hasil Aktual Hasil Teoritis x 100 3. 10

Kimia Dalam Kehidupan: Pupuk Kimia Tumbuhan membutuhkan: N, P, K, Ca, S, & Mg 3 H 2 (g) + N 2 (g) NH 3 (aq) + HNO 3 (aq) 2 NH 3 (g) NH 4 NO 3 (aq) fluorapatite 2 Ca 5(PO 4)3 F (s) + 7 H 2 SO 4 (aq) 3 Ca(H 2 PO 4)2 (aq) + 7 Ca. SO 4 (aq) + 2 HF (g)
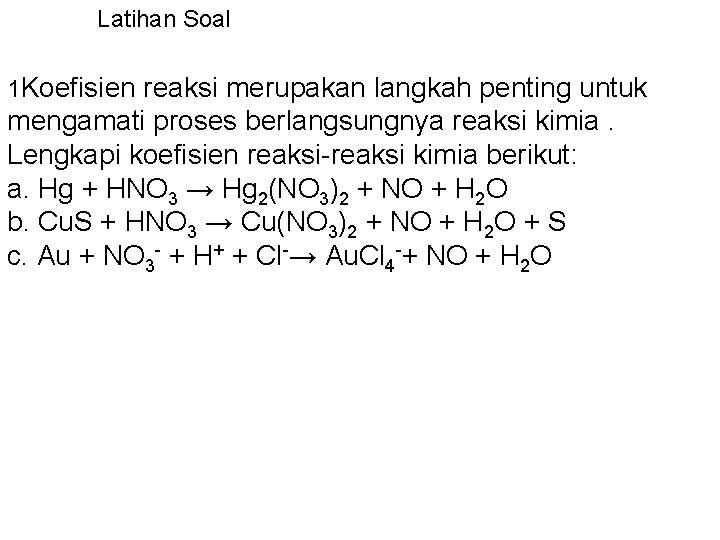
Latihan Soal 1 Koefisien reaksi merupakan langkah penting untuk mengamati proses berlangsungnya reaksi kimia. Lengkapi koefisien reaksi-reaksi kimia berikut: a. Hg + HNO 3 → Hg 2(NO 3)2 + NO + H 2 O b. Cu. S + HNO 3 → Cu(NO 3)2 + NO + H 2 O + S c. Au + NO 3 - + H+ + Cl-→ Au. Cl 4 -+ NO + H 2 O

Logam Aluminium banyak digunakan sebagai wadah minuman ringan bersoda. Salah satu sifat dari logam aluminium adalah dapat larut dalam basa kuat ataupun dalam asam kuat. Bila anda melarutkan sebanyak 2, 05 gram kaleng minuman ringan yang terbuat dari Aluminium(27 g/mol) , 125 m. L larutan KOH 1, 25 M dan terjadi reaksi sebagai berikut : 2 Al(s) + 2 KOH(aq) +6 H 2 O 2 KAl(OH)4(aq) + 3 H 2 a. Hitung mol masing-masing pereaksi, apakah di akhir reaksi masih terdapat sisa aluminium ? b. Tentukan berapa banyak (gram) KAl(OH)4 yang terbentuk Dan berapa volume gas H 2 yang terbentuk ( 1 mol gas =22, 4 Liter) c. Apa Jenis reaksi yang tepat untuk reaksi diatas ? Asam basa, reduksi oksidasi atau penggaraman , Jelaskan jawaban anda

D Apakah jenis garam KAl(OH)4, dan tuliskan reaksi ionisasi dari. KAl(OH)4 dalam air e. Tuliskan reaksi yang terjadi bila ke dalam larutan tersebut ditambahkan sejumlah larutan asam misal HCL secukupnya

a. 2, 05 g Al = 2, 05 g / 27 g/mol = 0, 076 mol 125 m. L KOH 1, 25 M= 125 x 1, 25 x 10 -3 mol = 1, 56 mol 2 Mol Al = 2 mol. KOH atau 1 mol Al = 1 mol KOH Semua logam AL habis bereaksi, terdapat KOH berlebih KAl(OH)4 Yang terbentuk =0, 076 mol x 134 g/mol =10, 184 g Volume gas H 2 = (3/2) x 0, 076 mol x 22, 4 L = 2, 554 L c. Reaksi reduksi oksidasi karena bilangan oksidasi Al berubah dari 0 menjadi +3 dan H dari +1 menjadi 0 d. Garm kompleks /garam basa Dalam air : KAl(OH)4 aq K+(aq) + Al(OH)4 - (aq) e. Kal(OH)4 + HCl KCl + Al(OH)3 (s)

Anda melarutkan 1 gram Na. Cl dalam campuran 90 m. L larutan HCl p. H=1 dan 10 m. L larutan 0, 1 M HAsetat (Ka = 1, 8 x 10 -5). d. Perkiranlah berapa p. H campuran larutan tersebut. (2 poin) e. Berapa m. L larutan Na. OH 0, 1 M yang dibutuhkan untuk menetralkan semua kandungan asam dalam campuran larutan tersebut. Tuliskan reaksi yang terjadi (3 poin) f. Setelah semua asam dinetralkan, bagaimana p. H larutan tersebut ? Bersifat asam, basa atau netral. Jelaskan jawaban anda

- Slides: 33