BAB 3 PERSAMAAN KEADAAN OVERVIEW Persamaan keadaan adalah

BAB 3 PERSAMAAN KEADAAN

OVERVIEW Persamaan keadaan adalah persamaan yang menyatakan hubungan antara state variable yang menggambarkan keadaan dari suatu sistem pada kondisi fisik tertentu State variable adalah Property dari sistem yang hanya tergantung pada keadaan sistem saat ini, bukan pada jalannya proses. • • Temperatur Tekanan Density Enthalpy Entropy Kapasitas Panas Energi bebas Gibbs Fugasitas
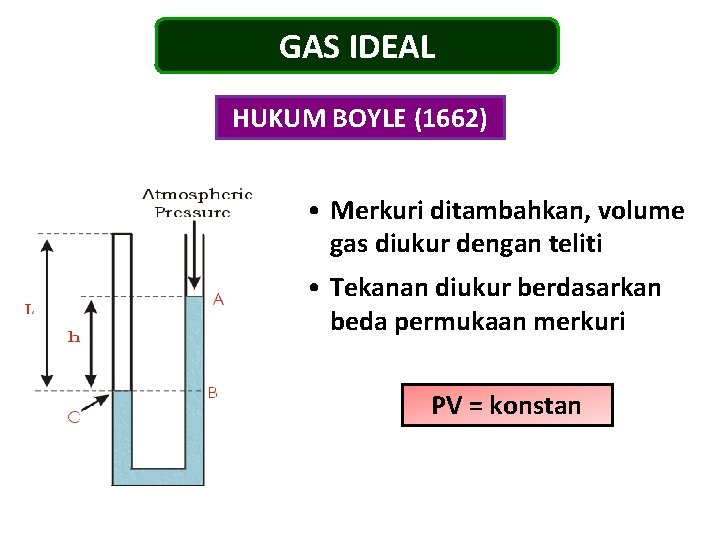
GAS IDEAL HUKUM BOYLE (1662) • Merkuri ditambahkan, volume gas diukur dengan teliti • Tekanan diukur berdasarkan beda permukaan merkuri PV = konstan
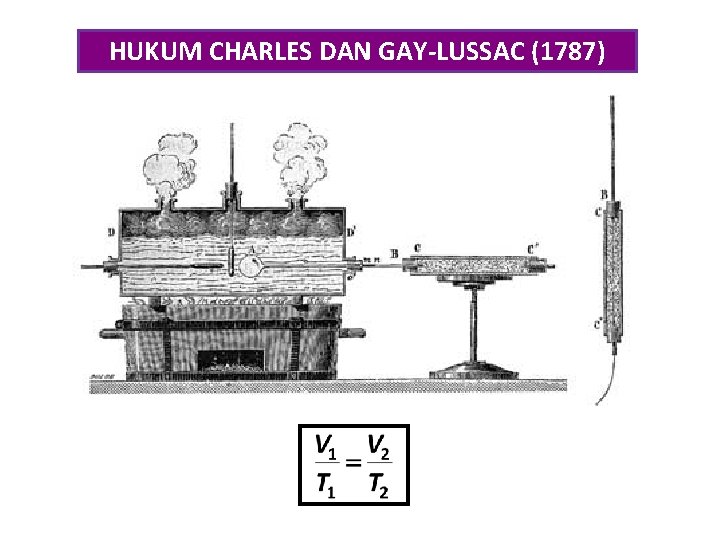
HUKUM CHARLES DAN GAY-LUSSAC (1787)

Pada tahun 1834 Émile Clapeyron menggabungkan Hukum Boyle dan Hukum Charles menjadi: Hukum Gas Ideal.

Asumsi: • Molekul/atom gas identik dan tidak menempati ruang • Tidak ada gaya antar molekul • Molekul/atom penyusunnya menabrak dinding wadah dengan tabrakan yang elastis sempurna Keberlakuan: P 0 (P < 1, 5 bar)
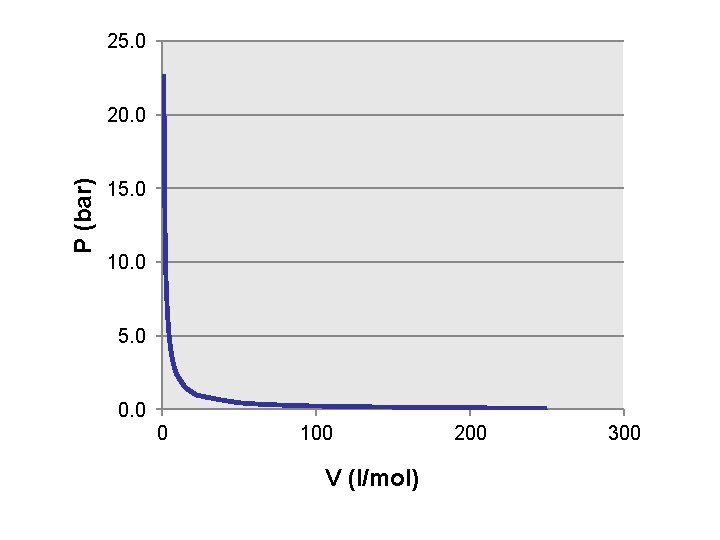
25. 0 P (bar) 20. 0 15. 0 10. 0 5. 0 0 100 V (l/mol) 200 300
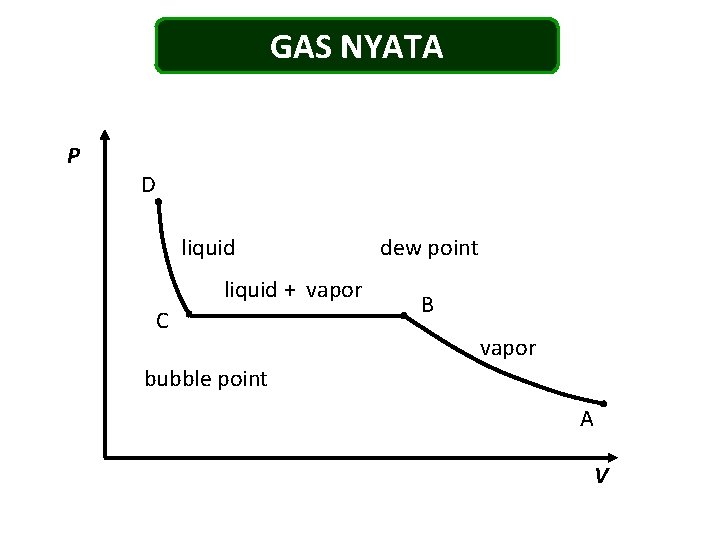
GAS NYATA P D liquid + vapor C dew point B vapor bubble point A V
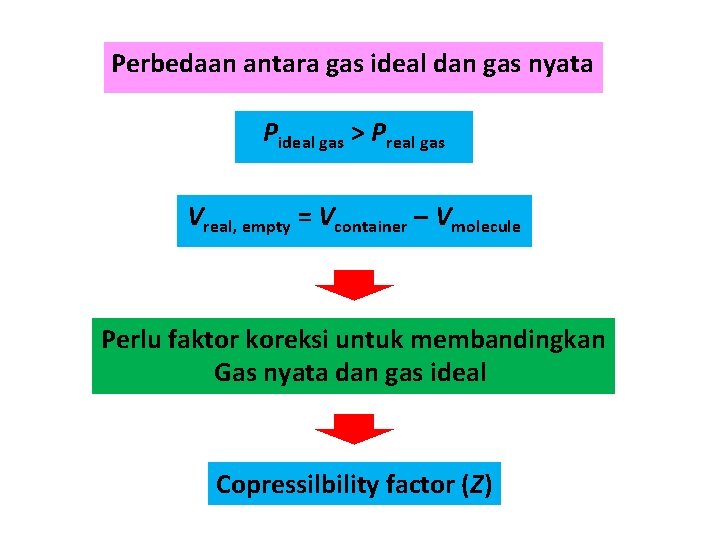
Perbedaan antara gas ideal dan gas nyata Pideal gas > Preal gas Vreal, empty = Vcontainer – Vmolecule Perlu faktor koreksi untuk membandingkan Gas nyata dan gas ideal Copressilbility factor (Z)
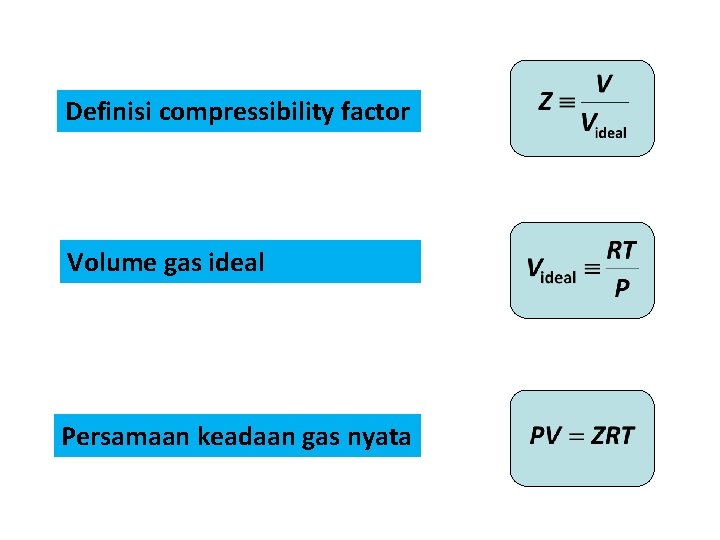
Definisi compressibility factor Volume gas ideal Persamaan keadaan gas nyata
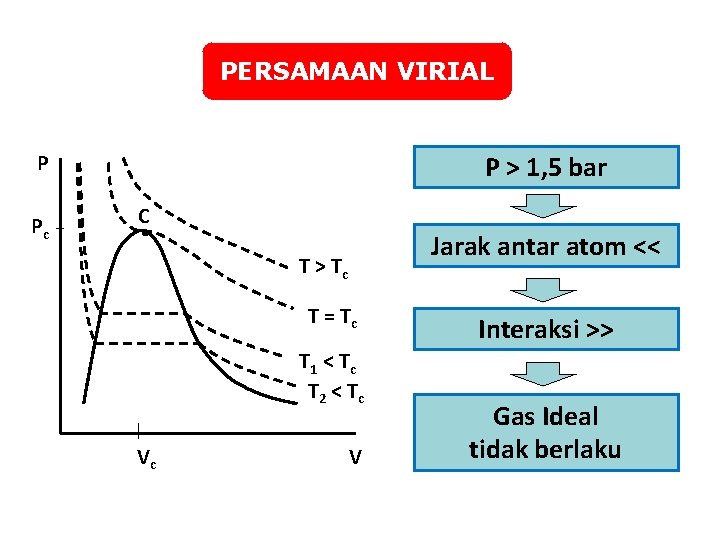
PERSAMAAN VIRIAL P > 1, 5 bar P Pc C Jarak antar atom << T > Tc T = Tc T 1 < T c T 2 < T c Vc V Interaksi >> Gas Ideal tidak berlaku
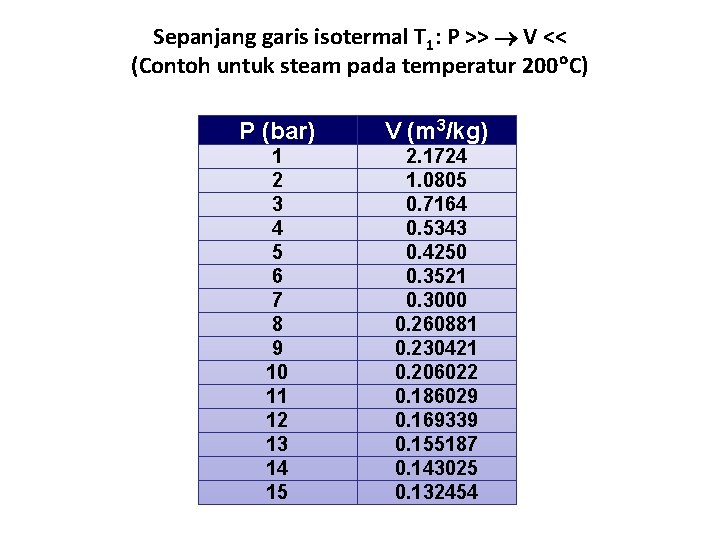
Sepanjang garis isotermal T 1: P >> V << (Contoh untuk steam pada temperatur 200 C) P (bar) V (m 3/kg) 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 2. 1724 1. 0805 0. 7164 0. 5343 0. 4250 0. 3521 0. 3000 0. 260881 0. 230421 0. 206022 0. 186029 0. 169339 0. 155187 0. 143025 0. 132454
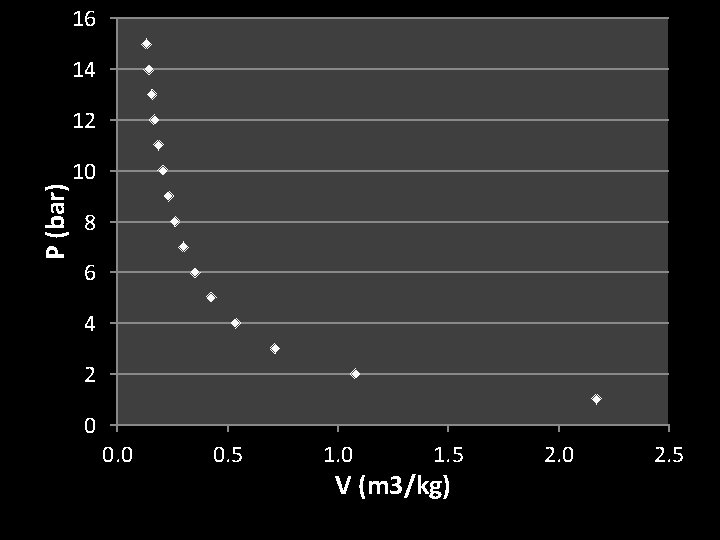
16 14 P (bar) 12 10 8 6 4 2 0 0. 5 1. 0 1. 5 V (m 3/kg) 2. 0 2. 5
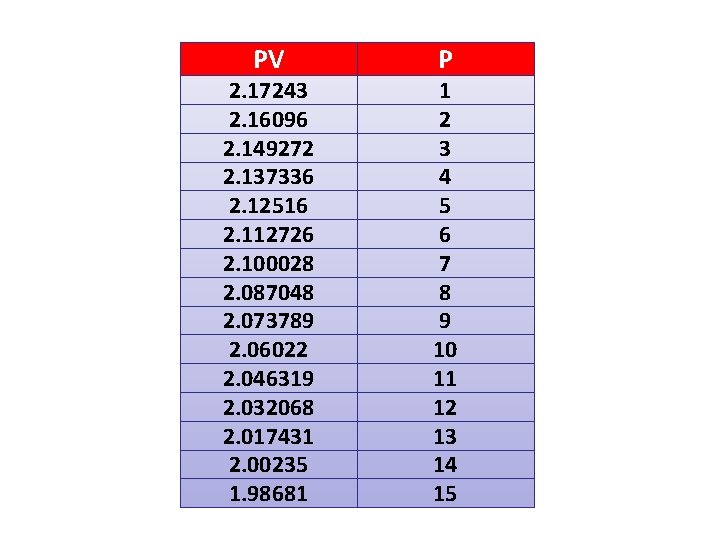
PV 2. 17243 2. 16096 2. 149272 2. 137336 2. 12516 2. 112726 2. 100028 2. 087048 2. 073789 2. 06022 2. 046319 2. 032068 2. 017431 2. 00235 1. 98681 P 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
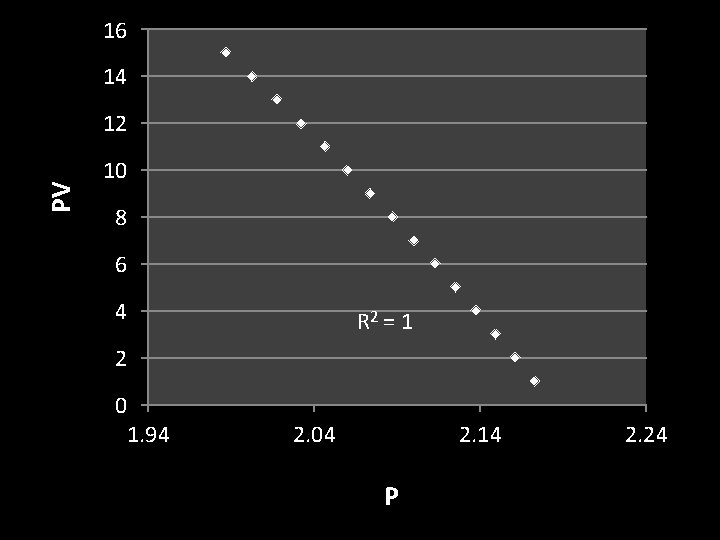
16 14 PV 12 10 8 6 4 R 2 = 1 2 0 1. 94 2. 04 2. 14 P 2. 24

Pada contoh di atas: PV = – 117, 4 + 196, 5 P – 65, 37 P 2 Secara umum: PV = a + b. P + c. P 2 + … Jika b a. B’, c a. C”, dst, maka PV = a (1 + B’P + C’P 2 +. . . )
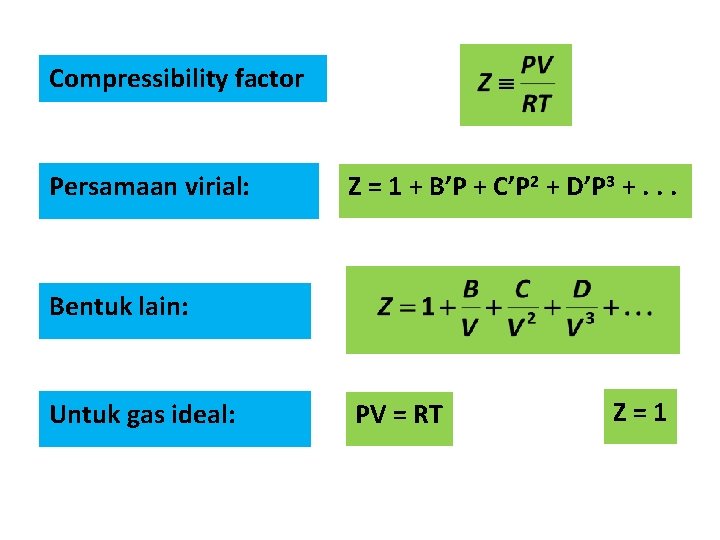
Compressibility factor Persamaan virial: Z = 1 + B’P + C’P 2 + D’P 3 +. . . Bentuk lain: Untuk gas ideal: PV = RT Z=1
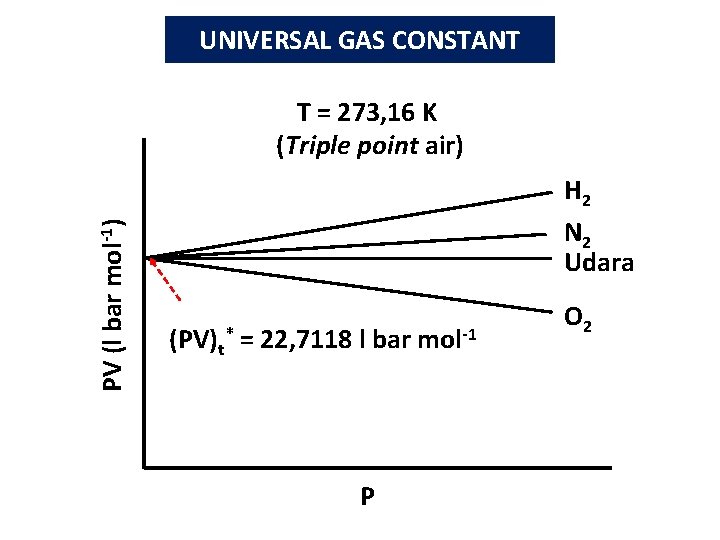
UNIVERSAL GAS CONSTANT PV (l bar mol-1) T = 273, 16 K (Triple point air) H 2 N 2 Udara (PV)t = 22, 7118 l bar * P mol-1 O 2
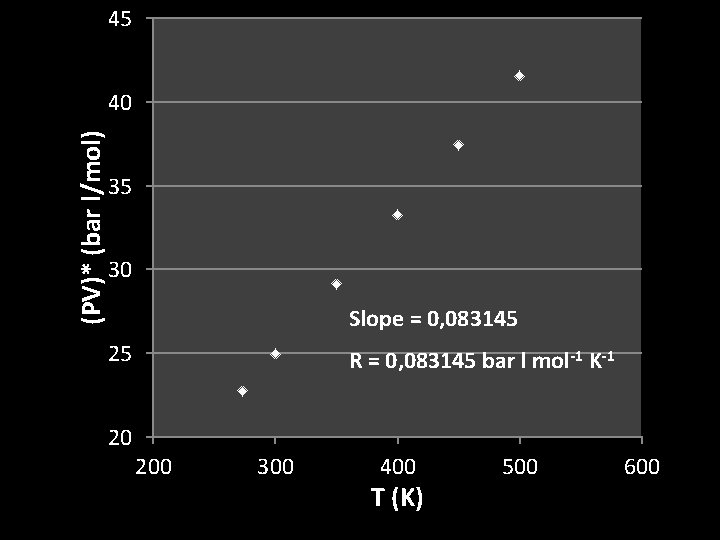
45 (PV)* (bar l/mol) 40 35 30 Slope = 0, 083145 25 R = 0, 083145 bar l mol-1 K-1 20 200 300 400 T (K) 500 600

CONTOH SOAL Diketahui koefisien virial untuk uap isopropanol pada 200 C: B = 388 cm 3 mol 1 C = 26. 000 cm 6 mol 2 Hitung Z dan V dari uap isopropanol pada 200 C dan 10 bar dengan menggunakan persamaan sbb. : a) Persamaan keadaan gas ideal b) Persamaan keadaan virial dengan 2 suku c) Persamaan keadaan virial dengan 3 suku

PENYELESAIAN T = 200 C = 473, 15 K R = 83, 14 cm 3 bar mol 1 K 1 a) Persamaan gas ideal Z=1
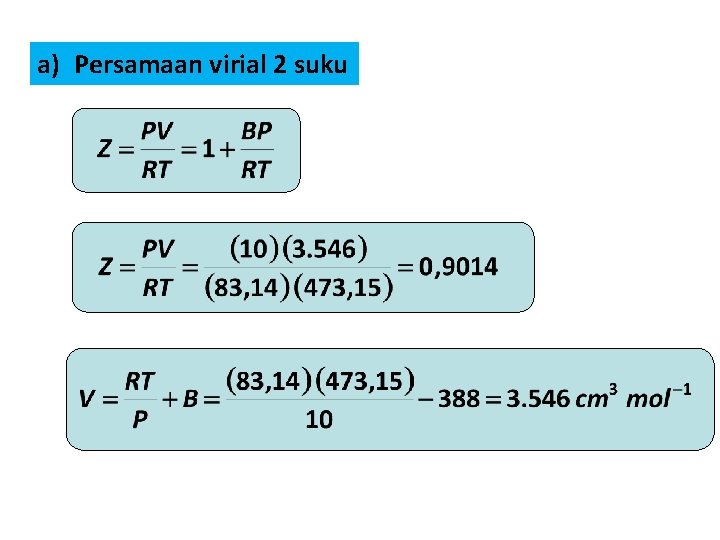
a) Persamaan virial 2 suku
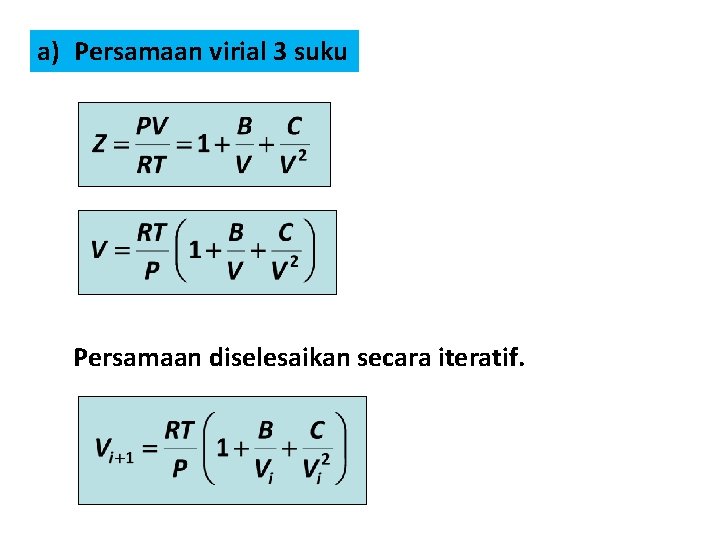
a) Persamaan virial 3 suku Persamaan diselesaikan secara iteratif.

Iterasi 1: Sebagai tebakan awal digunakan V 0 = Vgas ideal = 3. 934 Iterasi 2: Iterasi diteruskan sampai selisih antara Vi+1 Vi sangat kecil Setelah iterasi ke 5 diperoleh hasil : V = 3. 488 cm 3 mol 1 Z = 0, 8866

PERSAMAAN KEADAAN KUBIK: VAN DER WAALS Terobosan baru terhadap pers. gas ideal van der Waals (1873): pengusul pertama persamaan keadaan kubik • Molekul dipandang sebagai partikel yang memiliki volume, sehingga V tidak boleh kurang dari suatu konstanta V diganti dengan (V – b) • Pada jarak tertentu molekul saling berinteraksi mempengaruhi tekanan, P diganti dengan (P + a/V 2)

Kondisi kritikalitas: Derivat parsial pertama dari P terhadap V

Derivat parsial kedua dari P terhadap V Pada titik kritis, kedua derivat sama dengan nol: Ada 2 persamaan dengan 2 bilangan anu (a dan b)

Mengapa disebut persamaan kubik? Samakan penyebut ruas kanan: Kalikan dengan V 2 (V – b): PV 2 (V – b) = RTV 2 – a (V – b)
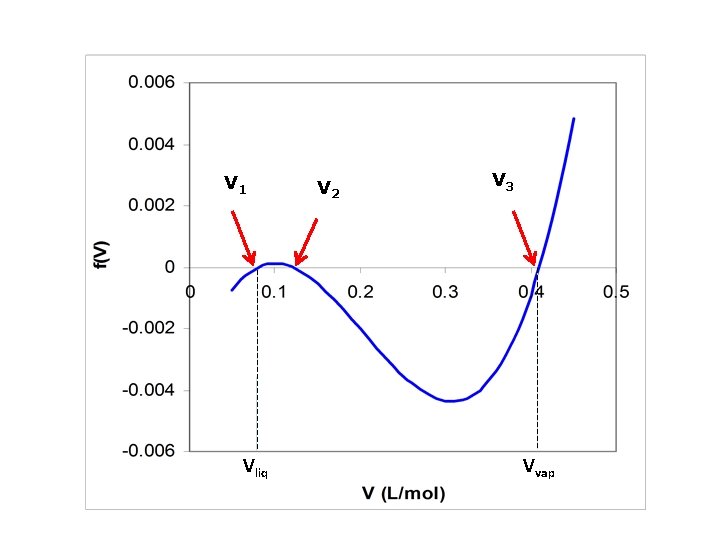
V 1 Vliq V 2 V 3 Vvap

Jika dikalikan dengan (P/RT)3: dengan:
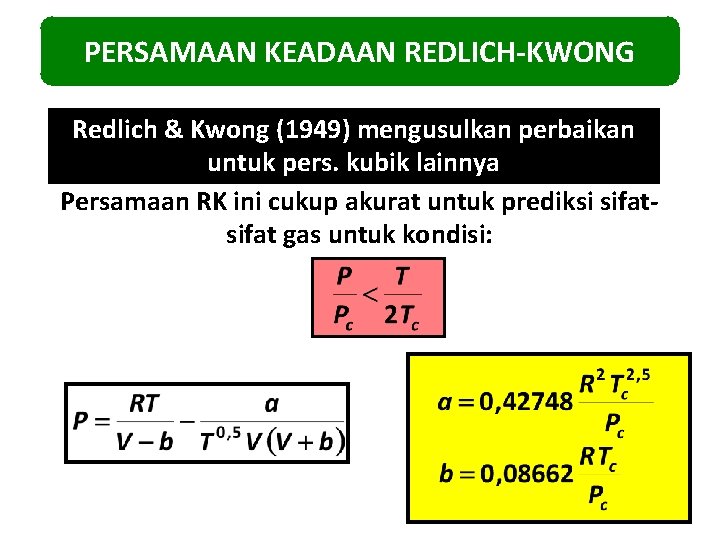
PERSAMAAN KEADAAN REDLICH-KWONG Redlich & Kwong (1949) mengusulkan perbaikan untuk pers. kubik lainnya Persamaan RK ini cukup akurat untuk prediksi sifat gas untuk kondisi:

Bentuk kubik (dalam Z) dari persamaan RK: dengan:
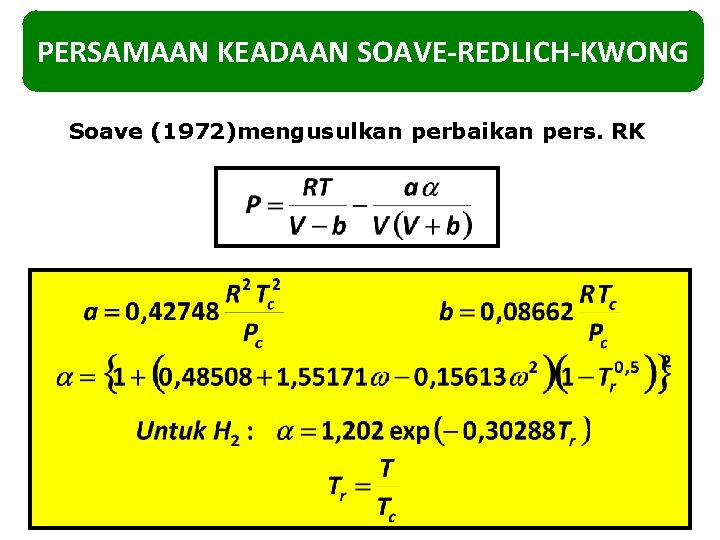
PERSAMAAN KEADAAN SOAVE-REDLICH-KWONG Soave (1972)mengusulkan perbaikan pers. RK

Bentuk kubik (dalam Z) dari persamaan SRK: dengan:

PERSAMAAN KEADAAN PENG-ROBINSON Peng & Robinson (1976): mengusulkan persamaan yang lebih baik untuk memenuhi tujuan-tujuan: 1. Parameter-parameter yang ada harus dapat dinyatakan dalam sifat kritis dan faktor asentrik. 2. Model harus bisa memprediksi berbagai macam property di sekitar titik kritis, terutama untuk perhitungan faktor kompresibilitas dan density cairan. 3. Mixing rule harus menggunakan satu binary interaction parameter yang tidak tergantung pada T, P, dan komposisi. 4. Persamaan harus berlaku untuk semua perhitungan semua property dalam proses natural gas.
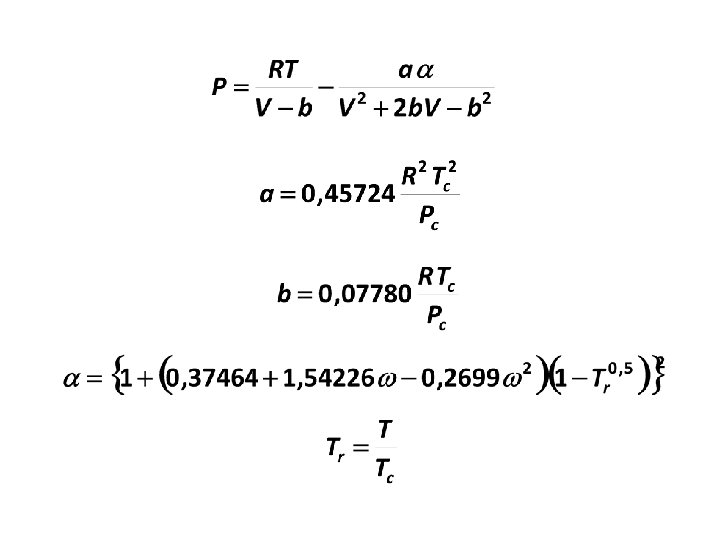
(12)

Bentuk kubik (dalam Z) dari persamaan PR: dengan:
- Slides: 37