Bab 12 Gaya Antarmolekul dan Cairan dan Padatan

Bab 12 Gaya Antarmolekul dan Cairan dan Padatan

Fasa merupakan bagian homogen suatu sistem yang bersentuhan dengan bagian sistem yang lain tetapi dipisahkan dengan batas yang jelas. 2 Fasa padatan- es Fasa cair - air 12. 1

Gaya antar molekul Gaya antarmolekul gaya tarik antar molekul-molekul. Gaya intramolekul mengikat atom-atom dalam molekul. antarmolekul vs intramolekul • 41 k. J untuk menguapkan 1 mol air (antar) • 930 k. J untuk memutus ikatan 2 O-H dlm 1 mol air (intra) Biasanya, gaya antarmolekul jauh lebih lemah dari gaya intramolekul. “Pengukuran” gaya antarmolekul Titik didih Titik leleh DHvap DHfus DHsub 12. 2

Gaya Antarmolekul Gaya Dipol-Dipol Gaya yang bekerja antara molekul-molekul polar Arah Molekul Polar dalam Padatan 12. 2
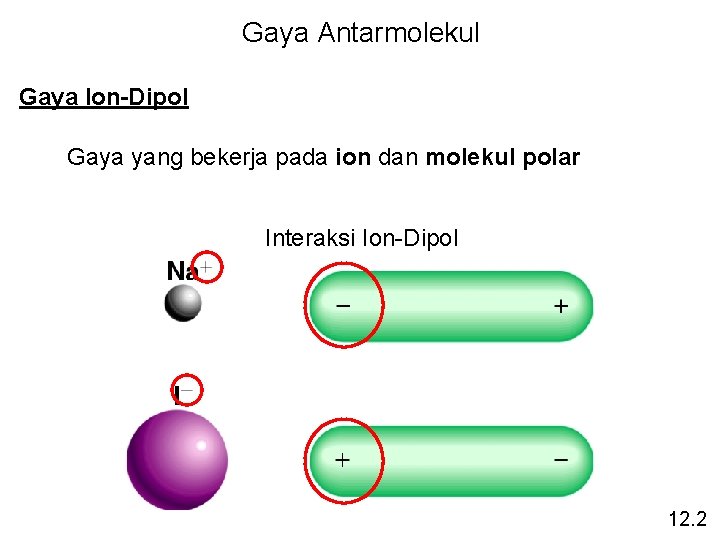
Gaya Antarmolekul Gaya Ion-Dipol Gaya yang bekerja pada ion dan molekul polar Interaksi Ion-Dipol 12. 2
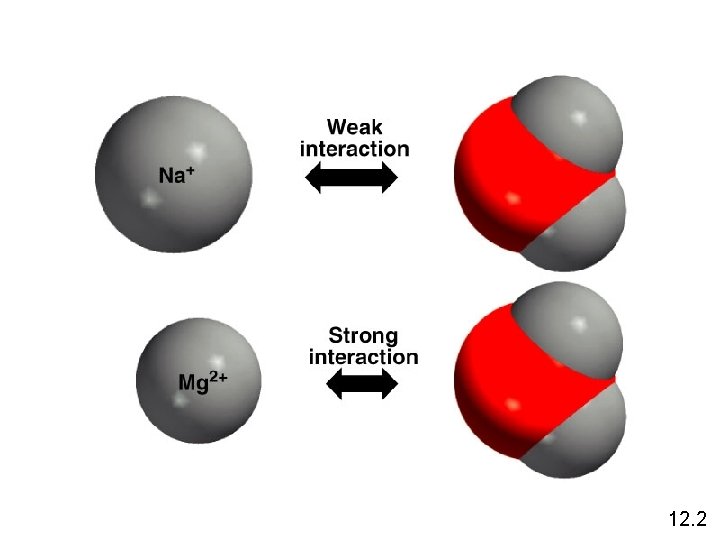
12. 2
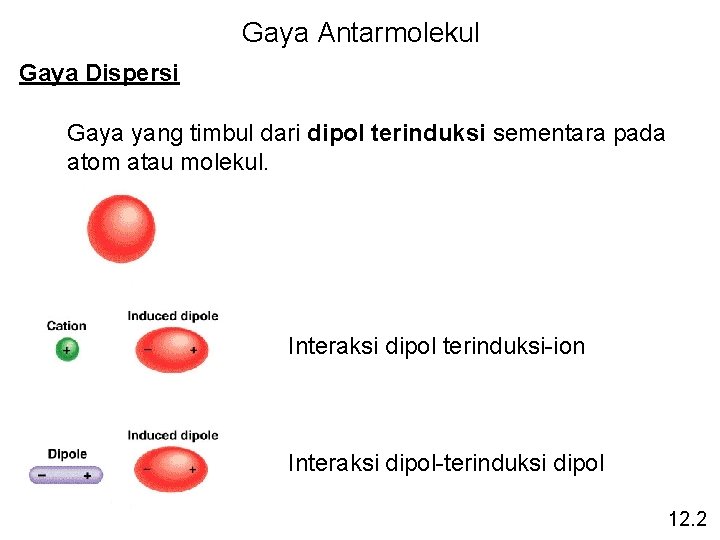
Gaya Antarmolekul Gaya Dispersi Gaya yang timbul dari dipol terinduksi sementara pada atom atau molekul. Interaksi dipol terinduksi-ion Interaksi dipol-terinduksi dipol 12. 2

Gaya Antarmolekul Lanjutan gaya Dispersi Keterpolaran adalah kemudahan terganggunya distribusi elektron dalam suatu atom (atau molekul). Keterpolaran meningkat seiring dg: • Semakin banyaknya jumlah elektron • Semakin banyak awan elektron menyebar Gaya Dispersi biasanya meningkat seiring peningkatan massa molar. 12. 2

Apakah jenis gaya antarmolekul yang terjadi pada molekul 2 berikut? HBr adalah molekul polar: gaya dipol-dipol. Terdapat juga gaya dispersi antar molekul 2 HBr. CH 4 merupakan molekul nonpolar: gaya dispersi. SO 2 O SO 2 adalah molekul polar: gaya dipol-dipol. Terdapat juga gaya dispersi antar molekul 2 SO 2. 12. 2
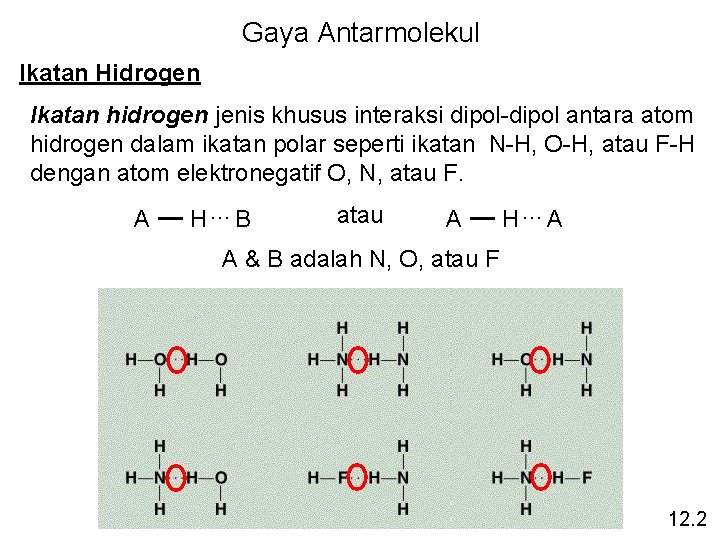
Gaya Antarmolekul Ikatan Hidrogen Ikatan hidrogen jenis khusus interaksi dipol-dipol antara atom hidrogen dalam ikatan polar seperti ikatan N-H, O-H, atau F-H dengan atom elektronegatif O, N, atau F. A H…B atau A H…A A & B adalah N, O, atau F 12. 2
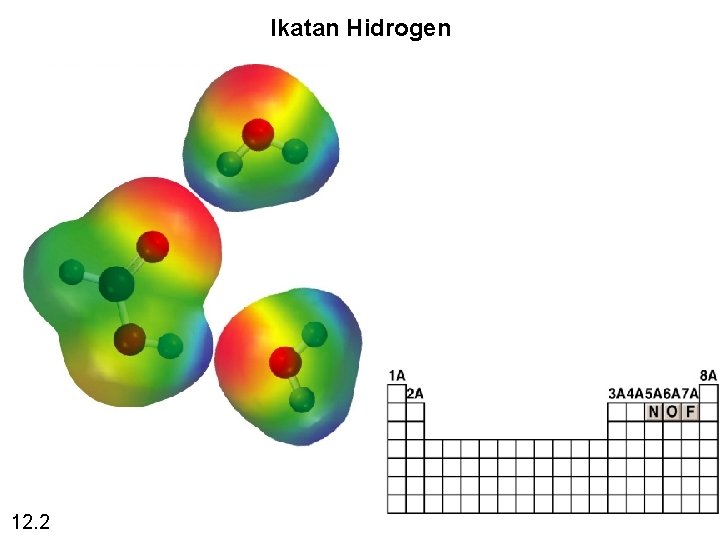
Ikatan Hidrogen 12. 2
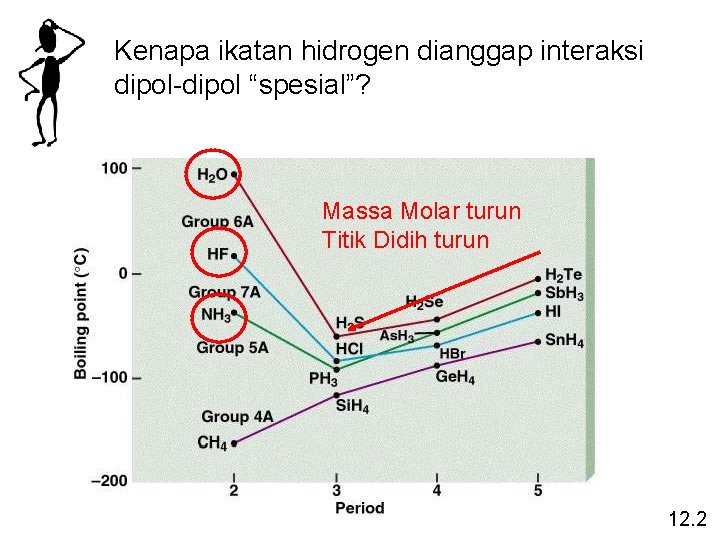
Kenapa ikatan hidrogen dianggap interaksi dipol-dipol “spesial”? Massa Molar turun Titik Didih turun 12. 2
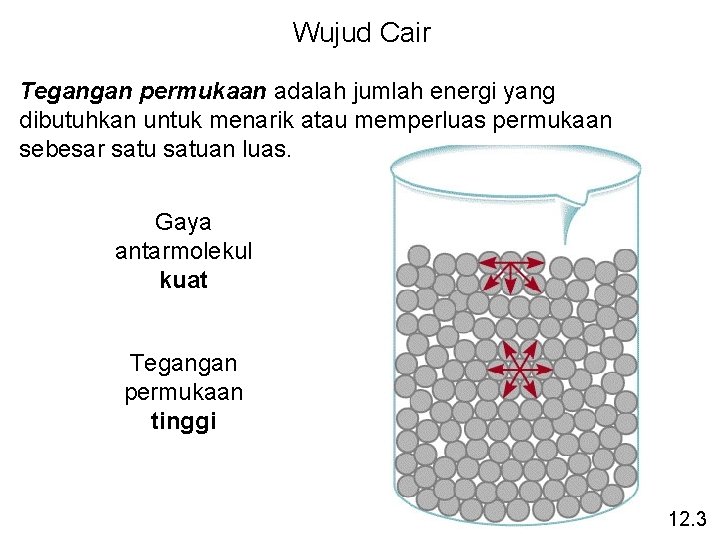
Wujud Cair Tegangan permukaan adalah jumlah energi yang dibutuhkan untuk menarik atau memperluas permukaan sebesar satuan luas. Gaya antarmolekul kuat Tegangan permukaan tinggi 12. 3
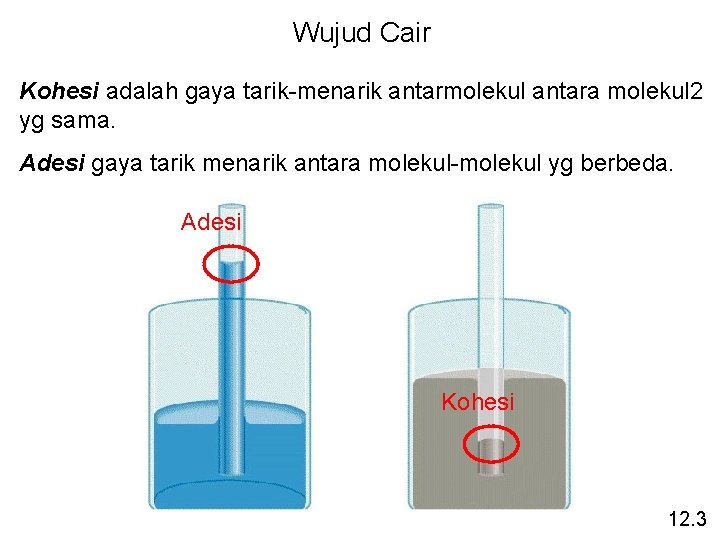
Wujud Cair Kohesi adalah gaya tarik-menarik antarmolekul antara molekul 2 yg sama. Adesi gaya tarik menarik antara molekul-molekul yg berbeda. Adesi Kohesi 12. 3

Wujud Cair Viskositas adalah ukuran hambatan suatu fluida untuk mengalir. Gaya antarmolekul kuat Viskositas tinggi 12. 3
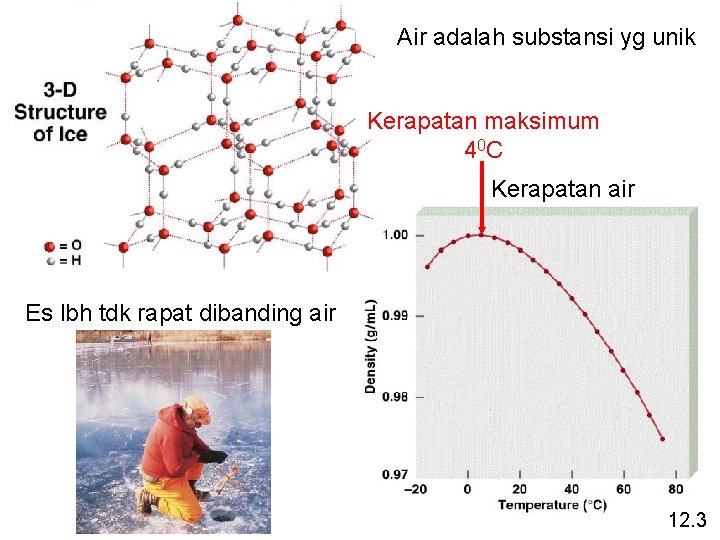
Air adalah substansi yg unik Kerapatan maksimum 4 0 C Kerapatan air Es lbh tdk rapat dibanding air 12. 3
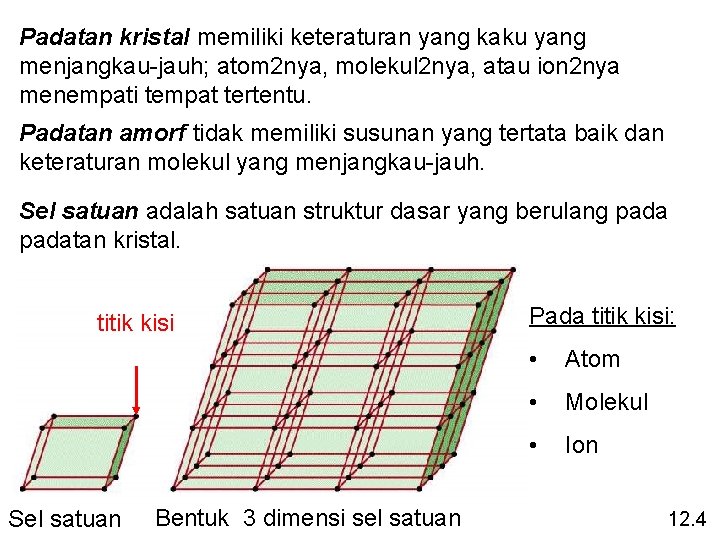
Padatan kristal memiliki keteraturan yang kaku yang menjangkau-jauh; atom 2 nya, molekul 2 nya, atau ion 2 nya menempati tempat tertentu. Padatan amorf tidak memiliki susunan yang tertata baik dan keteraturan molekul yang menjangkau-jauh. Sel satuan adalah satuan struktur dasar yang berulang padatan kristal. titik kisi Sel satuan Bentuk 3 dimensi sel satuan Pada titik kisi: • Atom • Molekul • Ion 12. 4
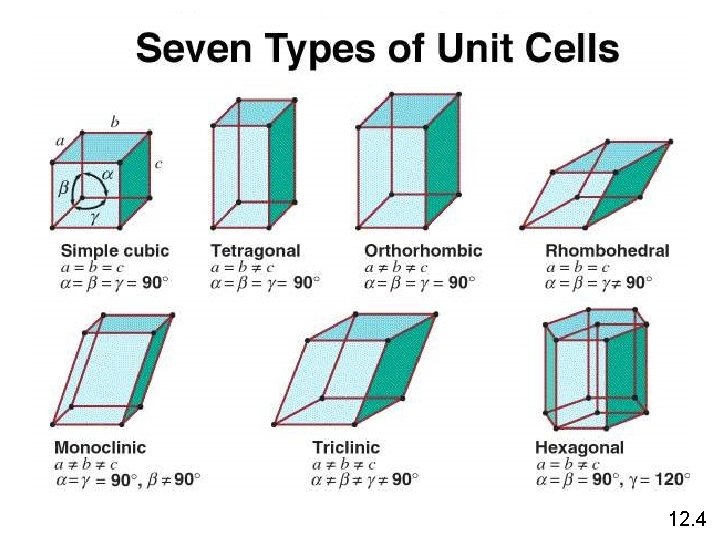
12. 4
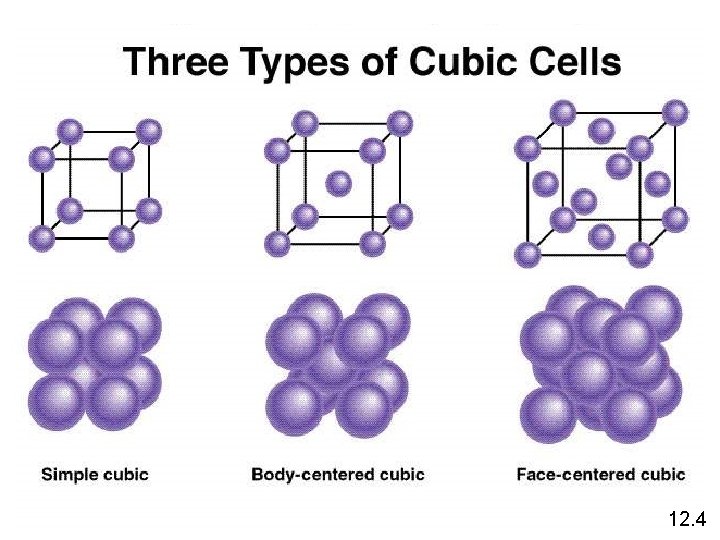
12. 4
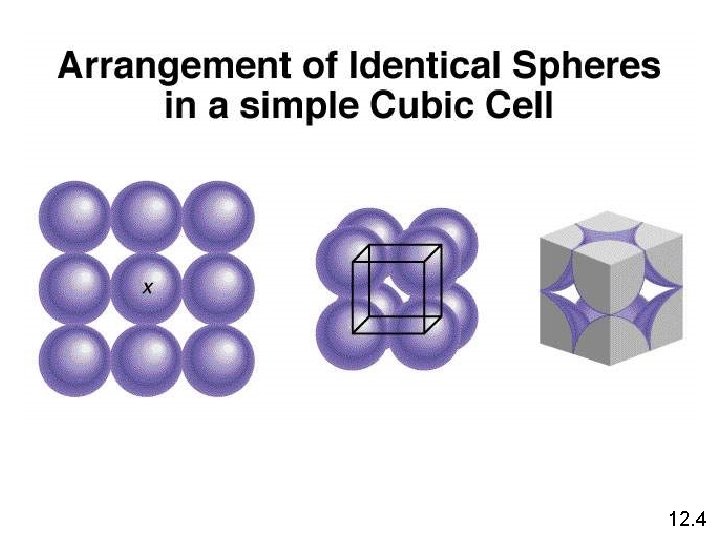
12. 4
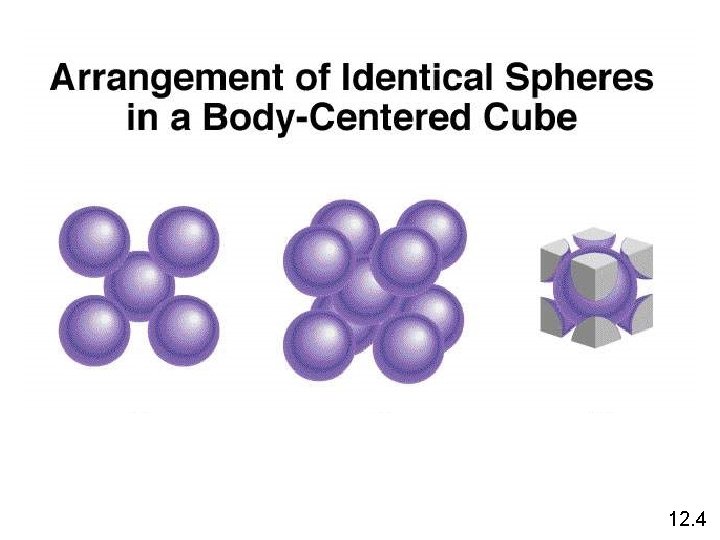
12. 4
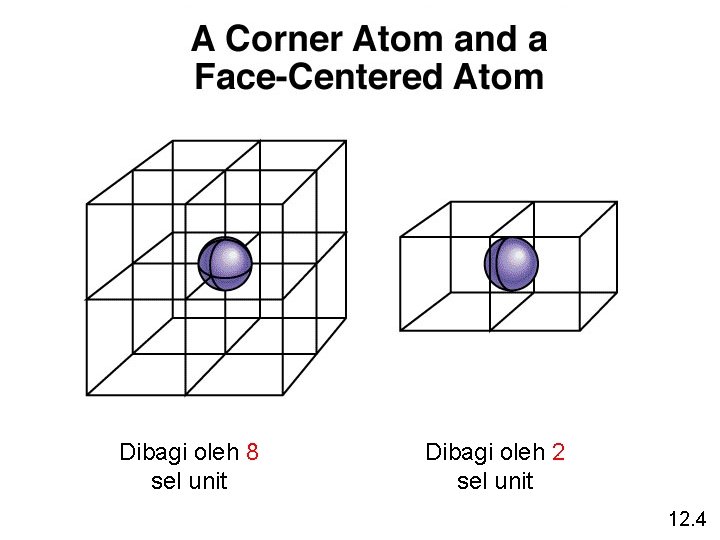
Dibagi oleh 8 sel unit Dibagi oleh 2 sel unit 12. 4
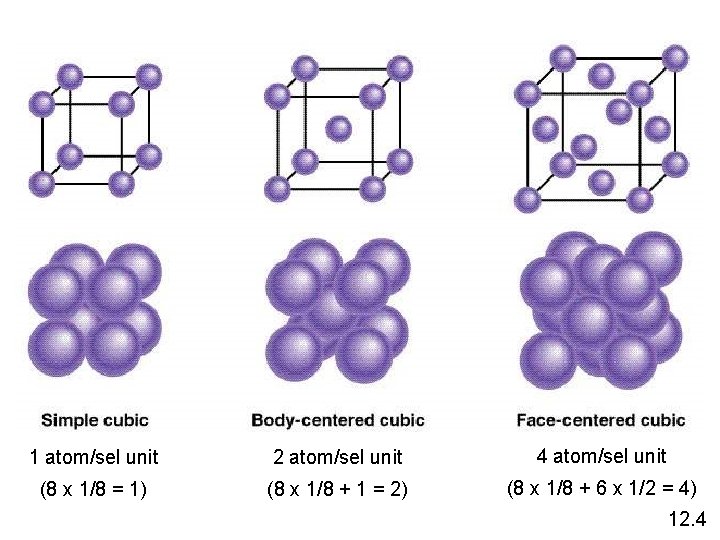
1 atom/sel unit 2 atom/sel unit 4 atom/sel unit (8 x 1/8 = 1) (8 x 1/8 + 1 = 2) (8 x 1/8 + 6 x 1/2 = 4) 12. 4
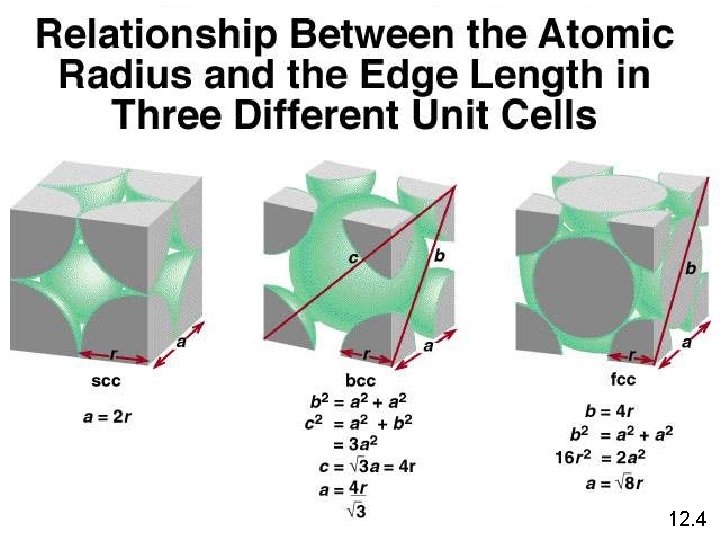
12. 4

Ketika perak mengkristal, terbentuk sel kubik terpusat. Panjang sisi sel unit adalah 409 pm. Hitung kerapatan dari perak tsb. d= m V V = a 3 = (409 pm)3 = 6, 83 x 10 -23 cm 3 4 atom/sel satuan pada sel kubik terpusat 1 mol Ag 107, 9 g x m = 4 Ag atom x mol Ag 6, 022 x 1023 atom = 7, 17 x 10 -22 g m 3 = = 10, 5 g/cm d= V 6, 83 x 10 -23 cm 3 12. 4
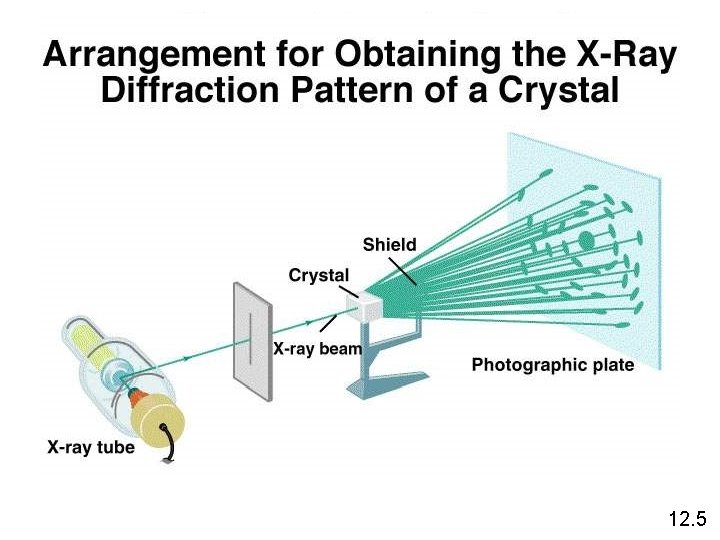
12. 5
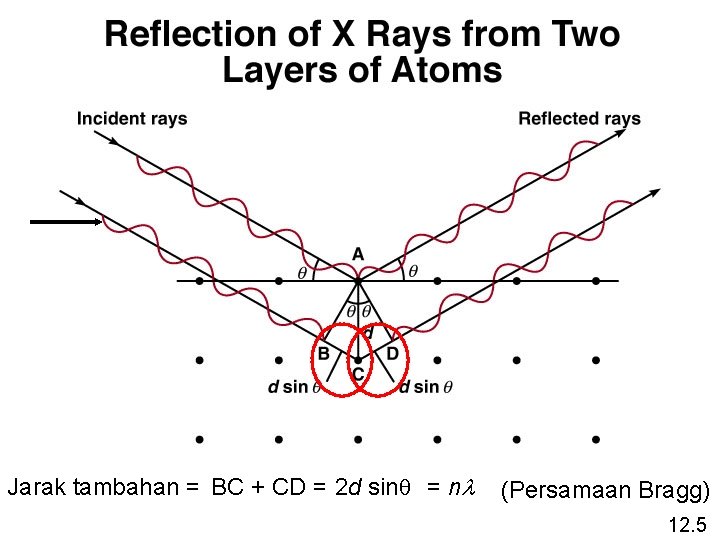
Jarak tambahan = BC + CD = 2 d sinq = nl (Persamaan Bragg) 12. 5

Sinar X sepanjang 0, 154 nm dipisahkan dari suatu kristal dg sudut 14, 170. Jika diasumsikan n = 1, berapakah jarak (dlm pm) antar lapisan dlm kristal? nl = 2 d sin q n=1 q = 14, 170 l = 0, 154 nm = 154 pm nl 1 x 154 pm = = 77, 0 pm d= 2 x sin 14, 17 2 sinq 12. 5
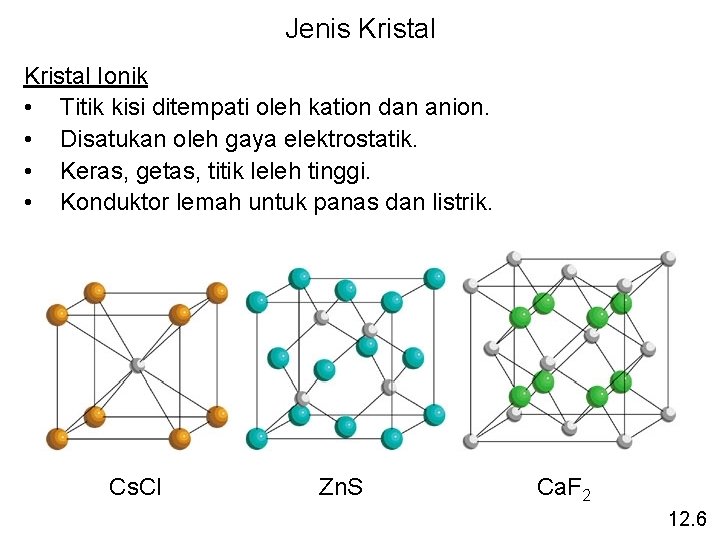
Jenis Kristal Ionik • Titik kisi ditempati oleh kation dan anion. • Disatukan oleh gaya elektrostatik. • Keras, getas, titik leleh tinggi. • Konduktor lemah untuk panas dan listrik. Cs. Cl Zn. S Ca. F 2 12. 6
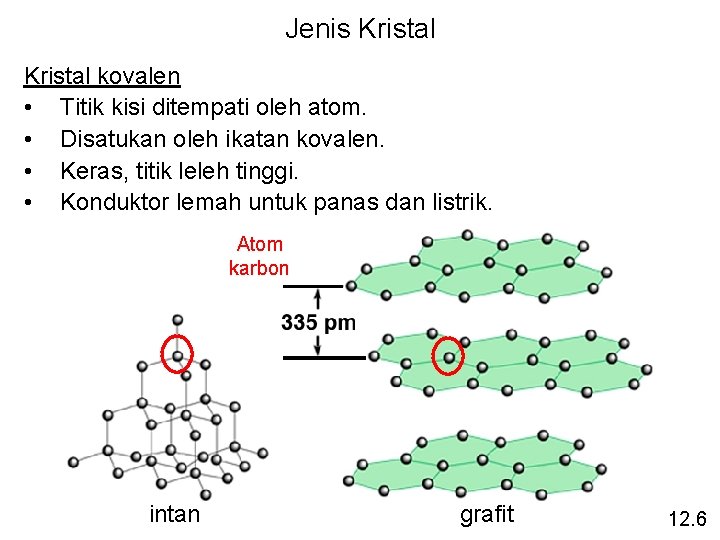
Jenis Kristal kovalen • Titik kisi ditempati oleh atom. • Disatukan oleh ikatan kovalen. • Keras, titik leleh tinggi. • Konduktor lemah untuk panas dan listrik. Atom karbon intan grafit 12. 6

Jenis Kristal Molekular • Titik kisi ditempati oleh molekul. • Gaya antar molekul. • Lunak, titik leleh rendah. • Konduktor lemah bagi panas dan listrik. 12. 6
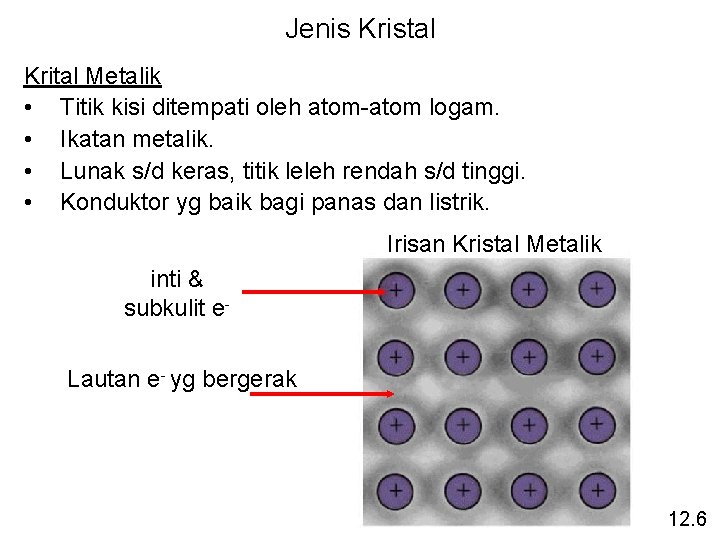
Jenis Kristal Krital Metalik • Titik kisi ditempati oleh atom-atom logam. • Ikatan metalik. • Lunak s/d keras, titik leleh rendah s/d tinggi. • Konduktor yg baik bagi panas dan listrik. Irisan Kristal Metalik inti & subkulit e. Lautan e- yg bergerak 12. 6

Jenis Kristal 12. 6
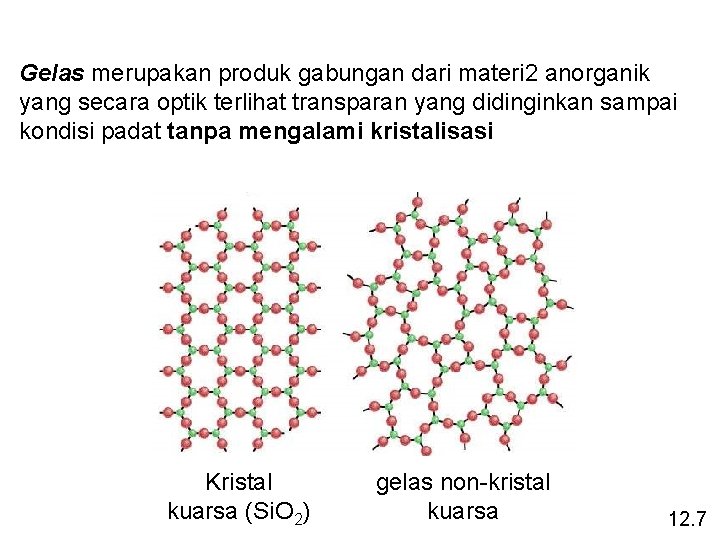
Gelas merupakan produk gabungan dari materi 2 anorganik yang secara optik terlihat transparan yang didinginkan sampai kondisi padat tanpa mengalami kristalisasi Kristal kuarsa (Si. O 2) gelas non-kristal kuarsa 12. 7
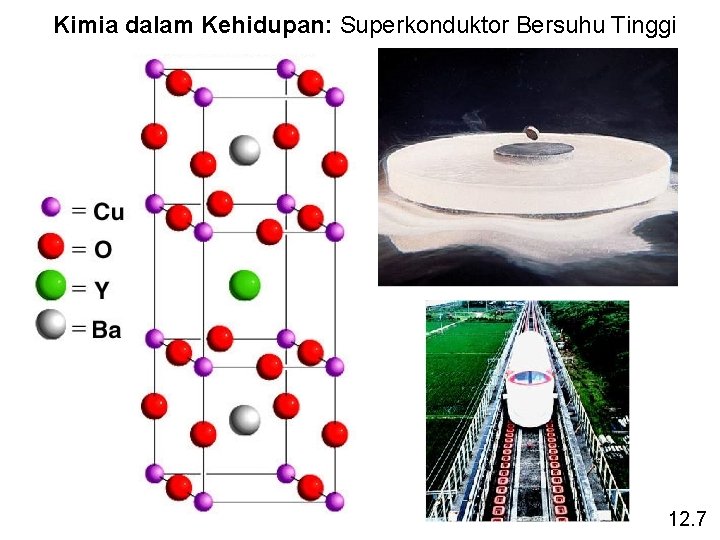
Kimia dalam Kehidupan: Superkonduktor Bersuhu Tinggi 12. 7
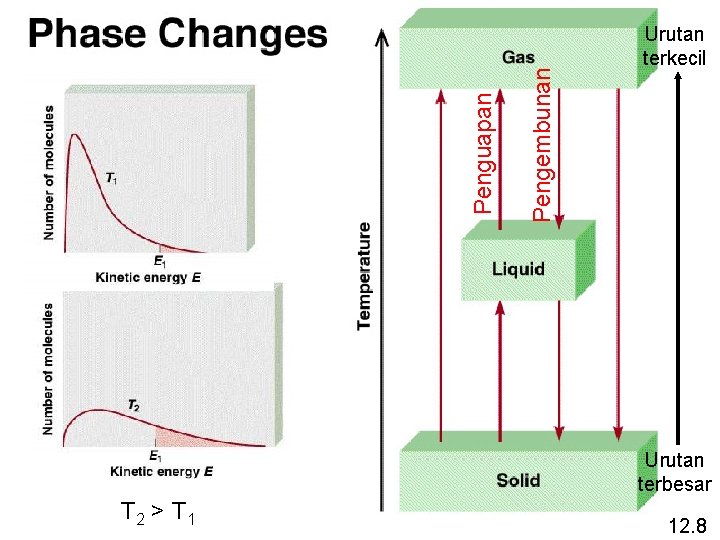
Pengembunan Penguapan Urutan terkecil Urutan terbesar T 2 > T 1 12. 8
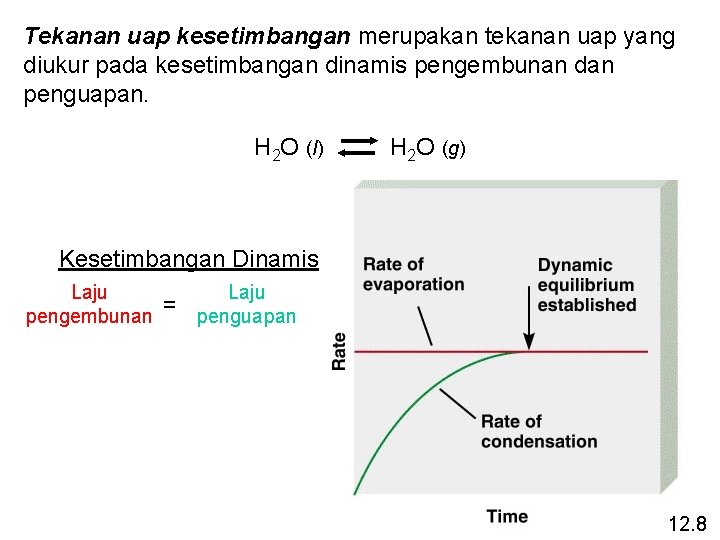
Tekanan uap kesetimbangan merupakan tekanan uap yang diukur pada kesetimbangan dinamis pengembunan dan penguapan. H 2 O (l) H 2 O (g) Kesetimbangan Dinamis Laju pengembunan = Laju penguapan 12. 8
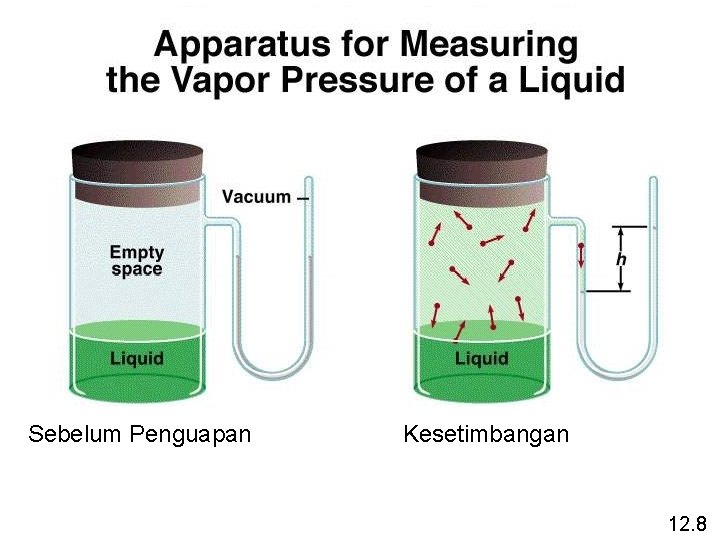
Sebelum Penguapan Kesetimbangan 12. 8
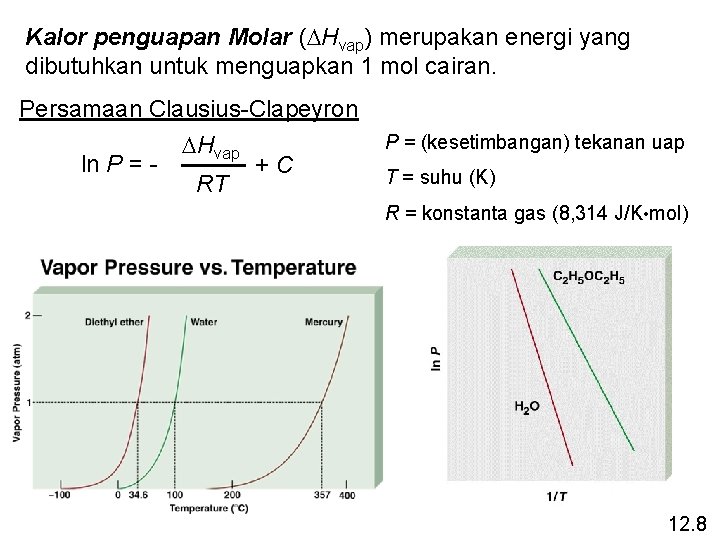
Kalor penguapan Molar (DHvap) merupakan energi yang dibutuhkan untuk menguapkan 1 mol cairan. Persamaan Clausius-Clapeyron ln P = - DHvap RT +C P = (kesetimbangan) tekanan uap T = suhu (K) R = konstanta gas (8, 314 J/K • mol) 12. 8
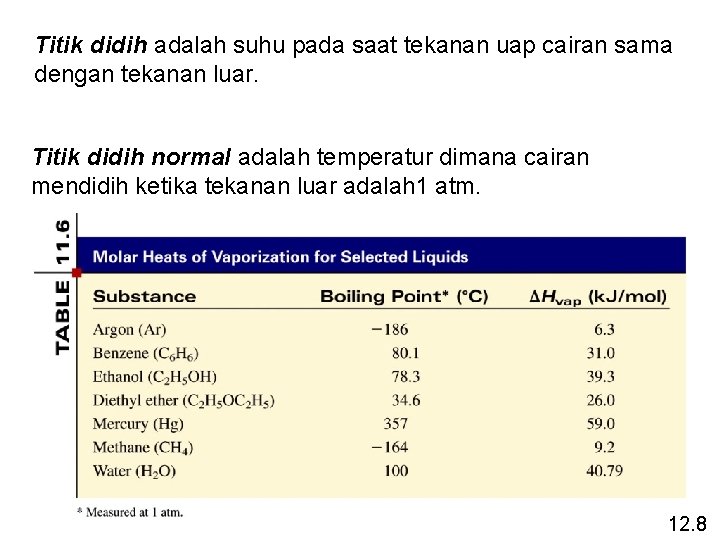
Titik didih adalah suhu pada saat tekanan uap cairan sama dengan tekanan luar. Titik didih normal adalah temperatur dimana cairan mendidih ketika tekanan luar adalah 1 atm. 12. 8

Suhu kritis (Tc) adalah ketinggian temperatur dimana gas tidak dapat dibuat menjadi cair, seberapa besarpun tekanan yang diberikan. Tekanan kritis (Pc) adalah tekanan minimum yang harus diberikan untuk menyebabkan pencairan pada suhu kritis. 12. 8
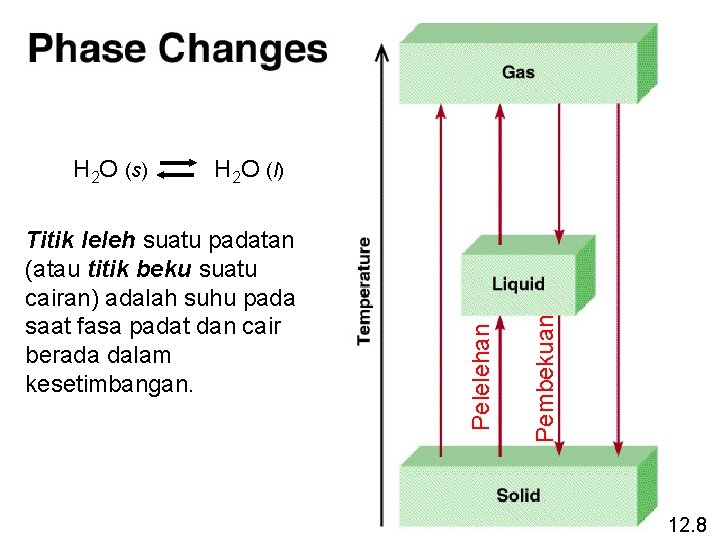
Titik leleh suatu padatan (atau titik beku suatu cairan) adalah suhu pada saat fasa padat dan cair berada dalam kesetimbangan. Pembekuan H 2 O (l) Pelelehan H 2 O (s) 12. 8
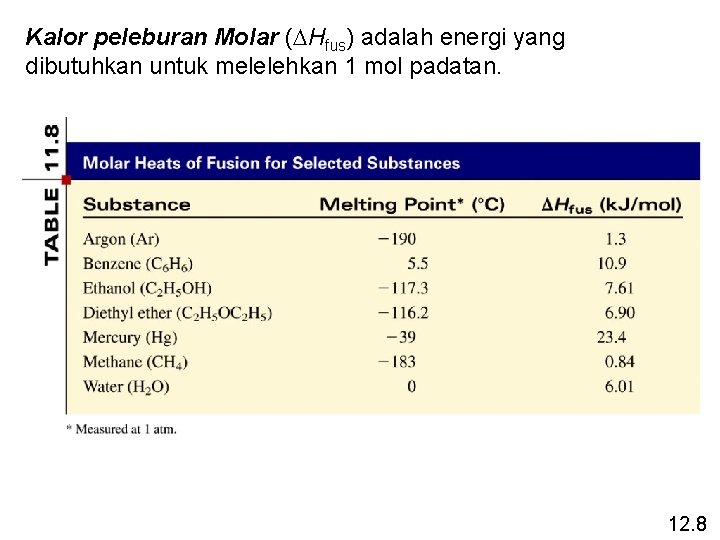
Kalor peleburan Molar (DHfus) adalah energi yang dibutuhkan untuk melelehkan 1 mol padatan. 12. 8
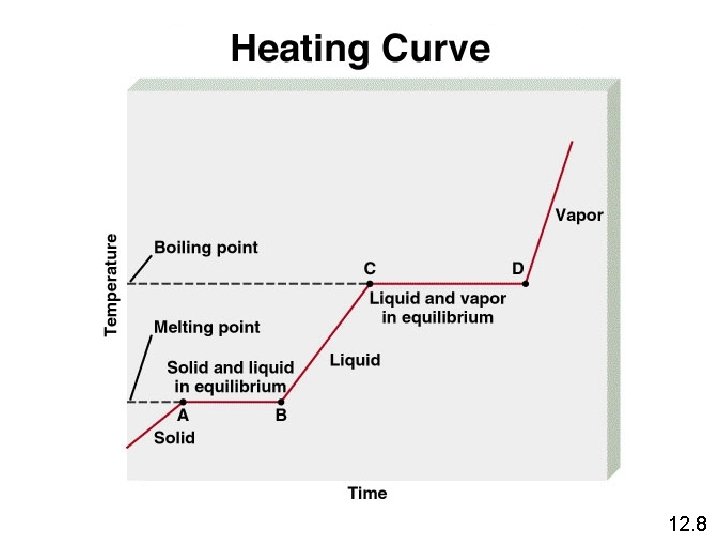
12. 8
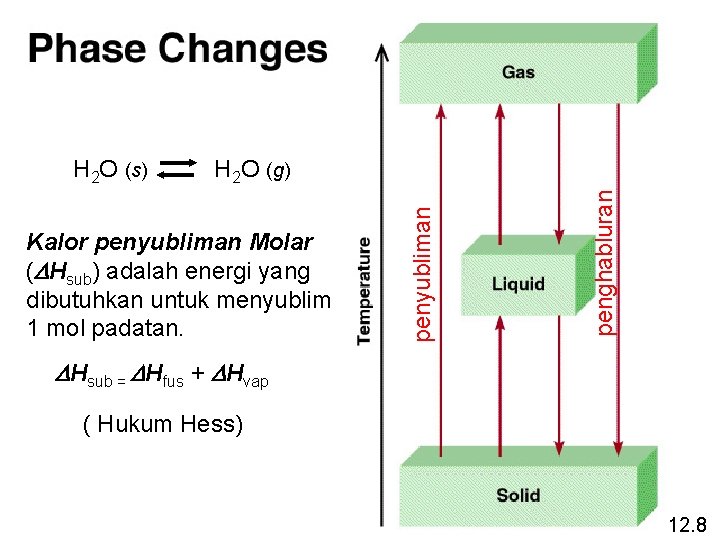
Kalor penyubliman Molar (DHsub) adalah energi yang dibutuhkan untuk menyublim 1 mol padatan. penghabluran H 2 O (g) penyubliman H 2 O (s) DHsub = DHfus + DHvap ( Hukum Hess) 12. 8
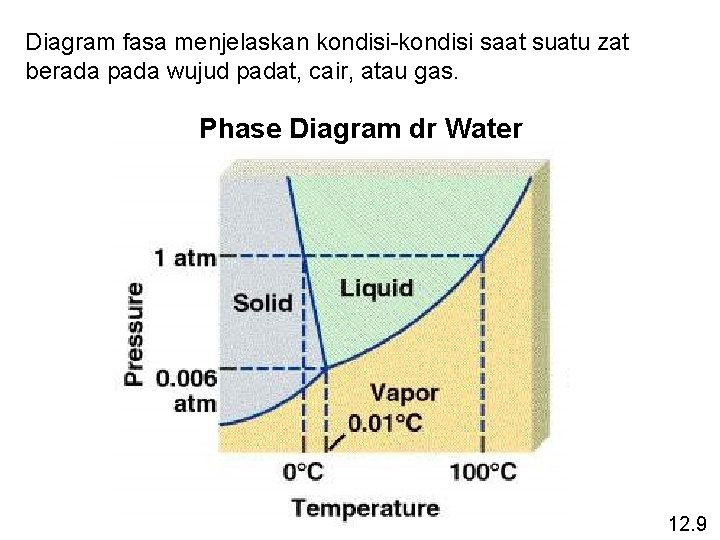
Diagram fasa menjelaskan kondisi-kondisi saat suatu zat berada pada wujud padat, cair, atau gas. Phase Diagram dr Water 12. 9
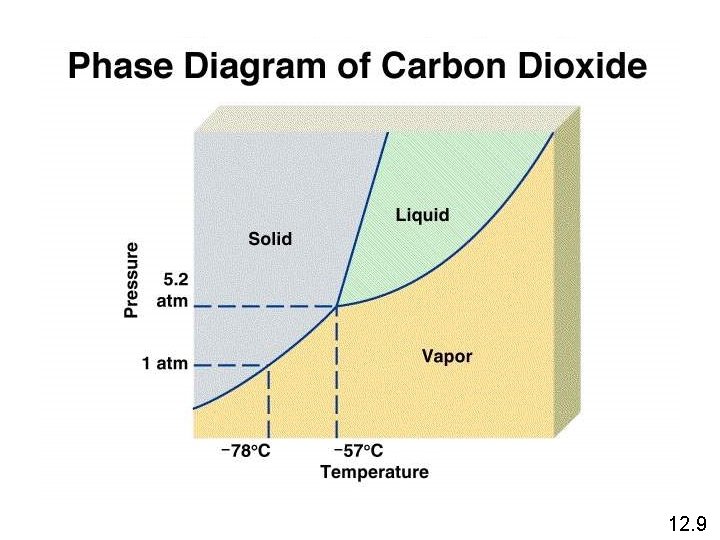
12. 9
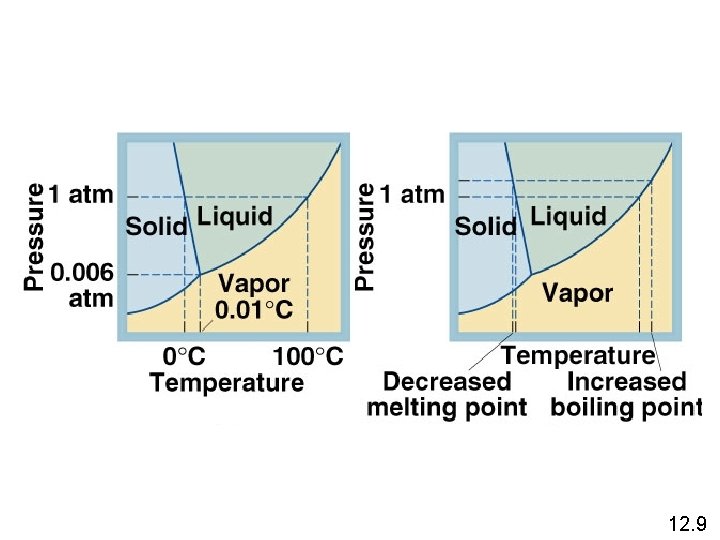
12. 9
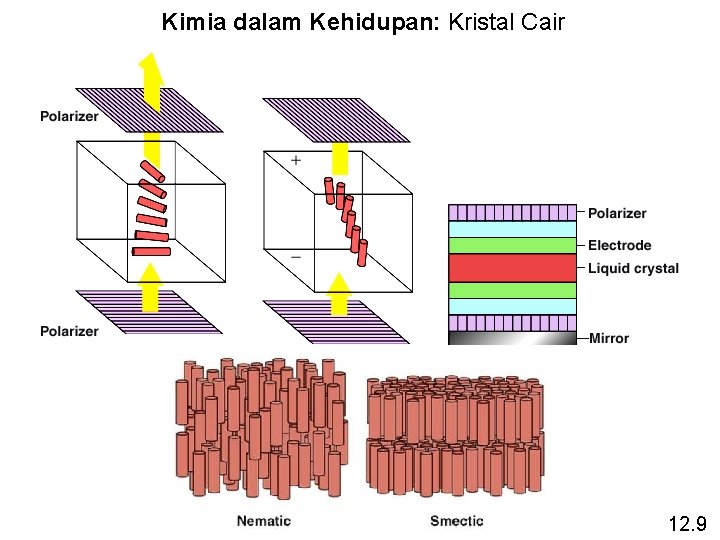
Kimia dalam Kehidupan: Kristal Cair 12. 9
- Slides: 49