Bab 10 Ikatan Kimia II Geometri Molekular dan
Bab 10 Ikatan Kimia II: Geometri Molekular dan Hibridasasi Orbital Atom

10. 1

Model Tolakan pasangan-elektron kulit-valensi (TPEKV) : Meramalkan bentuk geometris molekul dari pasangan elektron di sekitar atom pusat sebagai akibat tolak-menolak antara pasangan elektron. Rumus Jumlah pasangan elektron Jumlah ps. bebas pd atom pusat Susunan pasangan elektron Geometri Molekul AB 2 2 0 linier B B 10. 1
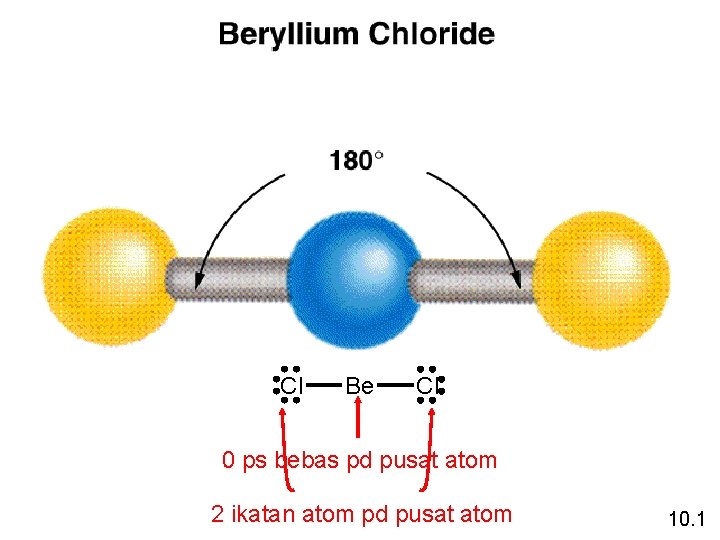
Cl Be Cl 0 ps bebas pd pusat atom 2 ikatan atom pd pusat atom 10. 1
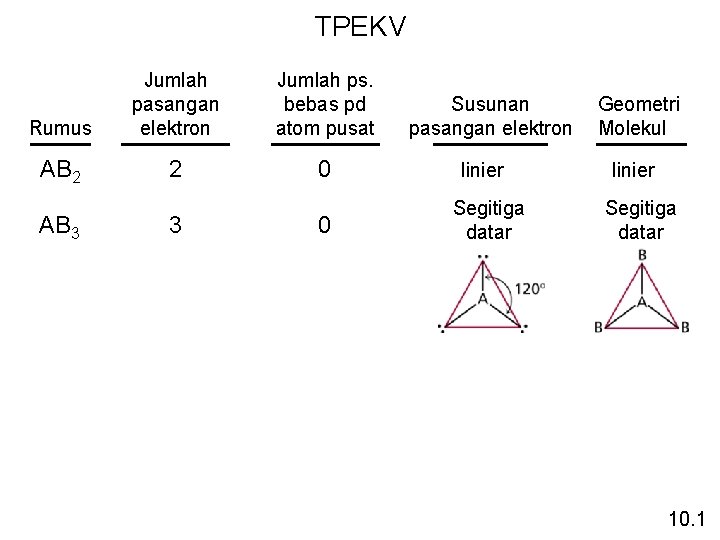
TPEKV Rumus Jumlah pasangan elektron Jumlah ps. bebas pd atom pusat AB 2 2 0 AB 3 3 0 Susunan pasangan elektron linier Segitiga datar Geometri Molekul linier Segitiga datar 10. 1
10. 1
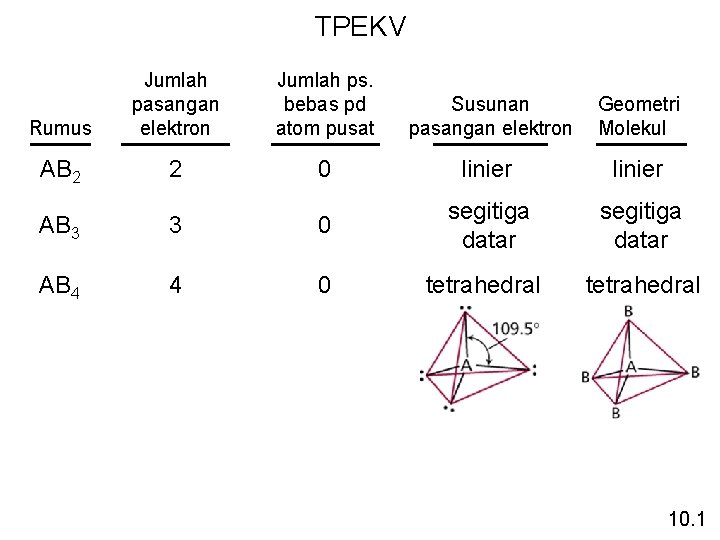
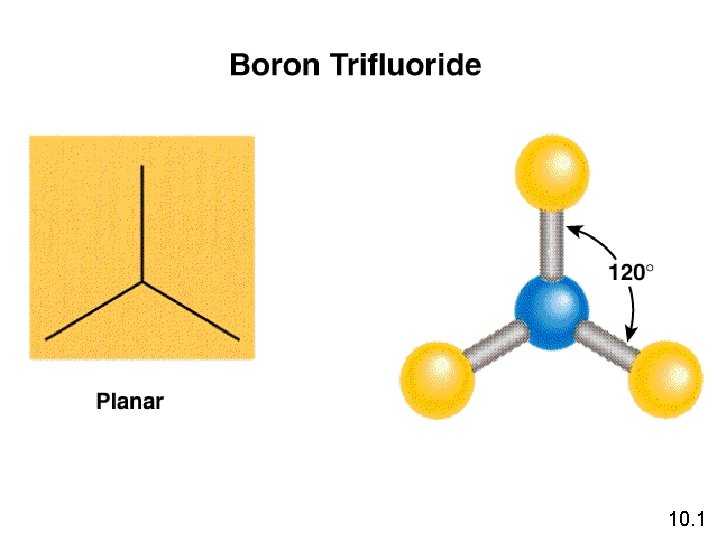
TPEKV Rumus Jumlah pasangan elektron Jumlah ps. bebas pd atom pusat Susunan pasangan elektron Geometri Molekul AB 2 2 0 linier segitiga datar tetrahedral AB 3 3 0 segitiga datar AB 4 4 0 tetrahedral 10. 1
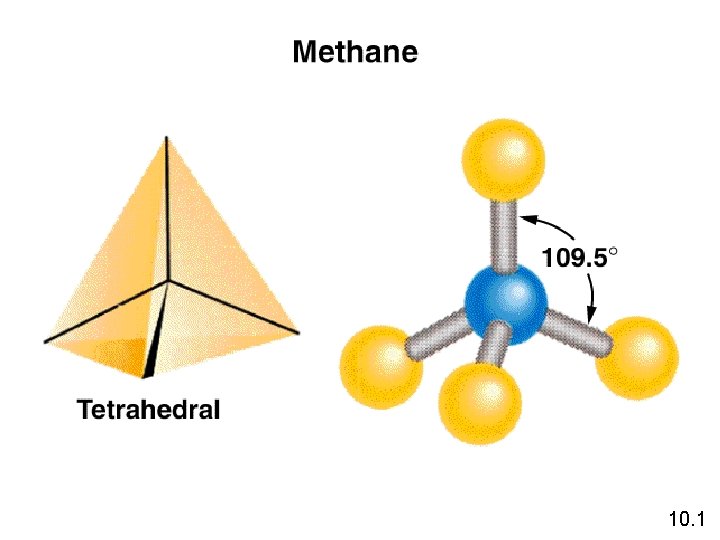
10. 1
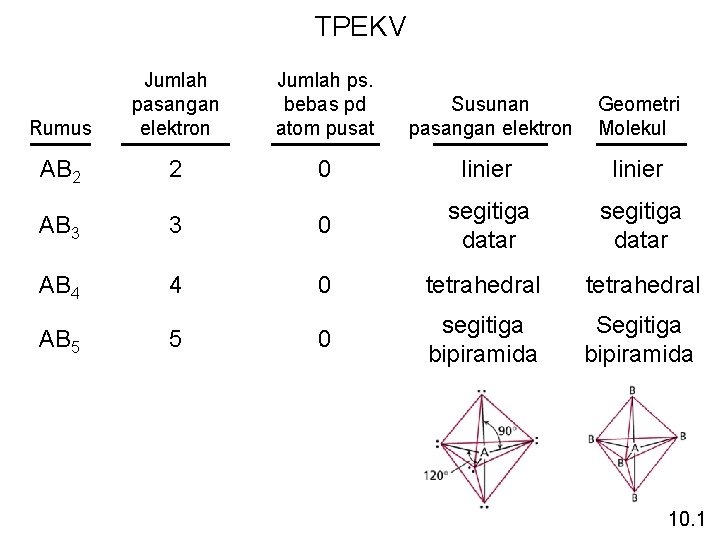
TPEKV Rumus Jumlah pasangan elektron Jumlah ps. bebas pd atom pusat Susunan pasangan elektron Geometri Molekul AB 2 2 0 linier segitiga datar AB 3 3 0 segitiga datar AB 4 4 0 tetrahedral AB 5 5 0 segitiga bipiramida Segitiga bipiramida 10. 1
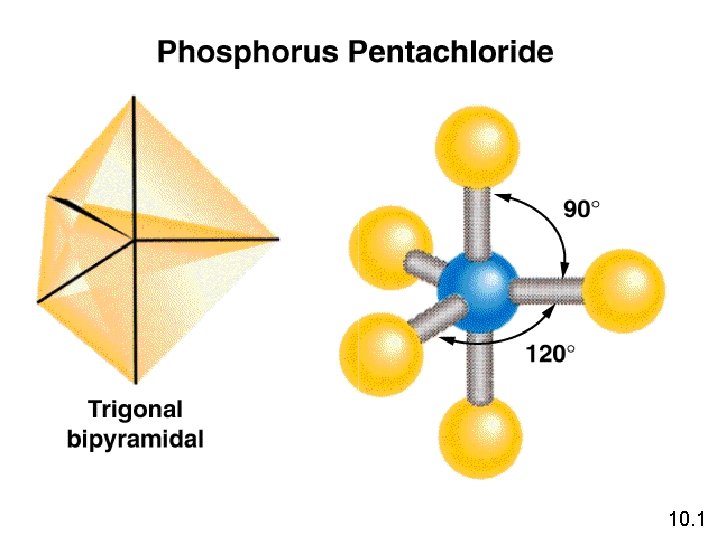
10. 1
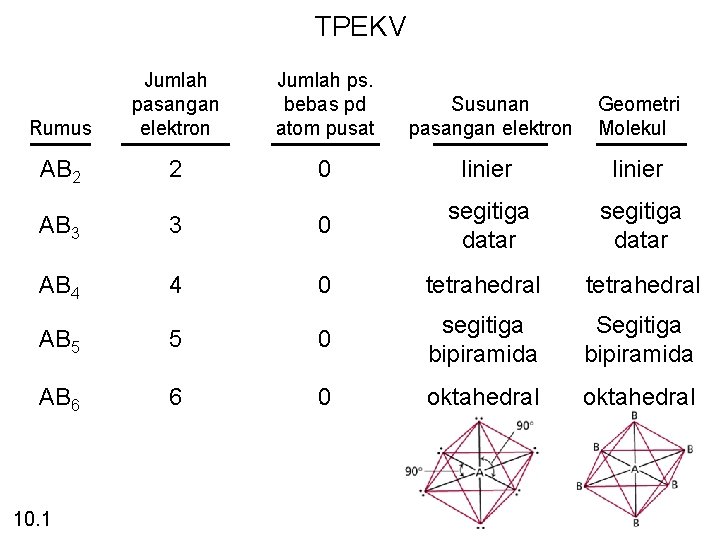
TPEKV Rumus Jumlah pasangan elektron Jumlah ps. bebas pd atom pusat Susunan pasangan elektron Geometri Molekul AB 2 2 0 linier segitiga datar AB 3 3 0 segitiga datar AB 4 4 0 tetrahedral AB 5 5 0 segitiga bipiramida Segitiga bipiramida AB 6 6 0 oktahedral 10. 1
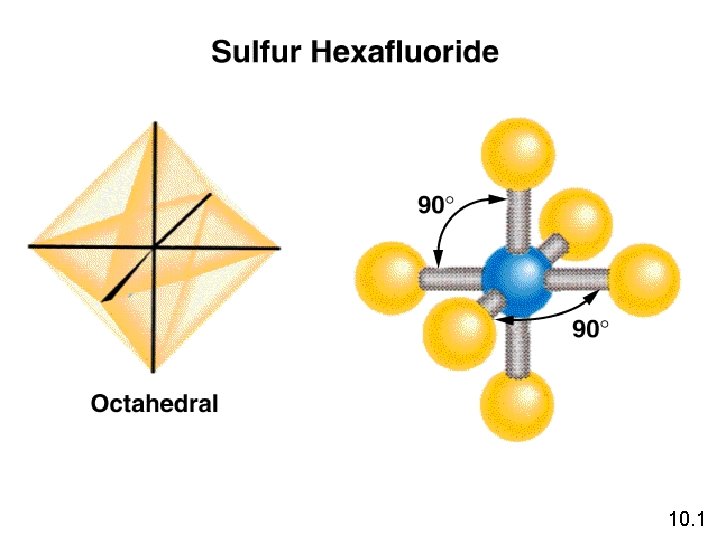
10. 1

10. 1
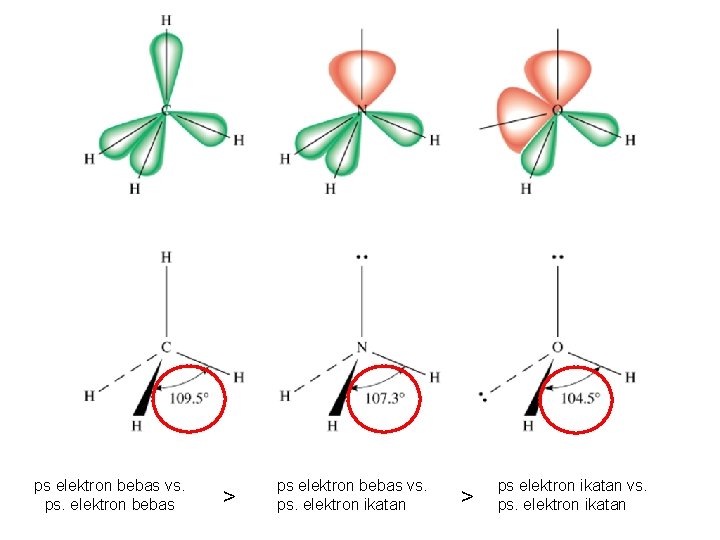
ps elektron bebas vs. ps. elektron bebas > ps elektron bebas vs. ps. elektron ikatan > ps elektron ikatan vs. ps. elektron ikatan
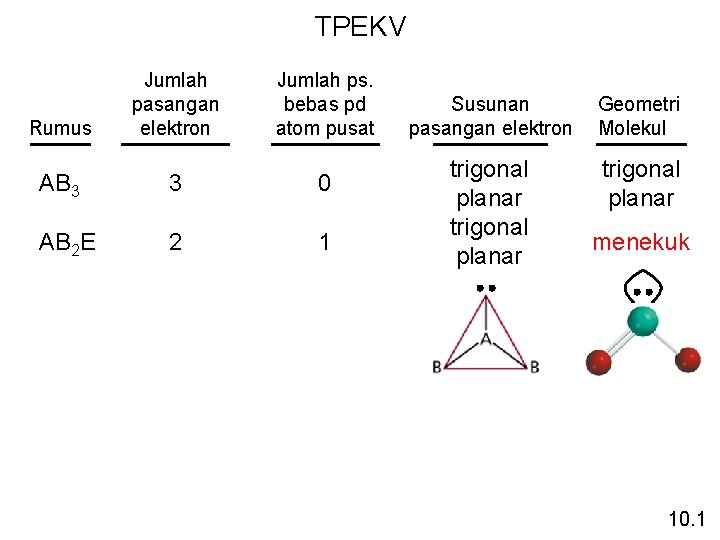
TPEKV Rumus Jumlah pasangan elektron Jumlah ps. bebas pd atom pusat AB 3 3 0 AB 2 E 2 1 Susunan pasangan elektron Geometri Molekul trigonal planar menekuk 10. 1
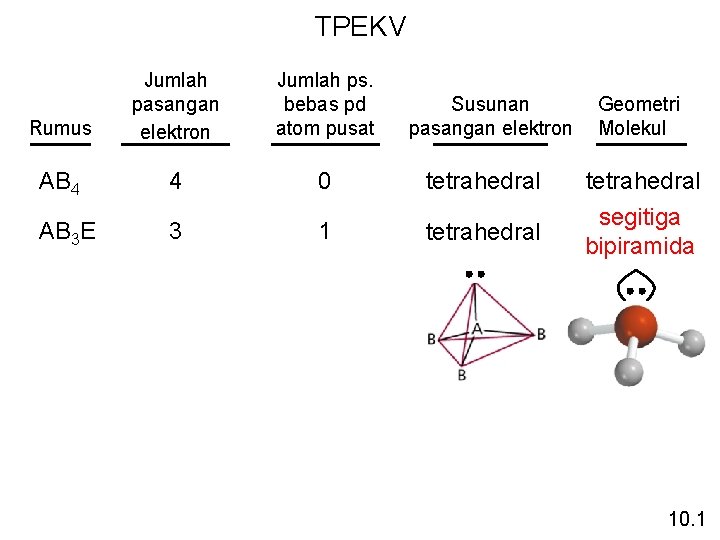
TPEKV Rumus Jumlah pasangan elektron Jumlah ps. bebas pd atom pusat AB 4 4 0 AB 3 E 3 1 Susunan pasangan elektron Geometri Molekul tetrahedral segitiga bipiramida 10. 1
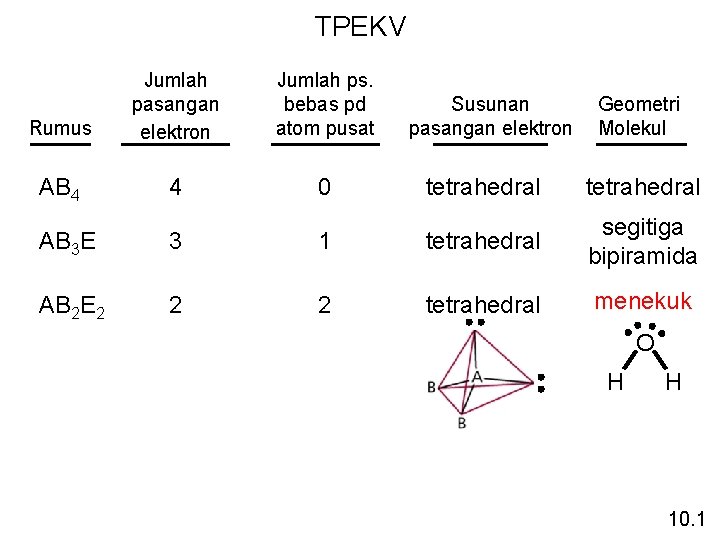
TPEKV Rumus Jumlah pasangan elektron Jumlah ps. bebas pd atom pusat AB 4 4 0 Susunan pasangan elektron Geometri Molekul tetrahedral AB 3 E 3 1 tetrahedral segitiga bipiramida AB 2 E 2 2 2 tetrahedral menekuk O H H 10. 1
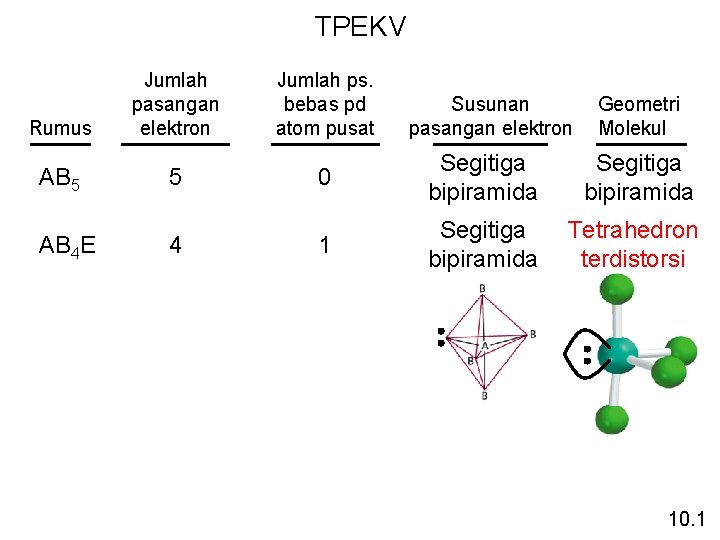
TPEKV Rumus AB 5 AB 4 E Jumlah pasangan elektron 5 4 Jumlah ps. bebas pd atom pusat Susunan pasangan elektron Geometri Molekul 0 Segitiga bipiramida 1 Segitiga bipiramida Tetrahedron terdistorsi 10. 1
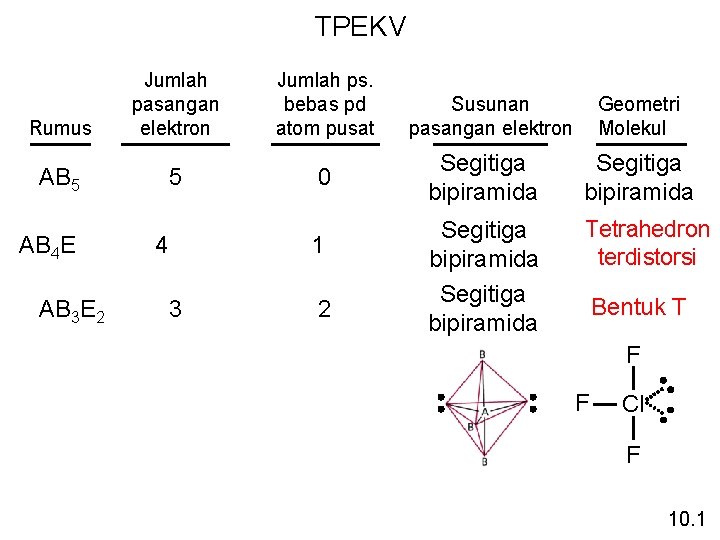
TPEKV Rumus Jumlah pasangan elektron AB 5 AB 4 E AB 3 E 2 5 4 Jumlah ps. bebas pd atom pusat 0 1 3 2 Susunan pasangan elektron Geometri Molekul Segitiga bipiramida Tetrahedron terdistorsi Bentuk T F F Cl F 10. 1
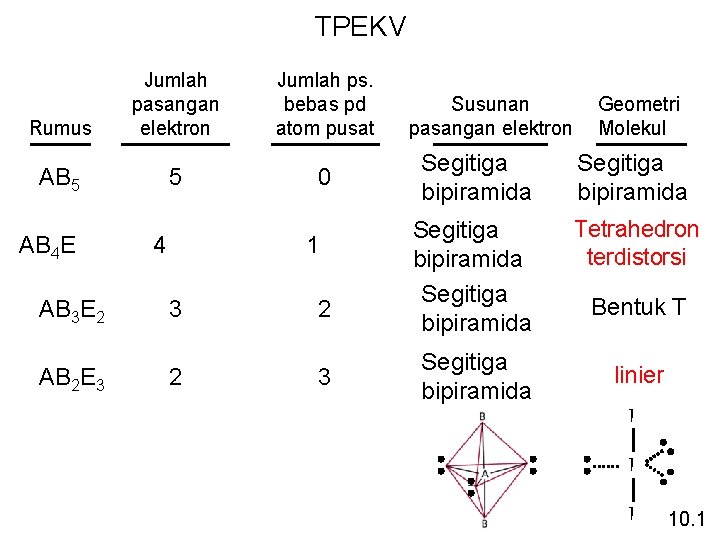
TPEKV Rumus Jumlah pasangan elektron AB 5 AB 4 E AB 3 E 2 AB 2 E 3 5 4 Jumlah ps. bebas pd atom pusat 0 1 3 2 2 3 Susunan pasangan elektron Geometri Molekul Segitiga bipiramida Tetrahedron terdistorsi Segitiga bipiramida Bentuk T linier I I I 10. 1
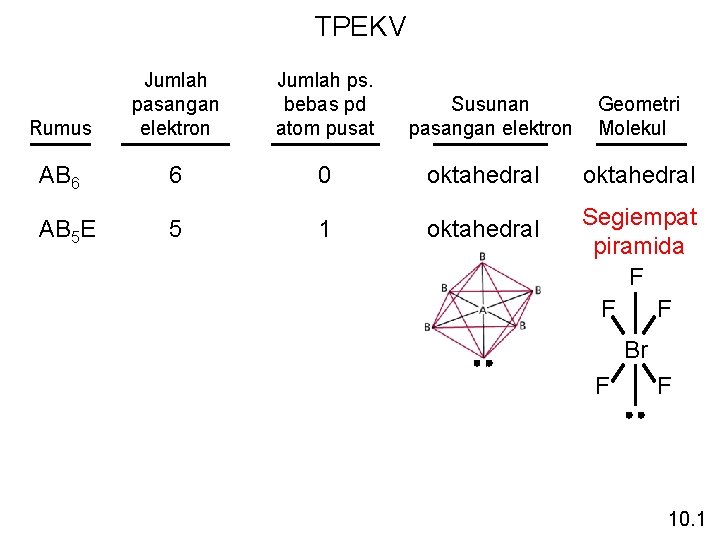
TPEKV Rumus Jumlah pasangan elektron Jumlah ps. bebas pd atom pusat AB 6 6 0 oktahedral AB 5 E 5 1 oktahedral Segiempat piramida F F F Susunan pasangan elektron Geometri Molekul Br F F 10. 1
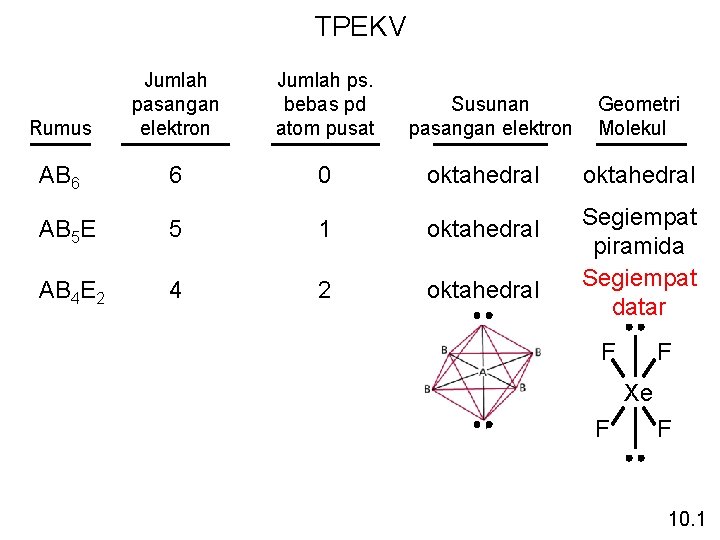
TPEKV Rumus Jumlah pasangan elektron Jumlah ps. bebas pd atom pusat AB 6 6 0 oktahedral AB 5 E 5 1 oktahedral AB 4 E 2 4 2 oktahedral Segiempat piramida Segiempat datar Susunan pasangan elektron Geometri Molekul F F Xe F F 10. 1
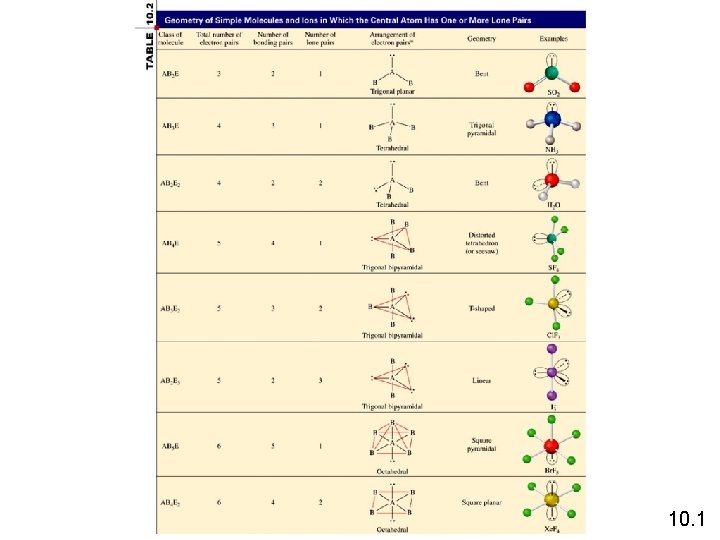
10. 1
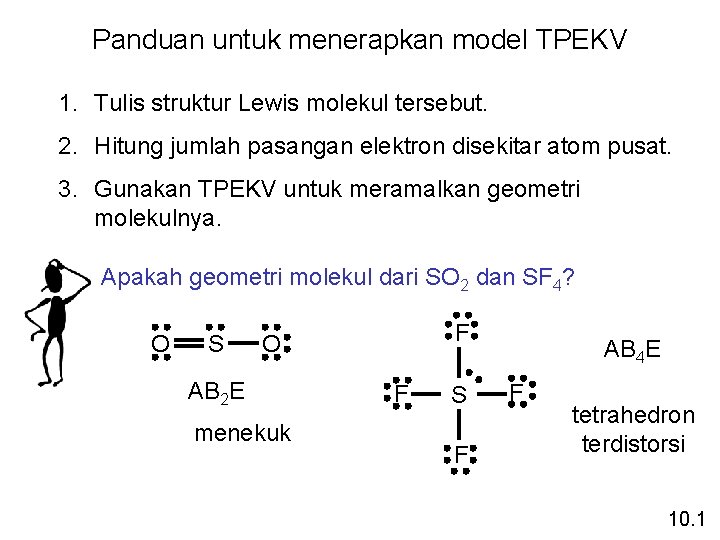
Panduan untuk menerapkan model TPEKV 1. Tulis struktur Lewis molekul tersebut. 2. Hitung jumlah pasangan elektron disekitar atom pusat. 3. Gunakan TPEKV untuk meramalkan geometri molekulnya. Apakah geometri molekul dari SO 2 dan SF 4? O S F O AB 2 E menekuk F S F AB 4 E F tetrahedron terdistorsi 10. 1
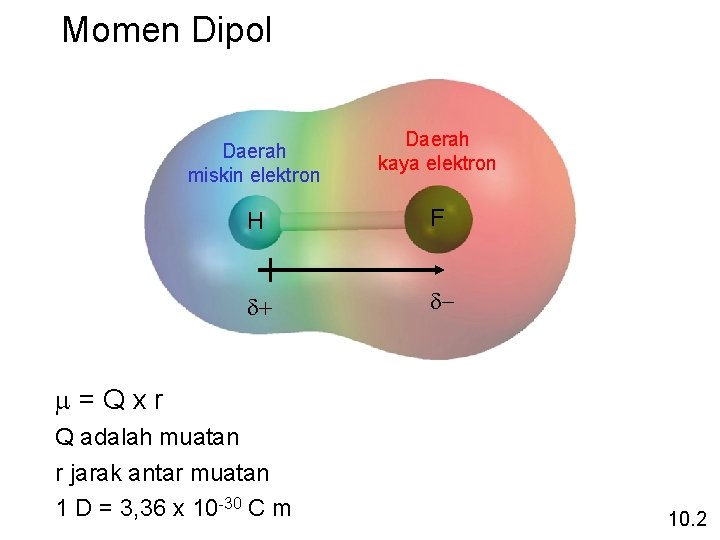
Momen Dipol Daerah miskin elektron Daerah kaya elektron H F d+ d- m=Qxr Q adalah muatan r jarak antar muatan 1 D = 3, 36 x 10 -30 C m 10. 2
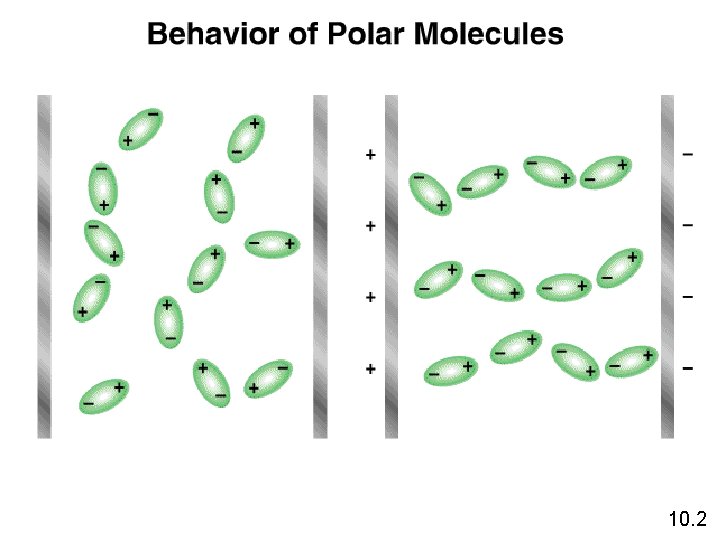
10. 2
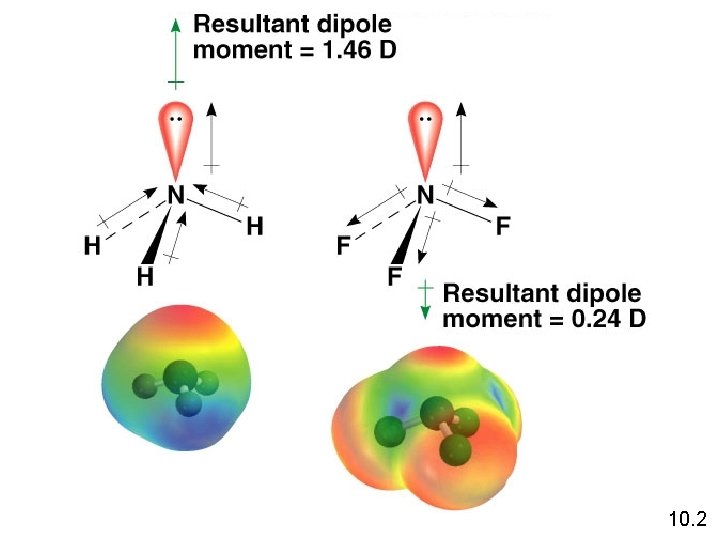
10. 2
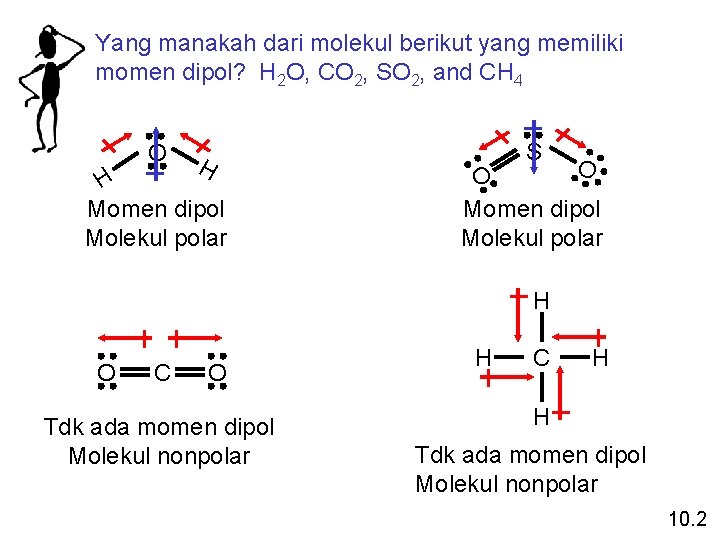
Yang manakah dari molekul berikut yang memiliki momen dipol? H 2 O, CO 2, SO 2, and CH 4 O H H Momen dipol Molekul polar S O O Momen dipol Molekul polar H O C O Tdk ada momen dipol Molekul nonpolar H C H H Tdk ada momen dipol Molekul nonpolar 10. 2
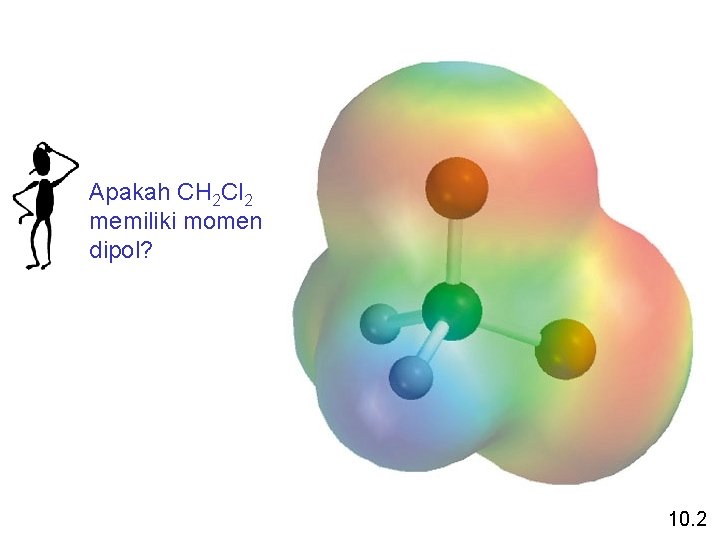
Apakah CH 2 Cl 2 memiliki momen dipol? 10. 2
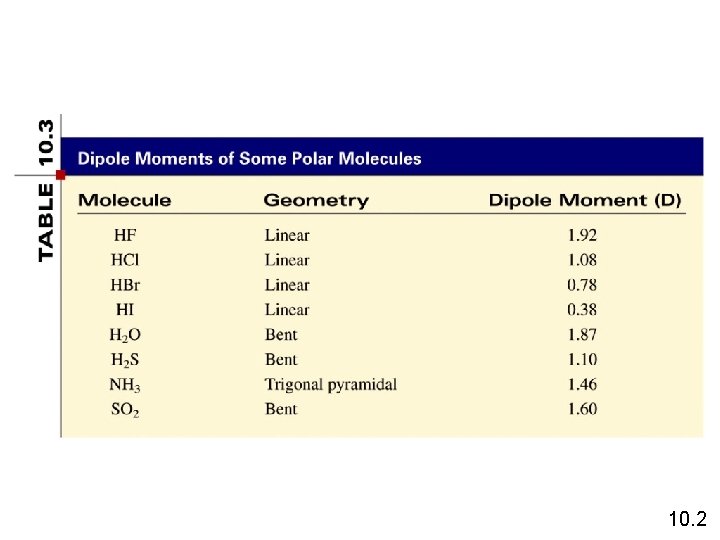
10. 2
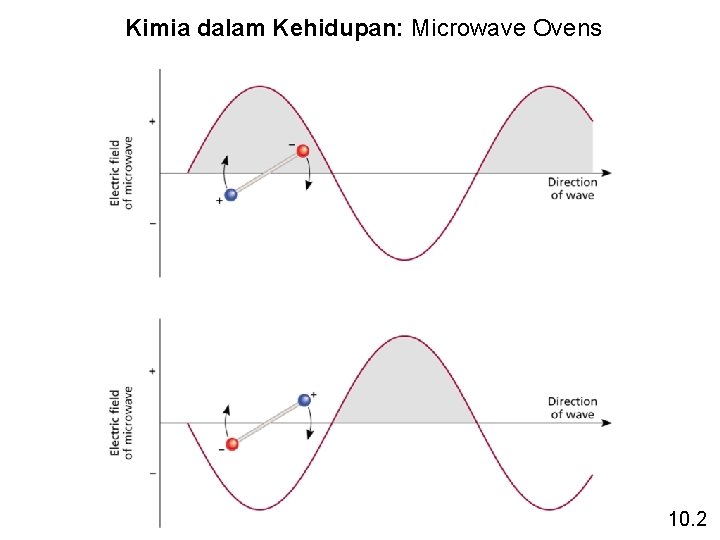
Kimia dalam Kehidupan: Microwave Ovens 10. 2

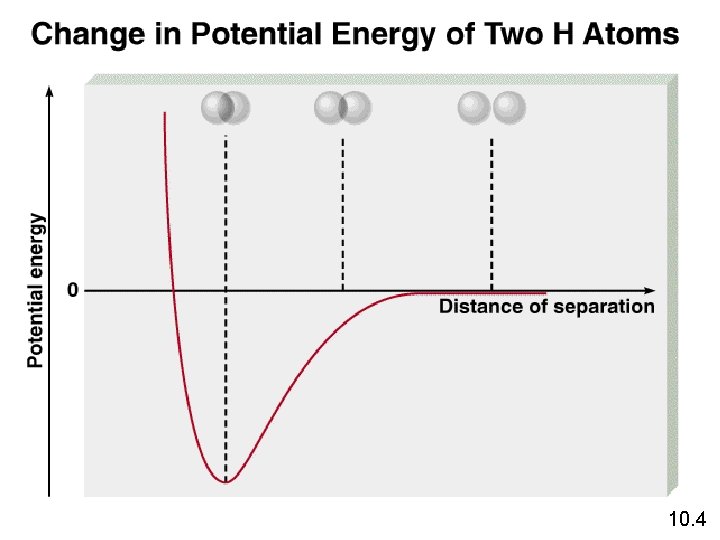
Bagaimana teori Lewis menerangkan ikatan pd H 2 dan F 2? Pembagian dua elektron antar dua atom. Energi Ikatan yg terdisosiasi Panjang Ikatan Tumpang-tindih H 2 436, 4 k. J/mol 74 pm 2 1 s F 2 150, 6 k. J/mol 142 pm 2 2 p Teori ikatan valensi – mengasumsikan bahwa elektron-elektron dalam molekul menempati orbital atom yang mengambil peranan dalam pembentukan ikatan. 10. 3
10. 4
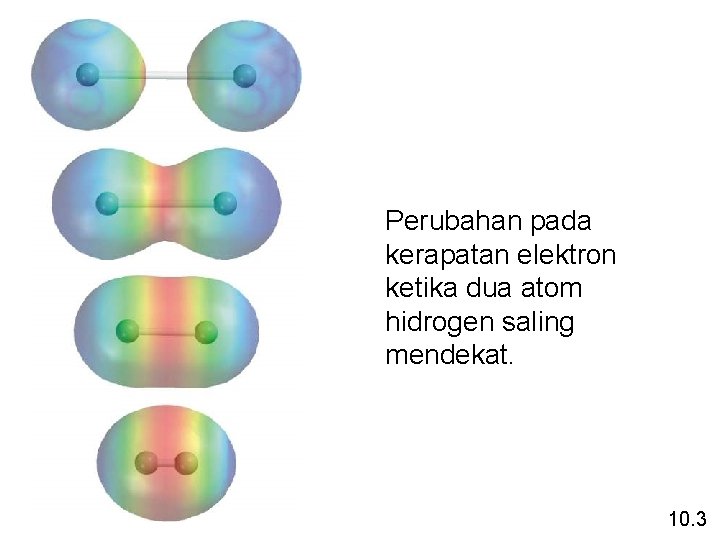
Perubahan pada kerapatan elektron ketika dua atom hidrogen saling mendekat. 10. 3
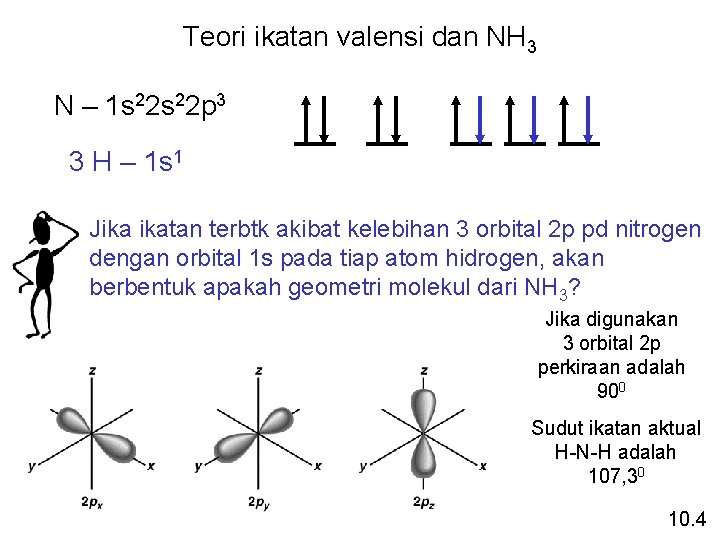
Teori ikatan valensi dan NH 3 N – 1 s 22 p 3 3 H – 1 s 1 Jika ikatan terbtk akibat kelebihan 3 orbital 2 p pd nitrogen dengan orbital 1 s pada tiap atom hidrogen, akan berbentuk apakah geometri molekul dari NH 3? Jika digunakan 3 orbital 2 p perkiraan adalah 900 Sudut ikatan aktual H-N-H adalah 107, 30 10. 4

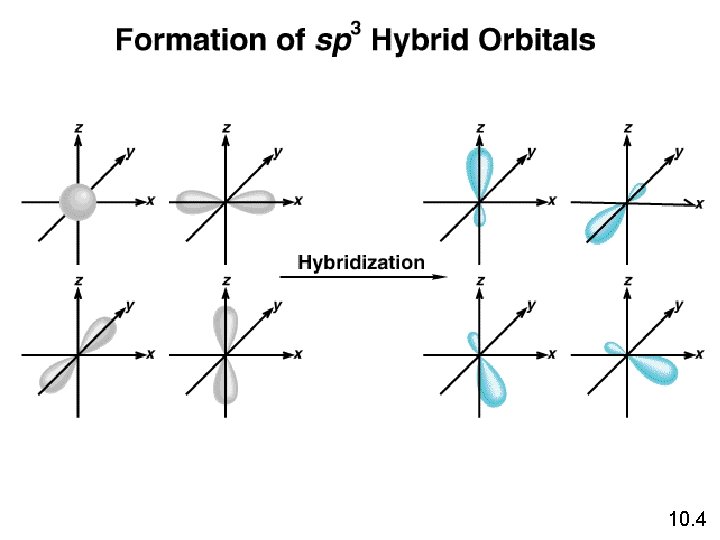
Hibridisasi– istilah yang digunakan untuk pencampuran orbital 2 atom dalam satu atom. 1. Tidak diterapkan pd atom yg terisolasi. 2. Merupakan pencampuran dari sedikitnya dua orbital atom yang tidak setara. 3. Jumlah orbital hibrida yg dihasilkan sama dengan jumlah orbital atom asli yang terlibat dalam proses hibridisasi 4. Hibridisasi membutuhkan energi; tetapi sistem memperoleh kembali energi ini, bahkan lebih selama pembentukan ikatan. 5. Ikatan kovalen terbentuk akibat tumpang-tindihnya orbital hibrida dengan orbital yang tidak terhibridisasi. 10. 4
10. 4
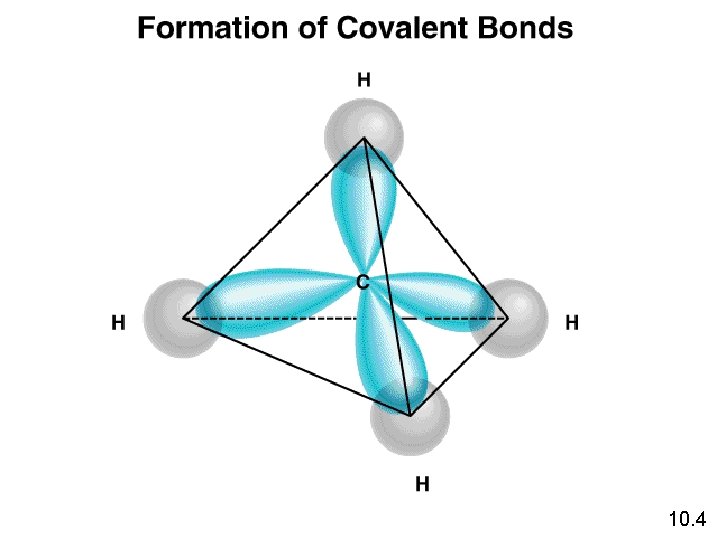
10. 4
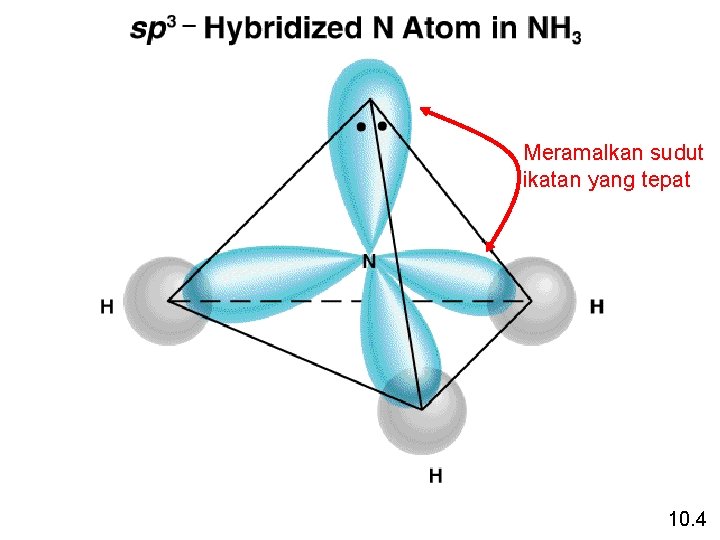
Meramalkan sudut ikatan yang tepat 10. 4
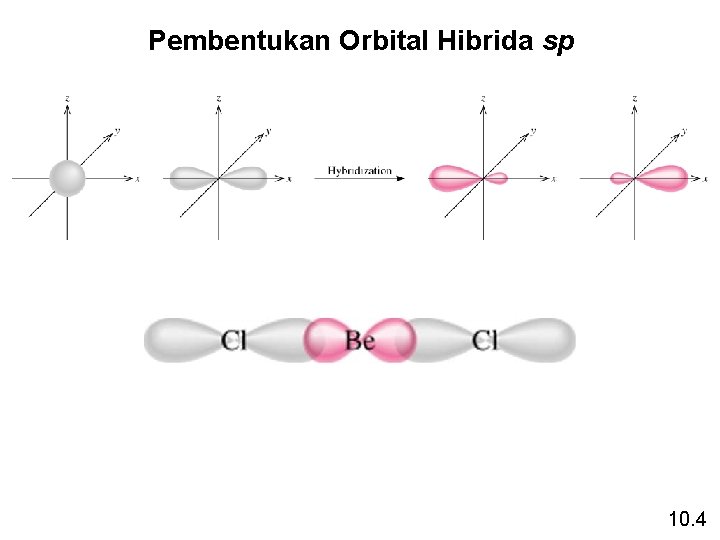
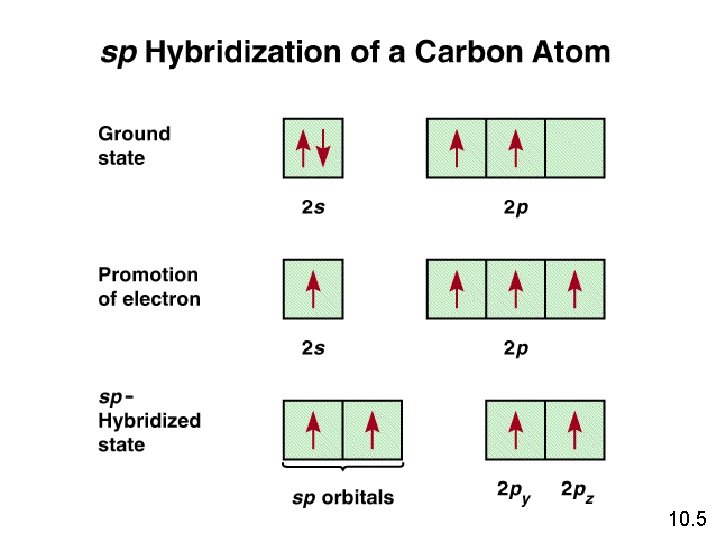
Pembentukan Orbital Hibrida sp 10. 4
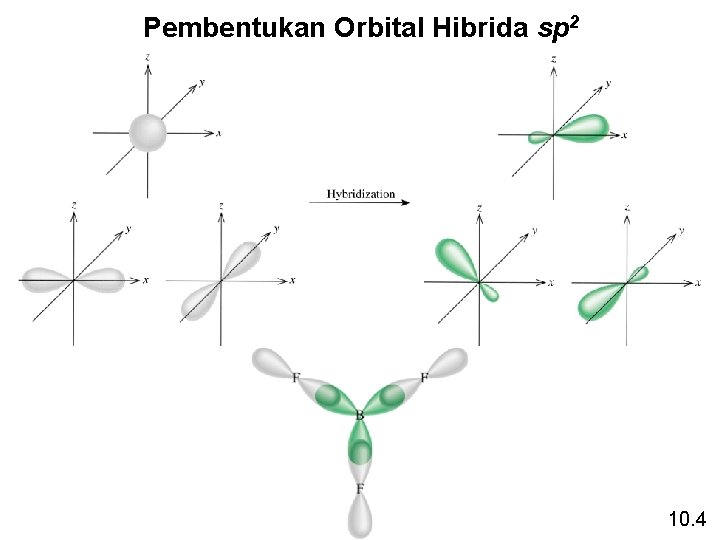
Pembentukan Orbital Hibrida sp 2 10. 4

Bagaimana meramalkan hibridisasi pusat atom? Hitung jumlah pasangan bebas DAN jumlah dari atoms yang terikat pada pusat atom # ps. bebas + # ikatan atom Hibridisasi Contoh 2 sp Be. Cl 2 3 sp 2 BF 3 4 sp 3 CH 4, NH 3, H 2 O 5 sp 3 d PCl 5 6 sp 3 d 2 SF 6 10. 4
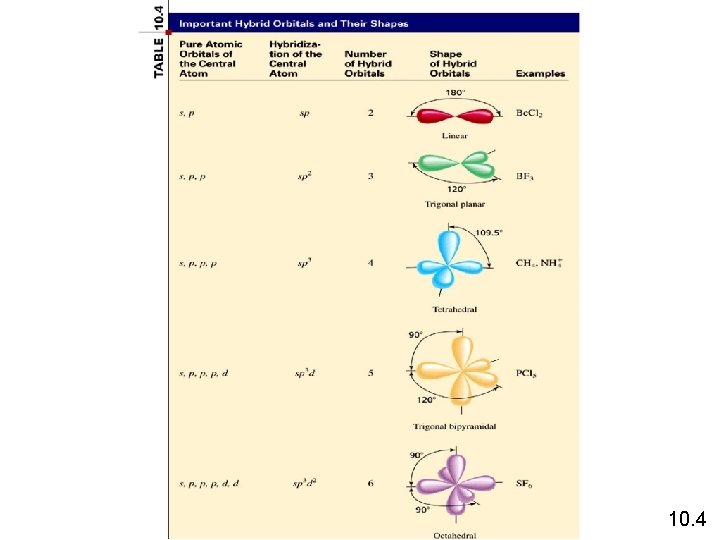
10. 4
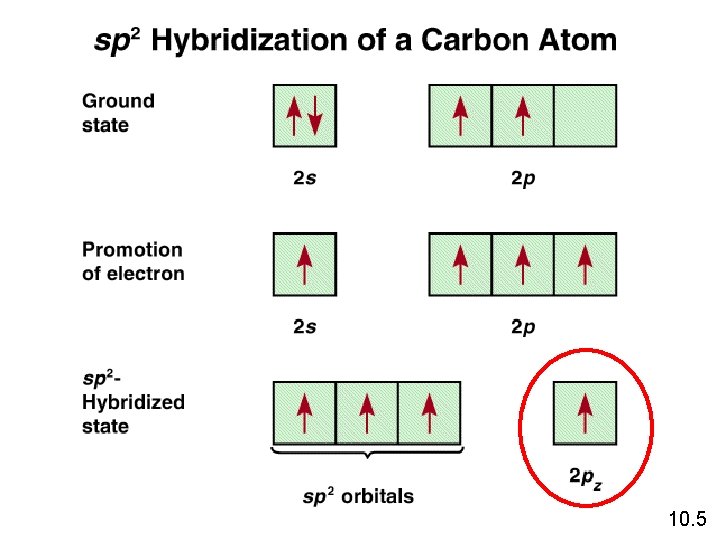
10. 5
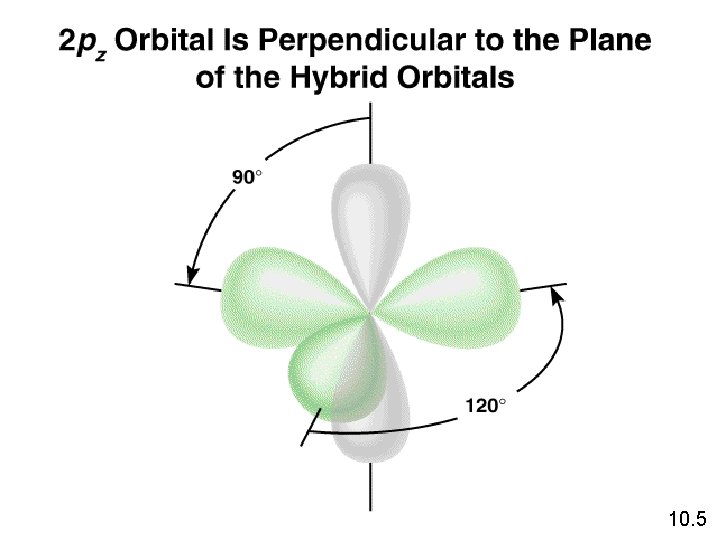
10. 5
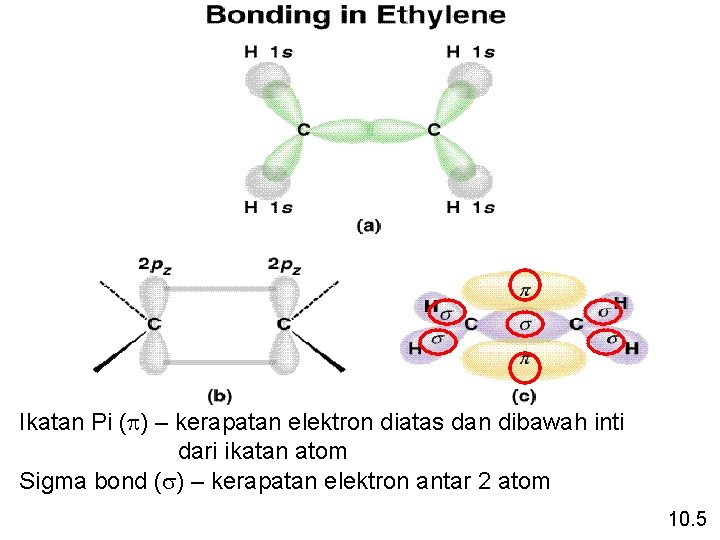
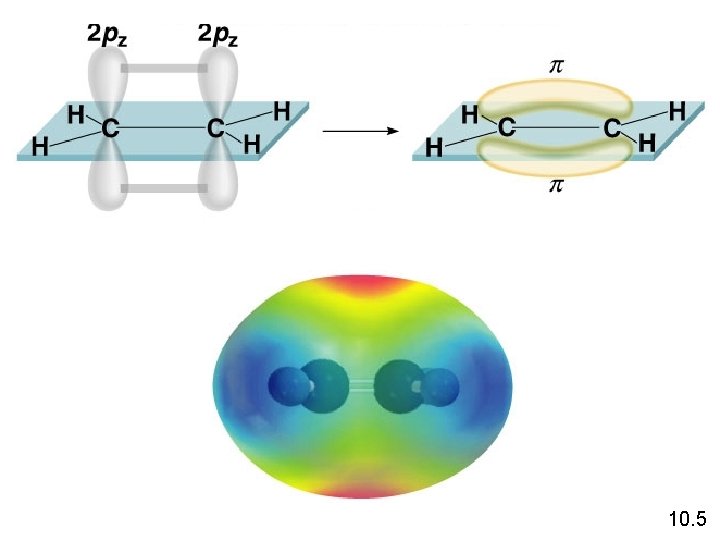
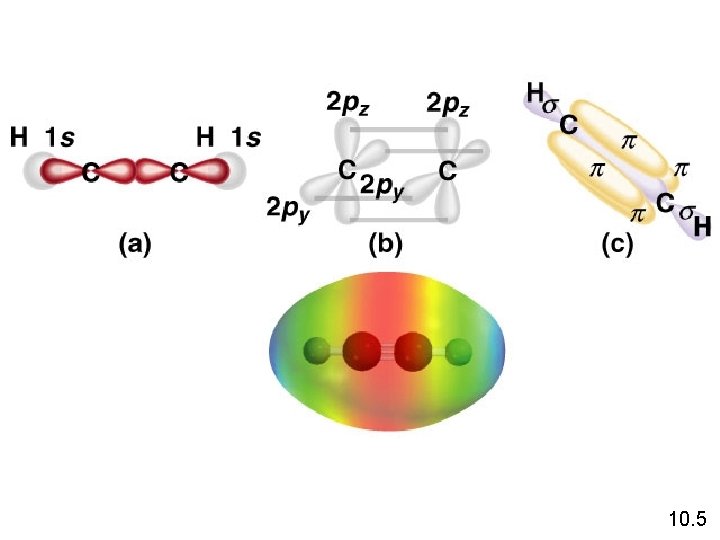
Ikatan Pi (p) – kerapatan elektron diatas dan dibawah inti dari ikatan atom Sigma bond (s) – kerapatan elektron antar 2 atom 10. 5
10. 5
10. 5
10. 5
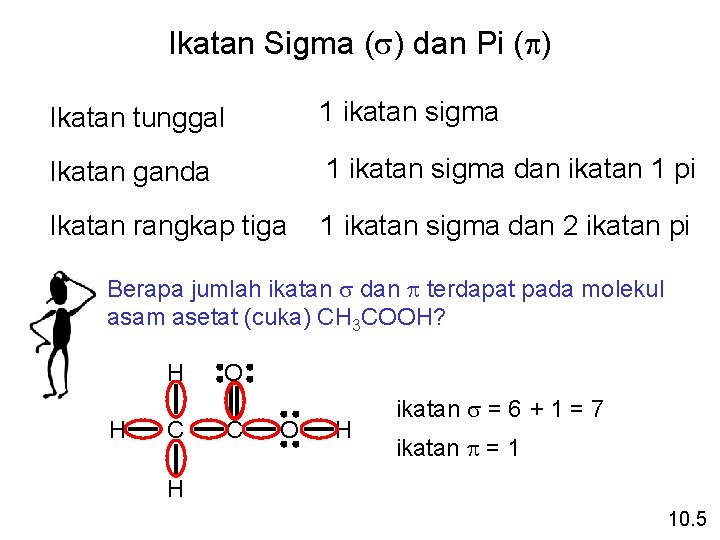
Ikatan Sigma (s) dan Pi (p) Ikatan tunggal 1 ikatan sigma Ikatan ganda 1 ikatan sigma dan ikatan 1 pi Ikatan rangkap tiga 1 ikatan sigma dan 2 ikatan pi Berapa jumlah ikatan s dan p terdapat pada molekul asam asetat (cuka) CH 3 COOH? H C O H ikatan s = 6 + 1 = 7 ikatan p = 1 H 10. 5

O O Percobaan menunjukkan O 2 adalah paramagnetik Tidak ada e- yang tdk berpasangan Maka disebut diamagnetik Teori Orbital Molekul – menggambarkan ikatan kovalen melalui istilah orbital molekul yg dihasilkan dr interaksi orbital 2 atom dr atom 2 yang berikatan dan yg terkait dg molekul secara keseluruhan. 10. 6
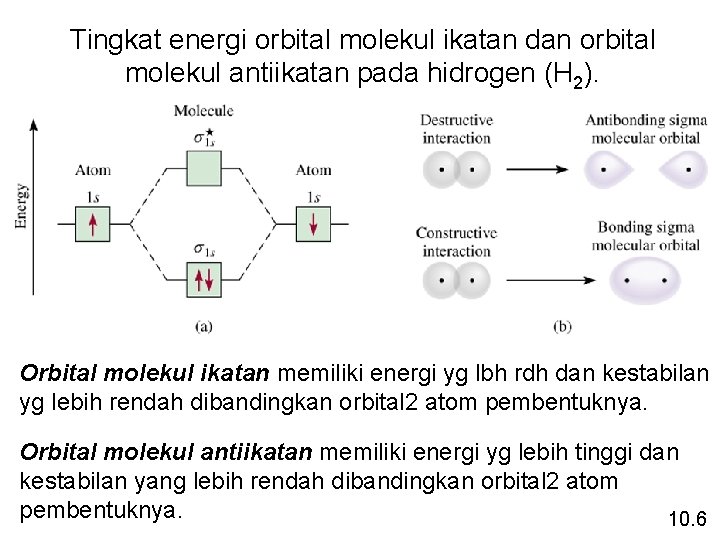
Tingkat energi orbital molekul ikatan dan orbital molekul antiikatan pada hidrogen (H 2). Orbital molekul ikatan memiliki energi yg lbh rdh dan kestabilan yg lebih rendah dibandingkan orbital 2 atom pembentuknya. Orbital molekul antiikatan memiliki energi yg lebih tinggi dan kestabilan yang lebih rendah dibandingkan orbital 2 atom pembentuknya. 10. 6
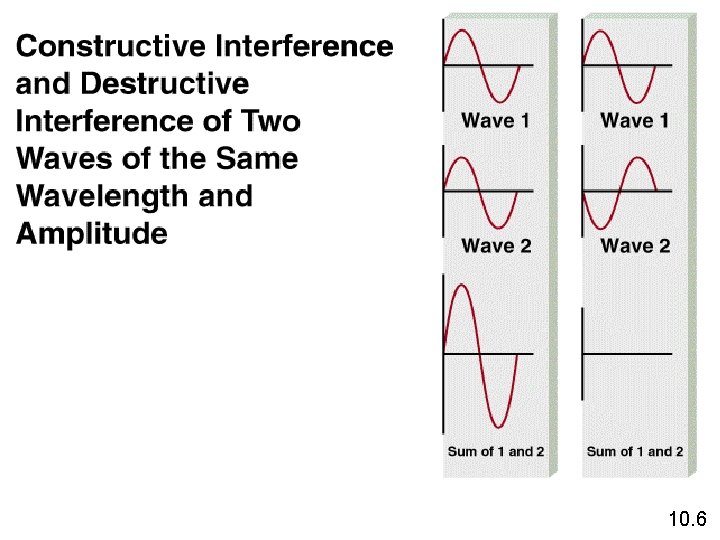
10. 6
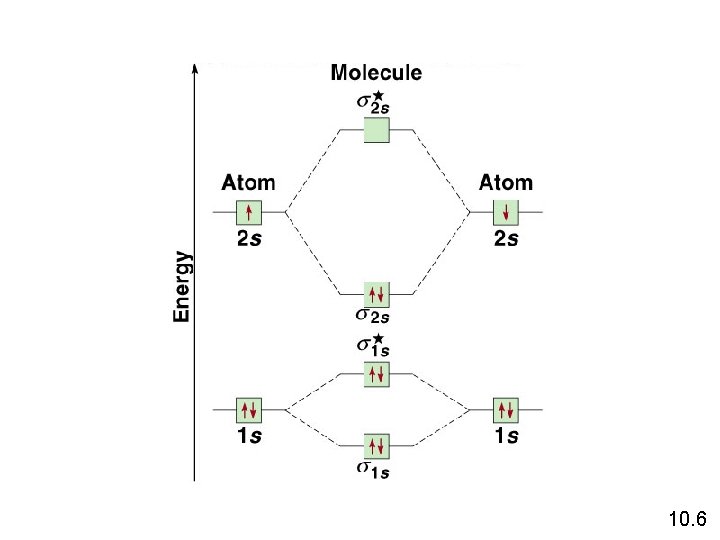
10. 6
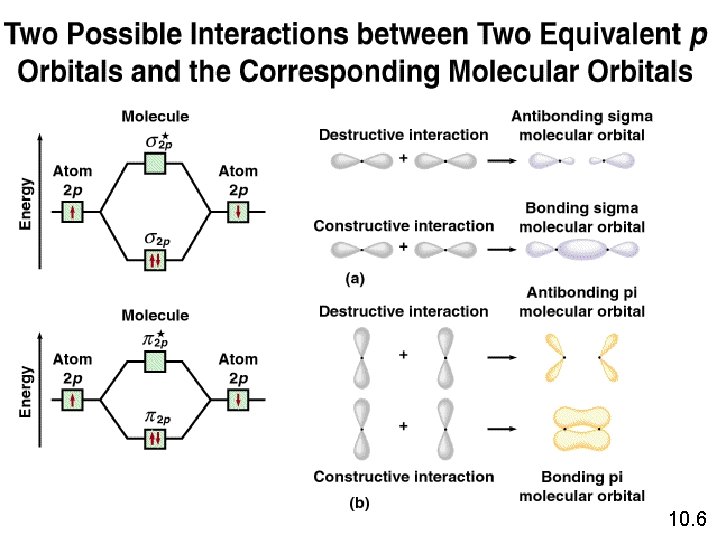
10. 6
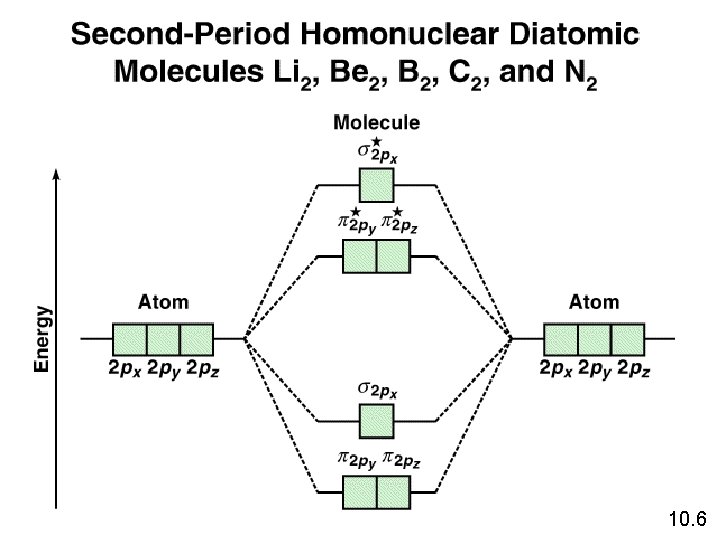
10. 6

Konfigurasi Orbital Molekul (OM) 1. Jumlah orbital molekul yg terbentuk selalu sama dg jumlah orbital atom yg bergabung. 2. Semakin stabil orbital molekul ikatan, semakin kurang stabil orbital molekul antiikatan yang berkaitan. 3. Pengisian orbital molekul dimulai dr energi rendah ke energi tinggi. 4. Setiap orbital molekul dpt menampung hingga dua elektron. 5. Gunakan aturan Hund ketika elektron ditambahkan ke orbital molekul dengan energi yang sama. 6. Jumlah elektron dalam orbital molekul sama dg jumlah semua elektron pada atom-atom yg berikatan. 10. 7
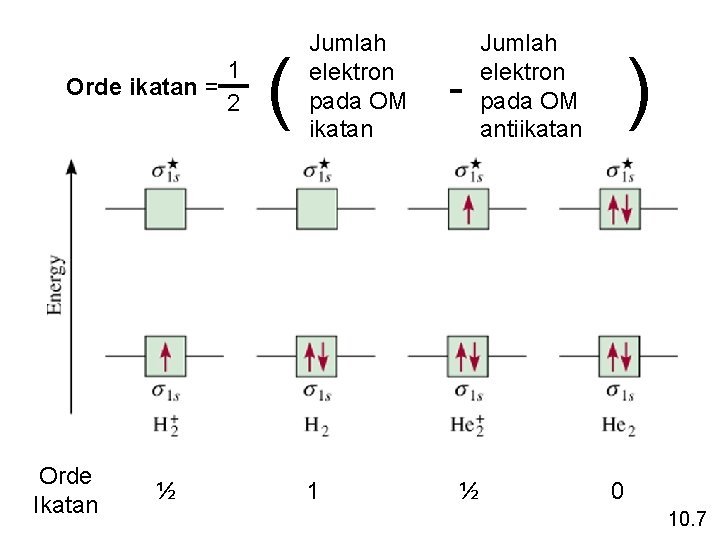
1 Orde ikatan = 2 Orde Ikatan ½ ( Jumlah elektron pada OM ikatan 1 - ½ Jumlah elektron pada OM antiikatan ) 0 10. 7
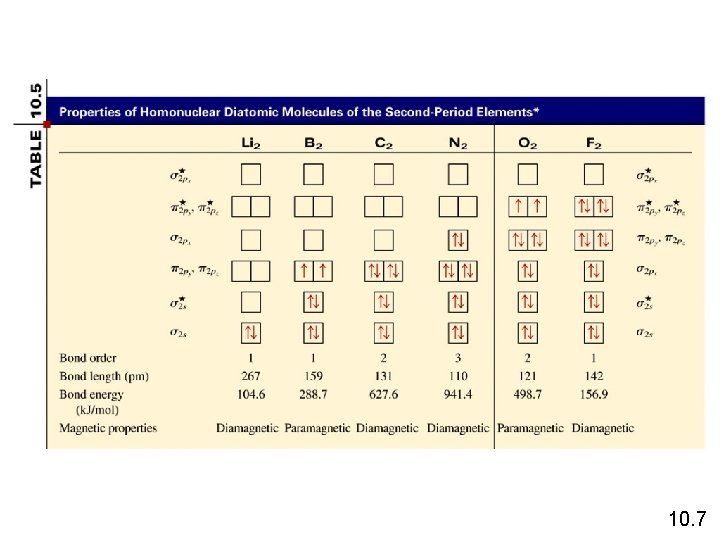
10. 7
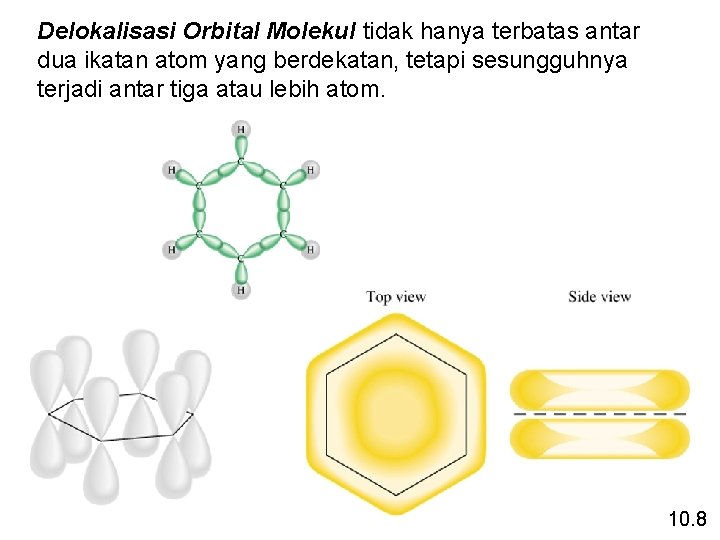
Delokalisasi Orbital Molekul tidak hanya terbatas antar dua ikatan atom yang berdekatan, tetapi sesungguhnya terjadi antar tiga atau lebih atom. 10. 8
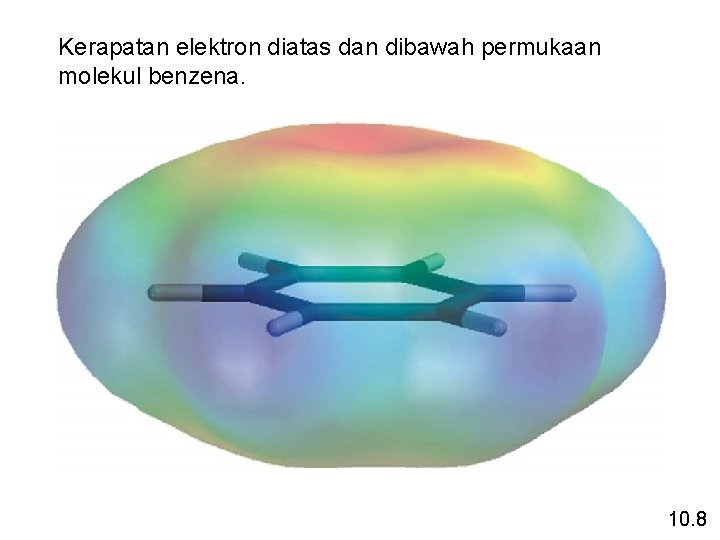
Kerapatan elektron diatas dan dibawah permukaan molekul benzena. 10. 8
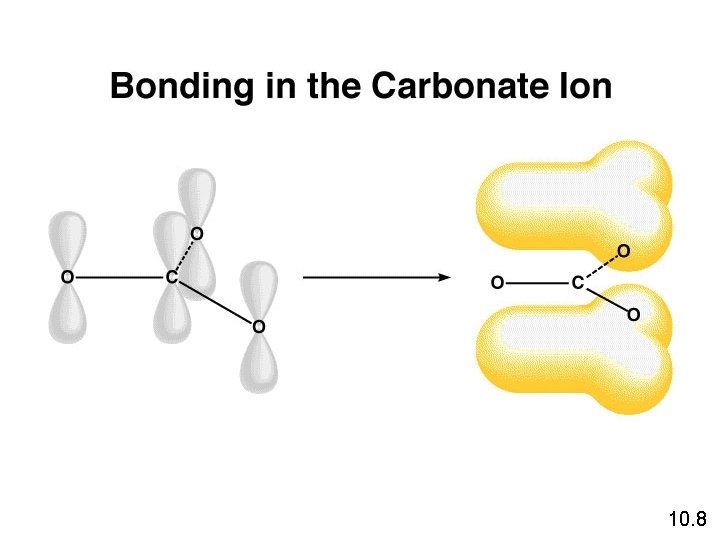
10. 8
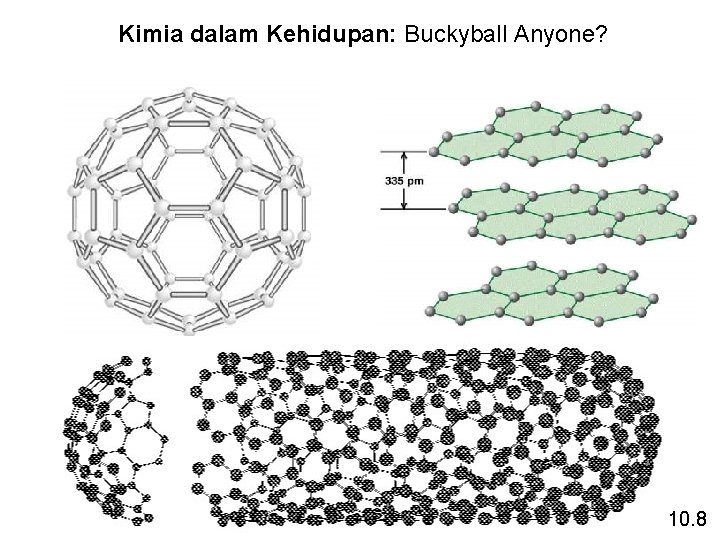
Kimia dalam Kehidupan: Buckyball Anyone? 10. 8
- Slides: 63