Bab 1 Struktur Atom A Struktur Atom 1

Bab 1 Struktur Atom

A. Struktur Atom 1. Model Atom Modern Teori mekanika kuantum : Posisi atau lokasi suatu elektron tidak dapat ditentukan secara pasti. Hal yang dapat dipastikan hanyalah kebolehjadian menemukan elektron pada jarak tertentu dari inti. Daerah dengan kemungkinan terbesar menemukan keberadaan elektron itu disebut orbital. oleh Erwin Schrodinger

2. Bilangan Kuantum a. Bilangan Kuantum Utama (n) Bilangan kuantum utama mempunyai harga 1, 2, 3, 4, dan seterusnya. Makin besar bilangan kuantum utama, makin besar pula energi elektron yang menempati kulit itu. Dari harga n dapat diketahui nomor kulit yang ditempati elektron tersebut. Jumlah maksimal elektron yang menempati bilangan kuantum utama dapat dirumuskan 2 n 2 elektron.
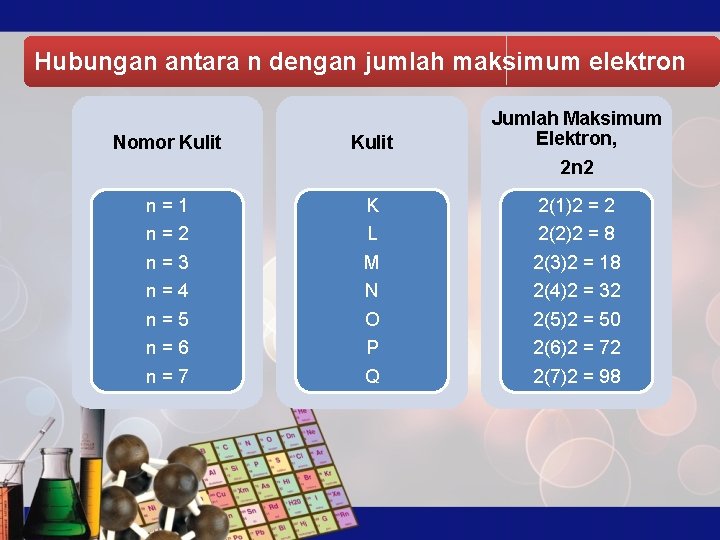
Hubungan antara n dengan jumlah maksimum elektron Nomor Kulit Jumlah Maksimum Elektron, 2 n 2 n=1 K 2(1)2 = 2 n=2 L 2(2)2 = 8 n=3 n=4 n=5 n=6 n=7 M N O P Q 2(3)2 = 18 2(4)2 = 32 2(5)2 = 50 2(6)2 = 72 2(7)2 = 98
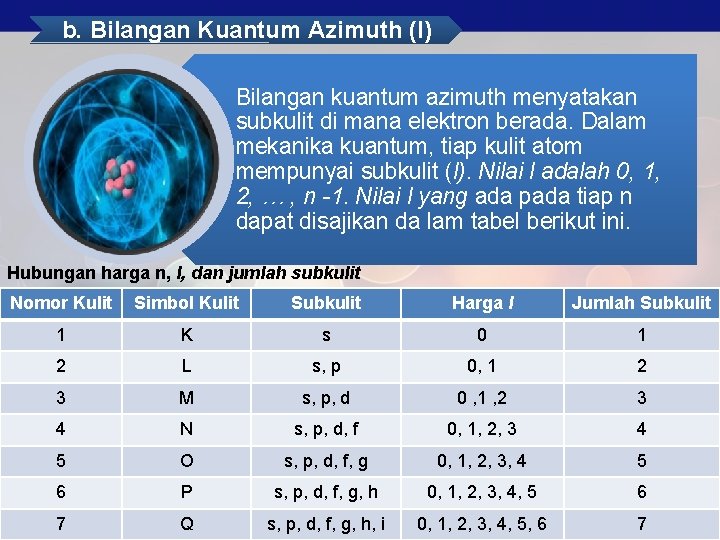
b. Bilangan Kuantum Azimuth (l) Bilangan kuantum azimuth menyatakan subkulit di mana elektron berada. Dalam mekanika kuantum, tiap kulit atom mempunyai subkulit (l). Nilai l adalah 0, 1, 2, … , n -1. Nilai l yang ada pada tiap n dapat disajikan da lam tabel berikut ini. Hubungan harga n, l, dan jumlah subkulit Nomor Kulit Simbol Kulit Subkulit Harga l Jumlah Subkulit 1 K s 0 1 2 L s, p 0, 1 2 3 M s, p, d 0 , 1 , 2 3 4 N s, p, d, f 0, 1, 2, 3 4 5 O s, p, d, f, g 0, 1, 2, 3, 4 5 6 P s, p, d, f, g, h 0, 1, 2, 3, 4, 5 6 7 Q s, p, d, f, g, h, i 0, 1, 2, 3, 4, 5, 6 7
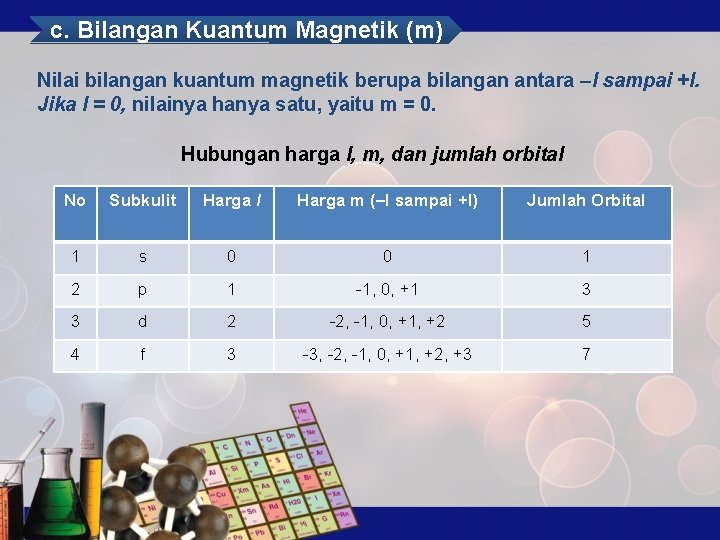
c. Bilangan Kuantum Magnetik (m) Nilai bilangan kuantum magnetik berupa bilangan antara –l sampai +l. Jika l = 0, nilainya hanya satu, yaitu m = 0. Hubungan harga l, m, dan jumlah orbital No Subkulit Harga l Harga m (–l sampai +l) Jumlah Orbital 1 s 0 0 1 2 p 1 -1, 0, +1 3 3 d 2 -2, -1, 0, +1, +2 5 4 f 3 -3, -2, -1, 0, +1, +2, +3 7
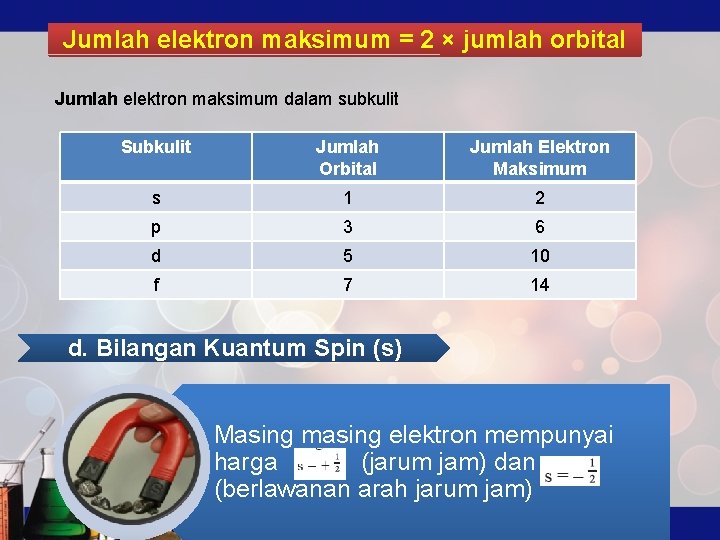
Jumlah elektron maksimum = 2 × jumlah orbital Jumlah elektron maksimum dalam subkulit Subkulit Jumlah Orbital Jumlah Elektron Maksimum s 1 2 p 3 6 d 5 10 f 7 14 d. Bilangan Kuantum Spin (s) Masing masing elektron mempunyai harga (jarum jam) dan (berlawanan arah jarum jam)
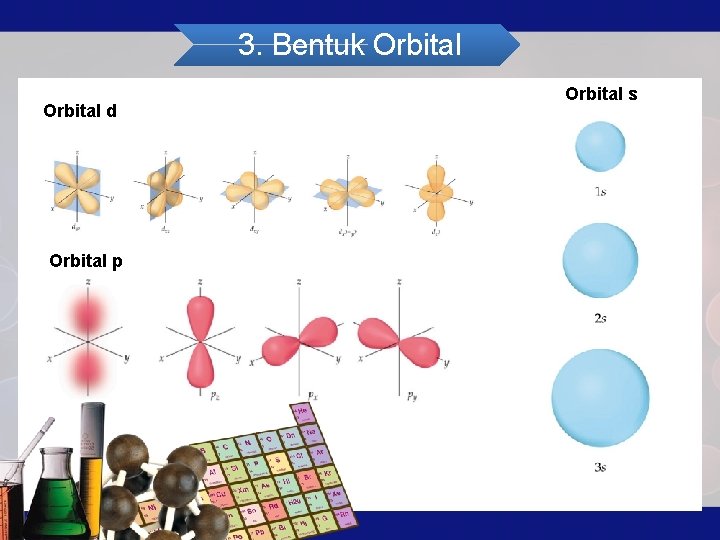
3. Bentuk Orbital d Orbital p Orbital s

4. Konfigurasi Elektron Cara penyusunan elektron di sekitar inti atom Asas Aufbau “Elektron secara bertahap menempati orbital dimulai dari energi yang paling rendah. Setelah orbital berenergi rendah terisi penuh, elektron menempati orbital yang energinya satu tingkat lebih tinggi, dan seterusnya sampai semua elektron dalam atom menempati orbitalnya. ”

Asas Larangan Pauli “Elektronelektron dalam satu atom tidak boleh mempunyai 4 bilangan kuantum yang nilainya sama semua. ” Kaidah Hund “Elektron-elektron pada orbital yang memiliki tingkat energi sama akan mengisi terlebih dahulu kotak yang kosong dengan arah spin tertentu. Kemudian, orbital diisi dengan elektron berikutnya dengan arah spin yang berlawanan. ”

5. Sistem Periodik Untuk mengetahui lebih jelas tentang penentuan nomor periode untuk semua unsur ditempuh dengan cara: a. menentukan konfigurasi elektron unsur tersebut, b. nomor periode = nomor kulit terbesar = harga n terbesar. a. Penggolongan Unsur Menurut Cara Tradisional 1) Golongan A terletak di blok s dengan elektron valensinya terletak di subkulit s dan di blok p dengan elektron valensinya terletak di subkulit p.

2) Golongan B terletak di blok d dengan elektron valensinya terletak di subkulit s dan d, serta di blok f dengan elektron valensinya terletak di subkulit s dan f. b. Penggolongan Unsur Menurut Cara IUPAC unsur-unsur dalam sistem periodik dibagi menjadi 18 golongan. Tidak ada pemisahan antara golongan A dan golongan B. Untuk lebih jelasnya, perhatikan tabel berikut ini!

Penggolongan dengan cara IUPAC memiliki kelemahan. Kelemahannya adalah agak sulit diterapkan untuk unsur yang memiliki nomor atom kurang dari 19.

B. Bentuk Molekul Teori Jumlah Pasangan Elektron di Sekitar Inti Urutan untuk merumuskan tipe molekul 1. Menentukan atom pusat. 2. Menentukan jumlah elektron valensi atom pusat (EV). 3. Menentukan jumlah elektron yang digunakan atom pusat untuk ikatan (e). 4. Menghitung jumlah pasangan elektron (domain elektron) bebas dengan rumus: jumlah pasangan elektron bebas =
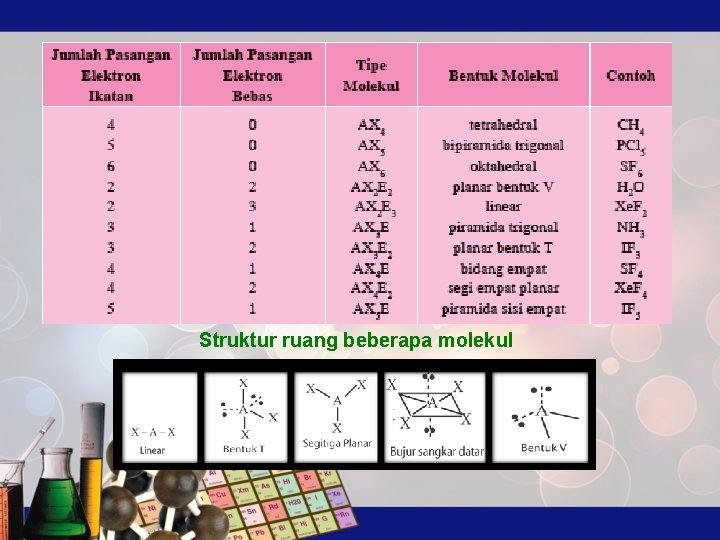
Struktur ruang beberapa molekul

1. Teori Hibridisasi Dasar dari teori hibridisasi adalah pembastaran orbital atom yang terlibat dalam ikatan. Macam-macam tipe hibridisasi

C. Interaksi Antarmolekul dengan Sifatnya 1. Gaya van der Waals a. Gaya London adalah gaya yang terjadi antarmolekul nonpolar. b. Gaya Antardipol adalah gaya tarik-menarik antarmolekul polar.

2. Ikatan Hidrogen Ikatan hidrogen adalah ikatan yang terjadi antara atom hidrogen dengan atom yang mempunyai keelektronegatifan tinggi, misalnya fluorin, oksigen, dan nitrogen. Ikatan hidrogen sangat kuat sehingga molekul yang berikatan hidrogen dengan molekul lain akan mempunyai titik didih lebih tinggi.
- Slides: 18