B A B 9 KELA RUTA N S

B A B 9: KELA RUTA N (S) HASI D A N L KALI KELA RUTA N (K sp) GRADE XI SENIOR HIGH SCHOOL Created by : I. F. Sari Indah, S. ST

N A T U R A L E ) K S / Y T I L I B U L (SO Created by : I. F. Sari Indah, S. ST

KELARUTAN (Solubility/S) Kelarutan adalah jumlah maksimum zat yang dapat larut dalam sejumlah tertentu pelarut. Created by : I. F. Sari Indah, S. ST

Satuan Kelarutan Untuk zat yang tergolong mudah larut, kelarutannya dinyatakan dalam gram per 100 gram air. Namun, untuk zat yang tergolong sukar larut, kelarutannya dinyatakan dalam mol/L, sama dengan KEMOLARAN Created by : I. F. Sari Indah, S. ST

Menentukan Cara Penulisan Kelarutan Pada Suatu Larutan Contoh Soal : Tentukan kelarutan Ag 2 Cr. O 4 (Mr = 332) dalam air murni adalah 33, 2 mg Jawab : per liter! S = n atau S = gr x 1000 V Mr V (m. L) S = 0, 0332 gr x 1000 332 g/mol 1000 = 10 -4 mol/L = 10 -4 M Created by : I. F. Sari Indah, S. ST

Contoh Soal Menentukan Kelarutan Pada Suatu Larutan: Soal 1 Sebanyak 4, 5 mg Magnesium hidrokisda (Mg(OH)2) dapat larut dalam 500 m. L air. Nyatakanlah kelarutan Mg(OH)2 dalam mol/L Jawab : S= n atau S = gr x 1000 V Mr V (m. L) S = 0, 0045 gr x 1000 = 0, 00015517 mol/L 58 g/mol Created by : I. F. Sari Indah, S. ST 500(m. L)

Contoh Soal Menentukan Kelarutan Pada Suatu Larutan: Soal 2 Kelarutan timbel (II) kromat (Pb. Cr. O 4) daam air adalah 1, 34 mol/L. Berapa gram timbel (II) kromat yang dapat dalam 200 S = n larut atau S= gr m. Lx air? 1000 V 1, 34 mol/L Mr = X gr x 58 g/mol X gr V (m. L) 1000 5 200(m. L) = 77, 72 g/L = 15, 544 gram, 5 L Jadi massa timbel (II) kromat (Pb. Cr. O 4) adalah 15, 544 gram Created by : I. F. Sari Indah, S. ST

TETAPAN HASIL KALI KELARUTAN (Ksp) Created by : I. F. Sari Indah, S. ST

TETAPAN HASIL KALI KELARUTAN Penjelasan Umum(Ksp) Perak kromat (Ag 2 Cr. O 4) merupakan contoh garam yang sukar larut dalam air. Jika kita memasukkan sedikit saja kristal garam perak kromat ke dalam segelas air, kemudian diaduk, kita akan melihat bahwa sebagian besar dari garam tersebut tidak larut (mengendap di dasar gelas) Larutan perak kromat mudah sekali jenuh. Apakah setelah mencapai keadaan jenuh proses melarut berhenti? Ternyata tidak. Melalui percobaan telah diketahui bahwa larutan jenuh Created by : I. F. Sari Indah, S. ST tetap terjadi proses melarut, tetapi pada saat yang sama

TETAPAN HASIL KALI KELARUTAN Penjelasan Umum(Ksp) Dengan kata lain, dalam keadaan jenuh terdapat kesetimbangan antara zat padat dengan tak larut dengan larutannya. Khusus untuk garam atau basa, kesetimbangan tersebut terjadi antara zat padat tak larut dengan ion-ionnya. Kesetimbangan dalam larutan jenuh perak kromat adalah sebagai Ag Cr. O 4 berikut : 2 Ag+(aq) + 2 (s) Cr. O 42 -(aq) Tetapan kesetimbangan dari kesetimbangan antara garam atau basa yang sedikit larut disebut TETAPAN HASIL Created by : I. F. Sari Indah, S. ST KALI KELARUTAN (Solubility product constant) dan
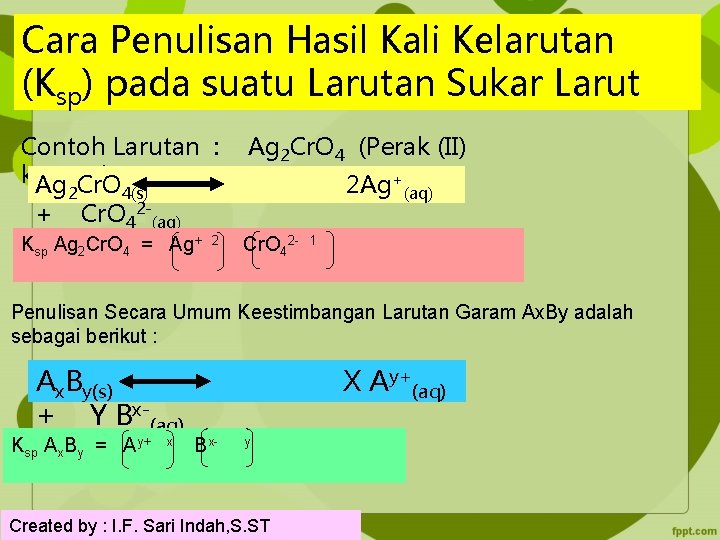
Cara Penulisan Hasil Kali Kelarutan (Ksp) pada suatu Larutan Sukar Larut Contoh Larutan : kromat) Ag Cr. O + 2 Ag 2 Cr. O 4 (Perak (II) 2 Ag+(aq) 4(s) Cr. O 42 -(aq) Ksp Ag 2 Cr. O 4 = Ag+ 2 Cr. O 42 - 1 Penulisan Secara Umum Keestimbangan Larutan Garam Ax. By adalah sebagai berikut : Ax. By(s) + Y Bx-(aq) Ksp Ax. By = Ay+ x Bx- y Created by : I. F. Sari Indah, S. ST X Ay+(aq)

Latihan Soal Cara Penulisan Hasil Kelarutan Pada Larutan Yang Sukar Larut Soal 1 Tuliskan persamaan tetapan hasil kali kelarutan untuk senyawa berikut : a. Pb. SO 4 Jawab : Pb. SO 4(s) Pb 2+(aq) + SO 42 -(aq) Ksp Pb. SO 4 = Pb 2+ 1 SO 42 - 1
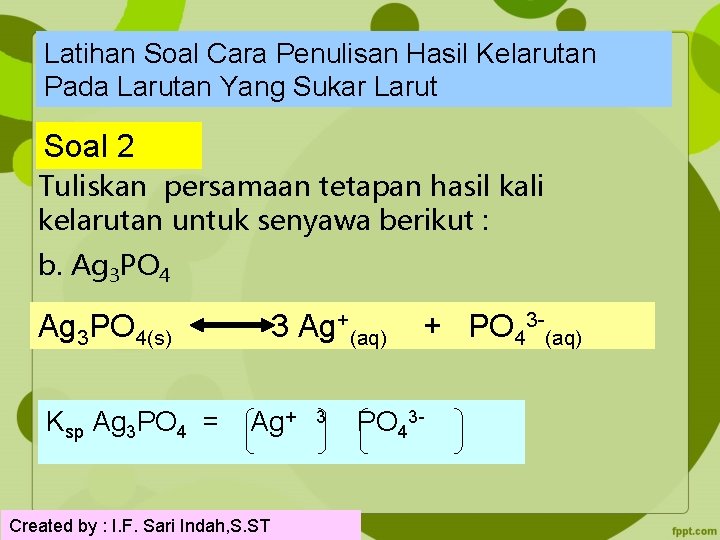
Latihan Soal Cara Penulisan Hasil Kelarutan Pada Larutan Yang Sukar Larut Soal 2 Tuliskan persamaan tetapan hasil kali kelarutan untuk senyawa berikut : b. Ag 3 PO 4(s) 3 Ag+(aq) + PO 43 -(aq) Ksp Ag 3 PO 4 = Ag+ 3 PO 43 - Created by : I. F. Sari Indah, S. ST

Hubungan Kelarutan (S) dan Tetapan Hasil Kelarutan (Ksp) Created by : I. F. Sari Indah, S. ST
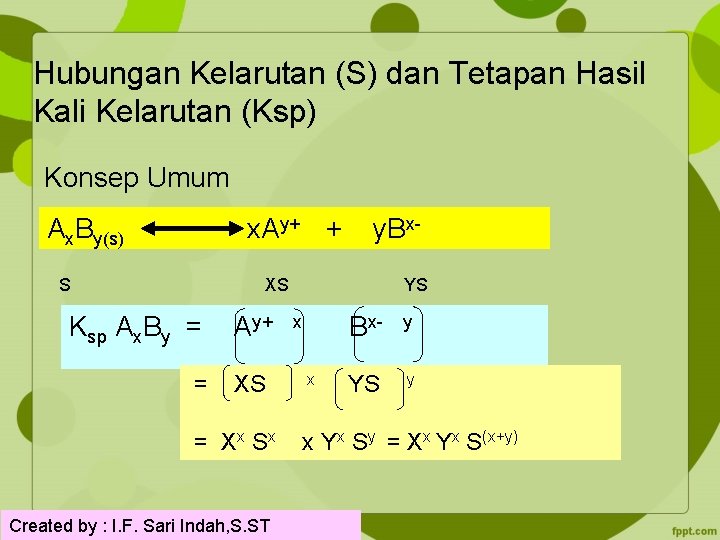
Hubungan Kelarutan (S) dan Tetapan Hasil Kali Kelarutan (Ksp) Konsep Umum Ax. By(s) x. Ay+ + y. Bx- S XS YS Ksp Ax. By = Ay+ x Bx- y = XS x YS y = Xx Sx x Yx Sy = Xx Yx S(x+y) Created by : I. F. Sari Indah, S. ST

Latihan Soal Hubungan Kelarutan (S) Dengan Hasil Kali Kelarutan (Ksp) Tuliskan Hubungan Kelarutan Dengan Tetapan hasil kelarutan untuk zat elektrolit berikut ! a. Ca. SO 4 Ca 2+ + SO 42 S S Ksp Ca. SO 4 = (S) = S 2

Latihan Soal Hubungan Kelarutan (S) Dengan Hasil Kali Kelarutan (Ksp) Tuliskan Hubungan Kelarutan Dengan Tetapan hasil kelarutan untuk zat elektrolit berikut ! b. Ni 3(As. O 4)2 3 Ni 2+ + 2 As. O 43 S 3 S 2 S Ksp Ni 3(As. O 4)2 = (3 S)3 (2 S)2 = 108 S 5

Latihan Soal Menentukan Ksp Berdasarkan Kelarutan Contoh 1 Kelarutan Magnesium Oksalat (Mg. C 2 O 4) dalam air sebesar 0, 0093 mol/L. Hitunglah Ksp magnesium oksalat tersebut. (Ar O = 16, C = 12, dan Mg = 24) Created by : I. F. Sari Indah, S. ST

Jawab : Mg. C 2 O 4 Mg 2+ + C 2 O 42 - S S Ksp = (S) 2 = S = ( 9, 3 x 10 -3)2 -6 = 86, 49 x 10 Created by : I. F. Sari Indah, S. ST

Latihan Soal Menentukan Ksp Berdasarkan Kelarutan Contoh 2 Tentukan konsentrasi ion Ag+ dalam larutan jenuh Ag 2 Cr. O 4 (Ksp -12 Ag 2 Cr. O 4 = 1, 1 x 10 ) Created by : I. F. Sari Indah, S. ST

Jawab : Created by : I. F. Sari Indah, S. ST

Latihan Soal Menentukan Ksp Berdasarkan Kelarutan Contoh 3 Diketahui Ksp Ca(OH)2 = 5 x 10 -6, tentukan p. H larutan jenuh Ca(OH)2! Created by : I. F. Sari Indah, S. ST

Pengaruh Ion Senama Terhadap Kelarutan Created by : I. F. Sari Indah, S. ST

Pengaruh Ion Senama Dalam Kelarutan Pengaruh Ion Senama adalah dapat memperkecil kelarutan Created by : I. F. Sari Indah, S. ST

Contoh Soal Pengaruh Ion Senama Soal 1 Diketahui Ksp Ag. Cl = 1 x 10 -10. Tentukan kelarutan Ag. Cl dalam larutan : a. Na. Cl 0, 1 M dan b. Ca. Cl 2 0, 1 M Created by : I. F. Sari Indah, S. ST
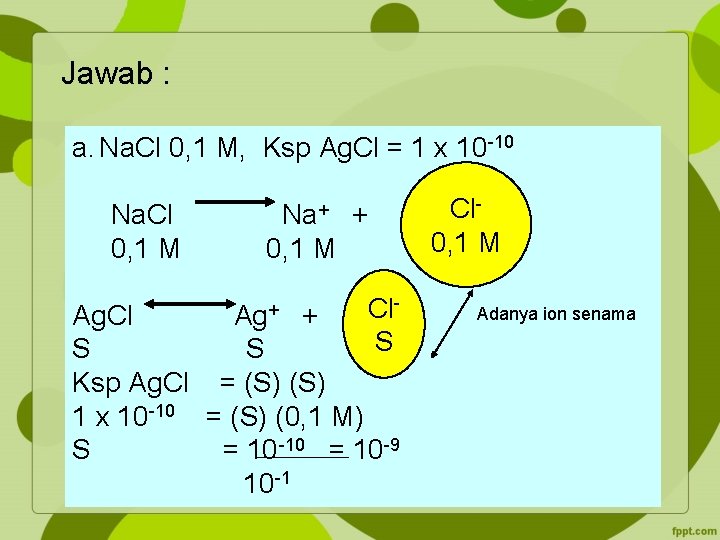
Jawab : a. Na. Cl 0, 1 M, Ksp Ag. Cl = 1 x 10 -10 Na. Cl Na+ + 0, 1 M Cl. S S Ksp Ag. Cl = (S) 1 x 10 -10 = (S) (0, 1 M) S = 10 -10 = 10 -9 10 -1 Ag. Cl Ag+ + Cl 0, 1 M Adanya ion senama
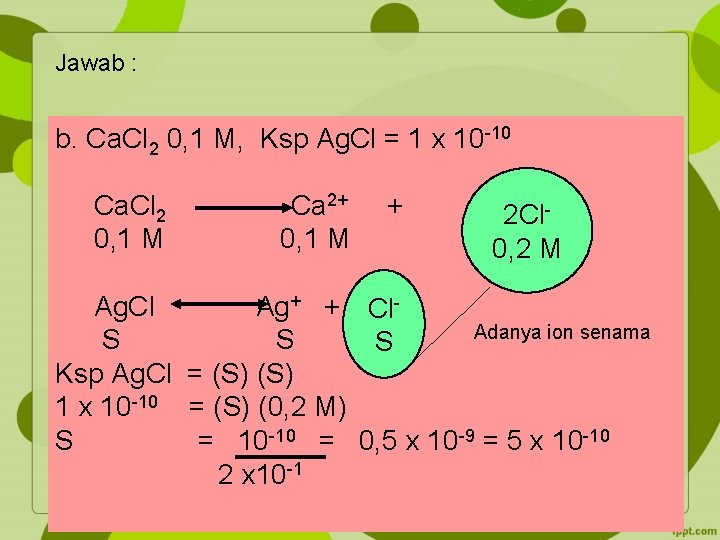
Jawab : b. Ca. Cl 2 0, 1 M, Ksp Ag. Cl = 1 x 10 -10 Ca. Cl 2 Ca 2+ + 0, 1 M 2 Cl 0, 2 M Ag. Cl Ag+ + Cl. Adanya ion senama S S S Ksp Ag. Cl = (S) 1 x 10 -10 = (S) (0, 2 M) S = 10 -10 = 0, 5 x 10 -9 = 5 x 10 -10 2 x 10 -1

Pengaruh p. H Terhadap Kelarutan

Pengaruh p. H Terhadap Kelarutan Tingkat keasaman larutan (p. H) dapat memengaruhi kelarutan dari berbagai jenis zat. Suatu basa umumnya lebih larut dalam larutan yang bersifat asam, dan sebaliknya, lebih sukar larut dalam larutan yang bersifat basa. Garam-garam yang berasal dari asam lemah akan lebih mudah larut dalam larutan yang bersifat asam kuat.

Pengaruh p. H Terhadap Kelarutan 1. p. H dan Kelarutan Basa Sesuai dengan efek ion senama, suatu basa akan lebih sukar larut dalam larutan yang bersifat basa daripada larutan netral Contoh Soal : Diketahui Ksp Fe(OH)2 = 8 x 10 -16. Tentukan kelarutan Fe(OH)2 dalam : a. Akuades b. Larutan Na. OH 0, 01 M


- Slides: 32