Az orvosi biotechnolgiai mesterkpzs megfeleltetse az Eurpai Uni

Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4. 1. 2 -08/1/A-2009 -0011

Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4. 1. 2 -08/1/A-2009 -0011 Kvell Krisztián A Gerontológia Molekuláris és Klinikai Alapjai – 28. előadás ÖREGEDÉSSEL KAPCSOLATOS INTRACELLULÁRIS BETEGSÉGEK
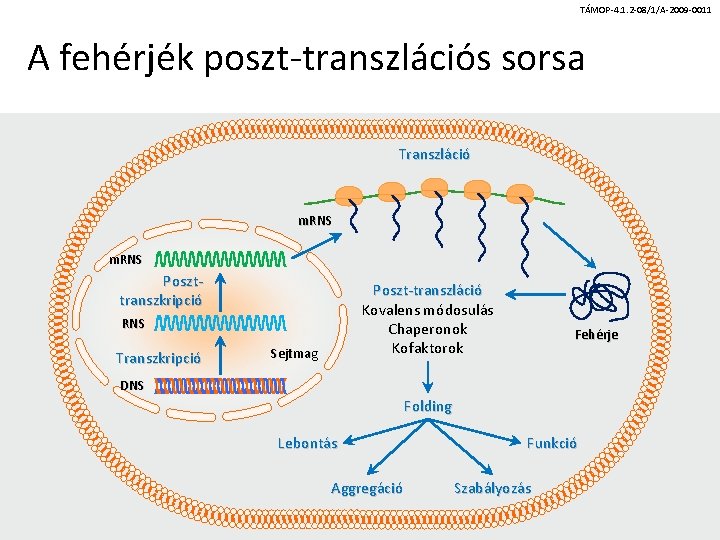
TÁMOP-4. 1. 2 -08/1/A-2009 -0011 A fehérjék poszt-transzlációs sorsa Transzláció m. RNS Poszttranszkripció Poszt-transzláció Kovalens módosulás Chaperonok Kofaktorok RNS Transzkripció Sejtmag Fehérje DNS Folding Lebontás Aggregáció Funkció Szabályozás
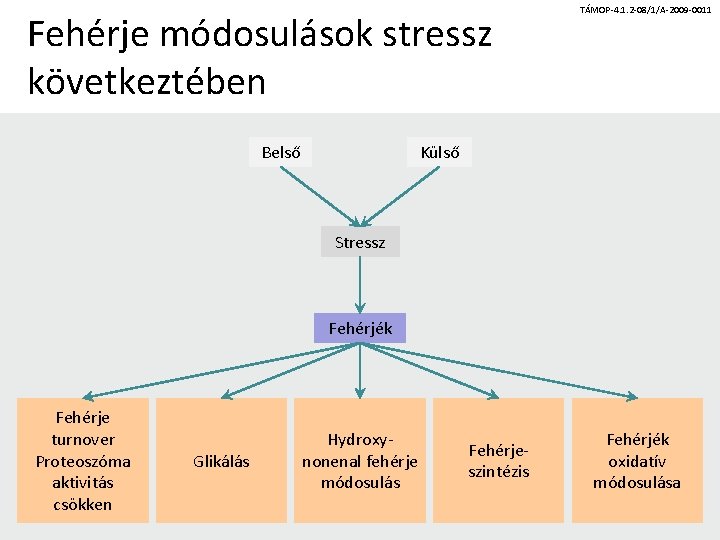
Fehérje módosulások stressz következtében Belső TÁMOP-4. 1. 2 -08/1/A-2009 -0011 Külső Stressz Fehérjék Fehérje turnover Proteoszóma aktivitás csökken Glikálás Hydroxynonenal fehérje módosulás Fehérjeszintézis Fehérjék oxidatív módosulása

TÁMOP-4. 1. 2 -08/1/A-2009 -0011 Lipofuscin, lizoszómális szemét • A lizoszómák nem képesek maradéktalanul megemészteni az elöregedett fehérjéket • Maradék: barnás-sárgás, autofluoreszcens, elektron-denz granulum: lipofuscin, ceroid, öregségi pigment • Megnövekedett oxidáció, különösen vas jelenlétében • A mitokondriumok a lipofuscin fő forrásai • A neuronok perikaryonjának akár 75%-t teheti ki • Amyloid képződés Alzheimer és Parkinson kórban
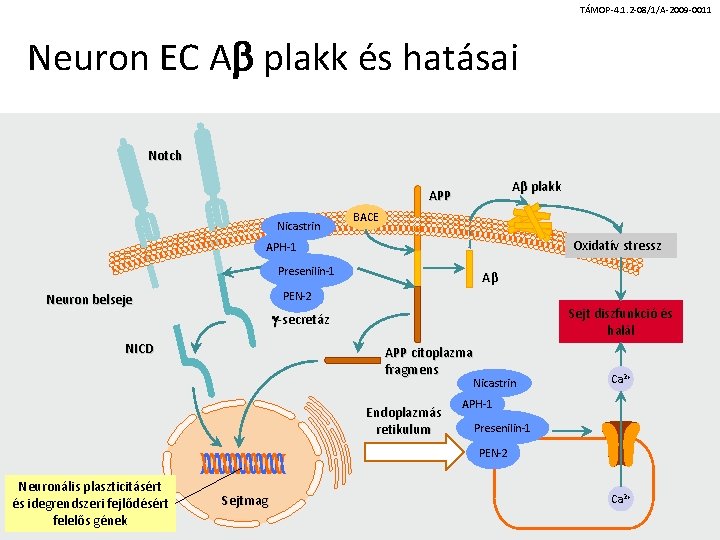
TÁMOP-4. 1. 2 -08/1/A-2009 -0011 Neuron EC Ab plakk és hatásai Notch Aβ plakk APP Nicastrin BACE Oxidatív stressz APH-1 Presenilin-1 Aβ PEN-2 Neuron belseje Sejt diszfunkció és halál -secretáz NICD APP citoplazma fragmens Nicastrin Endoplazmás retikulum Ca 2+ APH-1 Presenilin-1 PEN-2 Neuronális plaszticitásért és idegrendszeri fejlődésért felelős gének Sejtmag Ca 2+

Amyloid fibrillumok fejlődése és növekedése INKUBÁCIÓS FÁZIS Dimerizáció natív állapotban Natív monomer állapot TÁMOP-4. 1. 2 -08/1/A-2009 -0011 NÖVEKEDÉSI FÁZIS Natív dimer állapot Részleges denaturáció Amyloid-keltő aggregáció Kis amyloid-keltő oligomerek Protofibrillum csomózódás Fibrillum csomózódás Polimerizáció Misfold vagy globulus, amyloid-keltő? Amyloid magok Teljes denaturáció Denaturált állapotú monomerek Kolloid átalakulás/ folding Nem-specifikus aggregáció Strukturálatlan aggregátum Filamentum elongáció Amyloid magok Protofibrillum elongáció Érett Fibrillum elongáció
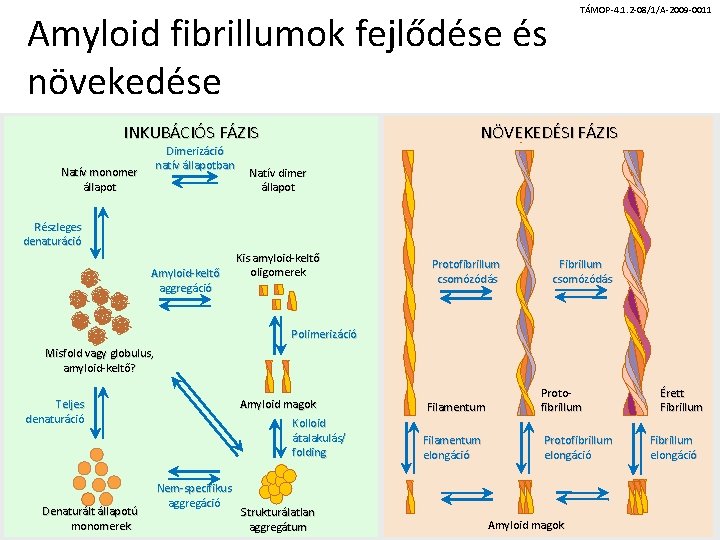
TÁMOP-4. 1. 2 -08/1/A-2009 -0011 Amyloid fibrillumok fejlődése és növekedése INKUBÁCIÓS FÁZIS Dimerizáció natív állapotban Natív monomer állapot NÖVEKEDÉSI FÁZIS Natív dimer állapot Részleges denaturáció Amyloid-keltő aggregáció Kis amyloid-keltő oligomerek Protofibrillum csomózódás Fibrillum csomózódás Polimerizáció Misfold vagy globulus, amyloid-keltő? Amyloid magok Teljes denaturáció Denaturált állapotú monomerek Kolloid átalakulás/ folding Nem-specifikus aggregáció Strukturálatlan aggregátum Filamentum elongáció Protofibrillum elongáció Amyloid magok Érett Fibrillum elongáció

TÁMOP-4. 1. 2 -08/1/A-2009 -0011 Nem-oxidatív DNS károsodás I. • Spontán változások • Depurináció és depirimidináció • Deamináció • Egyesláncú törések • Spontán metiláció • Glikáció • Keresztkötés

TÁMOP-4. 1. 2 -08/1/A-2009 -0011 Nem-oxidatív fehérje károsodás II. • Bioszintézis hibák • Transzkripciós hibák • Transzlációs hibák • Racemizáció és izomerizáció • Deamidálás (aszparagin és glutamin) • Reaktív karbonil-csoportok (nem-oxidatív) • Szerin defoszforiláció

Nem-oxidatív fehérje károsodás modulációja TÁMOP-4. 1. 2 -08/1/A-2009 -0011 • Fehérje turnover (magas turnover = öregedést ellensúlyozó hatás, hígulás) • Stressz fehérjék fokozott szintje, chaperonok, ubiquitin (hormesis, edzés) • Intramitokondriális proteolizis (Lon proteáz, miscoded és oxidált fehérjék, EGF↑)

TÁMOP-4. 1. 2 -08/1/A-2009 -0011 CR és nem-oxidatív fehérje károsodás CR→éhezés → hipoglikémia → csökkent EC és IC glikáció • Alacsonyabb inzulin szint, magasabb proteoszóma aktivitás • Magasabb NADPH arány, glutathion redukált formában tartása

TÁMOP-4. 1. 2 -08/1/A-2009 -0011 Transzkripciós és transzlációs szabályozás zavara öregedés során Transzkripciós változások, 15 -30%-al csökkent aktivitás t. RNS ás aminoaciláció m. RNS feldolgozás és stabilitás, teljes poly(A+) csökkenés Transzlációs módosulások, csökkenő fehérjeszintézis, de CR képes visszaállítani • A fehérjeszintézis hatékonysága és pontossága csökken • Iniciáció, elongáció és termináció hatékonysága csökken (EF 1 a-aktivitás csökken 35 -45%-al) • •
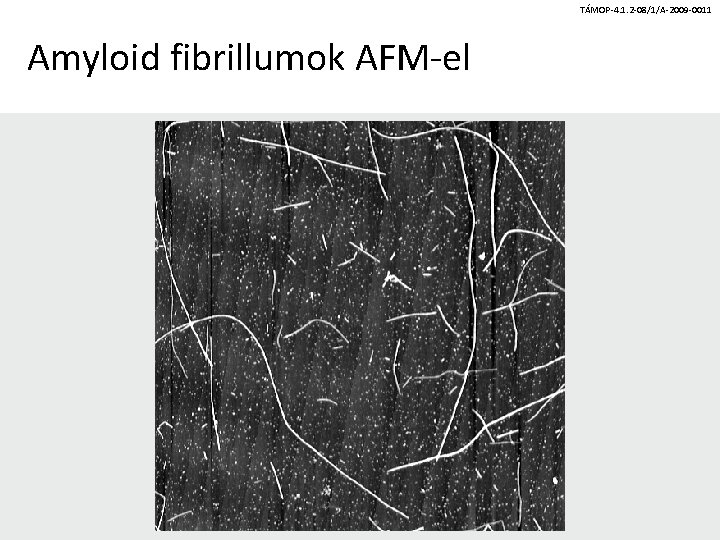
TÁMOP-4. 1. 2 -08/1/A-2009 -0011 Amyloid fibrillumok AFM-el
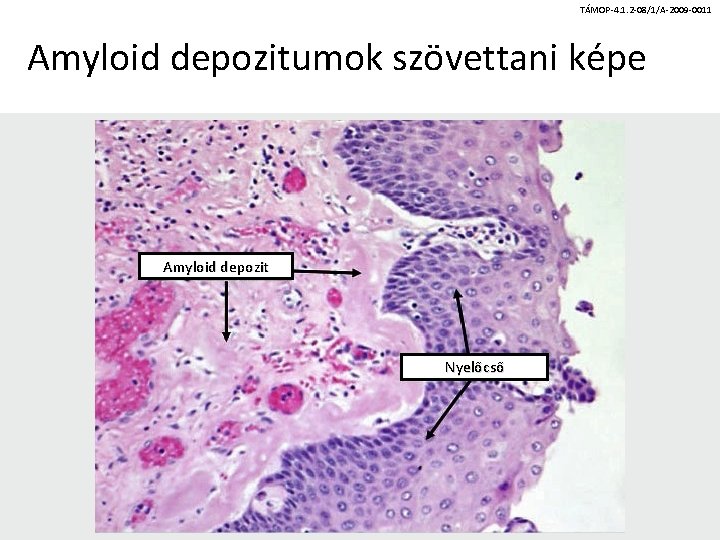
TÁMOP-4. 1. 2 -08/1/A-2009 -0011 Amyloid depozitumok szövettani képe Amyloid depozit Nyelőcső

TÁMOP-4. 1. 2 -08/1/A-2009 -0011 Proteoszóma funkciók • Fő nem-lizoszomális proteolitikus gépezet • Aktivitások: – Chimotripszin-szerű (CT-szerű) – Tripszin-szerű (T-szerű) – Peptidil-glutamil peptid hydroláz (PGPH) • Nem csak ‘housekeeping’ funkció: – Apoptosis – Sejtciklus – Sejt differenciáció

TÁMOP-4. 1. 2 -08/1/A-2009 -0011 Proteoszóma funkció öregedés során • Oxidált, ubiquitinált fehérjék lebontása • A proteoszóma funkció csökken idős korban • Makromolekulák fokozott módosulásai • Fokozott terhelés, csökkent hatékonyság, emiatt ideg- és és immunrendszeri öregedés

TÁMOP-4. 1. 2 -08/1/A-2009 -0011 Proteoszóma funkció és CR • Csökkent inzulin szint, fokozott proteoszóma aktivitás • CR visszaállítja a PGPH aktivitást (amely 50%-al csökkent öregedésben) • Fenntartja / stimulálja a proteoszóma subunit (Rpt 5) és aktivátor (PA 28 a subunit) expressziót • Egészséges százévesekben normális a proteoszóma aktivitás

TÁMOP-4. 1. 2 -08/1/A-2009 -0011 Proteoszóma funkció és immunológiai öregedés • Csökkent mértékű Ik. B lebontás, csökkent NF-k. B aktiváció, immunológiai hanyatlás • CT-szerű aktivitás csökkenése T-sejtekben • A 26 S subunit specifikus módosulása, központi az antigén feldolgozásban

TÁMOP-4. 1. 2 -08/1/A-2009 -0011 Proteoszóma funkció és idegrendszeri öregedés • CT-aktivitás csökken (kivéve cerebellum / agytörzs) • A proteoszóma hanyatlása sebezhetővé teszi a neuronokat • Sérült fehérjék felgyülemlése, aggregációja • Elszaporodó Lewis testek, huntingtin fragmensek • Aktív szerep Alzhemier és Parkinson-kórban • Lipofuscin felgyülemlése, küszöbérték jelenség
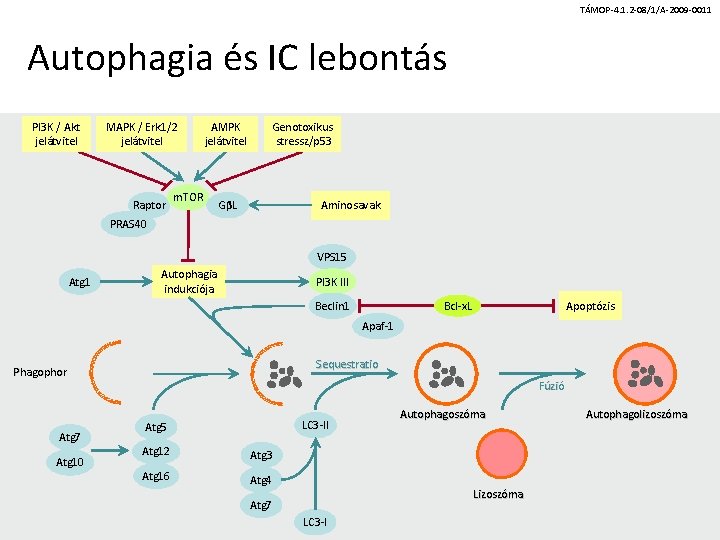
TÁMOP-4. 1. 2 -08/1/A-2009 -0011 Autophagia és IC lebontás PI 3 K / Akt jelátvitel MAPK / Erk 1/2 jelátvitel Raptor AMPK jelátvitel m. TOR Genotoxikus stressz/p 53 GβL Aminosavak PRAS 40 VPS 15 Atg 1 Autophagia indukciója PI 3 K III Apoptózis Bcl-x. L Beclin 1 Apaf-1 Sequestratio Phagophor Atg 7 Atg 10 Fúzió LC 3 -II Atg 5 Atg 12 Atg 3 Atg 16 Atg 4 Autophagoszóma Lizoszóma Atg 7 LC 3 -I Autophagolizoszóma

TÁMOP-4. 1. 2 -08/1/A-2009 -0011 Prion fehérje átalakulása átalakulás normál prion kóros prion
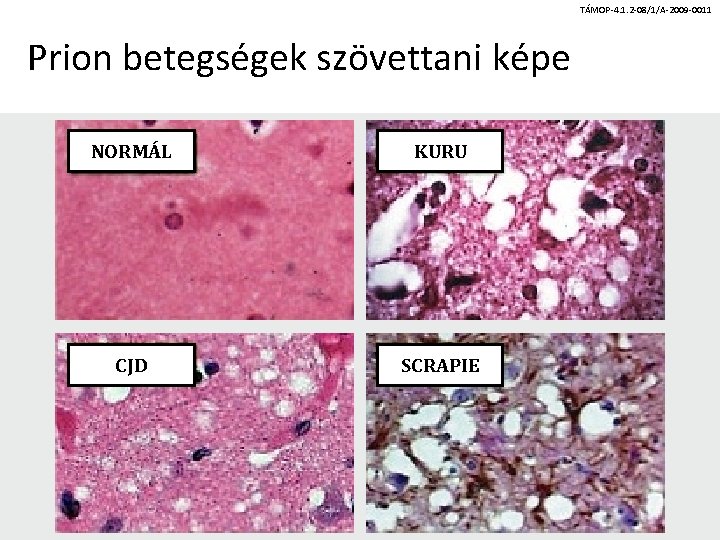
TÁMOP-4. 1. 2 -08/1/A-2009 -0011 Prion betegségek szövettani képe NORMÁL KURU CJD SCRAPIE

TÁMOP-4. 1. 2 -08/1/A-2009 -0011 Hutchinson-Guilford progéria • Lamin. A mutáció (sérülékeny mag-envelope) • Elsősorban a mesenchymális szöveteket érinti • HGPS sejtek stressz-tűrő képessége csökkent • Gyors progéria, korai halál

TÁMOP-4. 1. 2 -08/1/A-2009 -0011 Mag envelope összetétele Endoplazmatikus retikulum Magpórus komplexum mbrán Belső me Nurim C Emerin MAN-1 Citoplazma LAP-1 C LAP 2β C mbrán Külső me Lamin B LBR C N BAF N Lamin A/C N BAF N C HP 1 BAF N LAP 2α Kromatin BAF LEM domén N Magplazma C C Kromatin N
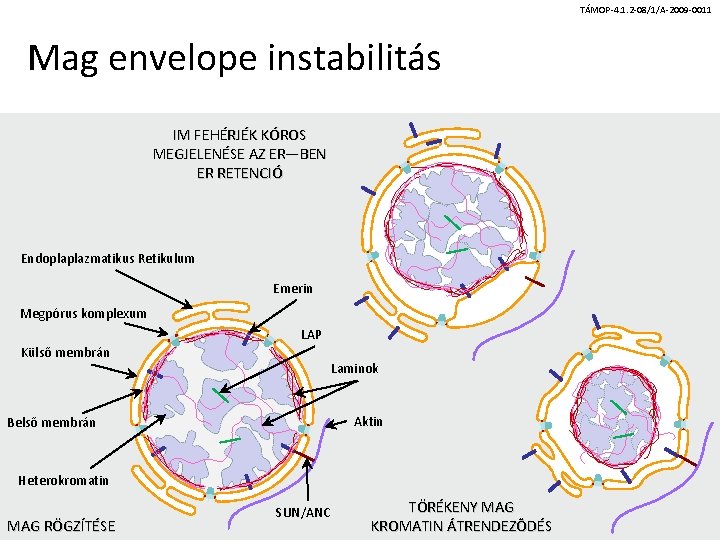
TÁMOP-4. 1. 2 -08/1/A-2009 -0011 Mag envelope instabilitás IM FEHÉRJÉK KÓROS MEGJELENÉSE AZ ER—BEN ER RETENCIÓ Endoplaplazmatikus Retikulum Emerin Megpórus komplexum LAP Külső membrán Laminok Aktin Belső membrán Heterokromatin MAG RÖGZÍTÉSE SUN/ANC TÖRÉKENY MAG KROMATIN ÁTRENDEZŐDÉS
- Slides: 26