Az immunizls s a vakcinci OK Buzs Edit

Az immunizálás és a vakcináció (ÁOK) Buzás Edit, Holub Marianna Fülöp A. K. (Szerk. ): Immunológiai szemináriumok, 6 -7. fejezet. 1

I. Immunizálás Immunválasz kiváltása egy adott szervezetben antigén bevitelével 2
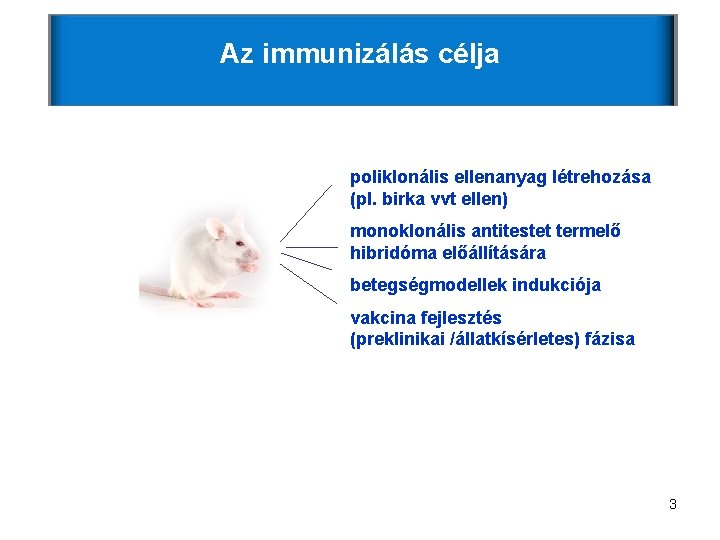
Az immunizálás célja poliklonális ellenanyag létrehozása (pl. birka vvt ellen) monoklonális antitestet termelő hibridóma előállítására betegségmodellek indukciója vakcina fejlesztés (preklinikai /állatkísérletes) fázisa 3
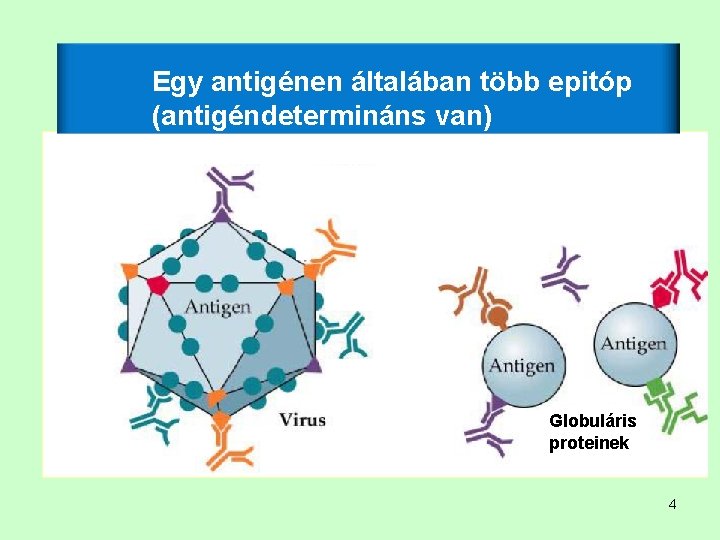
Egy antigénen általában több epitóp (antigéndetermináns van) Globuláris proteinek 4
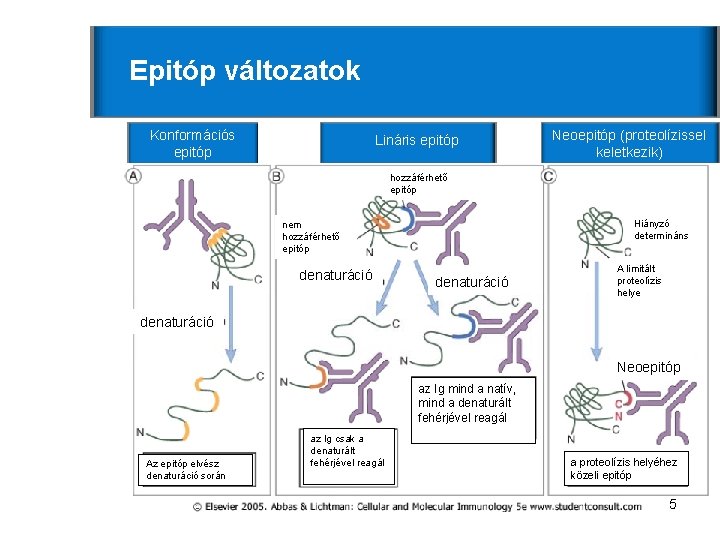
Epitóp változatok Konformációs epitóp Lináris epitóp Neoepitóp (proteolízissel keletkezik) hozzáférhető epitóp Hiányzó determináns nem hozzáférhető epitóp denaturáció A limitált proteolízis helye denaturáció Neoepitóp az Ig mind a natív, mind a denaturált fehérjével reagál Az epitóp elvész denaturáció során az Ig csak a denaturált fehérjével reagál a proteolízis helyéhez közeli epitóp 5
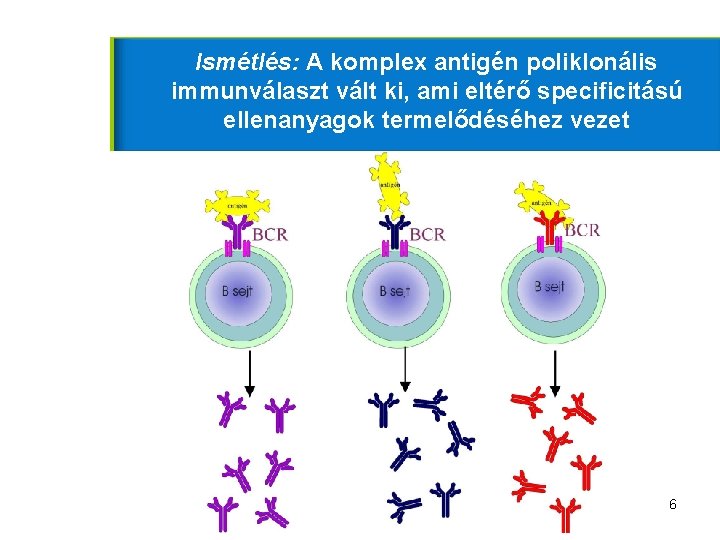
Ismétlés: A komplex antigén poliklonális immunválaszt vált ki, ami eltérő specificitású ellenanyagok termelődéséhez vezet 6
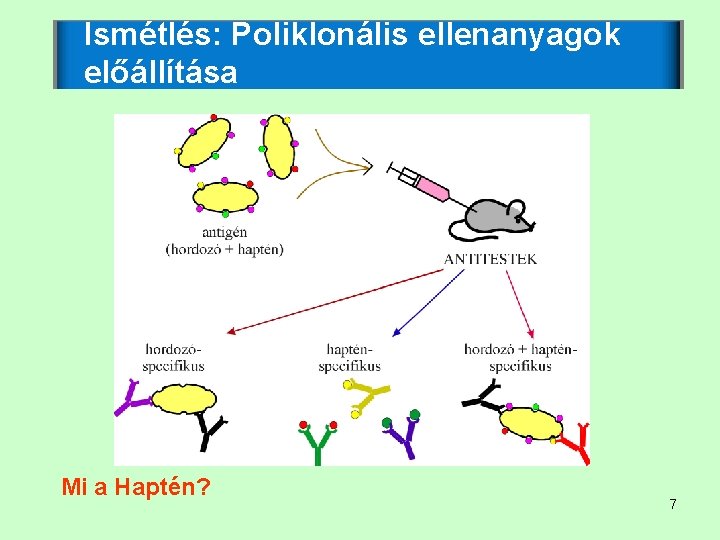
Ismétlés: Poliklonális ellenanyagok előállítása Mi a Haptén? 7

Immunizálás hibridóma + 8
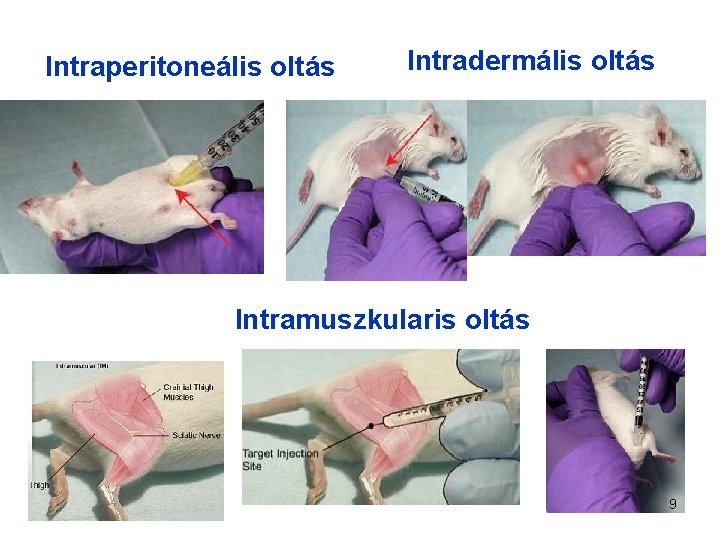
Intraperitoneális oltás Intradermális oltás Intramuszkularis oltás 9

Mi történik, ha a testidegen fehérjét intravénásan adjuk be immunizálás céljából? • Az antigén kihígul az érpályában • Enzimatikusan lebomlik egy idő után • Ha sejtek fel is veszik endocitózissal és processzálás után prezentálódik is MHC-vel kostimuláció nélkül anergia • nagyon kicsi a valószínűsége, hogy találkozik olyan recirkuláló T vagy B sejttel, melynek receptora specifikus az adott antigénre 10

Mi történik, ha szubkután oltunk szolubilis antigént? • az antigén szétdiffundál a bőr alatti kötőszövetben • enzimatikusan lebomlik egy idő után • a szöveti sejtek felvehetik és akár prezentálhatják is MHC-vel kostimuláció nélkül: anergia • nagyon kicsi a valószínűsége, hogy találkozik olyan recirkuláló T vagy B sejttel, melynek receptora specifikus az adott antigénre 11

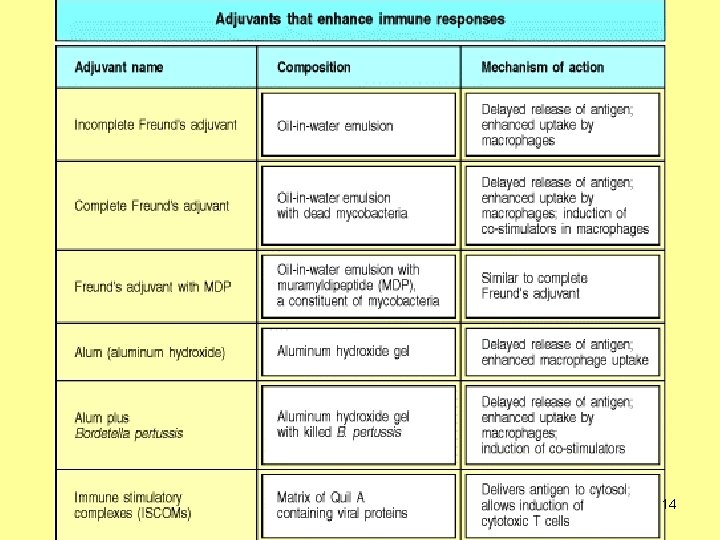
Mi lehet a megoldás? Mit célszerű együtt oltani az antigénnel annak érdekében, hogy legyen kostimuláció? Az antigénnel együtt danger signált (pl. PAMP-ot) tartalmazó adjuvánst is oltunk. Adjuváns (hatásfokozó szer): mely elősegíti egy adott antigénnel szembeni immunválasz kialakulását kostimulációs hatást biztosítva. Az adjuvánsok valamely danger receptoron (pathogen recognition receptor, PRR) keresztül hatnak 12
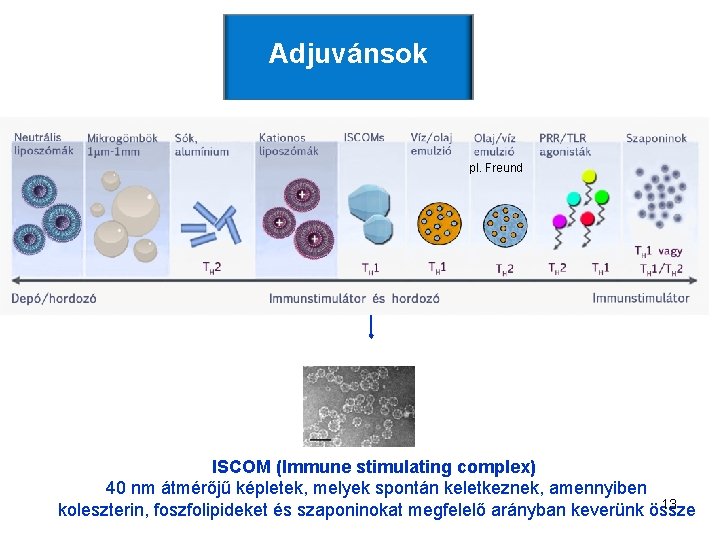
Adjuvánsok pl. Freund ISCOM (Immune stimulating complex) 40 nm átmérőjű képletek, melyek spontán keletkeznek, amennyiben 13 koleszterin, foszfolipideket és szaponinokat megfelelő arányban keverünk össze
14

Mi tehetünk annak érdekében, hogy növeljük a specifikus receptorral rendelkező limfocitával való találkozás esélyét Az antigén lassú felszabadulását eredményező adjuváns alkalmazása (pl. stabil emulzió) Szubkután oltás: antigén + adjuváns 9 nap múlva regionális nyirokcsomókban sok antigénspecifikus T sejt 15
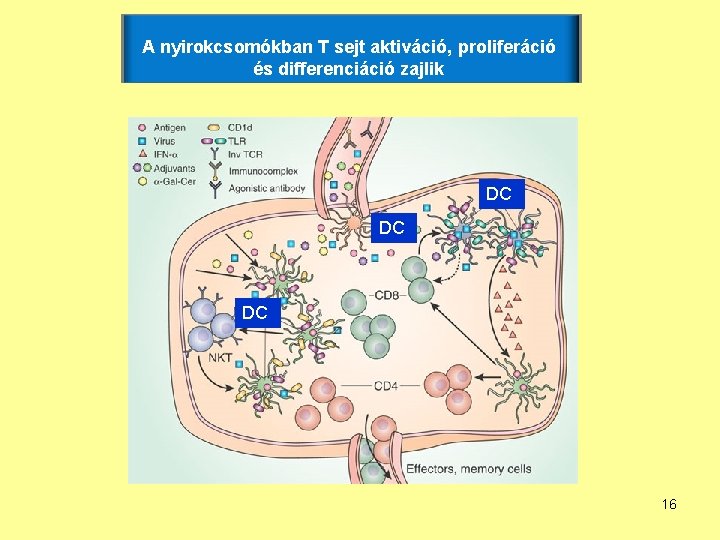
A nyirokcsomókban T sejt aktiváció, proliferáció és differenciáció zajlik DC DC DC 16
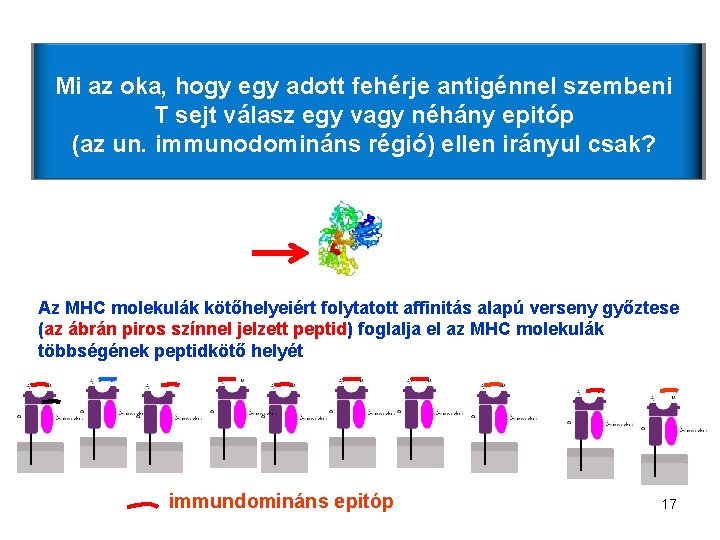
Mi az oka, hogy egy adott fehérje antigénnel szembeni T sejt válasz egy vagy néhány epitóp (az un. immunodomináns régió) ellen irányul csak? Az MHC molekulák kötőhelyeiért folytatott affinitás alapú verseny győztese (az ábrán piros színnel jelzett peptid) foglalja el az MHC molekulák többségének peptidkötő helyét immundomináns epitóp 17
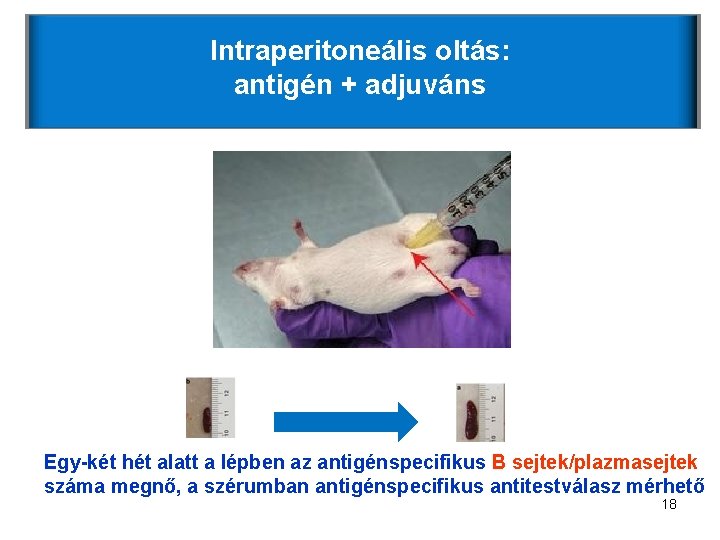
Intraperitoneális oltás: antigén + adjuváns Egy-két hét alatt a lépben az antigénspecifikus B sejtek/plazmasejtek száma megnő, a szérumban antigénspecifikus antitestválasz mérhető 18

Immune Epitope Database • http: //www. immuneepitope. org/ 19
20
Kialakul-e immunválasz, ha a testidegen fehérjét per os visszük be (pl. gyomorszonda segítségével)? Per os Általában orális tolerancia alakul ki a per os bejutó antigénekkel szemben (toleráljuk a táplálékfehérjéket illetőleg az normál bélflóra fehérjéit) 21
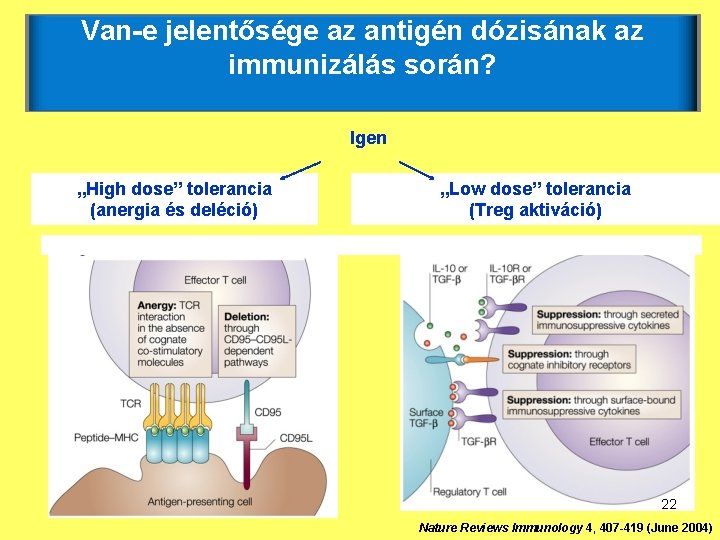
Van-e jelentősége az antigén dózisának az immunizálás során? Igen „High dose” tolerancia (anergia és deléció) „Low dose” tolerancia (Treg aktiváció) 22 Nature Reviews Immunology 4, 407 -419 (June 2004)

Van-e jelentősége az antigén dózisának az immunizálás során? Az immunizálás tanulságai az emberi vakcinák előállításának alapját képezik 23

II. VAKCINÁCIÓ Immunstimuláció -tumorsejtek elleni válasz elősegítése -kórokozók elleni válasz elősegítése 24

IMMUNSTIMULÁCIÓ CÉLJA terápia: hagyományos gyógyszeres (antibiotikumok, vírus anyagcsere gátlók) passzív immunizálás (ellenanyagok, sejtek) PREVENCIÓ: gyógyszer aktív vakcinálás: - a specifikus felismerő készlet arányának növelése - specifikus immunológiai memória létrehozása 25

ANTIGÉNEK T-dependens antigének: ált. fehérjék T-Independens antigének: ált. poliszacharidok T-B kooperáció Csak B-sejt aktiválódik Nagy affinitású antitestek, memória Rövid távú memória EPITÓPOK Epitóp Protektív epitóp Amit a TCR/BCR felismer Nagyon specifikus, az adott patogénre egyedi molekuláris felszín Neutralizáló antitest: gátolja a patogén elterjedését 26
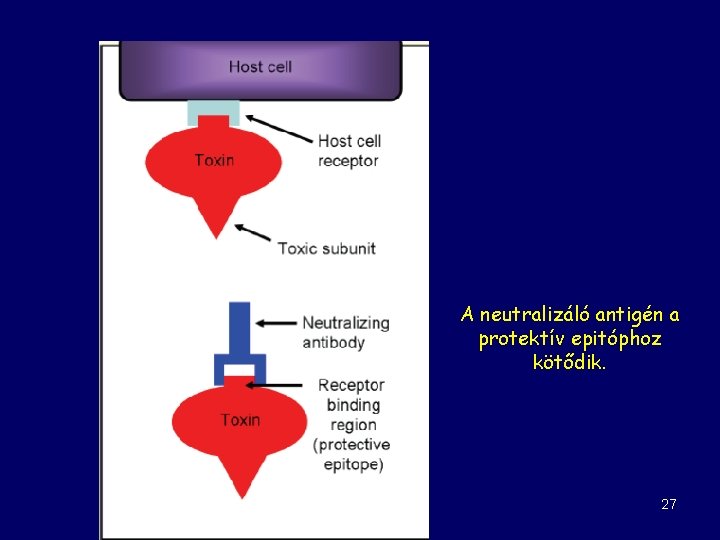
A neutralizáló antigén a protektív epitóphoz kötődik. 27
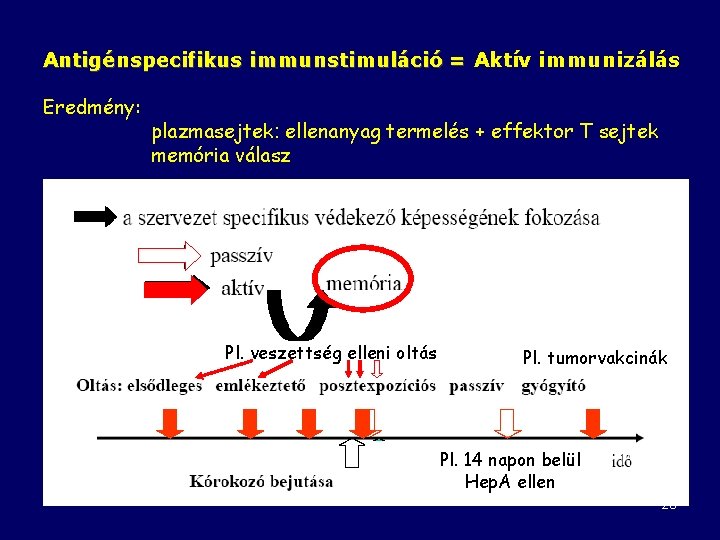
Antigénspecifikus immunstimuláció = Aktív immunizálás Eredmény: plazmasejtek: ellenanyag termelés + effektor T sejtek memória válasz Pl. veszettség elleni oltás Pl. tumorvakcinák Pl. 14 napon belül Hep. A ellen 28

AKTÍV VAKCINÁCIÓ -Legyengített, elölt teljes kórokozó, vagy kórokozó alegység -Antitestek, T-sejtek és memóriasejtek kialakulása : ADAPTÍV Immunválasz -7 -14 nap látencia -Fertőzéskor memóriasejtek aktiválódása, differenciálódása effektorsejtté PASSZÍV VAKCINÁCIÓ • Antitest • Nincs adaptív immunválasz: nem alakul ki antitest, T-sejt repertoir • Azonnali hatás: neutralizáció/ opszonizáció/ komplement aktiválás: (TERMÉSZETES IMMUNVÁLASZ) • Nincs memória 29

A hatékony aktív oltóanyag tulajdonságai biztonságos protektív Hosszú távú védelem Nem okozhat betegséget v. halált Élő kórokozó által előidézett betegséggel szemben véd Évekig tartó védettséget ad Serkenti a neutralizáló antitesteket Bizonyos kórokozók (pl. poliovírus) olyan sejteket fertőznek (pl. neuronok), amelyek nem pótolhatók. Neutralizáló antitest megelőzi ezeknek a sejteknek a megfertőződését Serkenti a protektív Tsejteket Bizonyos kórokozók (pl. intracellulárisok) sejt-mediálta immunválasszal hatékonyabban eliminálódnak Gyakorlati szempontok Biológiai stabilitás, könnyű bevitel, kevés mellékhatás, olcsó 30 előállítás
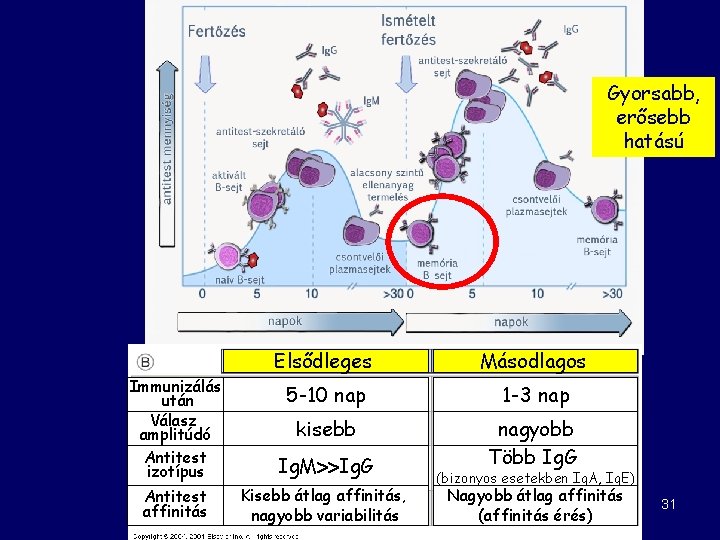
Gyorsabb, erősebb hatású Elsődleges Másodlagos 5 -10 nap 1 -3 nap kisebb nagyobb Több Ig. G Immunizálás után Válasz amplitúdó Antitest izotípus Ig. M Ig. G Antitest affinitás Kisebb átlag affinitás, nagyobb variabilitás (bizonyos esetekben Ig. A, Ig. E) Nagyobb átlag affinitás (affinitás érés) 31

A hatékony oltóanyag tulajdonságai biztonságos Nem okozhat betegséget v. halált protektív Élő kórokozó által előidézett betegséggel szemben véd Hosszú távú védelem Évekig tartó védettséget ad Serkenti a neutralizáló antitesteket Bizonyos kórokozók (pl. poliovírus) olyan sejteket fertőz (pl. neuronok), amelyek nem pótolhatók. Neutralizáló antitest megelőzi ezeknek a sejteknek a megfertőződését Serkenti a protektív Tsejteket Bizonyos kórokozók (pl. intracellulárisok) sejt-mediálta immunválasszal hatékonyabban eliminálódnak Gyakorlati szempontok Biológiai stabilitás, könnyű bevitel, kevés mellékhatás, olcsó 32 előállítás
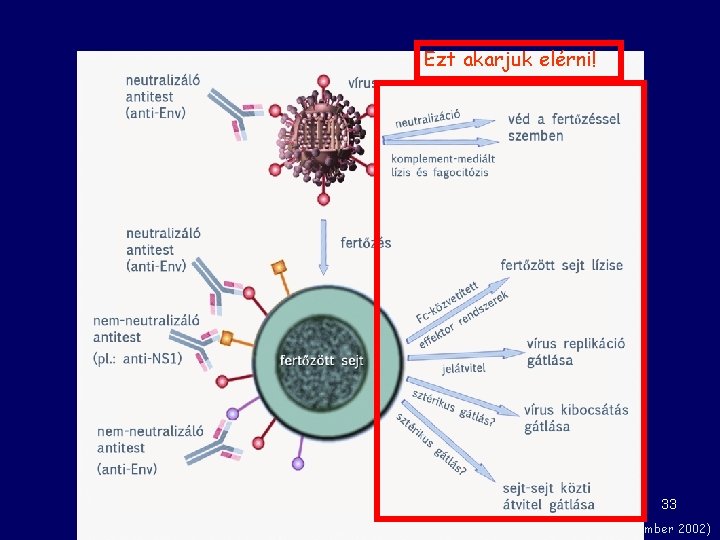
Ezt akarjuk elérni! 33 Nature Reviews Immunology 2, 706 -713 (September 2002)

A hatékony oltóanyag tulajdonságai biztonságos Nem okozhat betegséget v. halált protektív Élő kórokozó által előidézett betegséggel szemben véd Hosszú távú védelem Évekig tartó védettséget ad Serkenti a neutralizáló antitesteket Bizonyos kórokozók (pl. poliovírus) olyan sejteket fertőz (pl. neuronok), amelyek nem pótolhatók. Neutralizáló antitest megelőzi ezeknek a sejteknek a megfertőződését Serkenti a protektív Tsejteket Bizonyos kórokozók (pl. intracellulárisok) sejt-mediálta immunválasszal hatékonyabban eliminálódnak Gyakorlati szempontok Biológiai stabilitás, könnyű bevitel, kevés mellékhatás, olcsó 34 előállítás
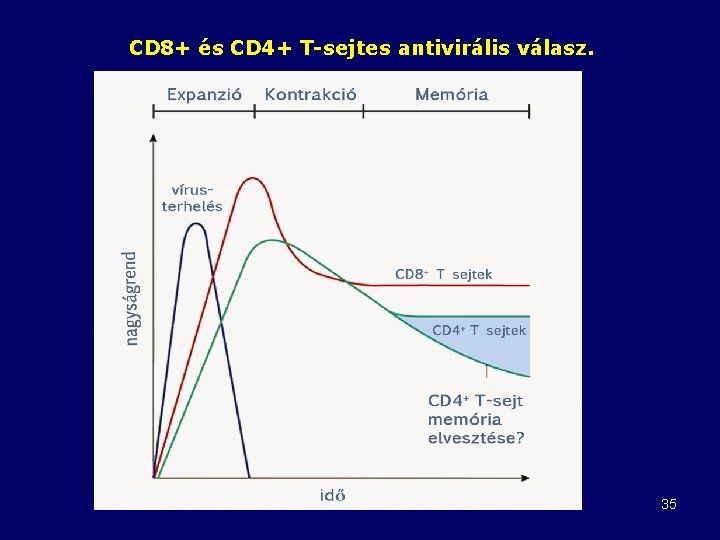
CD 8+ és CD 4+ T-sejtes antivirális válasz. 35
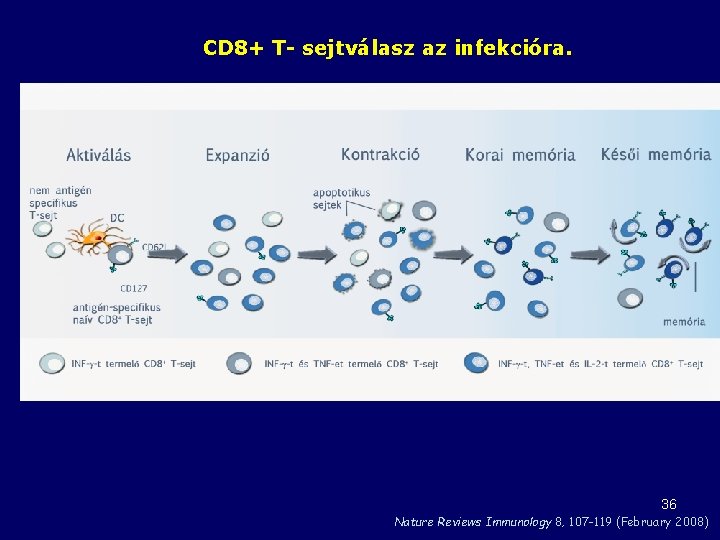
CD 8+ T- sejtválasz az infekcióra. 36 Nature Reviews Immunology 8, 107 -119 (February 2008)
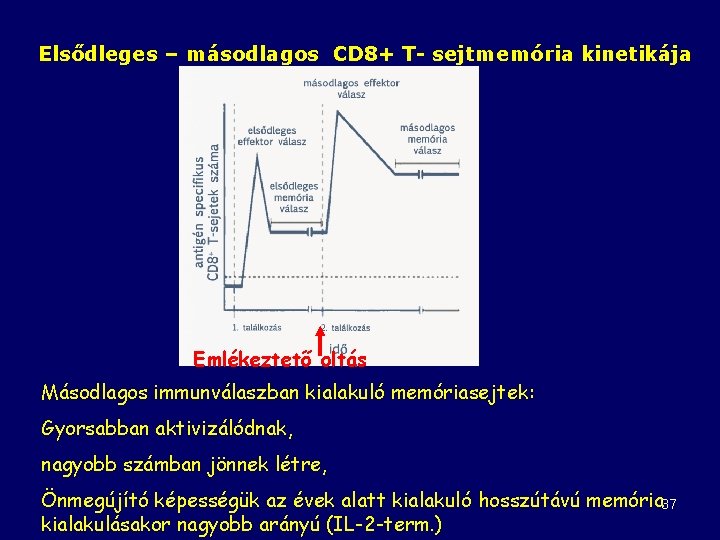
Elsődleges – másodlagos CD 8+ T- sejtmemória kinetikája Emlékeztető oltás Másodlagos immunválaszban kialakuló memóriasejtek: Gyorsabban aktivizálódnak, nagyobb számban jönnek létre, Önmegújító képességük az évek alatt kialakuló hosszútávú memória 37 kialakulásakor nagyobb arányú (IL-2 -term. )

Az oltási naptárban az egy oltásra vonatkozó megadott intervallumokat minimumként kell felfogni, amelyek nem csökkenthetők, de meghosszabbításuk általában nem zavarja a kellő immunválasz kialakulását. 38

Bejutattatás módja Injekció Intradermálisan, szubkután, intramuszkulárisan Mucosan át: orális, nazális 39

Mucosális vakcináció értelme: Ugyanarra az antigénre adott immunválasz függ a mikrokörnyezettől Subcután, intramusculárisan: Orálisan, nasálisan: nyirokcsomó immunválasz Mucosa immunválasz Luminális barrierek mentén: Nem processzált antigének pl. transzcitózis M-sejtekkel a barriereket penetráló antigéneket kiszűri DC termelte IL-12 hatására Th 1: IFN-gamma and IL-2 Ig. G: komplement aktiválás TGF beta-1 hatására Treg + Th 2, Ig. A: Virulencia faktorok, adhézió blokkolása, neutralizálás Szövet specifikusan migráló memóriasejtek A vérrel/ szövetnedvekkel terjedő mikroorganizmusok ellen véd: pl. Hep. B Luminális barrierek mentén terjedő mikroorganizmusok ellen véd: pl. polio vírus 40
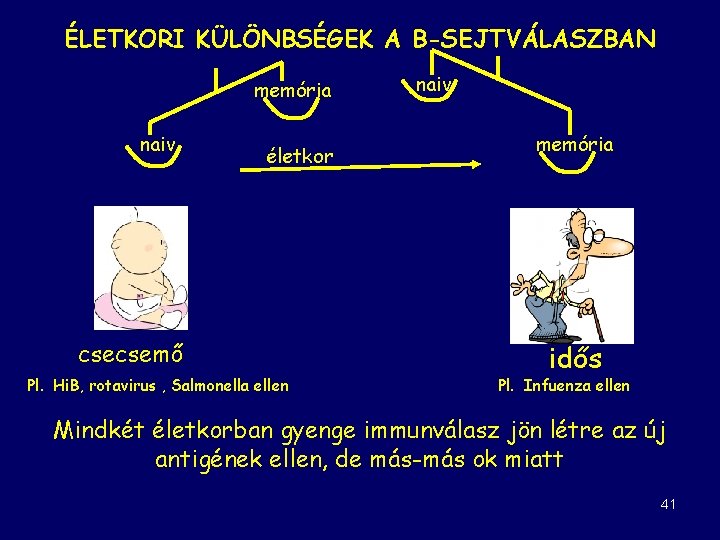
ÉLETKORI KÜLÖNBSÉGEK A B-SEJTVÁLASZBAN memória naiv életkor csecsemő Pl. Hi. B, rotavirus , Salmonella ellen naiv memória idős Pl. Infuenza ellen Mindkét életkorban gyenge immunválasz jön létre az új antigének ellen, de más-más ok miatt 41
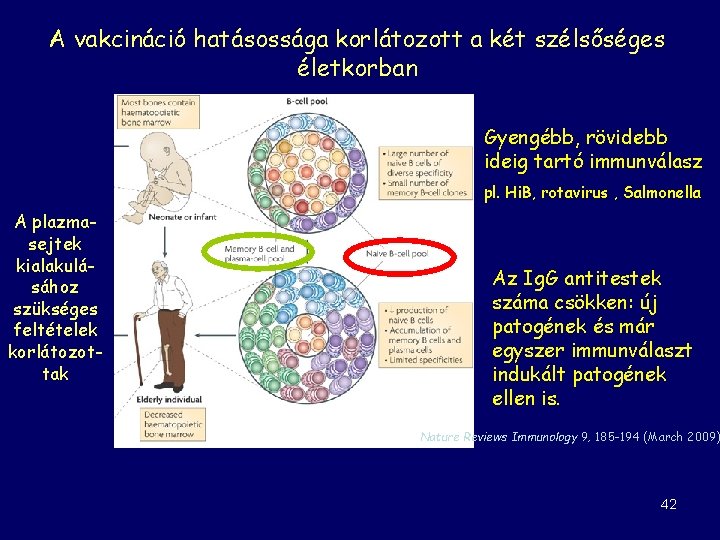
A vakcináció hatásossága korlátozott a két szélsőséges életkorban Gyengébb, rövidebb ideig tartó immunválasz pl. Hi. B, rotavirus , Salmonella A plazmasejtek kialakulásához szükséges feltételek korlátozottak Az Ig. G antitestek száma csökken: új patogének és már egyszer immunválaszt indukált patogének ellen is. Nature Reviews Immunology 9, 185 -194 (March 2009) 42
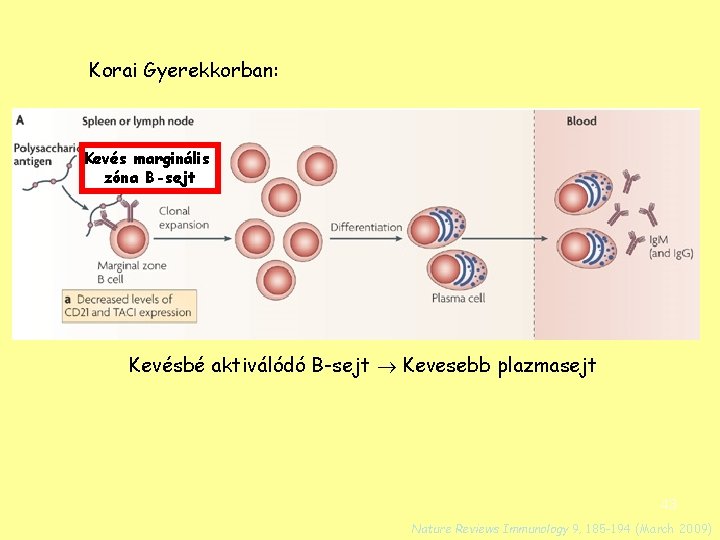
Korai Gyerekkorban: Kevés marginális zóna B-sejt Kevésbé aktiválódó B-sejt Kevesebb plazmasejt 43 Nature Reviews Immunology 9, 185 -194 (March 2009)
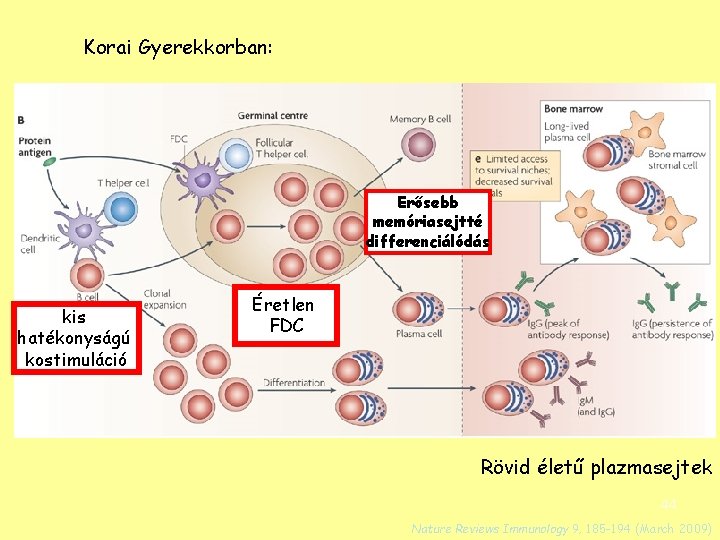
Korai Gyerekkorban: Erősebb memóriasejtté differenciálódás kis hatékonyságú kostimuláció Éretlen FDC Rövid életű plazmasejtek 44 Nature Reviews Immunology 9, 185 -194 (March 2009)

Oltási stratégiák csecsemők és idősek esetén Adjuvánsok optimalizálása A naiv B-sejt aktiváció serkentése: pl. Hib A naív B-sejtek másodlagos nyirokszervekbe vándorlásának serkentése depo vakcinákkal : pl. Fluval-P (H 1 N 1) Antigéndózis emelése A B-sejt aktiváció növelése, több germinális centrum kialakulásának elősegítése: pl. Fluval-P Többszöri oltás és többszöri emlékeztető oltás A naiv B-sejtek másodlagos nyirokszervekbe vándorlásának serkentése ; A memóriasejtek kialakulásának és fennmaradásának elősegítése: pl. Fluval-P 45

46

A vakcinák típusai Egész (teljes) vakcinák: • élő, attenuált • Inaktivált • élő, rekombináns Alegység vakcina: • protein • szintetikus peptid • DNS (RNS) 47
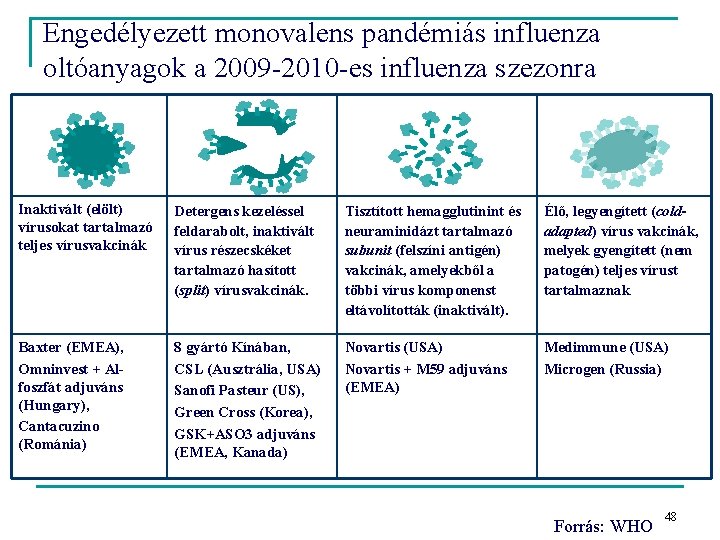
Engedélyezett monovalens pandémiás influenza oltóanyagok a 2009 -2010 -es influenza szezonra Inaktivált (elölt) vírusokat tartalmazó teljes vírusvakcinák Detergens kezeléssel feldarabolt, inaktivált vírus részecskéket tartalmazó hasított (split) vírusvakcinák. Tisztított hemagglutinint és neuraminidázt tartalmazó subunit (felszíni antigén) vakcinák, amelyekből a többi vírus komponenst eltávolították (inaktivált). Élő, legyengített (coldadapted) vírus vakcinák, melyek gyengített (nem patogén) teljes vírust tartalmaznak Baxter (EMEA), Omninvest + Alfoszfát adjuváns (Hungary), Cantacuzino (Románia) 8 gyártó Kínában, CSL (Ausztrália, USA) Sanofi Pasteur (US), Green Cross (Korea), GSK+ASO 3 adjuváns (EMEA, Kanada) Novartis (USA) Novartis + M 59 adjuváns (EMEA) Medimmune (USA) Microgen (Russia) Forrás: WHO 48

VAKCINAFEJLESZTÉS IRÁNYAI Jelenlegi vakcinák tökéletesítése Új vakcinák fejlesztése Empirikus módszerek biotechnológiai vakcinafejlesztés 49

Pl. alegység konjugátum vakcina esetén: Pl. Haemophilus influenzae B: T sejt-független (TI) B sejt válasz (poliszaharid a baktérium felszínén) diftéria toxoid protein + poliszaharid konjugátum Diftéria toxoidra specifikus T sejtek citokineket termelnek – hatékony T sejtektől függő (TD) B sejt válasz 2 éves kor alatt is a bakteriális poliszaharid ellen Mi a toxoid? 50

VAKCINAFEJLESZTÉS IRÁNYAI Jelenlegi vakcinák tökéletesítése Empirikus módszerek biotechnológiai vakcinafejlesztés Új vakcinák fejlesztése 51
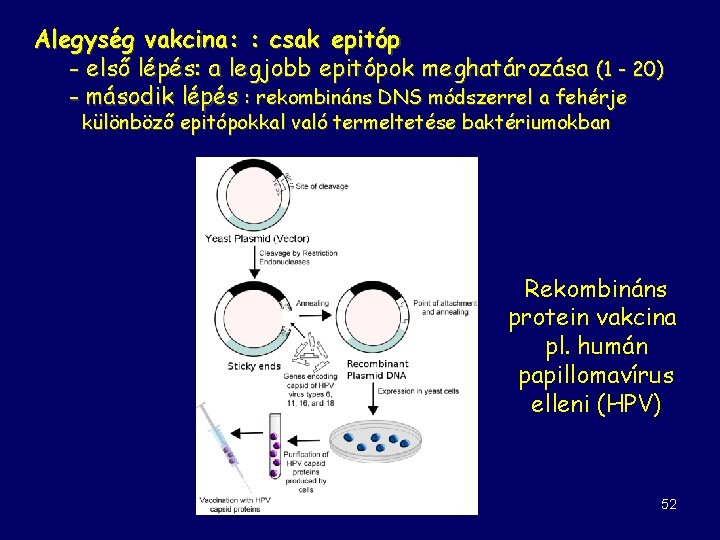
Alegység vakcina: : csak epitóp - első lépés: a legjobb epitópok meghatározása (1 - 20) - második lépés : rekombináns DNS módszerrel a fehérje különböző epitópokkal való termeltetése baktériumokban Rekombináns protein vakcina pl. humán papillomavírus elleni (HPV) 52

A patogén mikroorganizmus jellemző részletét expresszáltatják legtöbbször élesztőkben, ilyen például a Hepatitis B elleni vakcina növényekben történő expresszióval akár szájon át adható, „ehető vakcinát” is elő lehet előállítani 53

VAKCINAFEJLESZTÉS IRÁNYAI Jelenlegi vakcinák tökéletesítése Empirikus módszerek biotechnológiai vakcinafejlesztés Új vakcinák fejlesztése 54

Az új generációs vakcinák fejlesztésénél célzott fokozott immunogenitás alapja a megfelelő epitóp kiválasztása CÉL: Az „epitóp enhancement”: a peptid- MHC kötődés affinitásának növelése, Az MHCII-hoz horgonyzó aminosavak javítása, 55
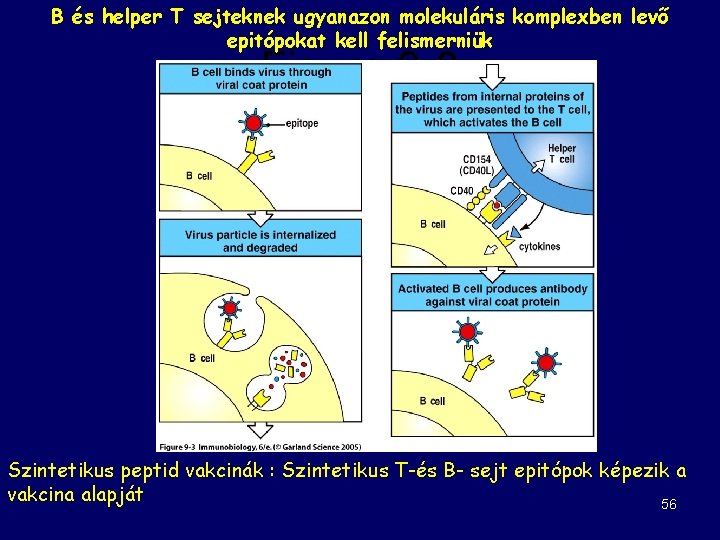
B és helper T sejteknek ugyanazon molekuláris komplexben levő epitópokat kell felismerniük Figure 9 -3 Szintetikus peptid vakcinák : Szintetikus T-és B- sejt epitópok képezik a vakcina alapját 56

A vakcinák előállítása Hagyományos stratégia: • Laboratóriumban szaporítják, majd egyenként izolálják azokat az antigén komponenseket, melyek a vakcina fejlesztés alapjául szolgálnak • Gyakran szükség van az antigén klónozására „Reverz vakcinológia”in silico vakcinológia • A patogén ismertté vált genomjából indul ki • A genomiális szekvencia bioinformatikai elemzése után kerül sor a kiválasztott szekvencia megklónozására és expresszáltatására • Immunogenitási tesztek követik 57
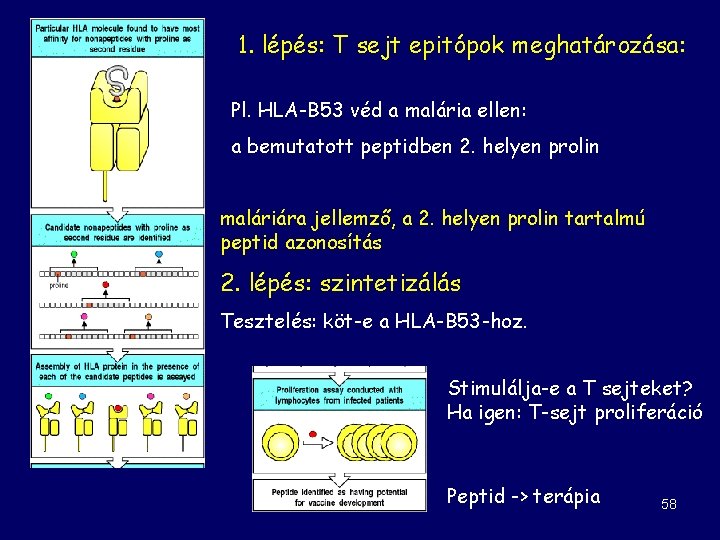
1. lépés: T sejt epitópok meghatározása: Pl. HLA-B 53 véd a malária ellen: a bemutatott peptidben 2. helyen prolin maláriára jellemző, a 2. helyen prolin tartalmú peptid azonosítás 2. lépés: szintetizálás Tesztelés: köt-e a HLA-B 53 -hoz. Stimulálja-e a T sejteket? Ha igen: T-sejt proliferáció Peptid -> terápia 58
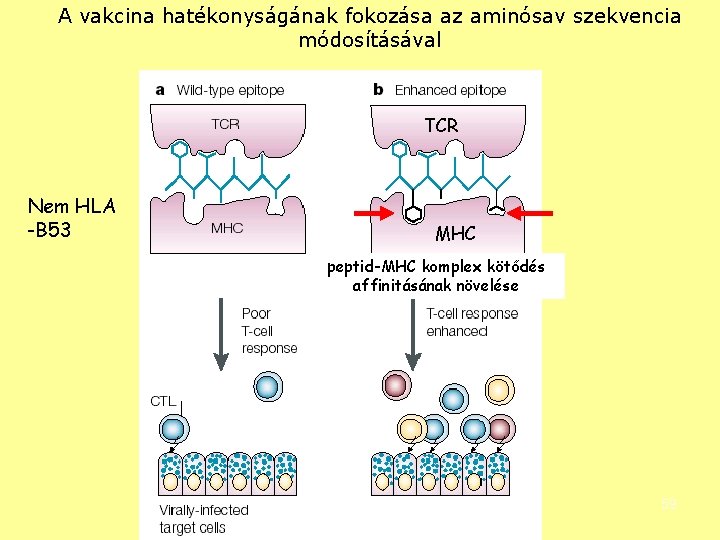
A vakcina hatékonyságának fokozása az aminósav szekvencia módosításával TCR Nem HLA -B 53 MHC peptid-MHC komplex kötődés affinitásának növelése 59
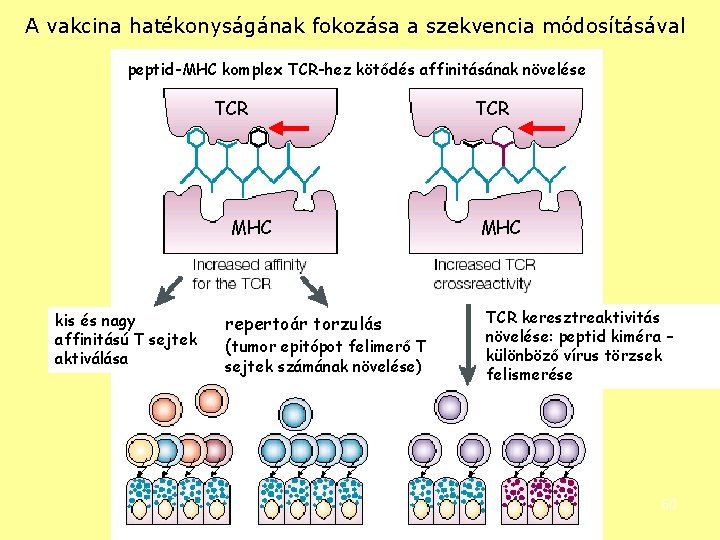
A vakcina hatékonyságának fokozása a szekvencia módosításával peptid-MHC komplex TCR-hez kötődés affinitásának növelése TCR MHC kis és nagy affinitású T sejtek aktiválása repertoár torzulás (tumor epitópot felimerő T sejtek számának növelése) TCR MHC TCR keresztreaktivitás növelése: peptid kiméra – különböző vírus törzsek felismerése 60

Az új generációs vakcinák fejlesztésénél célzott fokozott immunogenitás alapja a megfelelő epitóp és a megfelelő adjuváns kiválasztása 61
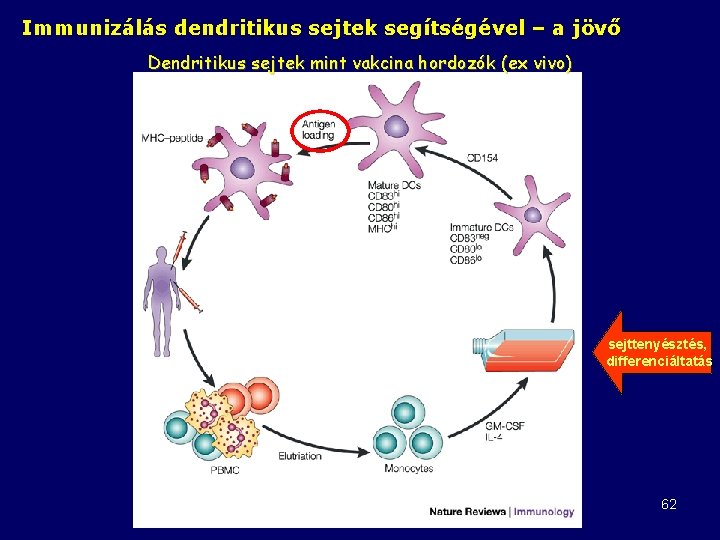
Immunizálás dendritikus sejtek segítségével – a jövő Dendritikus sejtek mint vakcina hordozók (ex vivo) sejttenyésztés, differenciáltatás 62
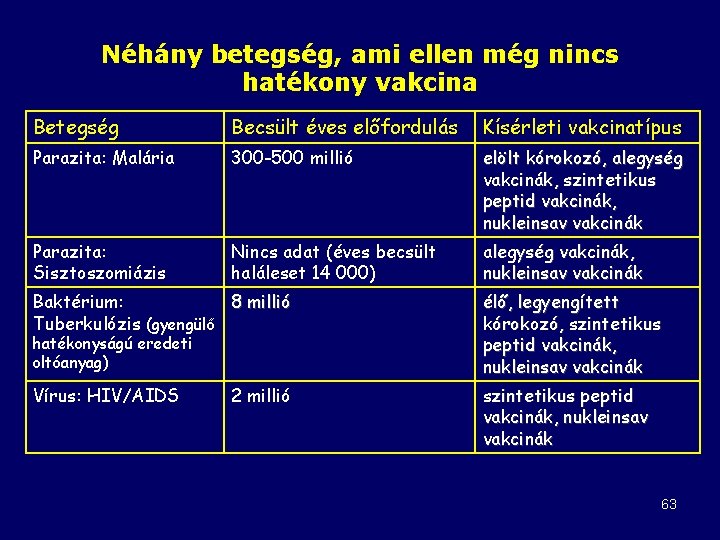
Néhány betegség, ami ellen még nincs hatékony vakcina Betegség Becsült éves előfordulás Kísérleti vakcinatípus Parazita: Malária 300 -500 millió elölt kórokozó, alegység vakcinák, szintetikus peptid vakcinák, nukleinsav vakcinák Parazita: Sisztoszomiázis Nincs adat (éves becsült haláleset 14 000) alegység vakcinák, nukleinsav vakcinák Baktérium: 8 millió Tuberkulózis (gyengülő élő, legyengített kórokozó, szintetikus peptid vakcinák, nukleinsav vakcinák Vírus: HIV/AIDS szintetikus peptid vakcinák, nukleinsav vakcinák hatékonyságú eredeti oltóanyag) 2 millió 63
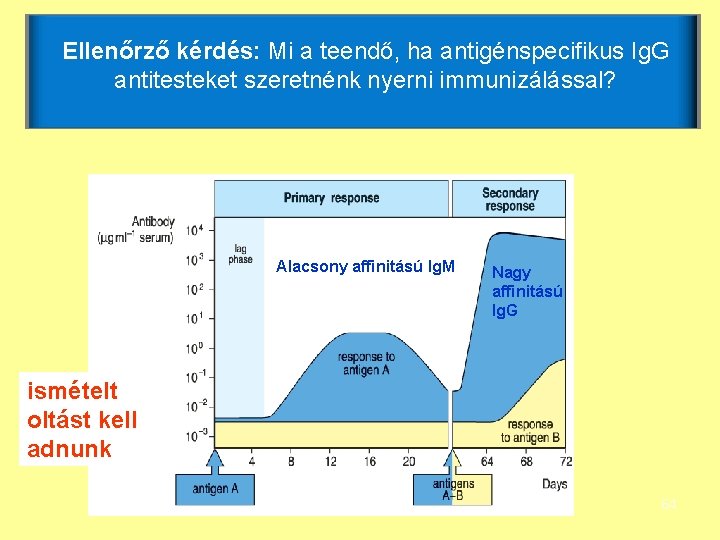
Ellenőrző kérdés: Mi a teendő, ha antigénspecifikus Ig. G antitesteket szeretnénk nyerni immunizálással? Alacsony affinitású Ig. M Nagy affinitású Ig. G ismételt oltást kell adnunk 64
- Slides: 64