AVVERTENZA Il presente materiale didattico viene fornito allo

















- Slides: 29

AVVERTENZA Il presente materiale didattico viene fornito allo scopo di facilitare la comprensione degli argomenti trattati e costituire il raccordo tra lezioni e studio individuale NON E’ PERTANO DA INTENDERSI COME SOSTITUTIVO DEL LIBRO DI TESTO Inoltre, nonostante la massima scrupolosità nella preparazione, è pur sempre possibile che siano presenti inaccuratezze e imprecisioni. E’ quindi necessario il costante controllo con i testi di riferimento Si invita a non diffondere, fotocopiare o utilizzare tale materiale per scopi diversi dalla preparazione individuale dell’esame Dr Monica MONTAGNANI – Cd. L Medicina e Chirurgia Esame Farmacologia – V Anno/II Semestre - Canale LZ

ANTICORPI MONOCLONALI ( bersaglio molecolare) Rituximab Trastuzumab Alemtuzumab Cetuximab Bevacizumab ( CD 20) ( HER 2) ( CD 52) ( EGFR) ( VEGF) INIBITORI TRASDUZIONE DEL SEGNALE ( bersaglio molecolare) Imatinib ( bcr-abl/c-kit-, PDGF-TKs) Gefitinib ( EGFR-TK) Erlotinib ( EGFR-TK) Bortezomib ( proteasoma) Sorafenib ( VEGFR/PDGFR/TKR/Raf)

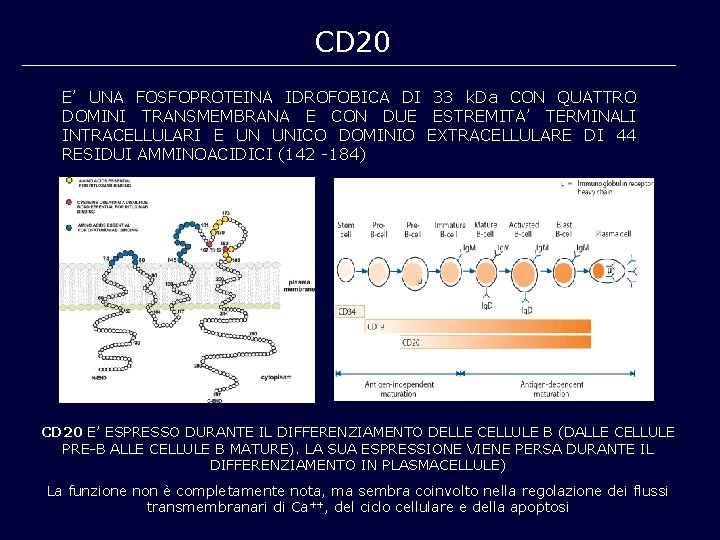
CD 20 E’ UNA FOSFOPROTEINA IDROFOBICA DI 33 k. Da CON QUATTRO DOMINI TRANSMEMBRANA E CON DUE ESTREMITA’ TERMINALI INTRACELLULARI E UN UNICO DOMINIO EXTRACELLULARE DI 44 RESIDUI AMMINOACIDICI (142 -184) CD 20 E’ ESPRESSO DURANTE IL DIFFERENZIAMENTO DELLE CELLULE B (DALLE CELLULE PRE-B ALLE CELLULE B MATURE). LA SUA ESPRESSIONE VIENE PERSA DURANTE IL DIFFERENZIAMENTO IN PLASMACELLULE) La funzione non è completamente nota, ma sembra coinvolto nella regolazione dei flussi transmembranari di Ca++, del ciclo cellulare e della apoptosi

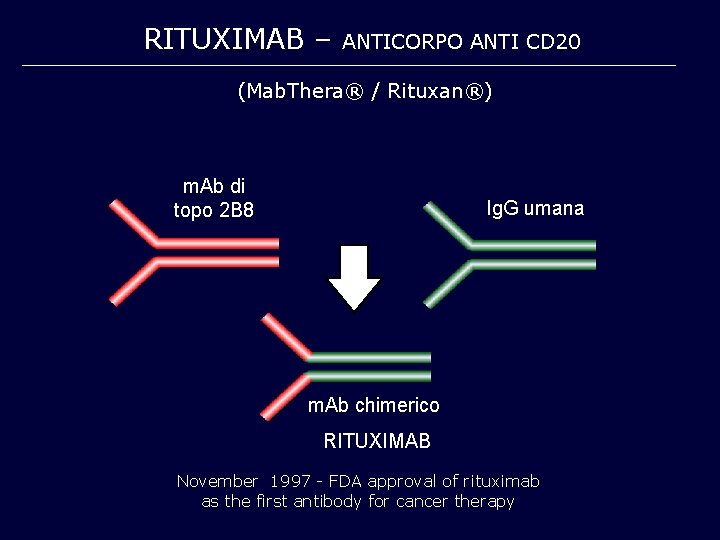
RITUXIMAB – ANTICORPO ANTI CD 20 (Mab. Thera® / Rituxan®) m. Ab di topo 2 B 8 Ig. G umana m. Ab chimerico RITUXIMAB November 1997 - FDA approval of rituximab as the first antibody for cancer therapy

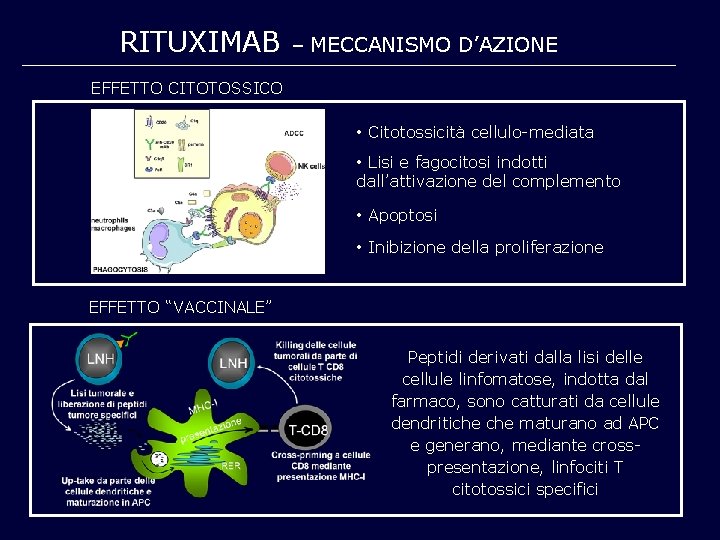
RITUXIMAB – MECCANISMO D’AZIONE EFFETTO CITOTOSSICO • Citotossicità cellulo-mediata • Lisi e fagocitosi indotti dall’attivazione del complemento • Apoptosi • Inibizione della proliferazione EFFETTO “VACCINALE” Peptidi derivati dalla lisi delle cellule linfomatose, indotta dal farmaco, sono catturati da cellule dendritiche maturano ad APC e generano, mediante crosspresentazione, linfociti T citotossici specifici

RITUXIMAB SOMMINISTRAZIONE EV – FARMACOCINETICA 375 mg/m 2 (infusione 50 mg/ora) una volta/settimana x 4 (Premedicazione: Paracetamolo, Antistaminico) Emivita plasmatica: 3, 2 - 8, 5 giorni (76, 4 - 205, 8 ore) • Emivita terminale media: 20. 8 giorni • Clearance sistemica media: 0. 23 l/giorno • Non mostra differenze farmacocinetiche clinicamente rilevanti correlate al sesso • Satura rapidamente le cellule B nel torrente ematico. Poi quelle a livello splenico, midollare e linfonodale. Conta periferica delle Cellule B aumenta dalla settimana 24 e il ripristino si osserva dalla settimana 40

RITUXIMAB – INDICAZIONI Linfoma non-Hodgking • TUMORI B CELLULARI • • Linfoma follicolare in III-IV stadio non trattati precedentemente, in associazione a chemioterapia (R-CVP) Linfoma diffuso a grandi cellule B, CD 20 pos, in associazione a chemioterapia CHOP (ciclofosfamide, doxorubicina, vincristina, prednisone) Off-label: Leucemia linfatica cronica a cellule B, in associazione con regimi di polichemioterapia impiegati per il trattamento di prima linea o di salvataggio Artrite Reumatoide • PATOLOGIE AUTOIMMUNI • Rituximab in associazione a metotrexato è indicato per il trattamento dell’artrite reumatoide attiva di grado grave in pazienti adulti che hanno mostrato inadeguata risposta o intolleranza ad altri farmaci antireumatici modificanti la malattia, comprendenti uno o più inibitori del fattore di necrosi tumorale (TNF) Off-label: Lupus eritematoso sistemico, porpora trombocitopenica idiopatica, dermatopolimiosite refrattaria, pemfigo, sindrome di Sjogren

RITUXIMAB – EFFETTI INDESIDERATI • Segni generali: astenia, algie addominali, toraciche o nella sede di infusione. • Sistema cardiovascolare: ipotensione, ipertensione, aritmie. • Apparato digerente: diarrea, dispepsia, anoressia. • Sistema nervoso: vertigini, ansia, parestesie, iperestesie. • Apparato respiratorio: tosse, sinusite, bronchite. • Cute e mucose: sudorazione, herpes simplex, herpes zoster. • Organi di senso: lacrimazione, congiuntivite, disgeusia. • REAZIONI AVVERSE • • Sindrome da rilascio di citochine: dispnea grave con broncospasmo e ipossia, ipotensione, febbre, brividi, orticaria, angioedema. Sindrome da lisi tumorale: iperuricemia, iperkaliemia, ipocalcemia, iperfosfatemia, insufficienza renale acuta, aumento di LDH, insufficienza respiratoria acuta ed exitus. Eventi infettivi: batterici e virali Leucoencefalopatia Multifocale Progressiva (rara)

ALEMTUXUMAB – ANTICORPO ANTI CD 52 Campath Anticorpo monoclonale umanizzato MECCANISMO D’AZIONE CD 53 Alemtuxumab lega il CD 52, una proteina presente sulla superficie dei linfociti maturi, ma non sulle linee progenitrici INDICAZIONI: Trattamento della Leucemia Linfatica Cronica (CLL) Linfoma cutaneo a cellule-T Non approvato dalla FDA per il trattamento della Sclerosi Multipla (2013)

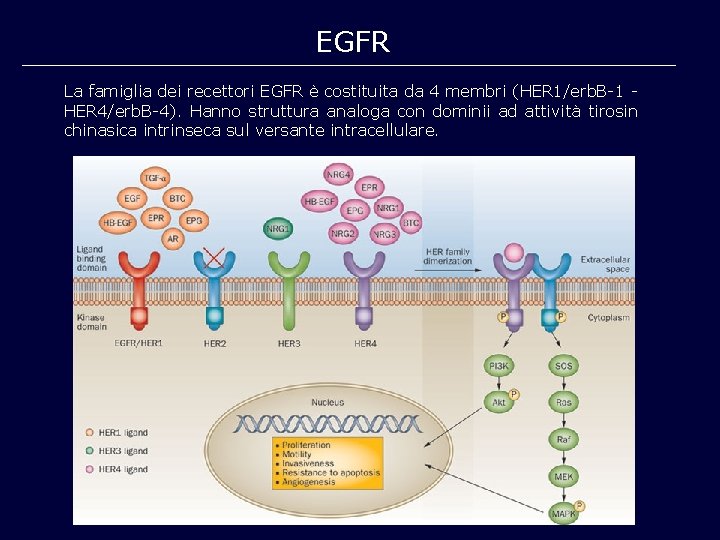
EGFR La famiglia dei recettori EGFR è costituita da 4 membri (HER 1/erb. B-1 HER 4/erb. B-4). Hanno struttura analoga con dominii ad attività tirosin chinasica intrinseca sul versante intracellulare.

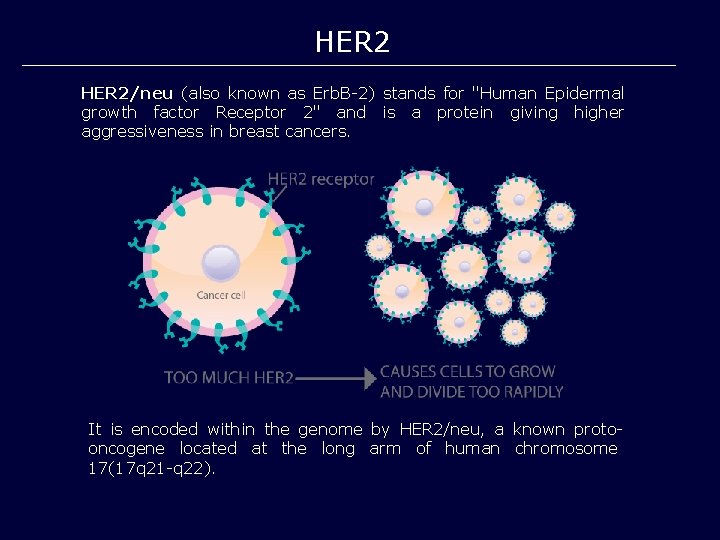
HER 2/neu (also known as Erb. B-2) stands for "Human Epidermal growth factor Receptor 2" and is a protein giving higher aggressiveness in breast cancers. It is encoded within the genome by HER 2/neu, a known protooncogene located at the long arm of human chromosome 17(17 q 21 -q 22).

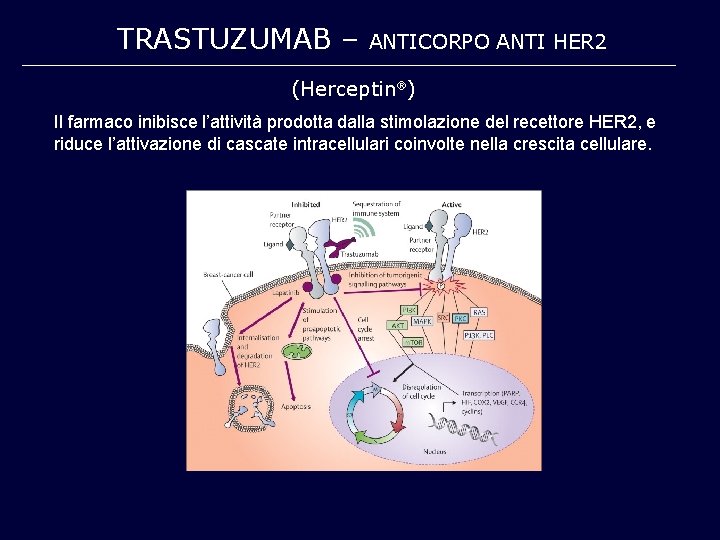
TRASTUZUMAB – ANTICORPO ANTI HER 2 (Herceptin ) Il farmaco inibisce l’attività prodotta dalla stimolazione del recettore HER 2, e riduce l’attivazione di cascate intracellulari coinvolte nella crescita cellulare.

TRASTUZUMAB – ANTICORPO ANTI HER 2 (Herceptin ) INDICAZIONI trattamento di pazienti affette da carcinoma mammario metastatico positivo per i recettori HER 2/neu Proposto per trattamento adenocarcinoma metastatico dello stomaco e della giunzione gastroesofagea HER 2+ FARMACOCINETICA EFFETTI INDESIDERATI • Somministrato in infusione EV a goccia lenta attraverso catetere venoso centrale • La prima infusione si somministra molto lentamente – di solito nell’arco di un’ora e mezzo; le successive sono somministrate a intervalli di una o tre settimane in circa 30 minuti. Di solito il ciclo prevede sei infusioni, ma può proseguire anche per tutto il tempo che riesce a controllare la malattia. Se il trattamento è in combinazione con paclitaxel, questo viene somministrato secondo il protocollo standard, di solito settimanale Sintomi simil-influenzali. Cefalea. Diarrea Dolore lieve nei siti raggiunti da metastasi. Modificazioni dell’attività cardiaca.

CETUXIMAB – ANTICORPO ANTI EGF Erbitux Anticorpo monoclonale chimerico MECCANISMO Il legame dell’anticorpo al recettore impedisce il legame del EGF e conseguentemente blocca i segnali di trasduzione che portano alla proliferazione della cellula Inibisce la proliferazione di linee cellulari di diversi tumori solidi: TUMORI DEL COLON RETTO, TUMORI DEL PANCREAS, TUMORI DELLA TESTA E COLLO, TUMORE POLMONARE NON A PICCOLE CELLULE

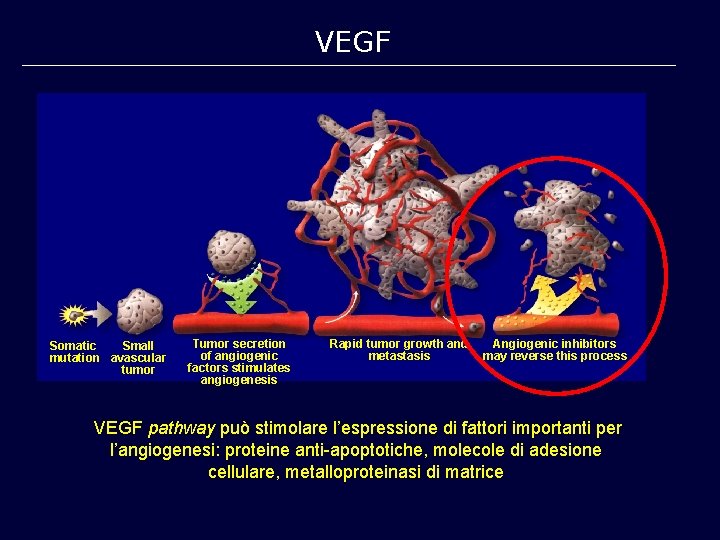
VEGF Somatic Small mutation avascular tumor Tumor secretion of angiogenic factors stimulates angiogenesis Rapid tumor growth and metastasis Angiogenic inhibitors may reverse this process VEGF pathway può stimolare l’espressione di fattori importanti per l’angiogenesi: proteine anti-apoptotiche, molecole di adesione cellulare, metalloproteinasi di matrice

BEVACIZUMAB – ANTICORPO ANTI VEGF Avastin Anticorpo monoclonale umanizzato MECCANISMO D’AZIONE L’interazione del VEGF con i suoi recettori causa proliferazione delle cellule endoteliali e la formazione di nuovi vasi (neoangiogenesi). Bevacizumab lega il VEGF e previene l’interazione del VEGF con i suoi recettori (Flt-1 e Flk-1) sulla superficie delle cellule endoteliali.

BEVACIZUMAB – INDICAZIONI FARMACOCINETICA ANTICORPO ANTI VEGF carcinoma del colon e del retto metastatico in associazione con 5 -FU Ø carcinoma mammario metastatico (prima linea) in associazione al Paclitaxel. Ø carcinoma polmonare non a piccole cellule, non resecabile, avanzato, metastatico o in recidiva, con istologia a predominanza non squamocellulare (prima linea) in associazione a cisplatino. Ø carcinoma renale avanzato e/o metastatico (prima linea) in associazione con Interferone alfa-2 a. Ø Viene somministrato in infusione e. v. La velocità di infusione dipende dalla tollerabilità, con una durata iniziale di infusione pari a 90 minuti. Il profilo farmacocinetico di Bevacizumab è risultato lineare a dosaggi da 1 a 10 mg/kg. Distribuzione: volume del compartimento centrale (Vc) è di 2, 92 l. Metabolismo ed eliminazione: simile a quello delle Ig. G endogene. L’eliminazione avviene attraverso i reni e il fegato. L’emivita terminale di eliminazione oscilla tra i 18 e i 23 giorni.

BEVACIZUMAB – ANTICORPO ANTI VEGF EFFETTI INDESIDERATI Ø Molto comuni (≥ 10%) : - leucopenia, trombocitopenia, neutropenia disturbi del metabolismo e della nutrizione (anoressia) patologie del SNC (neuropatia sensitiva, disgeusia, cefalea) patologia dell’occhio (disturbi del visus) patologie vascolari (ipertensione) patologie respiratorie (dispnea, epistassi, rinite) patologie gastrointestinali (diarrea, nausea, vomito, costipazione, stomatite) patologie della cute (dermatite esfoliativa, secchezza cutanea) patologie renali e urinarie (proteinuria) patologie sistemiche (astenia, febbre) altri disturbi (dolore nella sede di somministrazione) Ø Poco comuni (< 1%): - patologie del SNC (sindrome leucoencefalopatica posteriore reversibile) Ø Rari: - patologie del SNC (encefalopatia ipertensiva) - patologie cardiache (ipertensione polmonare) - altre (perforazione del setto nasale)

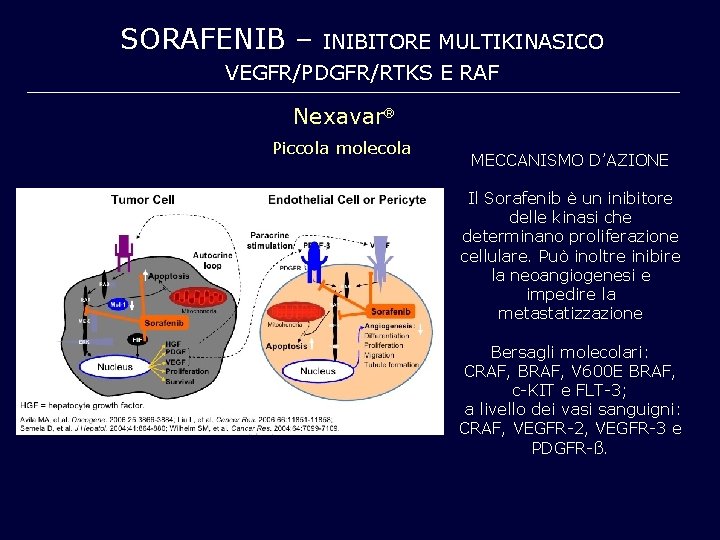
SORAFENIB – INIBITORE MULTIKINASICO VEGFR/PDGFR/RTKS E RAF Nexavar Piccola molecola MECCANISMO D’AZIONE Il Sorafenib è un inibitore delle kinasi che determinano proliferazione cellulare. Può inoltre inibire la neoangiogenesi e impedire la metastatizzazione Bersagli molecolari: CRAF, BRAF, V 600 E BRAF, c-KIT e FLT-3; a livello dei vasi sanguigni: CRAF, VEGFR-2, VEGFR-3 e PDGFR-ß.

SORAFENIB – INDICAZIONI INIBITORE VEGFR/PDGFR/RTKS E RAF Ø carcinoma renale avanzato e/o metastatico (dopo fallimento terapeutico ad una precedente terapia con IFN- o IL-2) Ø epatocarcinoma FARMACOCINETICA Somministrazione orale (cpr da 200 mg). Dose raccomandata negli adulti 400 mg/2 die senza interruzione fino ad osservazione di miglioramento clinico o di tossicità manifesta EFFETTI INDESIDERATI Ø diarrea, nausea, vomito, costipazione, stomatite rash, alopecia aumentato rischio di sanguinamento sindrome mano-piede (eritrodisestesia palmoplantare)

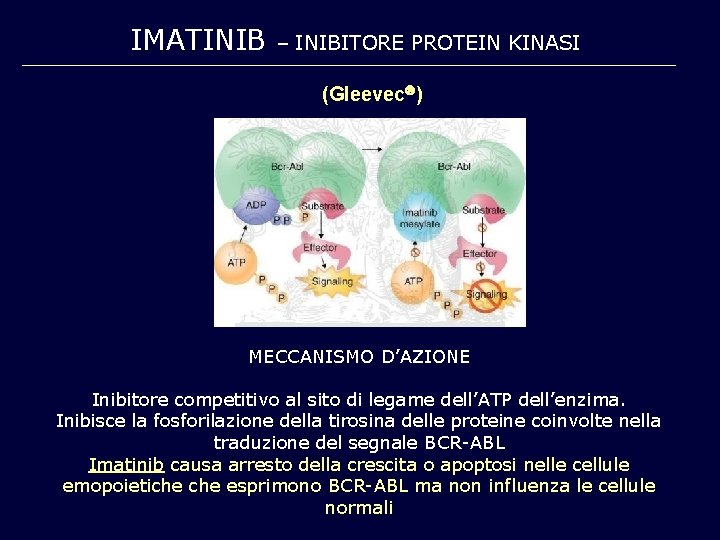
IMATINIB – INIBITORE PROTEIN KINASI (Gleevec ) MECCANISMO D’AZIONE Inibitore competitivo al sito di legame dell’ATP dell’enzima. Inibisce la fosforilazione della tirosina delle proteine coinvolte nella traduzione del segnale BCR-ABL Imatinib causa arresto della crescita o apoptosi nelle cellule emopoietiche esprimono BCR-ABL ma non influenza le cellule normali

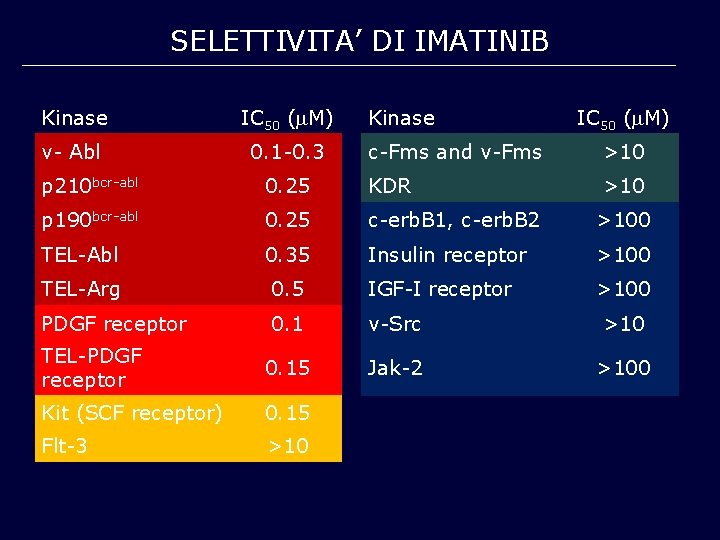
SELETTIVITA’ DI IMATINIB Kinase IC 50 ( M) v- Abl 0. 1 -0. 3 Kinase IC 50 ( M) c-Fms and v-Fms >10 p 210 bcr-abl 0. 25 KDR p 190 bcr-abl 0. 25 c-erb. B 1, c-erb. B 2 >100 TEL-Abl 0. 35 Insulin receptor >100 TEL-Arg 0. 5 IGF-I receptor >100 PDGF receptor 0. 1 v-Src >10 TEL-PDGF receptor 0. 15 Jak-2 >100 Kit (SCF receptor) 0. 15 Flt-3 >10

IMATINIB – FARMACOCINETICA • Completamente assorbito (biodisponibilità del 98%) dopo somministrazione orale • Assorbimento rapido (max concentrazione plasmatica tra 2 e 4 ore) • 95% legato a proteine plasmatiche • Emivita plasmatica = 18 ore circa • Metabolizzato a livello epatico dal sistema enzimatico di P 450 • Eliminato dalle feci (68%) e dalle urine (13%); il 25% in forma immodificata (20% per via fecale, 5% per via urinaria), la restante parte sotto forma di metaboliti. • Può alterare il metabolismo di farmaci substrati di CYP 3 A 4.

IMATINIB – INDICAZIONI • LEUCEMIA MIELOIDE CRONICA: nei pazienti con “cromosoma Philadelphia positivo” (Ph+) di nuova diagnosi nei quali il trapianto di midollo osseo non è consigliato come trattamento di prima scelta. Glivec è anche indicato per il trattamento di adulti e bambini nella “fase cronica” della malattia (400 mg/die), dopo il fallimento della terapia con interferone-alfa o in “fase accelerata” e “crisi blastica”(600 mg/die); • LEUCEMIA LINFOBLASTICA ACUTA con cromosoma Philadelphia positivo (LLA Ph+): usato in combinazione con altri farmaci antitumorali negli adulti di nuova diagnosi. • TUMORE STROMALE DEL TRATTO GASTROINTESTINALE (GIST): in pazienti adulti positivi alla proteina c. Kit, non operabili e/o metastatici (400 mg/die). • SINDROME IPER-EOSINOFILA CRONICA: AVANZATA O LEUCEMIA usato nel trattamento degli adulti nei quali si osserva una riorganizzazione specifica di due geni, chiamati FIP 1 L 1 e PDGFR (400 mg/die 100 mg/die come mantenimento dopo remissione)

IMATINIB – EFFETTI INDESIDERATI E TOSSICITA’ DERMATOLOGICA Rash; Angioedema Depigmentazione, vitiligo GASTROINTESTINALE Nausea e vomito Dispepsia Diarrea e disidratazione Dolore addominale MUSCOLO SCHELETRICA GENERALE EMATOLOGICA EPATICA NEUROLOGICA Artralgia, Mialgia, inclusi i crampi Edema Fatigue Febbre, sintomi similinfluenzali Aumento di peso Neutropenia (15% grade 3 or 4) Thrombocitopenia (9% grade 3 -4) Pancitopenia Aterazione transaminasi e bilirubina Insufficienza epatica Insonnia/sonnolenza Ansia, depressione Confusione, Vertigine, sincopi Edema ed emorragie cerebrali Neuropatia

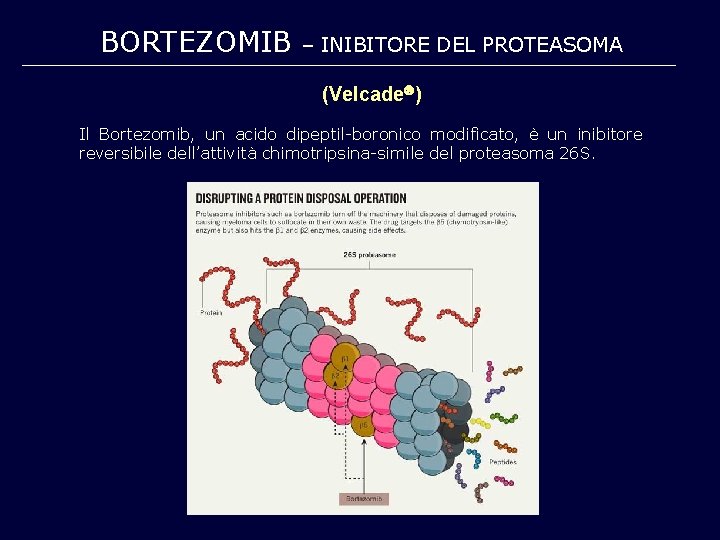
BORTEZOMIB – INIBITORE DEL PROTEASOMA (Velcade ) Il Bortezomib, un acido dipeptil-boronico modificato, è un inibitore reversibile dell’attività chimotripsina-simile del proteasoma 26 S.

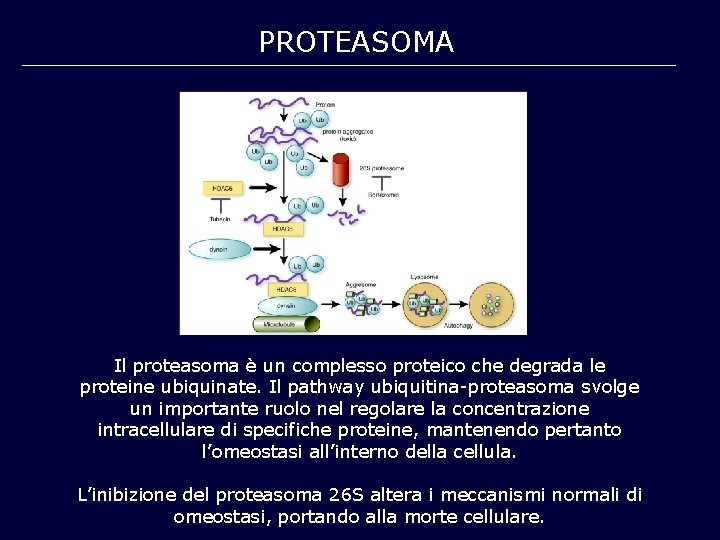
PROTEASOMA Il proteasoma è un complesso proteico che degrada le proteine ubiquinate. Il pathway ubiquitina-proteasoma svolge un importante ruolo nel regolare la concentrazione intracellulare di specifiche proteine, mantenendo pertanto l’omeostasi all’interno della cellula. L’inibizione del proteasoma 26 S altera i meccanismi normali di omeostasi, portando alla morte cellulare.

BORTEZOMIB INDICAZIONI FARMACOCINETICA – INIBITORE DEL PROTEASOMA Il Bortezomib trova indicazione nel trattamento dei pazienti con MIELOMA MULTIPLO che hanno ricevuto almeno due precedenti terapie e che presentavano una progressione della malattia durante l’ultimo trattamento. Il dosaggio raccomandato di Bortezomib è di 1, 3 mg/m 2, somministrato come bolo per via endovenosa, 2 volte alla settimana per 2 settimane (giorni 1, 4, 8 ed 11) con successivo periodo di riposo di 10 giorni (giorni 12 -21). Questo periodo di 3 settimane è considerato un ciclo di terapia.

BORTEZOMIB – EFFETTI INDESIDERATI Il trattamento con Bortezomib può causare: - astenia: 65% nausea: 64% diarrea: 51% riduzione dell’appetito: 43% costipazione: 43% trombocitopenia: 43% neuropatia periferica: 37% piressia: 36% vomito: 36% anemia: 32%