Autor Mgr Terezie Nohnkov Vzdlvac oblast lovk a

Autor : Mgr. Terezie Nohýnková Vzdělávací oblast : Člověk a příroda Obor : Chemie Téma : Názvosloví a chemické reakce Název : Chemické reakce Zdroje a použité materiály : vlastní Anotace : Postupným plněním úloh si žáci upevňují dovednosti úpravy ch. rovnic VY_32_INOVACE_24_CHEMICKE_REAKCE Vytvořeno jako DUM do předmětu chemie pro 8. ročník na ZŠ Studentská Mnichovo Hradiště dne 5. 3. 2011 Vytvořeno v rámci v projektu „EU peníze školám“ OP VK oblast podpory 1. 4 s názvem Zlepšení podmínek pro vzdělávání na základních školách

Opakování, procvičování CHEMICKÉ REAKCE

Pravidla pro úpravu rovnic podle ZZH • Počty atomů téhož prvku musí být na P a L straně rovnice stejné. př. 2 Cu + S Cu 2 S • Do zadané značky či vzorce se nezasahuje, veškeré úpravy se provádí zápisem před značku / vzorec - př. 4 F 2 , 3 HCl • Upravující číslice před vzorcem platí pro všechny prvky tvořící sloučeninu Př. 2 H 2 SO 4 - 2. 2 H = 4 H a 2. 1 S = 2 S a 2. 4 O = 8 O • Počty atomů téhož prvku se na jedné straně rovnice sčítají. Př. Zn(OH)2 + HNO 3 ------ 2 O + 3 O = 5 O • Vyskytne-li se ve vzorci malé číslo za závorkou, platí pro všechny prvky v závorce. Př. Cu(NO 3)2 - 2. N - 2. 3 O = 6 O

Urči počty atomů jednotlivých prvků tvořících sloučeninu : • 4 HNO 3 – • Pb(OH)2 – • 2 Al 2(SO 4)3 –

Přepiš následující ch. reakce ch. rovnicí a uprav podle ZZH : • Měď reaguje se sírou a vzniká sulfid měďnatý (Cu. S). • Peroxid vodíku (H 2 O 2) se rozkládá a vzniká kyslík a voda. • Hořčík se slučuje s kyslíkem za vzniku oxidu hořečnatého (Mg. O).
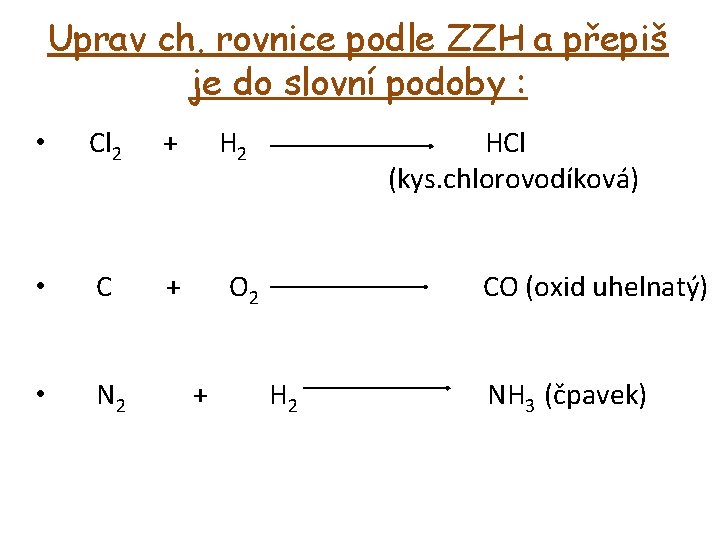
Uprav ch. rovnice podle ZZH a přepiš je do slovní podoby : • Cl 2 + H 2 HCl (kys. chlorovodíková) • C + O 2 CO (oxid uhelnatý) • N 2 + H 2 NH 3 (čpavek)
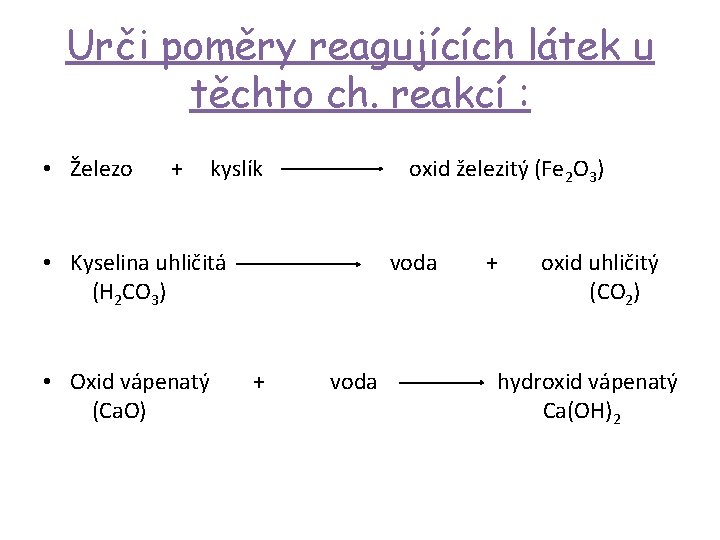
Urči poměry reagujících látek u těchto ch. reakcí : • Železo + kyslík oxid železitý (Fe 2 O 3) • Kyselina uhličitá voda + oxid uhličitý (H 2 CO 3) (CO 2) • Oxid vápenatý + voda hydroxid vápenatý (Ca. O) Ca(OH)2

Za použití značek označujících skupenství látek zapiš ch. rovnicí a uprav : • Rozklad plynného jodovodíku (HI) na plynný vodík a pevný jod. • Slučování plynného vodíku a kyslíku na vodu. • Sloučení plynného chloru s pevným sodíkem za vzniku pevného chloridu sodného (Na. Cl).
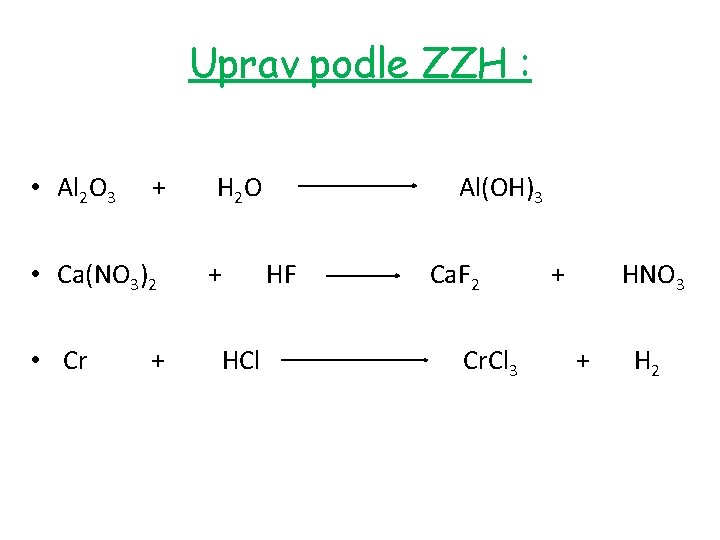
Uprav podle ZZH : • Al 2 O 3 + H 2 O Al(OH)3 • Ca(NO 3)2 + HF Ca. F 2 + HNO 3 • Cr + HCl Cr. Cl 3 + H 2
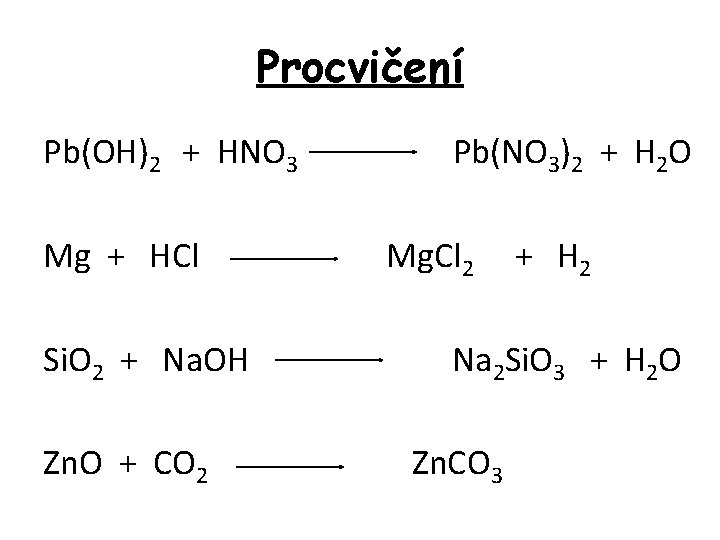
Procvičení Pb(OH)2 + HNO 3 Pb(NO 3)2 + H 2 O Mg + HCl Mg. Cl 2 + H 2 Si. O 2 + Na. OH Na 2 Si. O 3 + H 2 O Zn. O + CO 2 Zn. CO 3
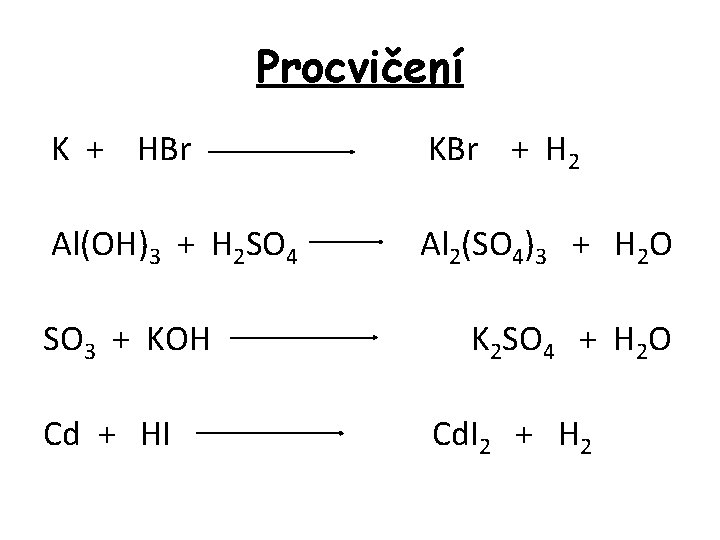
Procvičení K + HBr KBr + H 2 Al(OH)3 + H 2 SO 4 Al 2(SO 4)3 + H 2 O SO 3 + KOH K 2 SO 4 + H 2 O Cd + HI Cd. I 2 + H 2
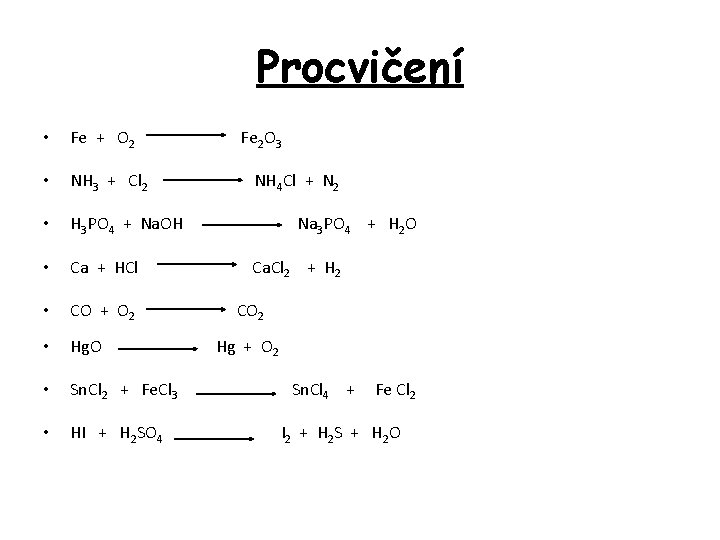
Procvičení • • • • Fe + O 2 Fe 2 O 3 NH 3 + Cl 2 NH 4 Cl + N 2 H 3 PO 4 + Na. OH Na 3 PO 4 + H 2 O Ca + HCl Ca. Cl 2 + H 2 CO + O 2 CO 2 Hg. O Hg + O 2 Sn. Cl 2 + Fe. Cl 3 Sn. Cl 4 + Fe Cl 2 HI + H 2 SO 4 I 2 + H 2 S + H 2 O
- Slides: 12