AUTOMATISMOS ELECTROMAGNETICOS Generadores Qumicos GENERADORES QUIMICOS Introduccin BATERIAS

AUTOMATISMOS ELECTROMAGNETICOS Generadores Químicos

GENERADORES QUIMICOS Introducción BATERIAS PILAS Acumulador Elementos del acumulador Introducción Parámetros del acumulador Instrumentos de medidas Métodos de carga Galvanómetro Cargadores de la batería Amperímetro Emplazamiento de las baterías Voltímetro El electrolito Óhmetro Operación y mantenimiento de las baterías de Pb Polímetro (tester) Operación y mantenimiento de las baterías de Ni Cd Watímetro Operación y mantenimiento de las baterías de Ni Fe Osciloscopio Tabla comparativa de los diferentes tipos de acumulador Determinación de la capacidad de la batería Diversos modos de acoplar las baterías

Introducción Batería, batería eléctrica, acumulador eléctrico o simplemente acumulador, se le denomina al dispositivo que almacena energía eléctrica, usando procedimientos electroquímicos y que posteriormente la devuelve casi en su totalidad; este ciclo puede repetirse por un determinado número de veces. Un acumulador es un generador de tipo químico que tiene la propiedad de poder generarse una vez que la carga acumulada en su interior está agotada. Se trata de un generador eléctrico secundario; es decir, un generador que no puede funcionar sin que se le haya suministrado electricidad previamente mediante lo que se denomina proceso de carga. Una pila eléctrica es un dispositivo que convierte energía química en energía eléctrica por un proceso químico transitorio, tras de lo cual cesa su actividad y han de renovarse sus elementos constituyentes, puesto que sus características resultan alteradas durante el mismo. Se trata de un generador eléctrico primario. Esta energía resulta accesible mediante dos terminales que tiene la pila, llamados polos, electrodos o bornes. Uno de ellos es el polo positivo o ánodo (+) y el otro es el polo negativo o cátodo ( ). La estructura fundamental de una pila consiste en dos electrodos, metálicos en muchos casos, introducidos en una disolución conductora de la electricidad o electrolito. Las pilas pueden ser irreversibles o pilas primarias o pueden recargarse nuevamente, son las pilas secundarias o acumuladores.

El término pila, denomina a los generadores de electricidad basados en procesos químicos normalmente no reversibles, o acumuladores de energía eléctrica no recargables; mientras que batería se aplica generalmente a los dispositivos electroquímicos reversibles, o acumuladores de energía eléctrica que sí se pueden recargar. El término acumulador se aplica indistintamente a uno u otro tipo, así como a los capacitores eléctricos o a futuros métodos de acumulación, erigiéndose de este modo como el término neutro capaz de englobar y describir a todos ellos. Las pilas secundarias o acumuladores son aquellas que pueden recargarse, es decir pueden reiniciar el proceso mediante el aporte de energía de una fuente exterior normalmente un generador, que hace que los compuestos químicos se transformen en los compuestos de partida, al hacer pasar corriente a través de ellos en sentido opuesto

Baterías

Acumulador El funcionamiento de un acumulador está basado esencialmente en un proceso reversible llamado reducción oxidación (redox), un proceso en el cual uno de los componentes se oxida (pierde electrones) y el otro se reduce (gana electrones); es decir, un proceso cuyos componentes no resulten consumidos, sino que meramente cambian su estado de oxidación, que a su vez puedan retornar al estado primero en las circunstancias adecuadas. Estas circunstancias son, en el caso de los acumuladores, el cierre del circuito externo, durante el proceso de descarga, y la aplicación de una corriente, igualmente externa, durante la carga.

Un acumulador eléctrico es un generador de tipo químico que tiene la propiedad de poder regenerarse una vez que la carga acumulada en su interior está agotada. De acuerdo con el tipo de electrolito utilizado, los acumuladores pueden ser de tipo ácido, que utilizan ácido sulfúrico, y los alcalinos, que utilizan hidróxido potásico. También los electrodos pueden ser de distintos materiales dando lugar igualmente a diferentes denominaciones de los acumuladores; así, las pilas ácidas utilizan electrodos de plomo, por lo que se las conoce como acumuladores de plomo; en las pilas alcalinas nos encontramos también con distintas denominaciones según que los electrodos utilizados sean de ferro níquel o de níquel cadmio. § Por lo que a su naturaleza interna se refiere, se encuentran habitualmente en el comercio acumuladores de los siguientes tipos de electrodos o electrolitos: Acumulador de plomo (Pb) Batería alcalina Baterías alcalinas de manganeso Baterías de níquel-cadmio (Ni-Cd) Baterías de iones de litio (Li ion) Baterías de polímero de litio (Li Po) Pilas de combustible Condensador de alta capacidad Baterías de níquel-hidruro metálico (Ni-MH)
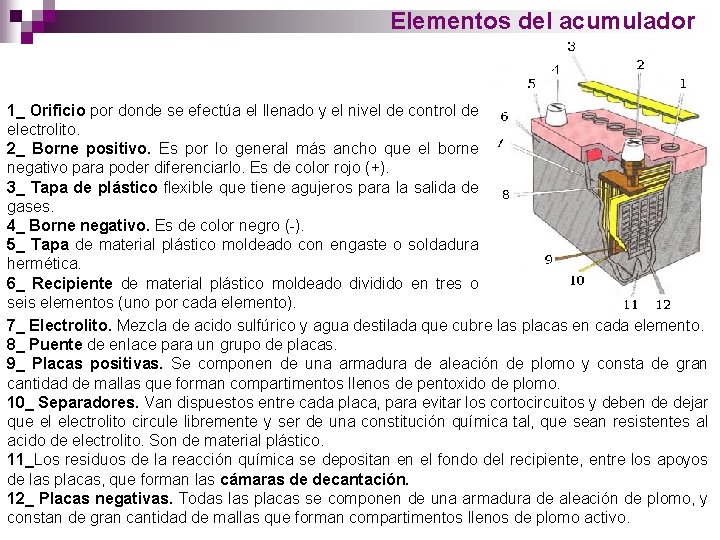
Elementos del acumulador 1_ Orificio por donde se efectúa el llenado y el nivel de control de electrolito. 2_ Borne positivo. Es por lo general más ancho que el borne negativo para poder diferenciarlo. Es de color rojo (+). 3_ Tapa de plástico flexible que tiene agujeros para la salida de gases. 4_ Borne negativo. Es de color negro ( ). 5_ Tapa de material plástico moldeado con engaste o soldadura hermética. 6_ Recipiente de material plástico moldeado dividido en tres o seis elementos (uno por cada elemento). 7_ Electrolito. Mezcla de acido sulfúrico y agua destilada que cubre las placas en cada elemento. 8_ Puente de enlace para un grupo de placas. 9_ Placas positivas. Se componen de una armadura de aleación de plomo y consta de gran cantidad de mallas que forman compartimentos llenos de pentoxido de plomo. 10_ Separadores. Van dispuestos entre cada placa, para evitar los cortocircuitos y deben de dejar que el electrolito circule libremente y ser de una constitución química tal, que sean resistentes al acido de electrolito. Son de material plástico. 11_Los residuos de la reacción química se depositan en el fondo del recipiente, entre los apoyos de las placas, que forman las cámaras de decantación. 12_ Placas negativas. Todas las placas se componen de una armadura de aleación de plomo, y constan de gran cantidad de mallas que forman compartimentos llenos de plomo activo.

Parámetros del acumulador § La tensión o potencial (V), es el primer parámetro a considerar, es el que suele determinar si el acumulador conviene al uso a que se le destina. Viene fijado por el potencial de reducción del par redox utilizado; suele estar entre 1 V y 4 V por elemento. § La cantidad de corriente que puede almacenar el acumulador, se mide en Amperios/hora (Ah) y es el segundo parámetro a considerar. Especial importancia tiene en algunos casos la intensidad de corriente máxima obtenible ampere (A). Por ejemplo, los motores de arranque de los automóviles exigen esfuerzos muy grandes de la batería cuando se ponen en funcionamiento (centenas de A), pero actúan durante poco tiempo. § La energía que puede suministrar una batería depende de su capacidad y de su voltaje, se mide habitualmente en Wh (vatios hora). La unidad en el SI es el julio (J) § La resistencia de los acumuladores es muy inferior a la de las pilas, lo que les permite suministrar cargas mucho más intensas que las de éstas, sobre todo de forma transitoria. Por ejemplo, la resistencia interna de un acumulador de plomo ácido es de 0, 006 ohm, y la de otro de Ni Cd, de 0, 009 ohm.

Téngase en cuenta, sin embargo, que, cuando le den indicaciones en el cuerpo de las baterías, como: "Cárguese a 120 m. A durante 12 horas", el producto resultante excederá la capacidad del acumulador. El exceso de "carga" se disipa dentro de la batería en forma de calor a causa de su "resistencia interna". Si la capacidad del acumulador fuesen 1200 m. Ah y se le aplicara una corriente de carga de 120 m. A durante 12 horas. 120 x 12 = 1440 m. Ah, por lo que 240 m. Ah (1200 m. Ah – 1440 m. Ah) será la carga convertida en calor dentro de la batería y 1200 m. Ah la efectivamente almacenada en ella. Para calcular la energía perdida bastaría multiplicar los 240 m. Ah de "exceso" de carga por la tensión de carga. 1 Ah = 3600 C 1 C = 1 Ah/3600 = 0, 278 m. Ah. 1 Wh = 3600 J

§ Otra de las características importantes de un acumulador es su masa o su peso, y la relación entre ella y la capacidad eléctrica (Ah/kg) o la energía (Wh/kg) que puede restituir. En algunos casos puede ser también importante el volumen que ocupe (Ah/m 3) o (Ah/litro). § El rendimiento es la relación porcentual entre la energía eléctrica recibida en el proceso de carga y la que el acumulador entrega durante la descarga. El acumulador de plomo ácido tiene un rendimiento de más del 90% y las baterías Ni Cd un 83% § La capacidad eléctrica se mide en la práctica por referencia a los tiempos de carga y de descarga en amperios (A). La capacidad vendrá dada por la expresión: Q = I · t. Donde t es el tiempo estimado de la batería sin posibilidad de carga. La unidad en el SI es el coulomb (C). Métodos de carga Una batería puede cargarse utilizando dos métodos diferentes: § Método de voltaje constante; consiste en suministrar a la batería una intensidad varias veces superior a la final durante el primer momento y reducirla paulatinamente a medida que va aumentando la carga. § Método de corriente constante; consistente en suministrar a la batería una corriente de intensidad moderada durante un periodo de tiempo más dilatado.
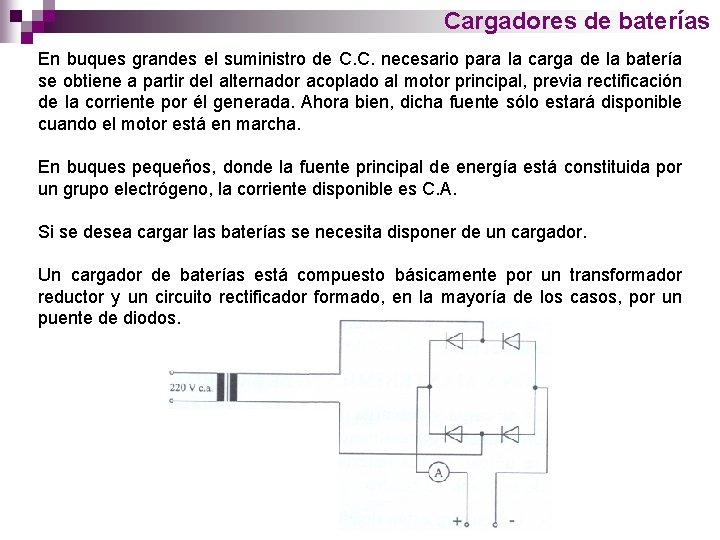
Cargadores de baterías En buques grandes el suministro de C. C. necesario para la carga de la batería se obtiene a partir del alternador acoplado al motor principal, previa rectificación de la corriente por él generada. Ahora bien, dicha fuente sólo estará disponible cuando el motor está en marcha. En buques pequeños, donde la fuente principal de energía está constituida por un grupo electrógeno, la corriente disponible es C. A. Si se desea cargar las baterías se necesita disponer de un cargador. Un cargador de baterías está compuesto básicamente por un transformador reductor y un circuito rectificador formado, en la mayoría de los casos, por un puente de diodos.

Emplazamientos de las baterías Las baterías de acumuladores estarán instaladas en compartimentos de fácil acceso con el fin de realizar tareas de mantenimiento: cambiar elementos, hacer inspecciones y pruebas, rellenar el electrolito, efectuar la limpieza, etc. Deberán estar sujetas de tal forma que no sufran desplazamientos como consecuencia de los movimientos del buque. El compartimento donde estén ubicadas no debe estar expuesto a temperaturas excesivamente altas o bajas. Las baterías de plomo y las alcalinas no pueden instalarse en un compartimento común, ni tampoco demasiado próximas. Las baterías de arranque y precalentamiento de motores deben instalarse lo más cerca posible de las respectivas máquinas. El emplazamiento debe estar protegido contra goteo, suciedad y caída de objetos y que no se obstaculice el escape de los gases. La protección debe compaginar el escape de los gases y evitar, al mismo tiempo, que las chispas o llamas pueden producir un incendio.

Se tomarán medidas para lograr una ventilación suficiente. El aire debe penetrar por la parte inferior y ser evacuado por la parte supe riory conducido verticalmente hacia el exterior. En caso de utilizar ventilación forzada, se empleará material antideflagrante, motores cuyo rotor no produzca chispas, etc. El sistema de ventilación forzada debería ponerse en marcha, de forma automática, cuando las baterías están en carga. Finalmente, a la entrada a los compartimentos de baterías deberán colocarse avisos señalizando el peligro de explosión.
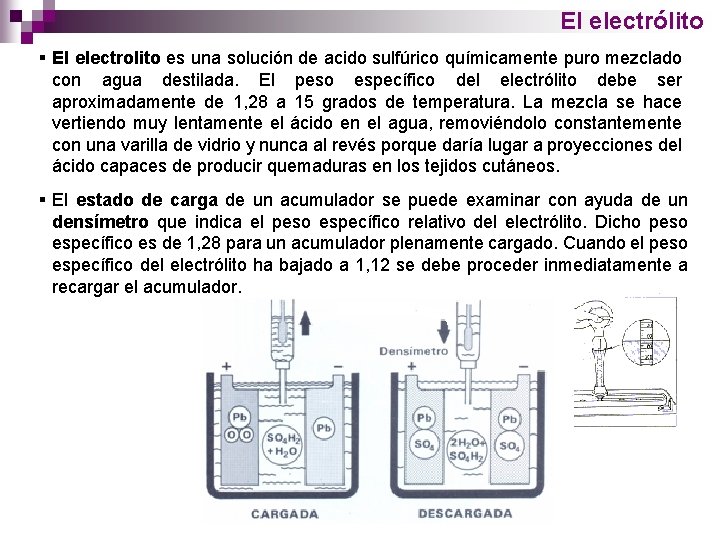
El electrólito § El electrolito es una solución de acido sulfúrico químicamente puro mezclado con agua destilada. El peso específico del electrólito debe ser aproximadamente de 1, 28 a 15 grados de temperatura. La mezcla se hace vertiendo muy lentamente el ácido en el agua, removiéndolo constantemente con una varilla de vidrio y nunca al revés porque daría lugar a proyecciones del ácido capaces de producir quemaduras en los tejidos cutáneos. § El estado de carga de un acumulador se puede examinar con ayuda de un densímetro que indica el peso específico relativo del electrólito. Dicho peso específico es de 1, 28 para un acumulador plenamente cargado. Cuando el peso específico del electrólito ha bajado a 1, 12 se debe proceder inmediatamente a recargar el acumulador.
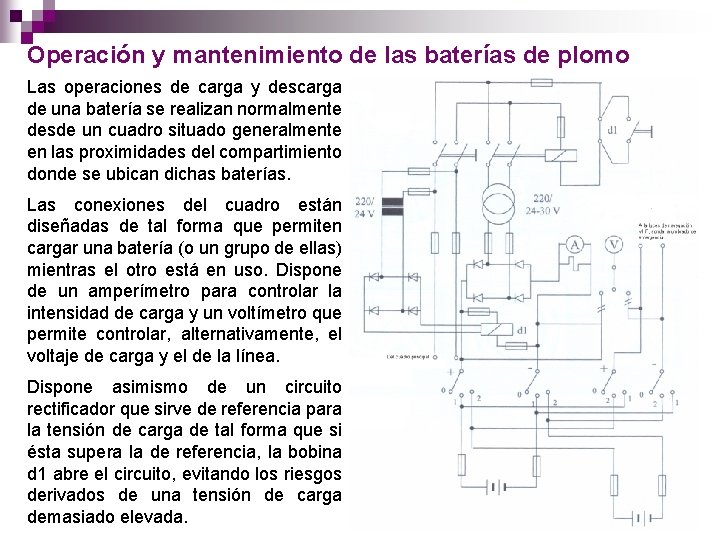
Operación y mantenimiento de las baterías de plomo Las operaciones de carga y descarga de una batería se realizan normalmente desde un cuadro situado generalmente en las proximidades del compartimiento donde se ubican dichas baterías. Las conexiones del cuadro están diseñadas de tal forma que permiten cargar una batería (o un grupo de ellas) mientras el otro está en uso. Dispone de un amperímetro para controlar la intensidad de carga y un voltímetro que permite controlar, alternativamente, el voltaje de carga y el de la línea. Dispone asimismo de un circuito rectificador que sirve de referencia para la tensión de carga de tal forma que si ésta supera la de referencia, la bobina d 1 abre el circuito, evitando los riesgos derivados de una tensión de carga demasiado elevada.

Carga de la batería Aunque pueden utilizarse los dos métodos ya explicados, es preferible, en la mayoría de los casos, utilizar el de voltaje constante, porque la corriente de carga se va reduciendo progresivamente a medida que la batería va adquiriendo su régimen normal de carga, debido a que la f. e. m. de la batería se eleva cuando se alcanza la carga completa. La tensión aplicada debe ser de unos 2, 3 voltios. Con esa tensión por elemento, la corriente al empezar la carga es, por lo general, excesiva, por lo que se recomienda intercalar una pequeña resistencia en serie. En este caso el voltaje de carga necesario es de 2, 5 o 2, 6 V. Si el sistema de carga está, como en el caso de la figura, conectado a una fuente de c. c. constante, puede ser suficiente con una tensión menor para mantener el grupo de baterías con carga suficiente; aunque si por alguna razón se necesitara más voltaje para recargar las baterías (por ejemplo después de una prolongada descarga) sería necesario disponer de un transformador con una salida regulable).

Durante los procesos de carga/descarga del acumulador el electrólito va cediendo iones de sulfato y aumentando su proporción en agua. El electrólito va rebajándose progresivamente y las placas se van recubriendo intensamente de sulfato. Por último, el electrólito puede quedar reducido a agua y las placas convertidas totalmente en sulfato. Sin embargo, mucho antes de que se llegue a este estado se pone de manifiesto la necesidad de recargarlo haciendo pasar una corriente eléctrica en sentido contrario a la descarga, con ello devolvemos los iones de sulfato a la solución volviendo a formar las placas. Es decir, cambia la composición del electrólito, de tal forma que cuando el acumulador se encuentra totalmente cargado la densidad del electrólito es máxima y va disminuyendo a medida que el acumulador se descarga. Por lo tanto, la medición de dicha densidad nos permitirá averiguar el estado de carga de la batería. Para ello se utilita un aparato llamado densímetro. Que es un aparato que consta de una ampolla de vidrio dotado de un contrapeso y una escala graduada.

Mantenimiento de la batería Con respecto al compartimento donde están instaladas, debe estar ventilado, limpio y seco. Tanto las estanterías, como los mamparos y cubiertas adyacentes a las baterías, deben estar pintadas con pinturas resistentes a los ácidos. Periódicamente mantenimiento: deben llevarse a cabo las siguientes operaciones de § Limpieza de las baterías y sus bornes (pueden protegerse con grasa). § Comprobación del estado de las conexiones. § Revisión del electrolito. Este debe estar siempre unos 10 mm por encima de los cantos superiores de las placas. En el relleno debe utilizarse únicamente agua destilada. § Revisión periódica del electrolito, tal como hemos explicado con anterioridad. § En caso de baterías fuera de servicio deberán tomarse las siguientes medidas: o Si la inactividad es superior a los 2 3 meses, se realizará una recarga mensual. o Si la inactividad abarca un periodo superior a los 3 meses, es conveniente vaciar el electrolito y rellenar la batería de agua destilada.

Averías mas frecuentes en los acumuladores de plomo Como consecuencia de la sobrecarga continua de la batería se puede producir fenómenos indeseables tales como el sobrecalentamiento interno, la destrucción mecánica de las placas, la destrucción de los separadores o los cortocircuitos internos. Estas anomalías pueden ocurrir por falta de control en los procesos de carga o por avería del regulador, si se dispone de él. Otro tipo de avería común es la sulfatación de la batería producida por una descarga excesiva de la misma, que ocurre como consecuencia, entre otras, cosas, de: § La falta de agua. § La inactividad de la batería por largos periodos de tiempo. § La carga insuficiente por defecto del regulador de tensión (si existe) o defectuosa conexión de los terminales. § El cortocircuito exterior de la batería, por suciedad en la misma o mal aislamiento de los conductores del circuito de utilización. § Por cortocircuitos internos por impurezas del electrólito o por desprendimiento de la sustancia activa de las placas.

Operación y mantenimiento de baterías de níquel-cadmio La carga de estas baterías puede realizarse utilizándose los métodos conocidos, si bien es más recomendable el de tension constante. Normalmente la batería debe cargarse en siete horas, si bien puede hacerse en menos tiempo. Durante dicho proceso la tensión se mantiene constante, aproximadamente entre 1. 4 y 1. 5 voltios hasta casi al final de la carga, en cuyo momento asciende a unos 1. 8 voltios. La batería debe cargarse de modo continuo. Se consideran descargadas cuando el voltaje baja de 1. 2 voltios. Como quiera que la densidad del electrólito no varía, el estado de carga se comprueba con un voltímetro. El mantenimiento consistirá básicamente en las siguientes operaciones: § Mantener la batería limpia y seca. Si en los tapones, bornes, conexión entre elementos, aparece una costra blanca (cristales de carbonato potásico) debe utilizarse un cepillo blando o un trapo mojado en agua. § Los bornes, conexiones, etc. pueden protegerse con un aceite anticorrosivo, aunque también puede usarse vaselina neutra como protector.

§ Para el relleno debe utilizarse exclusivamente agua destilada. Debe utilizarse agua destilada especialmente fabricada para el relleno de baterías de plomo porque suele contener algo de ácido sulfúrico. La batería debe rellenarse cada vez que está por debajo del mínimo no debiendo sobrepasarse el nivel máximo recomendado. § En este tipo de baterías puede darse el denominado efecto memoria consistente en que, por el hecho de recibir carga sin haberse descargado la batería totalmente, su capacidad se va reduciendo progresivamente. § Para corregir este defecto deben seguirse las recomendaciones dadas por el fabricante. No obstante la solución puede consistir en efectuar periódicamente una descarga total de la batería. Las baterías de níquel cadmio son de una gran robustez mecánica, no se ven perjudicadas por las sobrecargas, ni los largos periodos de inactividad, trabajan bien con amplios márgenes de temperatura, tienen una resistencia interna muy baja y su tensión se mantiene casi constante para distintos valores de la corriente de descarga.

Operación y mantenimiento de baterías de níquel-hierro El voltaje de carga es de aproximadamente 1. 7 voltios salvo al final del periodo de carga (unas siete horas) que sube a 1. 8 voltios. Tal como sucede con las baterías de Ni Cd, la densidad del electrolito no varía durante los procesos de carga descarga. Por tal motivo el estado de carga ha comprobarse con un voltímetro. Se considera que está descargada la batería cuando el voltaje baja a 1. 2 V. En cuanto al mantenimiento de las baterías. Los acumuladores de Ni Fe se caracterizan, como los de Ni Cd, por su gran robustez. Pueden soportar sobrecargas, descargas excesivas, cortocircuitos accidentales, quedar fuera de servicio y descargados durante largo tiempo sin sufrir daño alguno, etc. Como en otros tipos de acumuladores, el nivel de la solución desciende con el servicio, por lo que debe ser repuesto periódicamente con agua destilada.
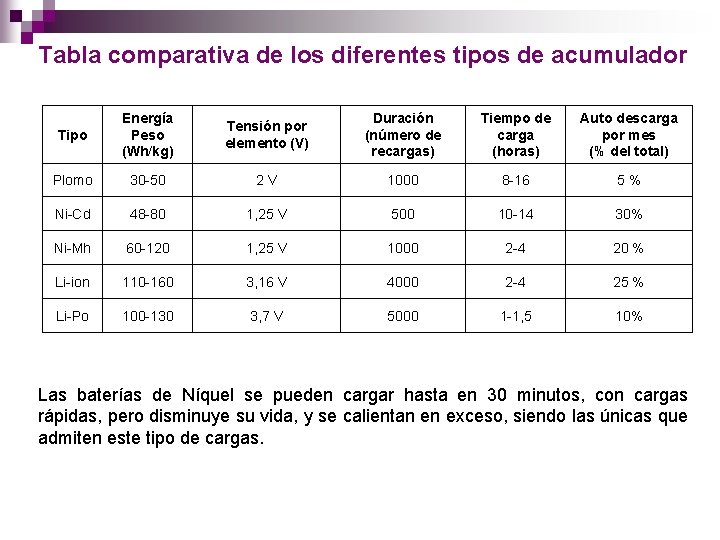
Tabla comparativa de los diferentes tipos de acumulador Tipo Energía Peso (Wh/kg) Tensión por elemento (V) Duración (número de recargas) Tiempo de carga (horas) Auto descarga por mes (% del total) Plomo 30 50 2 V 1000 8 16 5% Ni Cd 48 80 1, 25 V 500 10 14 30% Ni Mh 60 120 1, 25 V 1000 2 4 20 % Li ion 110 160 3, 16 V 4000 2 4 25 % Li Po 100 130 3, 7 V 5000 1 1, 5 10% Las baterías de Níquel se pueden cargar hasta en 30 minutos, con cargas rápidas, pero disminuye su vida, y se calientan en exceso, siendo las únicas que admiten este tipo de cargas.

Determinación de la capacidad de la batería Para determinar la capacidad de la batería es necesario, en primer lugar, saber cual es el uso que se le va a dar a bordo. Si la batería es para alimentar el motor de arranque del motor principal o de un generador de emergencia, nos atendremos a las recomendaciones especificadas por el fabricante de dicha máquina. Si la batería esta destinada a alimentar circuitos de alumbrado, bien como generador principal, bien como generador de emergencia, la capacidad se podrá calcular realizando unos sencillo cálculos. Una vez calculada la potencia consumida, procederemos a calcular el consumo de corriente con la expresión: La capacidad vendrá dada por la expresión: Donde t es el tiempo estimado de la batería sin posibilidad de carga. La unidad de capacidad en el SI es el coulomb (C).

En caso de baterías para circuitos de emergencia, la duración del servicio vendrá dada por las normas internacionales de seguridad o por las normas de las sociedades de clasificación. Teniendo en cuenta, además, que la batería no debe descargarse por comple to, que la capacidad de la batería indicada por el fabricante se refiere a unas condiciones determinadas en cuando a régimen de descarga o temperatura de funcionamiento y que raramente las baterías van a tener su carga al 100 %, la capacidad obtenida deberá multiplicarse por dos. En embarcaciones pequeñas donde la batería debe ser utilizada tanto para le arranque como para el alumbrado, hay que sumar ambas necesidades para determinar la capacidad de la batería.

Diversos modos de acoplarlas Para lograr tensiones mayores o una capacidad de batería distintos a los genéricos que tienen las baterías que existen en el mercado, se usa la técnica de unión de baterías. Acoplamiento en serie El acoplamiento serie tiene como particularidad principal que son sumadas las tensiones de las baterías y la capacidad permanece igual. Como punto para tener en cuenta en este acoplamiento es que la capacidad de la batería (Ah) tiene que ser la misma para todas las baterías. Si una de ellas tuviera menor capacidad, durante el proceso de carga de las baterías, este elemento alcanzaría la carga completa antes que los demás por lo que estaría sometido a una sobrecarga, con efectos que podrían deteriorar la batería. También en el proceso de descarga la batería de capacidad menor se descargara antes por lo que se pueden sulfatar sus placas. Acoplamiento en paralelo El acoplamiento paralelo tiene como particularidad principal que son sumadas las capacidades de la batería manteniéndose invariable las tensiones. Como punto para tener en cuenta en este acoplamiento es que todas las baterias tienen que tener igual valor de tensión (V) en sus bornes de no ser asi la de mayor tensión en bornes se descargara a través de la de menor.

ACOPLAMIENTO EN SERIE El acoplamiento en SERIE consiste en unir el polo positivo (+) de un elemento con el polo negativo (-) del elemento siguiente y así sucesivamente, de forma que los bornes libres del primero y del último elemento tengan distintas polaridades. La experiencia demuestra que la f. e. m. total es proporcional al número de elementos. Lo mismo sucede con la resistencia. Este modo de acoplamiento presenta la siguientes propiedades: § La f. e. m. de la asociación es igual a la suma de las f. e. m. s de cada elemento. § La resistencia interior de la asociación es igual a la suma de las resistencias interiores de cada elemento. § El régimen de descarga de la asociación es igual al de un solo elemento. § La capacidad eléctrica de la asociación es igual al de un solo elemento. La intensad de corriente suministrada al circuito exterior, esta designada por: e n r R I e·n r·n R+r·n f. e. m. Número de elementos de pila Resistencia interior Resistencia exterior Intensidad de corriente f. e. m. de la asociación Resistencia interior de la asociación Resistencia total

ACOPLAMIENTO EN PARALELO El acoplamiento en PARALELO consiste en unir todos los positivos (+) por un lado y todos los polos negativos (-) por el otro lado, de modo que los puntos o conductores de unión constituyen los bornes de la agrupación. Este modo de acoplamiento presenta la siguientes propiedades: § La f. e. m. de la asociación es igual a la f. e. m. de un solo elemento. § La resistencia interior de la asociación es igual a la de un solo elemento dividido por el número de ellos. § El régimen de descarga de la asociación es igual al de un solo elemento multiplicado por el número de ellos. § La capacidad eléctrica de la asociación es igual al de un solo elemento multiplicado por el número de ellos. La intensad de corriente suministrada al circuito exterior, esta designada por: e n r R I e r/n R+(r·/n) f. e. m. Número de elementos de pila Resistencia interior Resistencia exterior Intensidad de corriente f. e. m. de la asociación Resistencia interior de la asociación Resistencia total
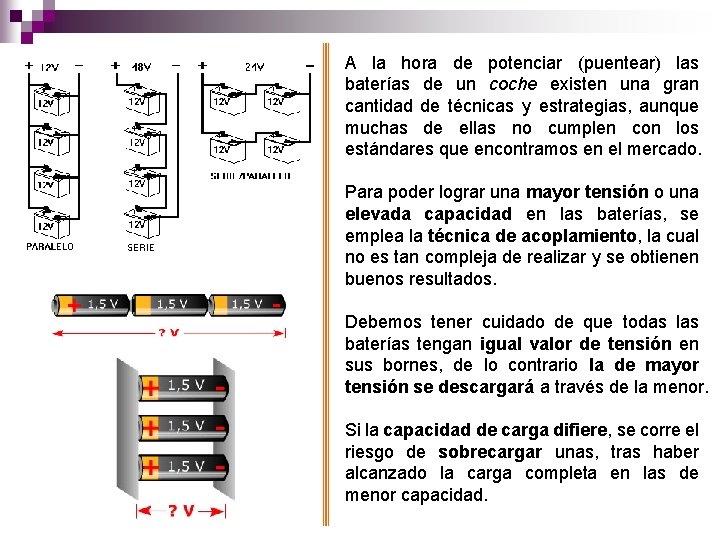
A la hora de potenciar (puentear) las baterías de un coche existen una gran cantidad de técnicas y estrategias, aunque muchas de ellas no cumplen con los estándares que encontramos en el mercado. Para poder lograr una mayor tensión o una elevada capacidad en las baterías, se emplea la técnica de acoplamiento, la cual no es tan compleja de realizar y se obtienen buenos resultados. Debemos tener cuidado de que todas las baterías tengan igual valor de tensión en sus bornes, de lo contrario la de mayor tensión se descargará a través de la menor. Si la capacidad de carga difiere, se corre el riesgo de sobrecargar unas, tras haber alcanzado la carga completa en las de menor capacidad.
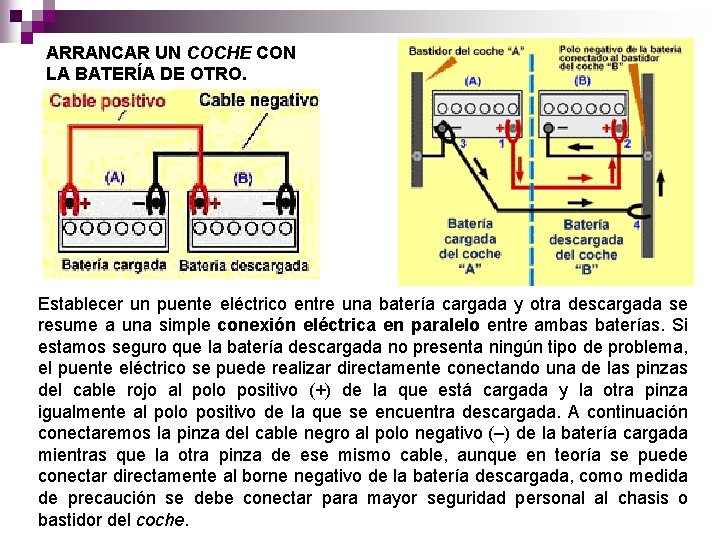
ARRANCAR UN COCHE CON LA BATERÍA DE OTRO. Establecer un puente eléctrico entre una batería cargada y otra descargada se resume a una simple conexión eléctrica en paralelo entre ambas baterías. Si estamos seguro que la batería descargada no presenta ningún tipo de problema, el puente eléctrico se puede realizar directamente conectando una de las pinzas del cable rojo al polo positivo (+) de la que está cargada y la otra pinza igualmente al polo positivo de la que se encuentra descargada. A continuación conectaremos la pinza del cable negro al polo negativo (–) de la batería cargada mientras que la otra pinza de ese mismo cable, aunque en teoría se puede conectar directamente al borne negativo de la batería descargada, como medida de precaución se debe conectar para mayor seguridad personal al chasis o bastidor del coche.
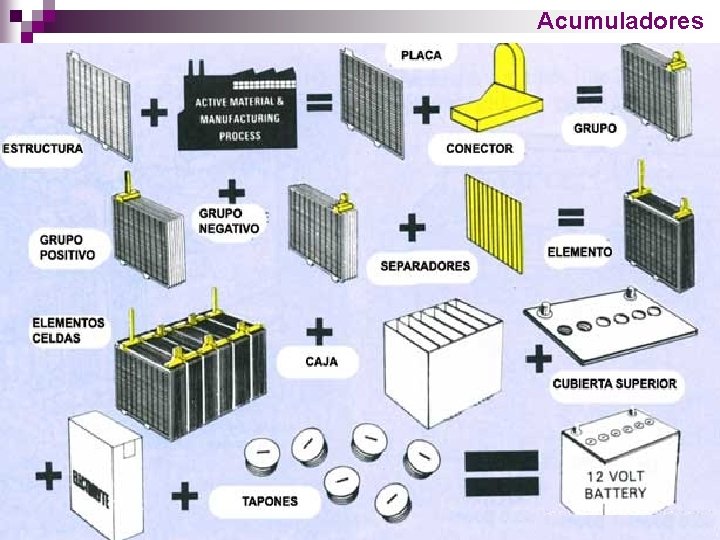
Acumuladores
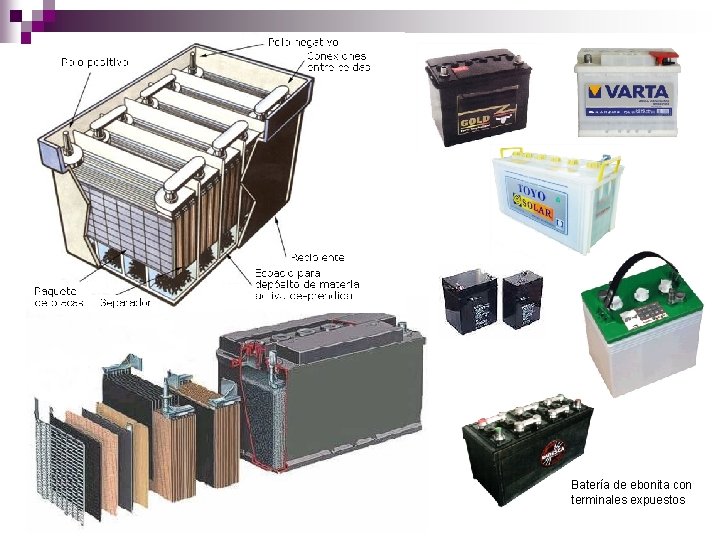
Batería de ebonita con terminales expuestos

Pilas

Funcionamiento de pila eléctrica Las pilas básicamente son dos electrodos metálicos sumergidos en un líquido, sólido o pasta que se llama electrolito. El electrolito es un conductor de iones. Cuando los electrodos reaccionan con el electrolito, en uno de los electrodos (el cátodo) se producen electrones (oxidación), y en el otro (ánodo) se produce un defecto de electrones (reducción). Cuando los electrones sobrantes del cátodo pasan al ánodo a través de un conductor externo a la pila se produce una corriente eléctrica. Como vemos, en el fondo, se trata de una reacción de oxidación y otra de reducción que se producen simultáneamente.

Tipos de acumuladores § Por lo que a sus tamaños y otras características externas se refiere, puede consultarse “tipos de pilas”, ya que muchas de ellas son comunes a pilas y acumuladores y están normalizadas. § La distinción entre pilas que utilizan un electrolito y las que utilizan dos, o entre pilas húmedas y secas, son exclusivamente de interés histórico y didáctico, pues todas las pilas que se utilizan actualmente son prefabricadas, estancas y responden a tipos bastante fijos, lo que facilita su comercialización y su uso. § Las pilas eléctricas y algunos acumuladores se presentan en unas cuantas formas normalizadas. Las más frecuentes comprenden la serie A (A, AAA, AAAA), AB, C, D, F, G, J y N, 3 R 12, 4 R 25 y sus variantes, PP 3, PP 9 y las baterías de linterna 996 y PC 926. Las características principales de todas ellas y de otros tipos menos habituales se incluyen en la tabla que puede verse en documento Word –Tipos de PILAS–.
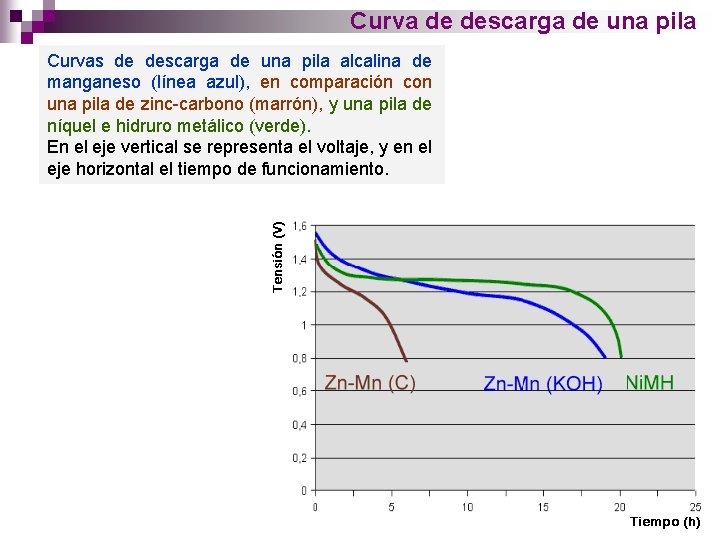
Curva de descarga de una pila Curvas de descarga de una pila alcalina de manganeso (línea azul), en comparación con una pila de zinc carbono (marrón), y una pila de níquel e hidruro metálico (verde). En el eje vertical se representa el voltaje, y en el eje horizontal el tiempo de funcionamiento.

Pilas y baterías alcalinas Las pilas alcalinas y baterías alcalinas (una batería es un conjunto de varias celdas electroquímicas individuales) son un tipo de pilas eléctricas desechables o baterías recargables que obtienen su energía de la reacción química entre el zinc y el dióxido de manganeso (Zn → Mn. O 2), empleando hidróxido de potasio como electrolito. En comparación con las pilas de zinc carbono o con las de cloruro de zinc, aunque todas producen aproximadamente 1, 5 voltios por celda o célula, las pilas alcalinas tienen una densidad de energía mayor y una vida útil más larga. En comparación con las pilas de óxido de plata, contra las que habitualmente compiten las alcalinas en el formato de botón, tienen menor densidad de energía y menor duración pero también más bajo costo. Las pilas y baterías alcalinas reciben su nombre porque contienen un electrolito alcalino de hidróxido de potasio, en lugar del cloruro de amonio en medio ácido o el cloruro de zinc electrolítico de la pilas de zinc carbono que ofrecen el mismo voltaje nominal y el mismo tamaño físico. Otros sistemas de pilas y baterías también utilizan electrolitos alcalinos, pero emplean distintos materiales activos en los electrodos.

Recarga de los acumuladores o baterías alcalinas Algunas pilas alcalinas están diseñadas para ser recargadas, pero la mayoría no lo son. Los intentos de recarga de una pila que no está preparada para este fin puede causar su ruptura, o la filtración de líquidos peligrosos, que corroen los equipos. Pila alcalina con fuga de electrolito El electrólito § Durante la descarga del acumulador el electrólito va cediendo iones de sulfato y aumentando su proporción en agua. El electrólito va rebajándose progresivamente y las placas se van recubriendo intensamente de sulfato. Por último, el electrólito puede quedar reducido a agua y las placas convertidas totalmente en sulfato. Sin embargo, mucho antes de que se llegue a este estado se pone de manifiesto la necesidad de recargarlo haciendo pasar una corriente eléctrica en sentido contrario a la descarga, con ello devolvemos los iones de sulfato a la solución volviendo a formar las placas.

Duración fuera de servicio Lo ideal sería que las reacciones químicas internas no se produjeran más que cuando la pila esté en servicio, pero la realidad es que las pilas se deterioran con el paso del tiempo, aunque no se usen, pues los electrodos resultan atacados en lo que se conoce con el nombre de acción local. Puede considerarse que una pila pierde unos 6 m. V por mes de almacenamiento, influyendo mucho en ello la temperatura. Actualmente esto no constituye un problema serio pues, dado el enorme consumo que hay de los tipos corrientes, las que se ofrecen en el comercio son de fabricación reciente. Las pilas y el medio ambiente Los metales y productos químicos constituyentes de las pilas pueden resultar perjudiciales para el medio ambiente, produciendo contaminación química. Es muy importante no tirarlas a la basura. Estudios indican que una micro pila de mercurio, puede llegar a contaminar 600. 000 litros de agua, una de zinc aire 12. 000 litros y una de óxido de plata 14. 000 litros.



- Slides: 43