Aula Prtica Atividade Enzimtica Celulase Biologia Geral e

Aula Prática Atividade Enzimática Celulase Biologia Geral e Aplicada II (SHS 0378) São Carlos, 12 de Novembro de 2020
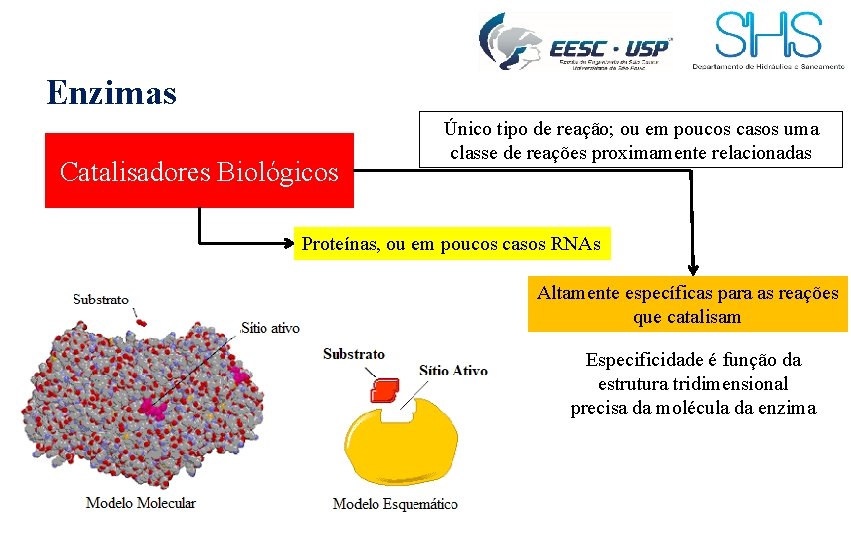
Enzimas Catalisadores Biológicos Único tipo de reação; ou em poucos casos uma classe de reações proximamente relacionadas Proteínas, ou em poucos casos RNAs Altamente específicas para as reações que catalisam Especificidade é função da estrutura tridimensional precisa da molécula da enzima
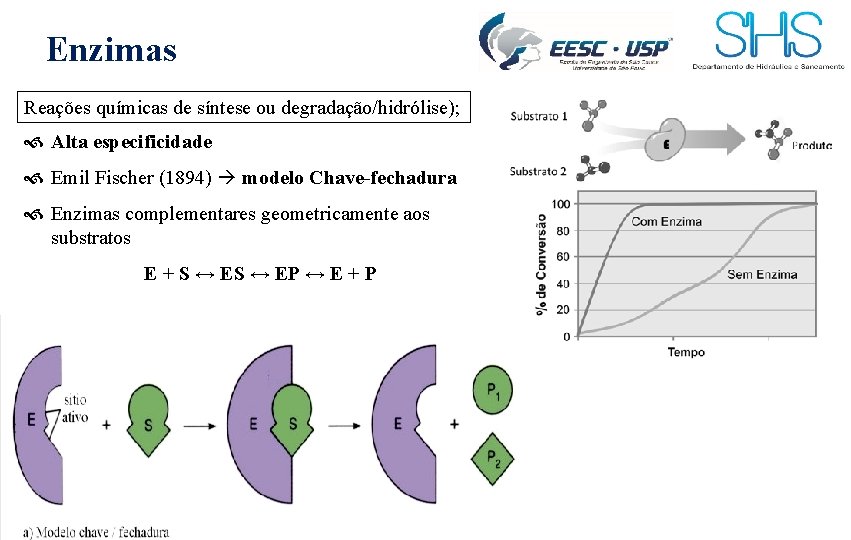
Enzimas Reações químicas de síntese ou degradação/hidrólise); Alta especificidade Emil Fischer (1894) modelo Chave-fechadura Enzimas complementares geometricamente aos substratos E + S ↔ EP ↔ E + P
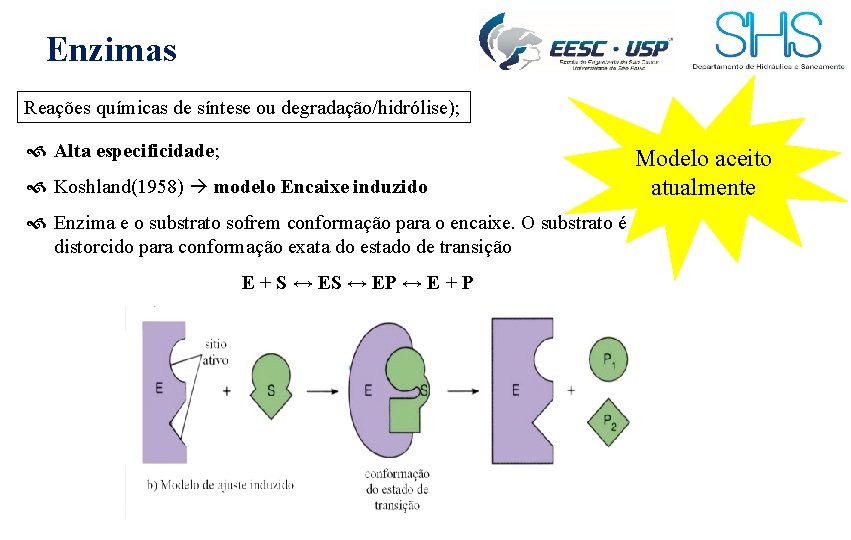
Enzimas Reações químicas de síntese ou degradação/hidrólise); Alta especificidade; Koshland(1958) modelo Encaixe induzido Enzima e o substrato sofrem conformação para o encaixe. O substrato é distorcido para conformação exata do estado de transição E + S ↔ EP ↔ E + P Modelo aceito atualmente
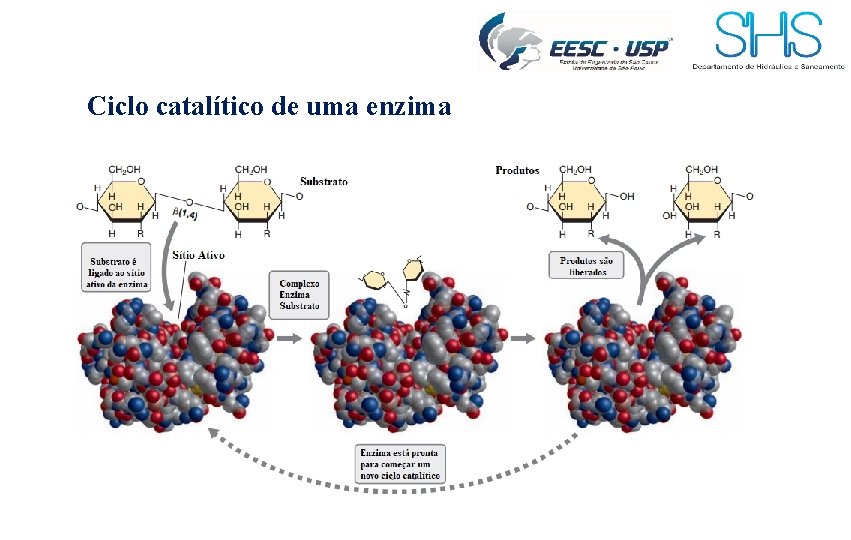
Ciclo catalítico de uma enzima
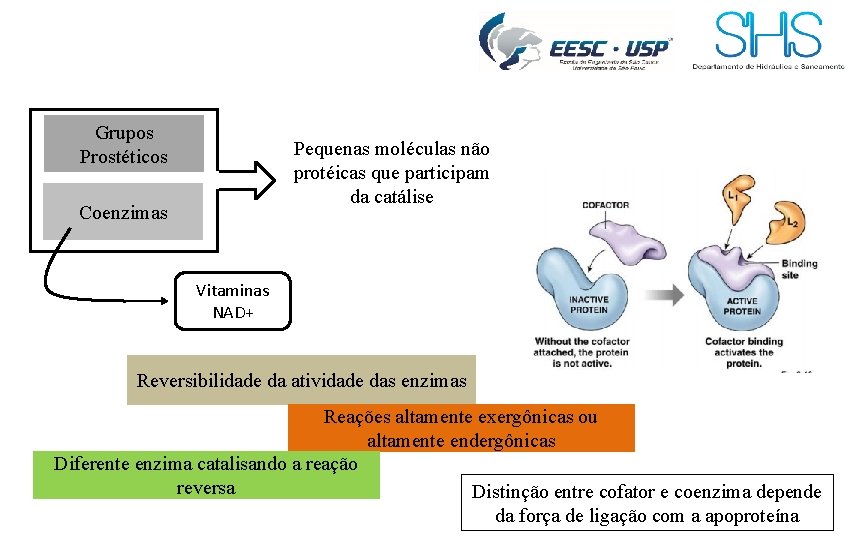
Grupos Prostéticos Pequenas moléculas não protéicas que participam da catálise Coenzimas Vitaminas NAD+ Reversibilidade da atividade das enzimas Reações altamente exergônicas ou altamente endergônicas Diferente enzima catalisando a reação reversa Distinção entre cofator e coenzima depende da força de ligação com a apoproteína
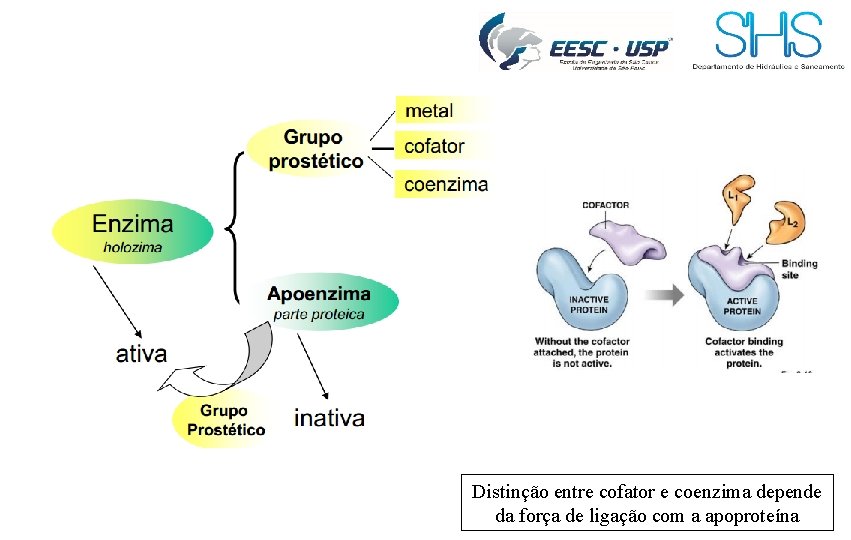
Distinção entre cofator e coenzima depende da força de ligação com a apoproteína
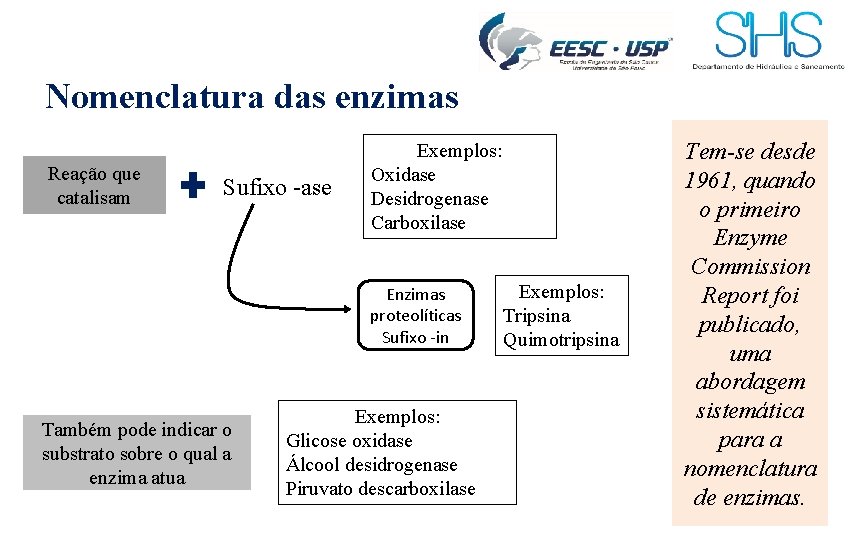
Nomenclatura das enzimas Reação que catalisam Sufixo -ase Exemplos: Oxidase Desidrogenase Carboxilase Enzimas proteolíticas Sufixo -in Também pode indicar o substrato sobre o qual a enzima atua Exemplos: Glicose oxidase Álcool desidrogenase Piruvato descarboxilase Exemplos: Tripsina Quimotripsina Tem-se desde 1961, quando o primeiro Enzyme Commission Report foi publicado, uma abordagem sistemática para a nomenclatura de enzimas.
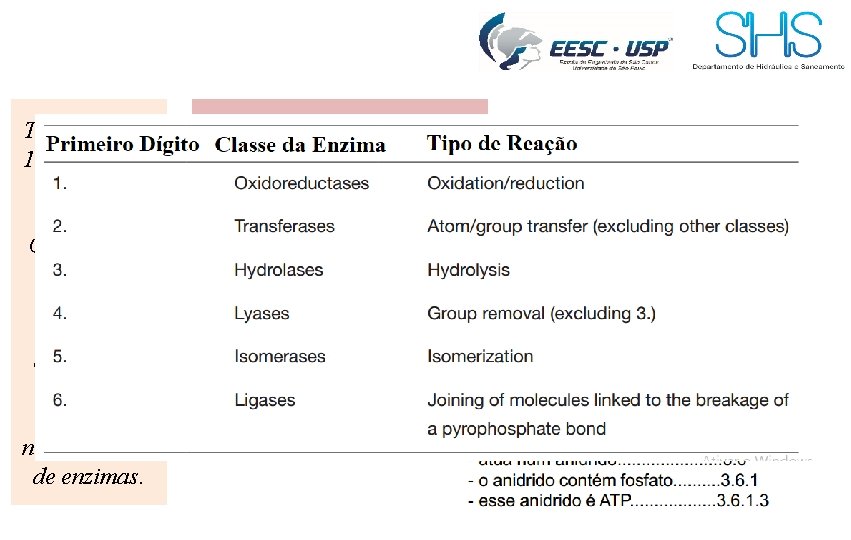
Tem-se desde 1961, quando o primeiro Enzyme Commission Report foi publicado, uma abordagem sistemática para a nomenclatura de enzimas. Todas as enzimas são descritas por um número de quatro partes Exemplo Nome trivial: lactato dehydrogenase Numeração: 1. 1. 1. 27 Diferentes significados de acordo com a natureza da reação identificada no primeiro dígito Reação que a enzima catalisa
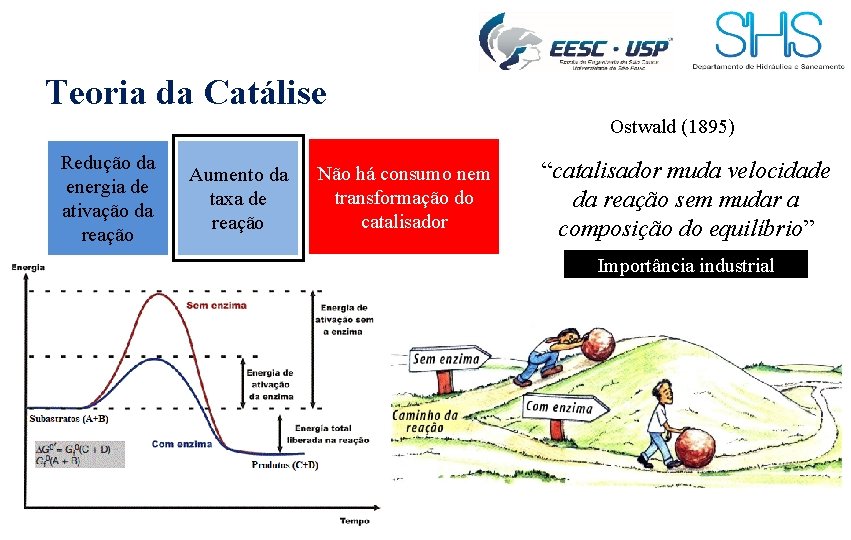
Teoria da Catálise Ostwald (1895) Redução da energia de ativação da reação Aumento da taxa de reação Não há consumo nem transformação do catalisador “catalisador muda velocidade da reação sem mudar a composição do equilíbrio” Importância industrial

- No equilíbrio da reação, as velocidades das reações se igualam Concentração de todos os reagentes não se altera mais, pode-se dizer que a reação terminou - Catalisador/Enzima acelera as velocidades de ambos os lados da reação Ponto de equilíbrio é atingido mais rápido, porém o ponto de equilíbrio não se altera em relação a reação não catalisada.
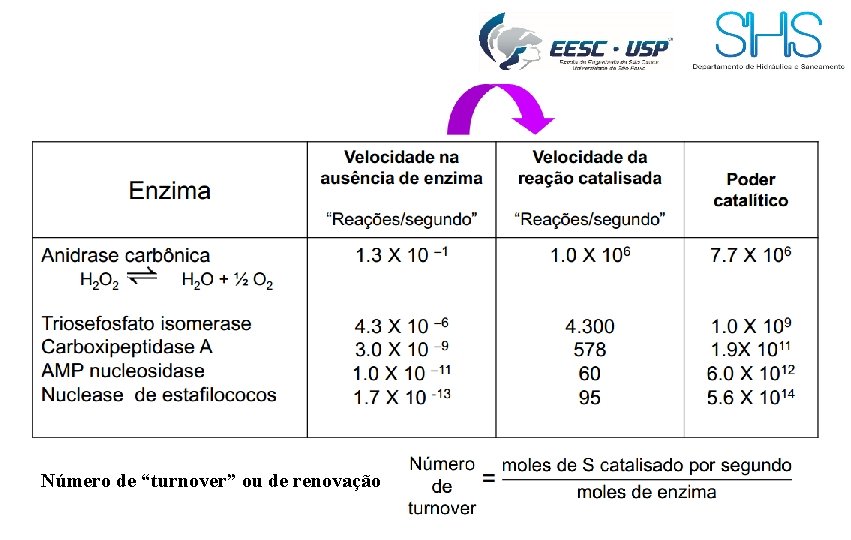
Número de “turnover” ou de renovação
Fatores que afetam a atividade enzimática p. H Afetam a estabilidade protéica Temperatura Tempo de reação Concentração dos reagentes Para se estudar o efeito isolado de um dos fatores acima, é necessário que todos os outros fatores sejam mantidos fixos.
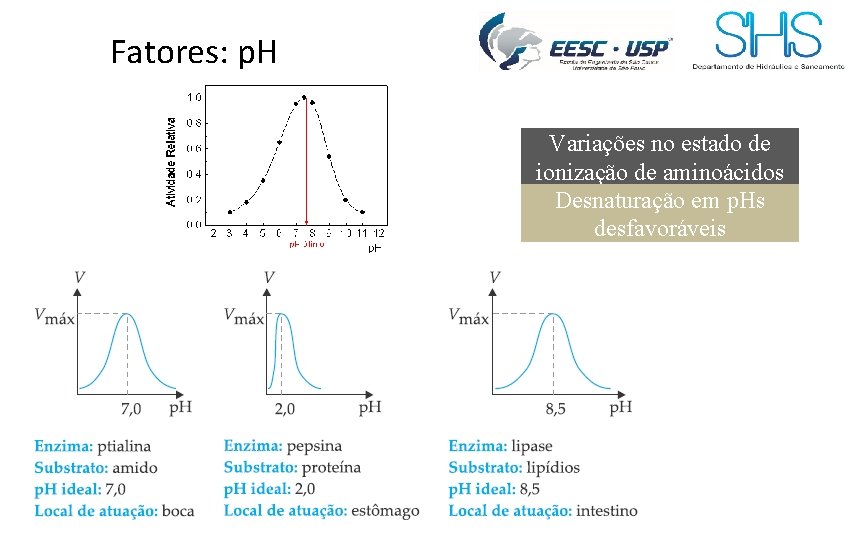
Fatores: p. H Variações no estado de ionização de aminoácidos Desnaturação em p. Hs desfavoráveis
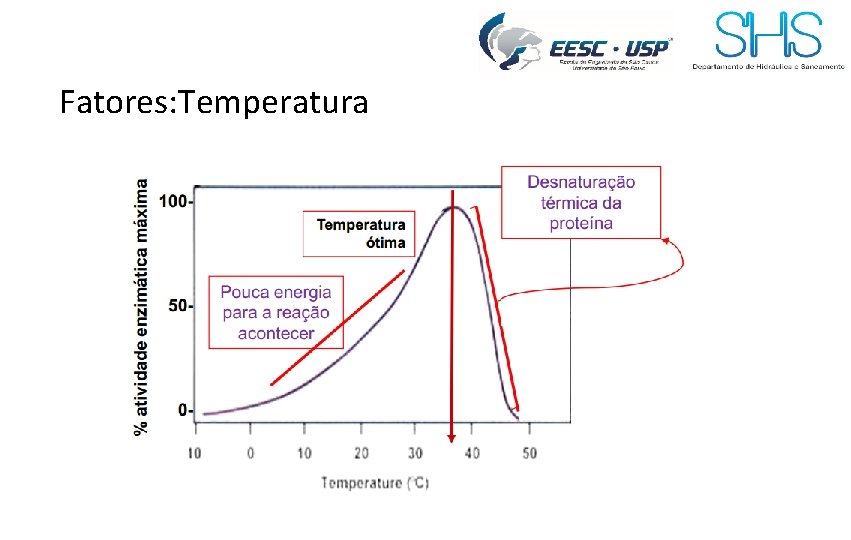
Fatores: Temperatura
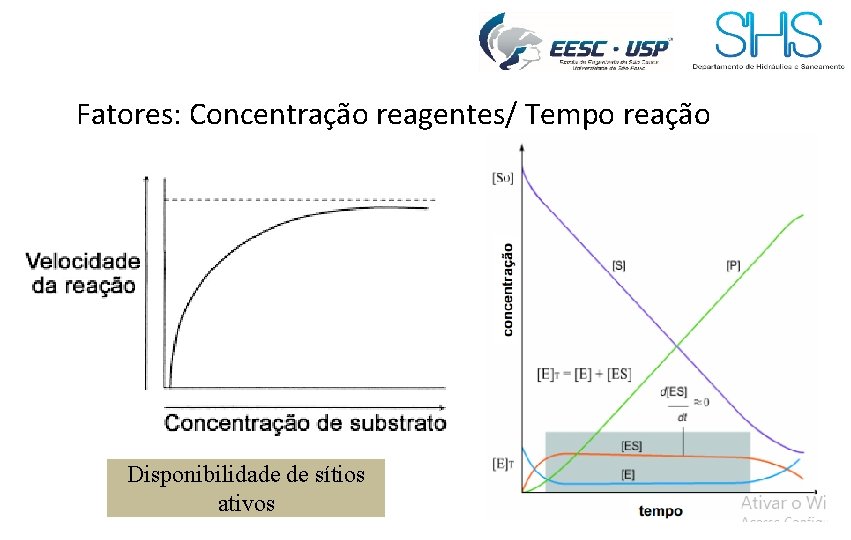
Fatores: Concentração reagentes/ Tempo reação Disponibilidade de sítios ativos
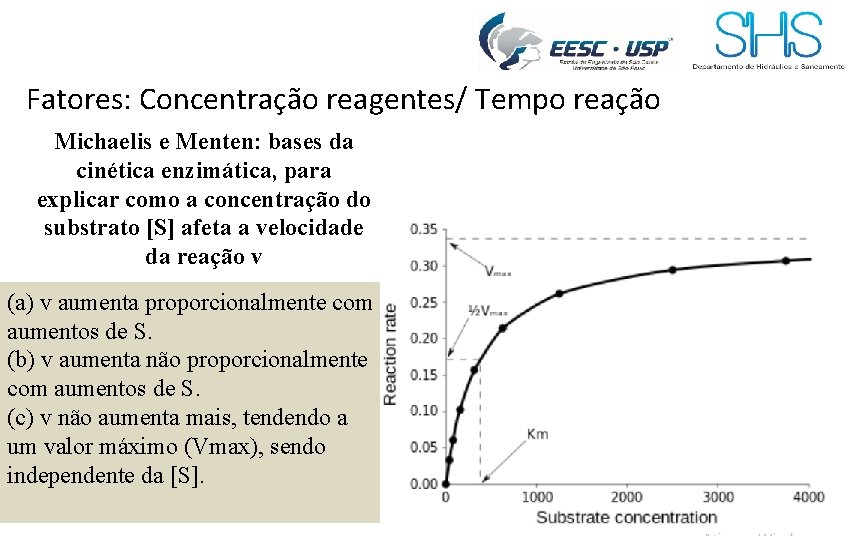
Fatores: Concentração reagentes/ Tempo reação Michaelis e Menten: bases da cinética enzimática, para explicar como a concentração do substrato [S] afeta a velocidade da reação v (a) v aumenta proporcionalmente com aumentos de S. (b) v aumenta não proporcionalmente com aumentos de S. (c) v não aumenta mais, tendendo a um valor máximo (Vmax), sendo independente da [S].

Fatores: Concentração reagentes/ Tempo reação A constante de Michaelis-Menten (KM) é um parâmetro cinético que traz informações sobre a afinidade que a enzima tem pelo substrato.

Fatores: Concentração reagentes/ Tempo reação A constante de Michaelis-Menten (KM) é um parâmetro cinético que traz informações sobre a afinidade que a enzima tem pelo substrato.
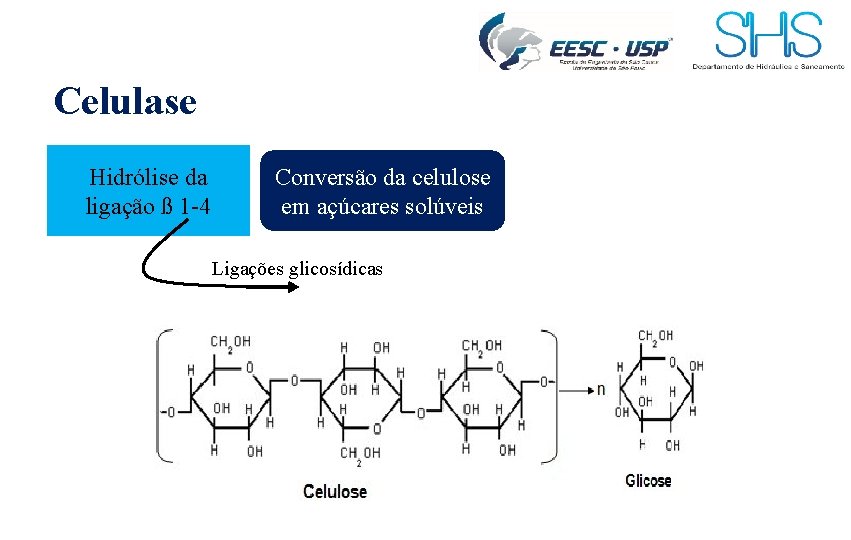
Celulase Hidrólise da ligação ß 1 -4 Conversão da celulose em açúcares solúveis Ligações glicosídicas

Celulase Estas enzimas começaram a ser estudadas durante a Segunda Guerra Mundial. A deterioração de fardas, barracas, bolsas e demais objetos dos acampamentos, fabricados de algodão, chamou a atenção de soldados das forças armadas norte-americanas, instalados nas ilhas Solomon, no Pacífico Sul. Uma linhagem de um fungo Foco das pesquisas deixou de filamentoso, identificado ser a prevenção da hidrólise posteriormente como Trichoderma viride, da celulose e passou a ser o foi isolada e a esta foi atribuída a característica de melhoramento da produção excretar enzimas capazes de das enzimas degradar celulose.
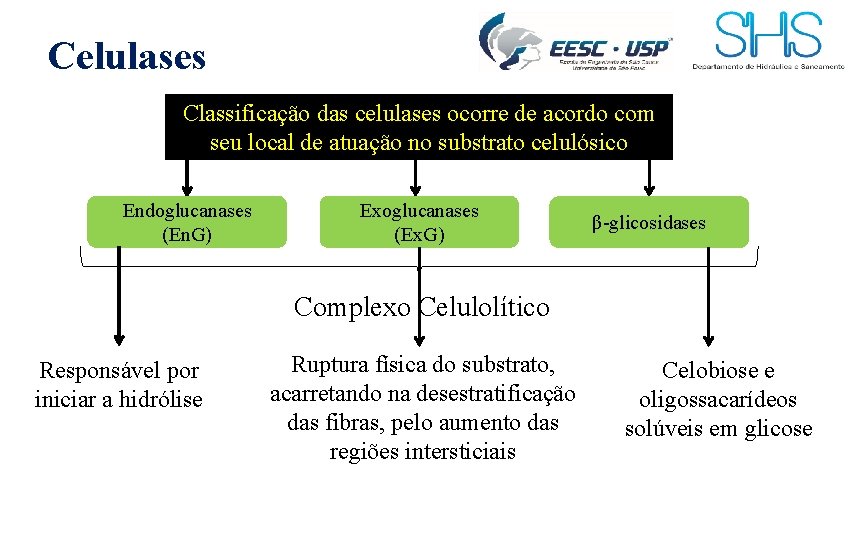
Celulases Classificação das celulases ocorre de acordo com seu local de atuação no substrato celulósico Endoglucanases (En. G) Exoglucanases (Ex. G) β-glicosidases Complexo Celulolítico Responsável por iniciar a hidrólise Ruptura física do substrato, acarretando na desestratificação das fibras, pelo aumento das regiões intersticiais Celobiose e oligossacarídeos solúveis em glicose

Aplicação: Celulase Produção: via Fermentação Grande parte das indústrias optam por produzir celulases a partir Trichoderma e Aspergillus $ Mercado biotecnológico de comercialização de enzimas para aplicações industriais movimenta altos valores anualmente Produção em escala industrial - Década de 80 Aplicação como um aditivo para ração animal, de forma a aumentar a digestibilidade de rações Insumo para a indústria de alimentos

Aplicações biotecnológicas da celulase • Indústria têxtil: – Dar melhor acabamento aos tecidos, tornando-os mais lisos, macios e com melhor caimento. – Processo de envelhecimento do jeans.

Aplicações biotecnológicas da celulase • Indústria de ração animal: – Aumentam a digestibilidade das fibras da parede celular vegetal, melhorando a conversão do alimento ingerido (pastagem) em carne e leite.

Aplicações biotecnológicas da celulase • Uma das mais emergentes aplicações das celulases é a hidrólise de biomassas. • Conversão de resíduos lignocelulósicos em glicose, por ação enzimática. • Em etapas seguintes, esse monossacarídeo pode ser utilizado para produção de biocombustíveis. Bagaço e palha de cana, talos, sabugo e palha de milho, cascas de arroz e demais grãos Restos de madeiras Resíduos sólidos urbanos Resíduos industriais Etanol, metano, hidrogênio

Aplicações biotecnológicas da celulase Conceito de biorrefinarias celulósicas Aproveitamento integral e integrado dos resíduos agroindustriais gerados em uma determinada cadeia produtiva, de modo a agregar valor à mesma Utilização de celulases na hidrólise da celulose ocorre em condições mais brandas de pressão, temperatura e p. H do que os processos químicos Elevada especificidade, eliminando a chance de ocorrência de substâncias tóxicas (furfurais e derivados de lignina)

Aplicações biotecnológicas da celulase Hidrólise enzimática da celulose e conversão dos açúcares liberados em moléculas de interesse Processo HSF, hidrólise separada SSF, sacarificação simultânea à da fermentação Etanol, ácidos orgânicos, hidrogênio, etc
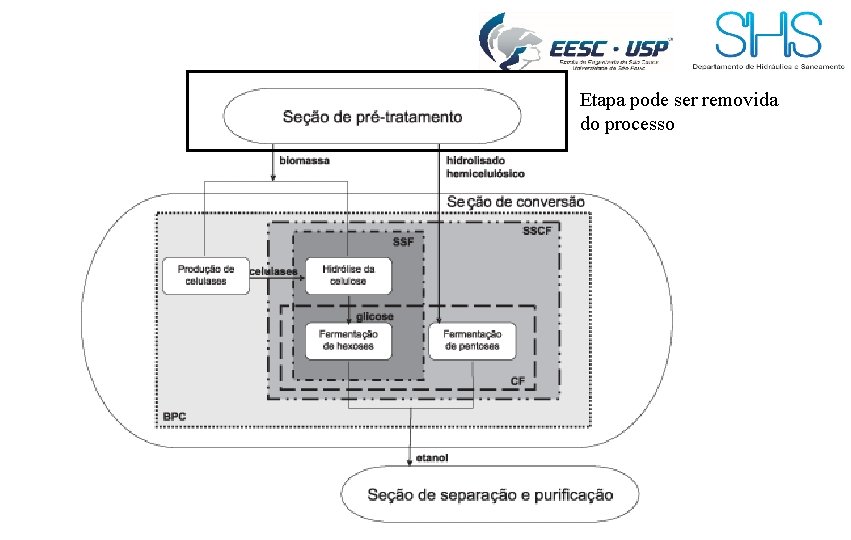
Etapa pode ser removida do processo

AULA PRÁTICA: Conceito: Papel Celulase Carboidratos solúveis A atividade de uma enzima é, geralmente, determinada por meio da quantificação dos subprodutos liberados durante a hidrólise
AULA PRÁTICA: Papel Celulase Carboidratos solúveis Objetivo: • Comparar a hidrólise enzimática sob diferentes valores de p. H, concentração de substrato e temperatura
AULA PRÁTICA: Papel Celulase • Celulase comercial Carboidratos solúveis

Hidrólise com celulase – Montagem Experimental 24, 5 m. L de tampão citrato 0, 5 m. L celulase Papel como substrato Medir a concentração de carboidratos solúveis após 40’ de reação.
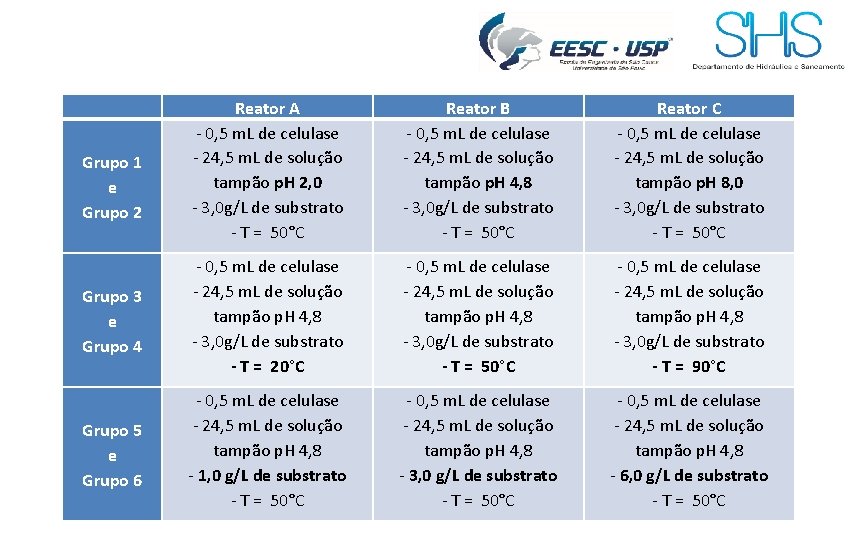
Reator A - 0, 5 m. L de celulase - 24, 5 m. L de solução tampão p. H 2, 0 - 3, 0 g/L de substrato - T = 50°C Reator B - 0, 5 m. L de celulase - 24, 5 m. L de solução tampão p. H 4, 8 - 3, 0 g/L de substrato - T = 50°C Reator C - 0, 5 m. L de celulase - 24, 5 m. L de solução tampão p. H 8, 0 - 3, 0 g/L de substrato - T = 50°C Grupo 3 e Grupo 4 - 0, 5 m. L de celulase - 24, 5 m. L de solução tampão p. H 4, 8 - 3, 0 g/L de substrato - T = 20°C - 0, 5 m. L de celulase - 24, 5 m. L de solução tampão p. H 4, 8 - 3, 0 g/L de substrato - T = 50°C - 0, 5 m. L de celulase - 24, 5 m. L de solução tampão p. H 4, 8 - 3, 0 g/L de substrato - T = 90°C Grupo 5 e Grupo 6 - 0, 5 m. L de celulase - 24, 5 m. L de solução tampão p. H 4, 8 - 1, 0 g/L de substrato - T = 50°C - 0, 5 m. L de celulase - 24, 5 m. L de solução tampão p. H 4, 8 - 3, 0 g/L de substrato - T = 50°C - 0, 5 m. L de celulase - 24, 5 m. L de solução tampão p. H 4, 8 - 6, 0 g/L de substrato - T = 50°C Grupo 1 e Grupo 2

Análise de DNS para avaliar a atividade da celulase por meio da liberação de carboidratos solúveis Após 40 minutos: 1. Coletar 1, 0 m. L do conteúdo líquido dos frascos s e transferir par a tubos contendo 0, 5 m. L de reagente DNS 2. Transferir os tubos para um termostato a 100ºC/10’ 3. Resfriar os tubos em banho de água 4. Acrescentar 5, 0 m. L de água aos tubos 5. Analisar a absorbância da amostra, usando-se o espectrofotômetro (λ 540 nm) 6. Calcular a concentração de açúcares solúveis: C = 292, 21 Abs - 4, 1945
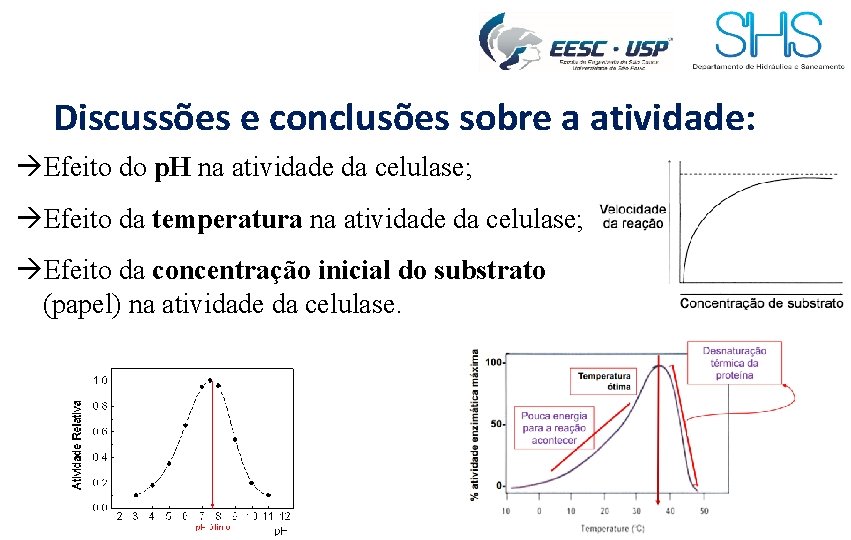
Discussões e conclusões sobre a atividade: Efeito do p. H na atividade da celulase; Efeito da temperatura na atividade da celulase; Efeito da concentração inicial do substrato (papel) na atividade da celulase.
![RESULTADOS Concentração de açúcares solúveis [g/L] Condições Temp. 50°C Subst. 3 g/L p. H RESULTADOS Concentração de açúcares solúveis [g/L] Condições Temp. 50°C Subst. 3 g/L p. H](http://slidetodoc.com/presentation_image_h2/393664506652fa224803476fb1f94af7/image-37.jpg)
RESULTADOS Concentração de açúcares solúveis [g/L] Condições Temp. 50°C Subst. 3 g/L p. H Variável Subst. 3 g/L p. H 4. 8 Temp. Variável p. H 4. 8 Temp. 50°C Subst. Variável Reator A Reator B Reator C Grupo 1 1, 06 2, 52 1, 35 Grupo 2 1, 04 2, 49 1, 29 Grupo 3 0, 19 2, 23 1, 07 Grupo 4 0, 20 2, 21 1, 05 Grupo 5 0, 77 2, 53 2, 55 Grupo 6 0, 75 2, 51 2, 52
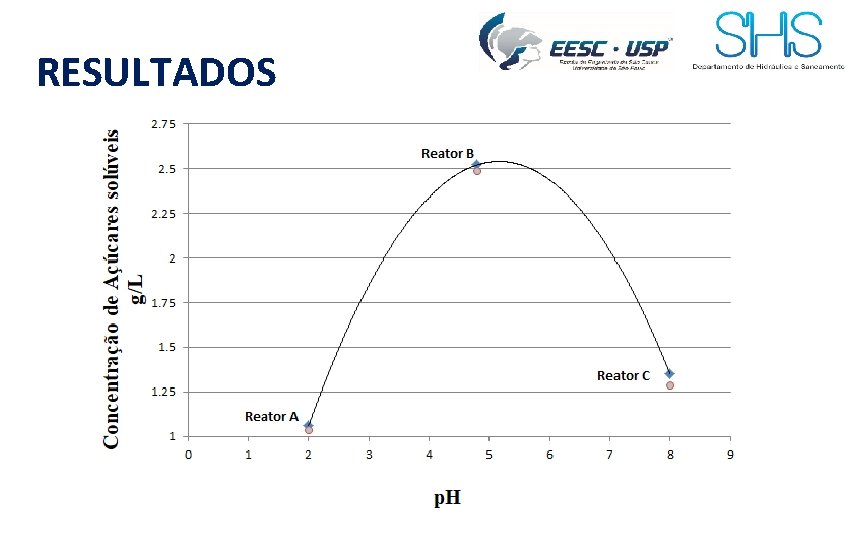
RESULTADOS
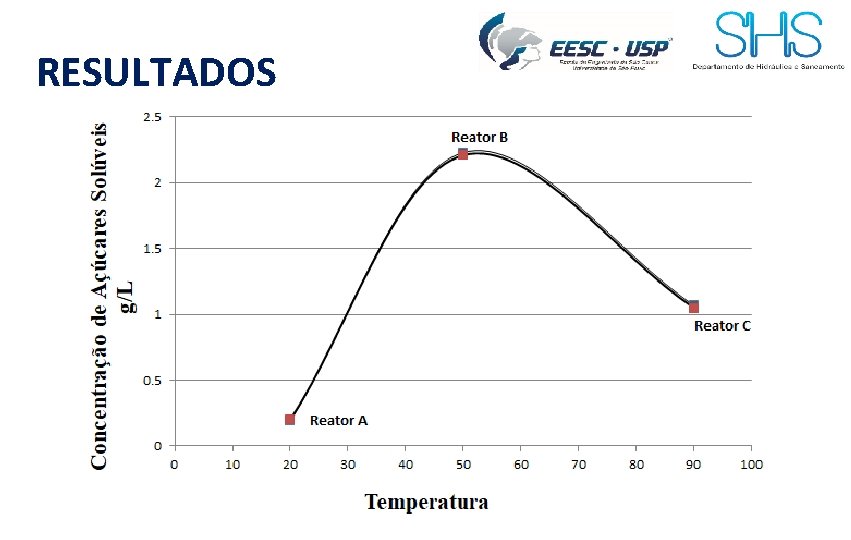
RESULTADOS
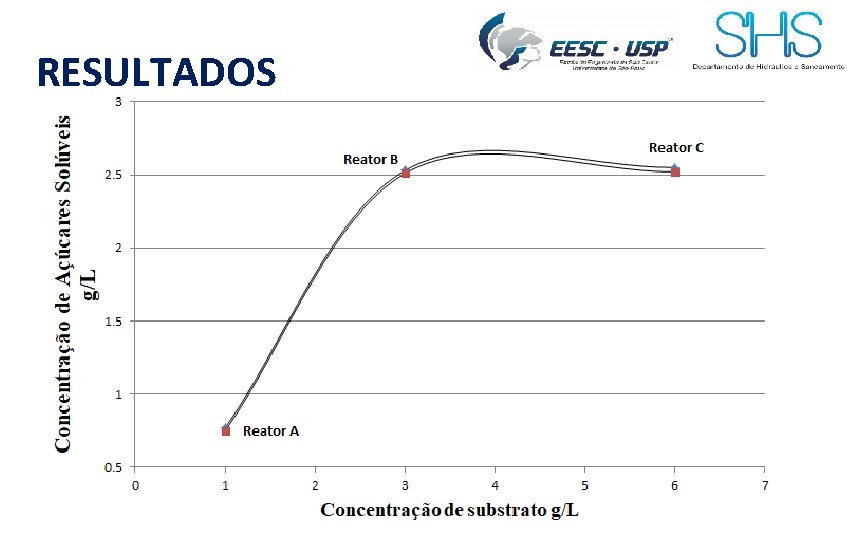
RESULTADOS

Dúvidas? “Nós nunca sabemos nada, pois o aprendizado é infindável. ”
- Slides: 41