AULA N 4 12017 CALORIMETRIA CURSO Engenharia Civil



















- Slides: 21

AULA Nº 4 – 1º/2017 CALORIMETRIA CURSO: Engenharia Civil Semestre: 3º 1 DISCIPLINA: Fundamentos de Termodinâmica PROFº: MSc. Demetrius Leão

a u g á m o Psicose. De Alfred c a a e i Hitchcock. u r f q a a u r ? l a g e á p v r e á a d d r a u e r t d g s i a a d m i e t u e n v q a i e f u d q o l ê h a c n u o a v Q b e o t d n que ratura e p tem

A necessidade de água quente • A água quente é imprescindível em hospitais, hotéis, motéis, lavanderias, restaurantes, etc. Hospitais e laboratórios 100°C ou mais Lavanderias 75°C a 85°C Cozinhas 60°C a 70°C Uso pessoal e banho 35°C a 50°C

CALOR • Calor é energia! Existindo dois corpos com temperaturas diferentes, o calor fluirá espontaneamente do corpo de maior para o de menor temperatura. Ou seja, o calor é energia térmica em trânsito. Atingido o equilíbrio térmico entre os corpos, o fluxo de calor termina. • 1 cal ≈ 4, 2 J • 1 kcal = 1000 cal

Nas mudanças de fase. . . • IMPORTANTÍSSIMO: Nas mudanças de fase de uma substância pura, a temperatura do material permanece constante. Se a substância estiver fundindo ou em ebulição, por exemplo, o calor recebido é empregado exclusivamente para o rompimento das ligações moleculares.

Quando um corpo recebe (ou perde) calor. . . • . . . Sua temperatura pode variar ou não! • Se a sua temperatura MUDAR – dizemos que o corpo recebeu CALOR SENSÍVEL (não há mudança de fase). • Se a sua temperatura NÃO MUDAR, significa que a substância está mudando de fase – dizemos que o corpo recebeu CALOR LATENTE.

Quando um corpo recebe (ou perde) calor. . . • . . . Sua temperatura pode variar ou não! • Se a sua temperatura MUDAR – dizemos que o corpo recebeu CALOR SENSÍVEL (não há mudança de fase). • Se a sua temperatura NÃO MUDAR, significa que a substância está mudando de fase – dizemos que o corpo recebeu CALOR LATENTE.

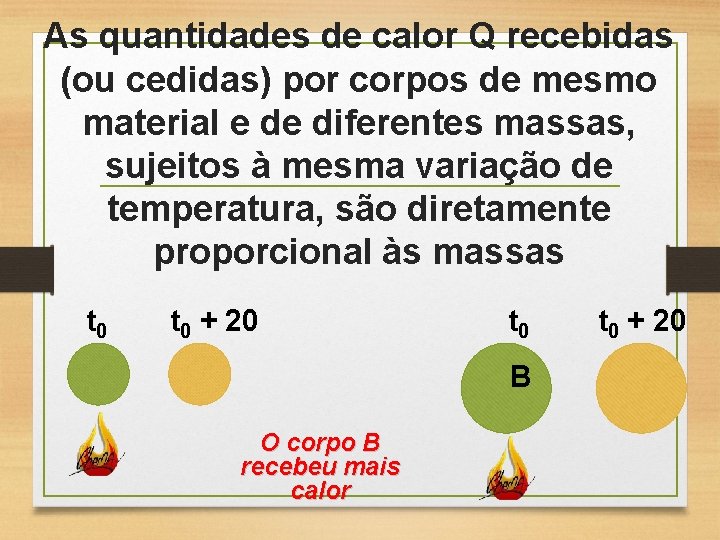
As quantidades de calor Q recebidas (ou cedidas) por corpos de mesmo material e de mesma massa são diretamente proporcionais às variações de temperatura t 0 + 20 A t 0 B O corpo B recebeu mais calor t 0 + 60

As quantidades de calor Q recebidas (ou cedidas) por corpos de mesmo material e de diferentes massas, sujeitos à mesma variação de temperatura, são diretamente proporcional às massas t 0 + 20 A t 0 B O corpo B recebeu mais calor t 0 + 20

Resumindo. . . • A quantidade de calor Q recebida (ou cedida) por um corpo é diretamente proporcional à sua massa m e a variação de temperatura Δt sofrida pelo corpo. Q = m. c. Δt

O calor específico • O calor específico c (“cezinho”) é um número associado às características de cada material (maior ou menor facilidade de trocar calor) • Ferro: 0, 11 cal/g°C • Água (liquida): 1, 0 cal/g°C

Numericamente, o calor específico é a quantidade de calor necessária para variar em 1°C a massa de 1 g da substância.

Esclarecendo um pouco mais sobre a sensação de frio e quente • Temos a sensação de frio quando perdemos calor para o meio ambiente de forma rápida.

O calor específico e as sensações de frio e quente • Materiais com baixo calor específico são mais fáceis de serem aquecidos e resfriados. Pelo contrário, quanto maior seu calor específico, maior a quantidade de calor necessária para serem aquecidos ou resfriados.

Quem está mais gelada: a maçaneta ou a porta?

Capacidade térmica de um corpo • Representa a quantidade de calor que um corpo pode trocar para sofrer uma variação unitária em sua temperatura.

EXEMPLO 1 Um corpo de massa 400 g é constituído por uma substância de calor específico 0, 6 cal/g°C. Determine: A) a quantidade de calor que o corpo deve receber para que sua temperatura varie de 15°C para 55°; B) que quantidade de calor deve ceder para que sua temperatura diminua em 15°C. C) a capacidade térmica do corpo

EXEMPLO 2 A temperatura de 100 g de água (c=1 cal/g°C) aumenta de 25°C para 65°C. Em quantos minutos será realizado esse aquecimento com uma fonte de calor que gera 50 cal por minuto?

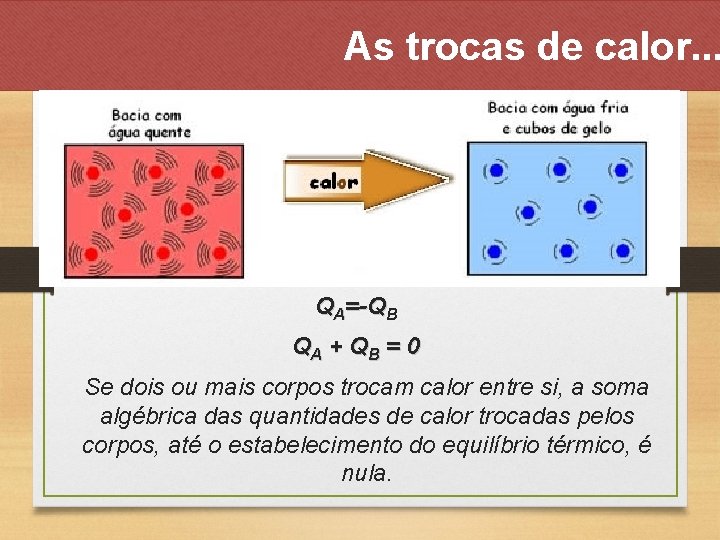
As trocas de calor. . . QA=-QB QA + Q B = 0 Se dois ou mais corpos trocam calor entre si, a soma algébrica das quantidades de calor trocadas pelos corpos, até o estabelecimento do equilíbrio térmico, é nula.

Os calorímetros. . . Os calorímetros são dispositivos especiais isolados termicamente do meio exterior. Um calorímetro ideal não participa das trocas de calor ocorridas em seu interior (mas é claro que um aparelho ideal não existe). Para efeito de cálculos, quando ele participa das trocas de calor, leva-se em conta a sua capacidade térmica C.

EXEMPLO 3 • Um broche de prata de massa 20 g a 160°C é colocado em 28 g de água inicialmente a 30°C. Qual será a temperatura final de equilíbrio térmico, admitindo trocas de calor apenas entre a prata e a água? (Dados: calor específico da prata = 0, 056 cal/g°C; calor específico da água = 1, 0 cal/g°C)