AULA 12 Fernando Luiz Pellegrini Pessoa TPQBq ESCOLA

AULA 12 Fernando Luiz Pellegrini Pessoa TPQBq ESCOLA DE QUÍMICA UNIVERSIDADE FEDERAL DO RIO DE JANEIRO

Caracterização de Fluido de Petróleo • As equações de estado cúbicas são capazes de descrever o comportamento de fases e as propriedades volumétricas, tanto de substâncias puras quanto de misturas (regras de mistura) • Qual a dificuldade de aplicá-las aos fluidos reservatórios de petróleo?

Caracterização de Fluido de Petróleo • Os fluidos reservatórios de petróleo são constituídos de milhares de componentes e sua composição é muito variável de óleo para óleo • Conseqüências: 3 Não é possível a total identificação dos componentes, o que permitiria a descrição completa do comportamento de fases e das propriedades volumétricas do fluido 3 O cálculo do equilíbrio de fases para um sistema com tantos componentes levaria muito tempo e inviabilizaria na prática as simulações dos reservatórios

Constituição do Óleo • Descrição individual: hidrocarbonetos até C 6 • Gases inorgânicos: N 2, CO 2 e H 2 S • Hidrocarbonetos não parafínicos tolueno, ciclohexano, xileno, etc. C 6 -C 9: benzeno, • Frações mais pesadas: grupos de hidrocarbonetos, determinados a partir dos seus pontos de ebulição, usando-se destilação ou cromatografia gasosa

Equações de Estado Cúbicas (EEC) • Propriedades críticas (dados de entrada): Tc, Pc, Vc, Zc, • Para o cálculo do equilíbrio de fases de fluidos de petróleo usando as EEC é preciso conhecer as propriedades críticas dos componentes ou das frações • Quando essas propriedades não estão disponíveis, são usadas correlações empíricas em termos de gravidade específica (S), temperatura normal de ebulição (Tb) e peso molecular (PM) das frações de hidrocarbonetos
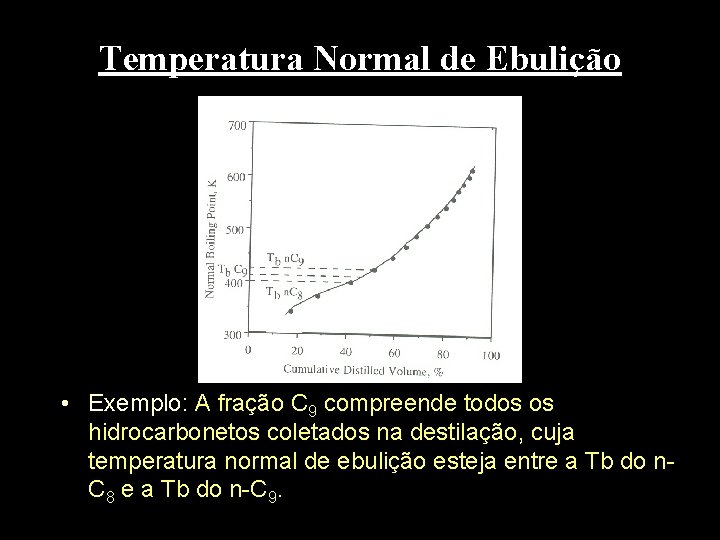
Temperatura Normal de Ebulição • Exemplo: A fração C 9 compreende todos os hidrocarbonetos coletados na destilação, cuja temperatura normal de ebulição esteja entre a Tb do n. C 8 e a Tb do n-C 9.

Fator de Watson (Kw) • Tb é a temperatura normal de ebulição (K) • S é a gravidade específica • Parafinas: 12, 5 < Kw < 13, 5 • Naftênicos: 11, 0 < Kw < 12, 5 • Aromáticos: 8, 5 < Kw < 11, 0
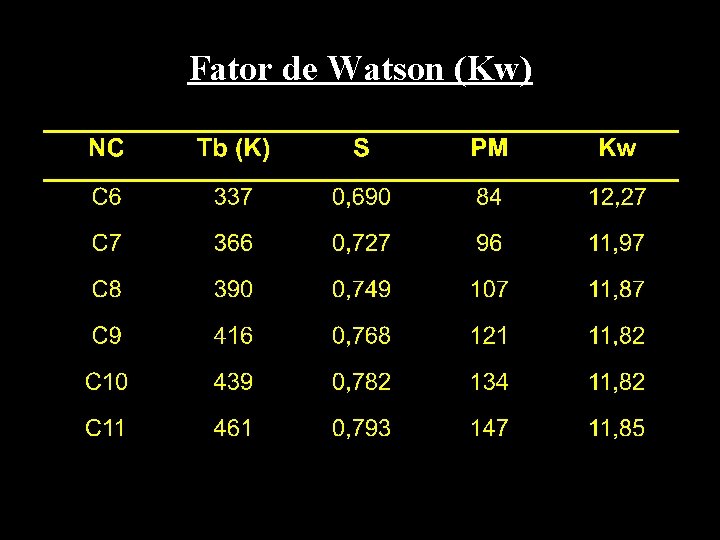
Fator de Watson (Kw)

Fator de Watson da Mistura • Correlação de Riazi-Daubert: • OBS: Essa correlação é particularmente útil quando não se conhece a temperatura de ebulição, como por exemplo para as frações pesadas. Porém, a precisão cai para PM>300 9/11/2021
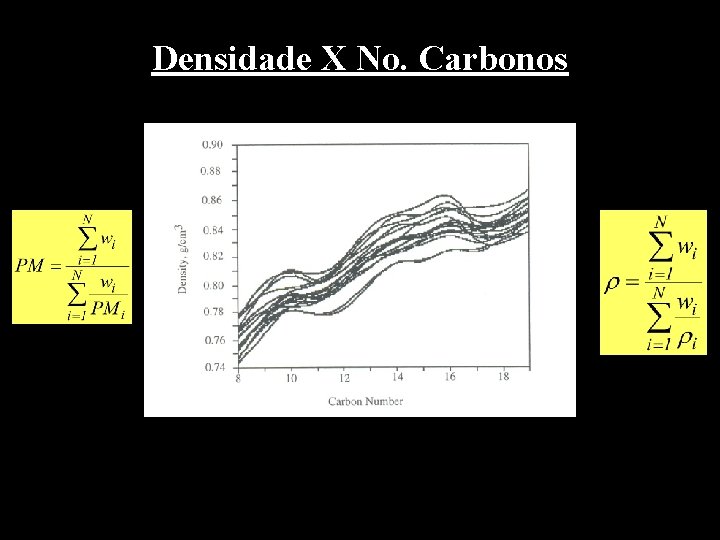
Densidade X No. Carbonos

Correlações de Lee-Kesler

Correlação de Edmister Fator acêntrico

Correlações de Riazi-Daubert • 1 e 2 podem ser quaisquer parâmetros característicos das forças intermoleculares e do tamanho molecular de uma substância. Ex. : Tb e PM, Tb e S, etc.
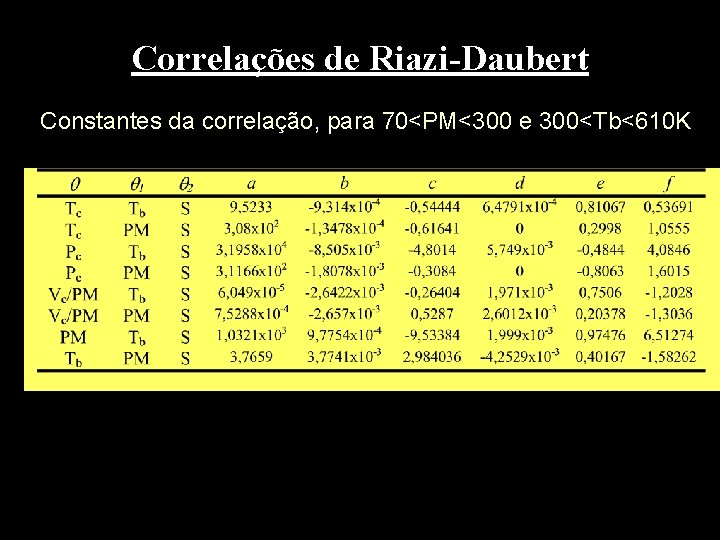
Correlações de Riazi-Daubert Constantes da correlação, para 70<PM<300 e 300<Tb<610 K

Correlações de Twu Consiste em primeiro correlacionar as propriedades das normal parafinas como referência e depois estender essas correlações para as frações de petróleo. Para isso, faz-se a diferença entre a gravidade específica da fração de hidrocarbonetos e a gravidade específica da n-parafina para o mesmo valor da temperatura de ebulição

Correlações de Twu O subscrito “p” identifica as propriedades das n-parafinas

Correlações de Twu O peso molecular das parafinas é calculado de forma implícita, pelas seguintes relações:

Correlações de Twu Para as frações de petróleo têmse as seguintes correlações: TEMPERATURA CRÍTICA 9/11/2021

Correlações de Twu Para as frações de petróleo têm-se as seguintes correlações: VOLUME CRÍTICO

Correlações de Twu Para as frações de petróleo têmse as seguintes correlações: PRESSÃO CRÍTICA 9/11/2021

Correlações de Twu Para as frações de petróleo têm-se as seguintes correlações: PESO MOLECULAR
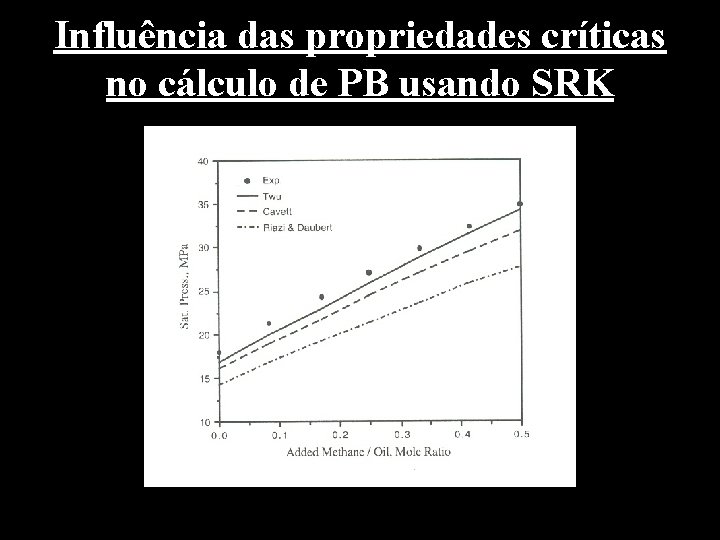
Influência das propriedades críticas no cálculo de PB usando SRK
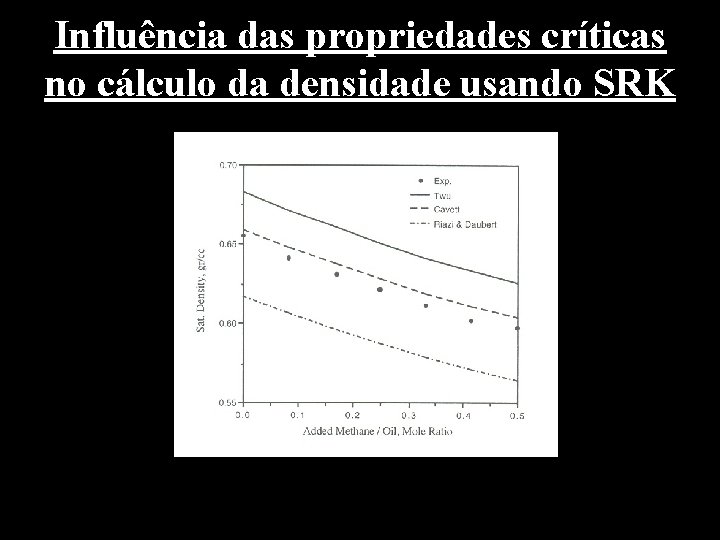
Influência das propriedades críticas no cálculo da densidade usando SRK

Observação Essas correlações foram desenvolvidas para caracterizar as frações de petróleo a partir do agrupamento por “número de carbono”. Porém, não se recomenda sua aplicação para frações cujos pontos de ebulição estejam numa faixa muito larga (C 7+). Essas frações mais pesadas (“heavy ends”) são caracterizadas usando-se outras metodologias.

Caracterização de Frações Pesadas Descrição Discreta X Descrição Contínua • D. Discreta: componentes ou grupos de componentes considerados individualmente (somatórios) • D. Contínua: propriedades dos componentes são funções matemáticas continuas (integrais) – Grande vantagem: extrapolação do cálculo das propriedade quando não há dados experimentais disponíveis
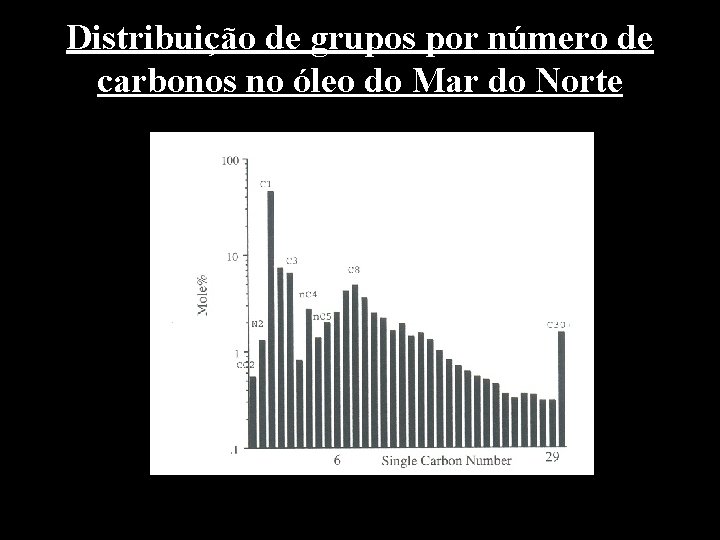
Distribuição de grupos por número de carbonos no óleo do Mar do Norte

Caracterização de Frações Pesadas Abordagem típica: DESCRIÇÃO SEMI-CONTÍNUA • Descrição Discreta: componentes leves • Descrição Contínua: componentes pesados (C 7+)

Caracterização de Frações Pesadas Descrição em função do número de carbonos • Correlação de KATZ onde x. Cn é fração molar do grupo Cn Normalmente, utiliza-se a seguinte relação linear entre o logaritmo da fração molar e o número de carbonos: onde A e B são constantes específicas de cada óleo

Caracterização de Frações Pesadas Para cálculos de equilíbrio de fases, é mais conveniente expressar a concentração em função de outras propriedades, como o peso molecular, ao invés do número de carbonos: onde é um parâmetro que depende da natureza química do grupo. Para a maioria dos casos, =4. Essa correlação sugere que a fração molar (ou fração mássica) pode ser expressa em termos do peso molecular, ao invés do número de carbonos:
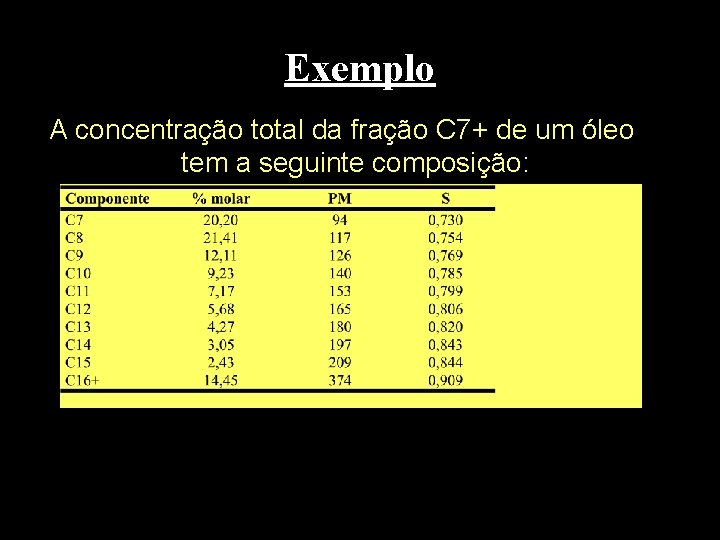
Exemplo A concentração total da fração C 7+ de um óleo tem a seguinte composição: Estenda a análise até C 30+ em função do número de carbonos

Solução do Exemplo Usando-se os dados da tabela (excluindo C 16+) é possível construir o gráfico do logaritmo da fração molar em função do peso molecular Assumindo-se uma relação praticamente linear entre o logaritmo da fração molar e o peso molecular, faz-se a regressão linear desses dados e obtém-se

Solução do Exemplo O peso molecular (PM) e a gravidade específica (S) dos grupos C 16 a C 29 são obtidos a partir da tabela de propriedades generalizadas. Substituindo-se os valores de PM na correlação obtida, calculam-se os valores das frações molares dos grupos C 16 a C 29 , conforme tabela a seguir.

Solução do Exemplo

Solução do Exemplo A fração molar do C 30+ é calculada por diferença: O peso molecular da fração C 7+ e a gravidade específica permanecem os mesmos quando se abre a fração até C 30: Logo, obtém-se

Solução do Exemplo O volume da fração C 7+ pode ser considerado igual à soma dos volumes de todos os componentes. Logo, uma abordagem análoga à usada para o peso molecular pode ser usada para calcular a gravidade específica da fração C 30: Logo, obtém-se:

Solução do Exemplo O balanço volumétrico para a fração C 7+ resulta em Logo, obtém-se:

Observação Quando a análise quantitativa da fração C 7+ não está disponível, as constantes A e B da correlação entre o logaritmo da fração molar e o peso molecular podem ser determinadas resolvendo-se o seguinte sistema de equações resultantes do balanço de massa: onde CN é o número de carbonos do componente mais pesado da mistura

Descrição Contínua das Frações Pesadas A abordagem apresentada anteriormente para a descrição das frações pesadas do petróleo, onde a concentração é uma função do número de carbono de cada fração, é essencialmente uma representação DISCRETA. Isto porque essa função só é válida para um número DISCRETO de carbonos (C 7, C 8, C 9, etc. ). Em termos matemáticos, pode-se dizer que essa função calcula o valor da integral da concentração entre os limites Cn-1 e Cn: “i” se refere a todos os componentes

Descrição Contínua das Frações Pesadas A abordagem contínua é mais apropriada para a descrição das frações pesadas do petróleo, pois, ao invés de considerar a concentração como uma função do número de carbono de cada fração, é considerada a distribuição de concentração de todos os componentes. Na prática, a abordagem contínua é mais realista, porque permite descrever a verdadeira característica dos fluidos de petróleo, constituídos de vários compostos, cujas propriedades variam tão gradualmente que não é possível identificá-las individualmente.
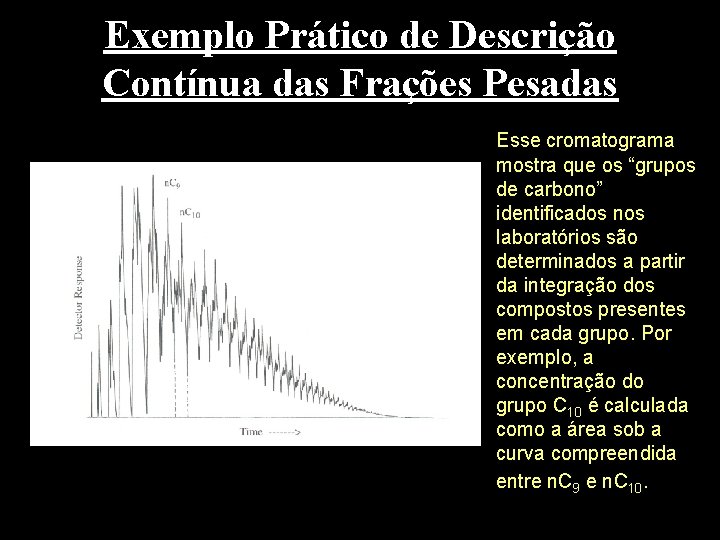
Exemplo Prático de Descrição Contínua das Frações Pesadas Esse cromatograma mostra que os “grupos de carbono” identificados nos laboratórios são determinados a partir da integração dos compostos presentes em cada grupo. Por exemplo, a concentração do grupo C 10 é calculada como a área sob a curva compreendida entre n. C 9 e n. C 10.

Descrição Contínua das Frações Pesadas A função de distribuição contínua dos componentes F(I) é dada por onde x é a concentração total de todos os “I” componentes. Se todos os componentes de um fluido são descritos pela abordagem contínua, tem-se que Na prática, adota-se a abordagem semi-contínua, ou seja, a descrição continua é aplicada apenas às frações pesadas (>C 7), e a concentração da fração pesada (x. P)é dada por

Observação A função de distribuição F(I) é normalmente escolhida de forma que o valor da sua integral seja igual a 1. Logo, esse valor deve ser considerado de forma relativa, já que a concentração se refere apenas à fração pesada. Nesse caso, para se conhecer a concentração real dos constituintes da fração pesada na mistura deve-se multiplicar a concentração relativa pelo valor de x. P, normalizando-se as suas concentrações.

Função de Distribuição Contínua A função de distribuição contínua (ou probabilidade de ocorrência) dos componentes F(I) normalmente é expressa como distribuição molar, embora possa ser usada numa base mássica (cromatografia) ou volumétrica (destilação). A variável “I” pode ser qualquer propriedade que caracterize os constituintes da mistura, como o número de carbono, o peso molecular, a temperatura de ebulição, etc. F(I) é válida para todos os valores de “I” dentro da faixa de componentes identificados, ao contrário da função discreta que só pode ser avaliada para cada número de carbono.

Função de Distribuição Contínua A fração molar de cada grupo Cn (ou pseudocomponente) é determinada por integração da função de distribuição contínua entre os limites de n-1 e n: Se I = PM (peso molecular), essa equação passa a ser: EQUAÇÃO 1 que representa a área sob a curva de F(PM) x PM entre PMn -1 e PMn

Função de Distribuição Contínua Analogamente, o peso molecular do grupo Cn (ou pseudocomponente) é determinado por integração da seguinte função entre os limites de n-1 e n: EQUAÇÃO 2 Para se resolver essa equação é preciso conhecer ou especificar uma função de distribuição contínua para F(PM). A estatística fornece várias funções de distribuição contínuas: exponencial, normal, log-normal, Weibull, gama, etc.
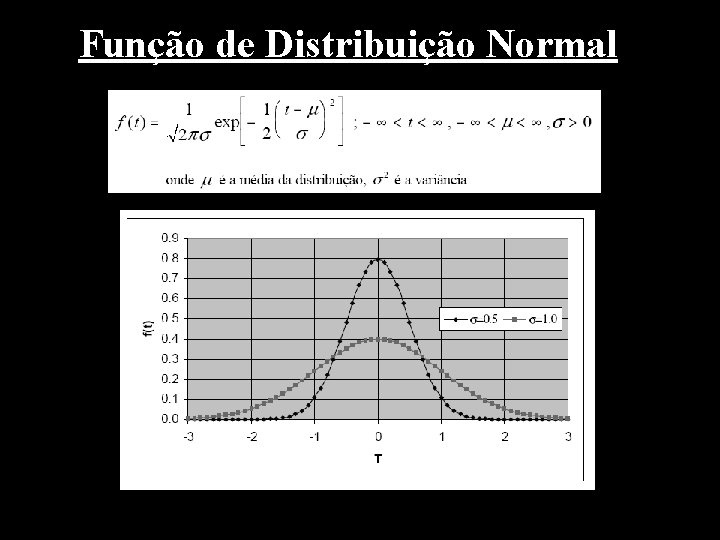
Função de Distribuição Normal
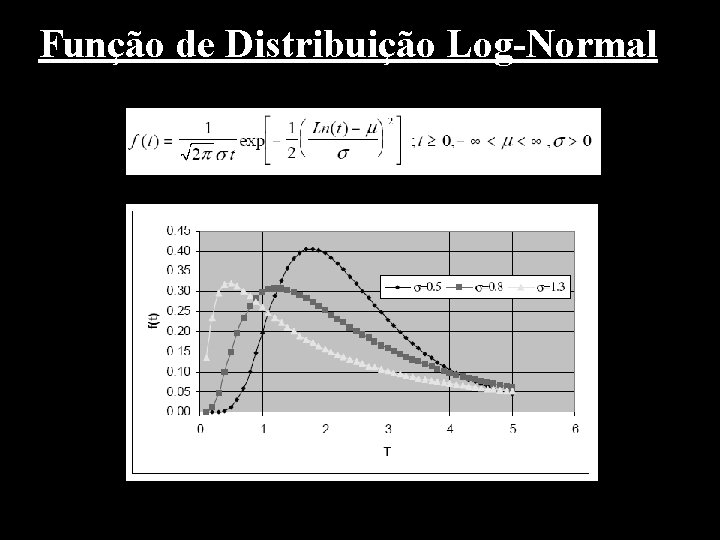
Função de Distribuição Log-Normal

Função Gama A função de distribuição contínua mais utilizada para fluidos de petróleo é a função de probabilidade GAMA. Assim, usando-se o peso molecular como variável, tem-se que EQUAÇÃO 3 onde ( ) é a função gama, definida como é o menor peso molecular da distribuição, e são parâmetros de forma da distribuição

Função Gama A média e a variância da função de distribuição contínua F(PM) são dadas respectivamente por Combinando-se essas 2 expressões obtém-se onde é o peso molecular médio da fração contínua, constituída dos compostos com peso molecular variando de ao infinito

Função Gama Para valores de 1 2, a função gama pode ser calculada através da seguinte expressão onde Ai são os parâmetros dessa aproximação polinomial. A 1 = -0, 577191652 A 5 = -0, 756704078 A 2 = 0, 988205891 A 6 = 0, 482199394 A 3 = -0, 897056937 A 7 = -0, 193527818 A 4 = 0, 918206857 A 8 = 0, 035868343 Para valores de 1 ou 2, a função gama pode ser calculada através da seguinte fórmula de recorrência:

Observação A função de distribuição gama é geralmente usada para descrever a fração C 7+ com seus parâmetros ajustados por regressão dos dados experimentais disponíveis para os grupos de carbono. Baseando-se na definição de C 7+, o valor de deve estar entre 86 e 100, ou seja, os pesos moleculares de n. C 6 e n. C 7. Na prática, pode-se considerar como um parâmetro de “ajuste fino”, e na ausência de dados experimentais dos grupos de carbono assume-se que =90.
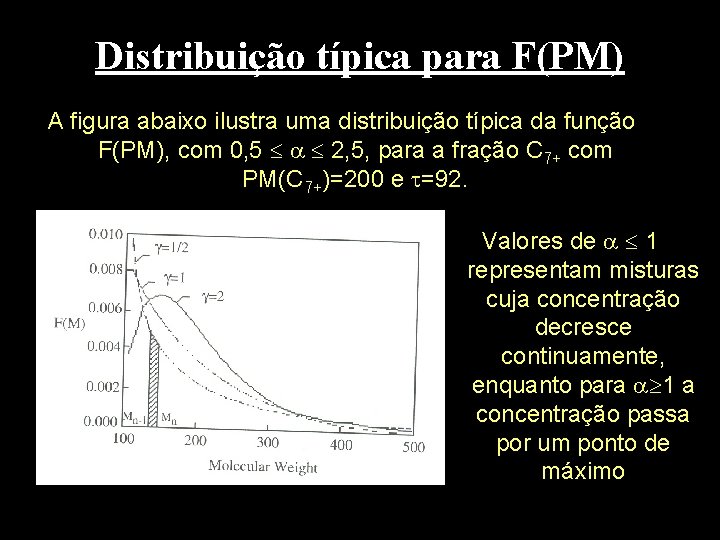
Distribuição típica para F(PM) A figura abaixo ilustra uma distribuição típica da função F(PM), com 0, 5 2, 5, para a fração C 7+ com PM(C 7+)=200 e =92. Valores de 1 representam misturas cuja concentração decresce continuamente, enquanto para 1 a concentração passa por um ponto de máximo
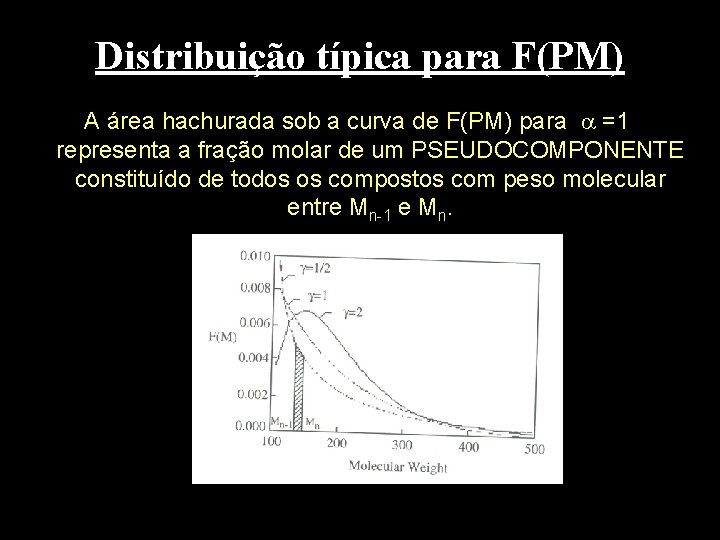
Distribuição típica para F(PM) A área hachurada sob a curva de F(PM) para =1 representa a fração molar de um PSEUDOCOMPONENTE constituído de todos os compostos com peso molecular entre Mn-1 e Mn.

Simplificando a Função Gama Para =1, a função de distribuição F(PM) passa a ser pois ou seja, a função de distribuição gama se reduz à função de distribuição exponencial, que pode ser escrita como EQUAÇÃO 4

Simplificando a Função Gama Substituindo-se a equação 4 na equação 1 e integrando-se, obtém-se: EQUAÇÃO 5 Substituindo-se a equação 4 na equação 2 e integrando-se, obtém-se: EQUAÇÃO 6

Simplificando a Função Gama A equação 5 pode ser escrita na forma logarítmica e assumindo-se Mn - Mn-1 = 100 - 86 = 14, obtém-se EQUAÇÃO 7 A equação 7 pode então ser escrita como onde
- Slides: 56