Aufbau des Periodensystems der Elemente Nebengruppenelemente und ihrer

Aufbau des Periodensystems der Elemente; Nebengruppenelemente und ihrer Einordnung in das Periodensystem Die Elektronen haben in einem Atom einer gegebenen OZ eine ganz bestimmte Anordnung, die man die Elektronenkonfiguration nennt. Das Schema der Energieniveaus des Elektrons für das Wasserstoffatom (H) und für wasserstoffähnliche Teilchen (He+, Li 2+ usw. ):

Wichtige Prinzipien, die streng gelten: Prinzip: Die Energien sind quantisiert, und können dementsprechend nummeriert werden. Die Nummern sind Hauptquantenzahlen. (n = 1, 2, 3, . . . ) Prinzip: Zu einem bestimmten Energieniveau gibt es n 2 verschiedenartige, aber energiegleiche (=entartete) Bewegungsarten. Eine bestimmte Bewegungsart eines Elektrons bezeichnet man als s-, p- oder d. Orbital.

In Atomen mit mehreren Elektronen sind die Bewegungsarten grundsätzlich ähnlich, allerdings werden gewisse Entartungen aufgehoben. Das Schema präsentiert sich dann wie folgt:

Die Auffüllung dieser Orbitale erfolgt nach gewissen Prinzipien: Auffüllprinzipien: 1. Die Niveaus werden entsprechend ihren Energien aufgefüllt; zuerst die tiefsten. 2. Pro Orbital haben zwei Elektronen Platz (Pauli-Prinzip). 3. Die zwei Elektronen, die einen Zustand besetzen, haben entgegengesetzten Spin. (Spin = Eigendrehimpuls, verbunden mit einem magnetischen Moment. Der Spin gehört untrennbar zum Elektron). 4. Haben zwei Elektronen die Wahl, ein Orbital doppelt, oder zwei Orbitalle je einfach zu besetzen, so wählen sie die zweite Möglichkeit (Hund'sche Regel).
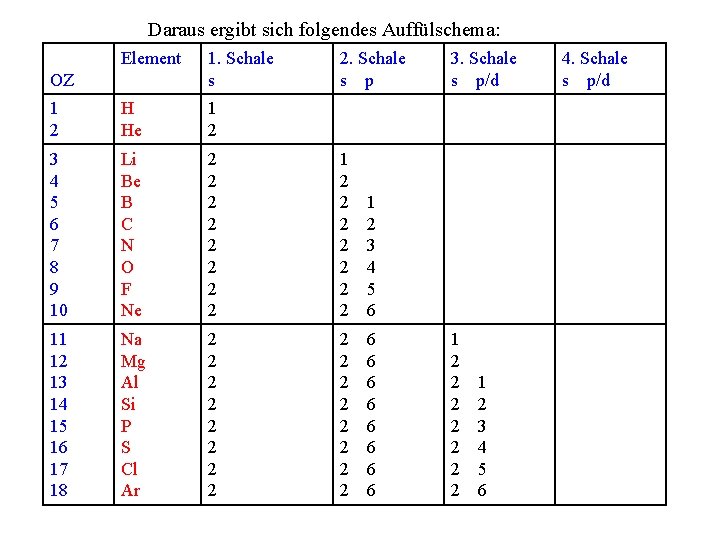
Daraus ergibt sich folgendes Auffülschema: Element 1. Schale s 1 2 H He 1 2 3 4 5 6 7 8 9 10 Li Be B C N O F Ne 2 2 2 2 1 2 3 4 5 6 11 12 13 14 15 16 17 18 Na Mg Al Si P S Cl Ar 2 2 2 2 6 6 6 6 OZ 2. Schale s p 3. Schale s p/d 1 2 2 2 2 1 2 3 4 5 6 4. Schale s p/d

19 20 2130 31 32 33 34 35 36 K Ca Sc-Zn Ga Ge As Se Br Kr 2 2 2 2 2 6 6 6 6 6 2 6 1 2 6 2 2 6/1 - 2 10 2 1 2 2 2 6/10 2 3 2 2 4 6/10 2 5 2 2 6 6/10 2 Jedes Element ist charakterisierbar 6/10 durch eine Elektronenkonfiguration. 2 Elektronenkonfiguration = Besetzungsschema der Orbitale. 6/10

Bezeichnungen im Periodensystem: Die Kolonnen sind die Gruppen. Die Zeilen im PS heissen Perioden. Innerhalb jeder Periode sind die Elemente nach steigenden Atomnummern angeordnet. Innerhalb jeder Gruppe stehen die besonders eng verwandten Elemente übereinander. Die äußeren, nicht abgeschlossenen Schalen beherbergen die VE.

Elemente, die zu einer Gruppe gehören haben analoge Valenzelektronenkonfigurationen: Elemente Gruppenname Li, Na, K, Rb, Cs, Fr Be, Mg, Ca, Ba, Sr, Ra B, Al, Ga, In, Tl C, Si, Ge, Sn, Pb N, P, As, Sb, Bi O, S, Se, Te, Po F, Cl, Br, I, At Ne, Ar, Kr, Xe, Rn Alkalimetalle Erdalkalimetalle Erdmetalle Kohlenstoffgrupp e Stickstoffgruppe Chalkogene Halogene Edelgase Valenzelektronen konfiguration ns ns 2 np 2 ns 2 np 3 ns 2 np 4 ns 2 np 5 ns 2 np 6 Total 42 Hauptgruppenelemente

3 dq 4 s 2 4 dq 5 s 2 5 dq 6 s 2 q = 1 - 10 Sc – Zn Y – Cd La, Hf – Hg 1. Übergangsmetallreihe 2. Übergangsmetallreihe 3. Übergangsmetallreihe Total: 30 Übergangsmetalle Ce – Lu 4 fq(5 d 6 s 2) q = 1 – 14 Lanthanoide oder Seltene Erden Total: 14 Elemente 5 fq(6 d 7 s 2) q = 1 – 14 Ac – Lr Actinoide Total: 14 Elemente

Oxidationsstufen HGM - stehen für chemische Bindungen nur s- und p- Elektronen zur Verfügung. Sie treten daher überwiegend in einer einzigen OZ auf, bei einigen kommen zwei OZ vor: Valenzelektronenkonfiguration: s 1 s 2 p 2 s 2 p 3 Oxidationszahlen: Li Be +I +II Na Mg +I +II K Ca +I +II Rb Sr +I +II Cs Ba +I +II Al +III Ga +III In +I +III Tl +I +III Sn +II +IV Pb +II +IV Bi +III +V

• Die Ionen haben meist Edelgaskonfiguration. Sie sind farblos und diamagnetisch. • Die HGM sind in Mehrzahl unedle Metalle. • Bei den äußeren ÜM werden die d-Orbitale (der zweitäußersten Schale) aufgefüllt. Außer den s-Elektronen der äußersten Schale können auch die d. Elektronen als VE wirken. • Die ÜM treten daher in vielen OZ auf.

Die wichtigsten OZ der 3 d-Elemente: Häufige Oxidationszahlen bei den 3 d-Elementen: Sc Ti V Cr Mn Fe Co Ni +Ib) +II)d +II +IIc) +II +IIIa) +III +IIIc) +III +IVa) +IV +Va) (+V) +VIa) (+VI) +VIIa) Cu Zn +IIb) „Edelgasionen“: Edelgas-Elektronenkonfiguration - 3 d 0 b) „Pseudo-Edelgasionen“: Edelgas-Elektronenkonfiguration und vollbesetzte 3 d-Unterschale - 3 d 10 c) stabil durch halbbesetzte 3 d-Unterschale - 3 d 5 d) in Klammern weniger häufige Oxidationszahlen a) Leere, vollbesetzte und halbbesetzte d-Unterschalen sind energetisch günstiger als andere Besetzungen {die Ligandenfeldtheorie erklärt die Stabilität weiterer Oxidationszahlen z. B. Cr 3+(d 3)}

• Die meisten Ionen der ÜM haben teilweise besetzte d-Niveaus. • Solche Ionen sind gefärbt und paramagnetisch und besitzen eine ausgeprägte Neigung zur Komplexbildung. • Unter den NGE finden sich die typischen Edelmetalle.

Die 1. Nebengruppe (Münzmetalle) Valenzelektronenkonfiguration (n-1)d 10 ns 1, n = 4, 5, 6 In allen Oxidationsstufen bilden die Münzmetalle Komplexverbindungen. Lineare zweifache Koordination Ag(I), Au(I) und Cu(I) Beispiel: Diamminsilber(I)-Komplex [H 3 N–Ag–NH 3]+ Tetraedrische Koordination Cu(I), z. B. [Cu(CN)4]3 -, Cu(I) ist sp 3 -hybridisiert. Bei Ag(I) ist der Energieaufwand für sp 3 -Hybridisierung zu groß (nur lineare Komplexe).
![Verzerrt oktaedrische Koordination [Cu(H 2 O)6]2+ ist ein tetragonal verzerrter Oktaeder. Diese Anordnung der Verzerrt oktaedrische Koordination [Cu(H 2 O)6]2+ ist ein tetragonal verzerrter Oktaeder. Diese Anordnung der](http://slidetodoc.com/presentation_image_h/1a3a2f6d9394a31e0bfc36932b8f0240/image-15.jpg)
Verzerrt oktaedrische Koordination [Cu(H 2 O)6]2+ ist ein tetragonal verzerrter Oktaeder. Diese Anordnung der Liganden ist energiegünstiger als in einem hochsymmetrischen Oktaeder. Für das Cu 2+-Ion ergibt sich durch tetragonale Verzerrung neben der LFSE im oktaedrischen Feld noch eine JTSE. Quadratisch-planare Koordination [Au. IIICl 4]- Tetrachloroaurat(III)-Ion

1. 1 Kupfer Vorkommen Kupferkies Cu. Fe. S 2 (50% aller Kupfervorkommen) Kupferglanz Cu 2 S Rotkupfererz Cu 2 O Malachit Cu 2 CO 3(OH)2 Gewinnung Aus Kupferkies wird zunächst durch Rösten das Eisen in Oxid überführt und zu Eisensilicat verschlackt: Fe. S + 1, 5 O 2 + Si. O 2 → Fe. Si. O 3 + SO 2 Aus dem verbleibenden Cu 2 S wird in Konvertern durch Einblasen von Luft das Rohkupfer erhalten: 2 Cu 2 S + 3 O 2 → 2 Cu 2 O + 2 SO 2 DH = -767 k. J/mol Cu 2 S + 2 Cu 2 O → 6 Cu + SO 2 DH = +115 k. J/mol 3 Cu 2 S + 3 O 2 → 6 Cu + 3 SO 2 DH = -652 k. J/mol Das Rohkupfer wird elektrolytisch gereinigt: Anode: Cu → Cu 2+ + 2 e- (Zn, Fe, Ni gehen in Lsg) (Anodenschlamm: Ag, Au) Kathode: Cu 2+ + 2 e- → Cu

Eigenschaften An der Luft oxidiert Kupfer langsam zu rotem Cu 2 O: 2 Cu + 0, 5 O 2 → Cu 2 O Die Cu 2 O-Schicht kann durch Reduktion mit Methanol entfernt werden: Cu. I 2 O + H 3 C-OH → 2 Cu 0 + H 2 C=O + H 2 O Ein Überzug von Cu. CO 3∙Cu(OH)2, Cu. SO 4∙Cu(OH)2 oder Cu. Cl 2∙ 3 Cu(OH)2 bezeichnet man als "Patina". Das Halbedelmetall Kupfer wird von oxidierender HNO 3 (E° = 0, 959 V) gelöst (ohne H 2 -Entwicklung!!): 3 Cu + 8 HNO 3(halbkonz. ) → 3 Cu(NO 3)2 + 2 NO↑ + 4 H 2 O oder in heißer verd. H 2 SO 4 bei Luftzutritt: Cu + 0, 5 O 2 + H 2 SO 4 → Cu. SO 4 + H 2 O
![Cu(II)-Verbindungen Cu. SO 4∙ 5 H 2 O oder [Cu(H 2 O)4]SO 4∙H 2 Cu(II)-Verbindungen Cu. SO 4∙ 5 H 2 O oder [Cu(H 2 O)4]SO 4∙H 2](http://slidetodoc.com/presentation_image_h/1a3a2f6d9394a31e0bfc36932b8f0240/image-18.jpg)
Cu(II)-Verbindungen Cu. SO 4∙ 5 H 2 O oder [Cu(H 2 O)4]SO 4∙H 2 O, blau Entwässerung: Cu. SO 4 (Nachweis kleiner Mengen H 2 O, z. B. im Alkohol) Cu. SO 4 reagiert in Wasser sauer, da Kupfer(II)-hydroxid eine schwache Base ist: p. H (0, 1 M Lsg) ≈ 3 Cu(OH)2: Cu 2+ + 2 OH- → Cu(OH)2↓ hellblau löst sich in starken Basen: Cu(OH)2 + 2 OH- → [Cu(OH)4]2 -

Bis(tartrato)cuprat(II)-Komplex: Bei Gegenwart von KNa. C 4 H 4 O 6 (Weinsäure = C 4 H 6 O 6), werden Kupfer(II)-Salze nicht gefällt. Es entsteht eine tiefblaue Lsg, in welcher der Bis(tartrato)cuprat(II)Komplex vorliegt: Unter dem Namen "Fehlingsche Lösung" dienen diese alkalische Kupfersalzlösungen zum qualitativen und quantitativen Nachweis "reduzierender Zucker" und Aldehyde z. B. in Harn. Fehlingsche Lösung: 70 g Cu. SO 4∙ 5 H 2 O im 1 L H 2 O (Fehling I) 340 g KNa. C 4 H 4 O 6 mit 100 g Na. OH im 1 L H 2 O (Fehling II)

In Gegenwart von reduzierenden Verbindungen erfolgt Reduktion zu Kupfer(I)-oxid↓ (ziegelroter Ndg. ): Versuch: Nachweis von D-Glucose Die Reaktion verläuft nicht stöchiometrisch.

Cu(I)-Verbindungen In Wasser lösliche Cu(I)-Verbindungen disproportionieren: Die Disproportionierung von Cu+ in Wasser ergibt sich aus der Spannungsreihe: Cu+ ist sein eigenes Reduktions- und Oxidationsmittel. Cu+ + Cu+ → Cu↓ + Cu 2+ DE ° = E °(Cu/Cu+) - E °(Cu/Cu 2+) = (0, 52 -0, 15) = 0, 37 V Über die freie Reaktionsenthalpie DG ergibt sich für K ein Wert von 106. Cu+ disproportioniert vollständig.

Schwerlösliche Cu(I)-Verbindungen (Cu 2 O, Cu. I, Cu. CN, Cu 2 S) sind in wässrigen Lösungen beständig. Sie sind ein Beispiel für den Einfluss der Löslichkeit auf das Redoxpotential. Cu. Cl 2 und Cu. Br 2 sind in Wasser gut löslich. Cu. I 2 ist in Wasser nicht stabil: Mit Hilfe von Iodid-Ionen kann Cu 2+ quantitativ bestimmt werden (Iodometrie). Das bei der Reduktion von Cu 2+ gebildete Iod wird durch Titration mit Thiosulfat bestimmt.

Verwendung Nach Fe und Al ist Cu das wichtigste Gebrauchsmetall. Elektroindustrie, Wärmeaustauscher (nach Ag die höhste elektrische und thermische Leitfähigkeit) Schiffbau, chemischer Apparatebau Legierungen (Cu-Zn-Legierungen: Weiß- (50 -80% Zn), Gelb (20 -50% Zn), Rot. Messing (>20% Zn)). Bronzen (Legierungen mit weniger als 40% Sn oder anderen Metallen außer Zn (Pb, Al, Ni, Si, P. . . ); Konstantan 40% Ni, elektrischer Widerstand fast unabhängig von der Temperatur. Ein essentielles Spurenelement für den Menschen und höhere Tiere. Es wird für den Aufbau von Kupferproteinen mit Enzymfunktion benötigt (z. B. Cu, Zn. Superoxid-Dismutase). SOD katalysiert die Disproportionierung von zelltoxischen Superoxid O 2 - zu O 2 und H 2 O 2.

Silber Vorkommen Silber gediegen, Ag 2 S (Argentit), Ag. Cl (Hornsilber) Ag(I)-Verbindungen Ag. NO 3 ist gut löslich in Wasser, Ausgangsprodukt für andere Silbersalze. Darstellung: 3 Ag + 4 HNO 3 → 3 Ag. NO 3 + NO↑ + 2 H 2 O Ag kann von Au abgetrennt werden, da Au nicht von HNO 3 angegrifen wird. Auf der Haut wirkt oxidierend und ätzend. - oxidierende Wirkung: - ätzende Wirkung: unter Mitwirkung von Feuchtigkeit wird Salpetersäure gebildet. Isolierung von Ag. OH ist nicht möglich: Viele Ag. I -Salze sind schwer löslich und kristallisieren als wasserfreie Salze.

Silber(I)-halogenide Lineare Silber(I)-Komplexe:
![Versuch: Reihe abnehmender Ag+-Konzentration: Ag. Cl > [Ag(NH 3)2]+ > Ag. Br > [Ag(S Versuch: Reihe abnehmender Ag+-Konzentration: Ag. Cl > [Ag(NH 3)2]+ > Ag. Br > [Ag(S](http://slidetodoc.com/presentation_image_h/1a3a2f6d9394a31e0bfc36932b8f0240/image-26.jpg)
Versuch: Reihe abnehmender Ag+-Konzentration: Ag. Cl > [Ag(NH 3)2]+ > Ag. Br > [Ag(S 2 O 3)2]3 - > Ag. I > [Ag(CN)2]- > Ag 2 S

Silberspiegel mit Tollens-Reagenz (Reagenz auf reduzierende Verbindungen, wie Zucker, Aldehyde, Hydrazide): Gemisch aus gleichen Volumina 10%-iger Ag. NO 3 -Lsg und 10%-iger Natronlauge, dem konzentrierter NH 3 bis zur Auflösung der Silberoxid-Fällung zugefügt wird. Im alkalischen Medium reduziert die Aldehydgruppe der D-Glukose Silberionen zu elementarem Silber, wobei die Aldehydgruppe selbst zur Carboxylatgruppe oxidiert wird: C 5 H 11 O 5 CHO + 2[Ag(NH 3)2]+ + 3 OH- → 2 Ag↓(Silberspiegel) + C 5 H 11 O 5 COO+ 4 NH 3 + 2 H 2 O Gealtertes Tollens-Reagenz ist wegen der möglichen Bildung von Knallsilber (Silberfulminat, Ag. ONC) explosionsgefährlich; das Reagenz kann nach Gebrauch durch Salzsäurezugabe vernichtet werden.

Verwendung Silber ist ein starkes Gift für Mikroorganismen (Ag+-Ionen blockieren die Wirkung der Thio-Enzyme). Silberne Essgeräte sind hygienisch. Das schwärzliche "Anlaufen" des Silbers an der Luft beruht auf einer Reaktion mit den Spuren von H 2 S, wobei sich schwarzes Silbersulfid bildet: 2 Ag + H 2 S + 0, 5 O 2 → Ag 2 S↓ + H 2 O, das z. B. durch Berühren mit Al-Folie in verdünnter Na 2 CO 3 -Lsg. leicht wieder zu Ag reduziert werden kann.

Gold Vorkommen Hauptsächlich gediegen, goldhaltiger Quarz Si. O 2 Gewinnung Goldwaschen Amalgamierung Cyanidlaugerei - das Gold mittels einer alkalischen Kalium- oder Natriumcyanid. Lsg. ausgelaugt wird: 4 Au 0 + 2 H 2 O + O 2 + 8 KCN → 4 K[Au. I(CN)2] + 4 KOH 2[Au(CN)2]- + Zn-Staub → [Zn(CN)4]2 - + 2 Au↓ Rohgold wird wie Rohkupfer elektrolysiert. Der Anodenschlamm dieser Elektrolyse enthält die sehr wertvollen Platinmetalle (Pt, Pd, Rh, Ir). In ähnlicher Weise wird Ag erhalten. E°(Au/Au+) = 1, 69 V Au + 2 CN- → [Au(CN)2]-, E = +0, 20 V Starke Verschiebung (um 1, 49 V) des Goldpotentials durch Komplexierung. Das Silberpotential (E(Ag/Ag+) = 0, 80 V) wird aus dem gleichen Grund (Bildung von [Ag(CN)2]-) um 1, 11 V erniedrigt (E = -0, 31 V).

Gold(III)-Verbindungen Gold weist positivere Standardredoxpotentiale als alle anderen Metalle. LM für Gold: starke Oxidationsmittel wie Chlorwasser und "Königswasser" oder Komplexbildner wie KCN bei Luftzutritt. Tetrachlorogold(III)-säure - Ausgangsprodukt für alle anderen Au(III)Verbindungen. Das Au(III)-Ion ist ein starkes Oxidationsmittel und tritt in wässr. Lsg. wegen seiner starken Komplexbildungstendenz nur in Form von Komplexen (KOZ 4, z. B. [Au. Cl 4]-, [Au. Cl 3(H 2 O)], [Au(NH 3)4]3+) auf.

Gold(I)-Verbindungen Das farblose Au(I)-Ion zeigt eine große Neigung zu disproportionieren: Nur in Form schwerlöslicher Verbindungen (Au. I, Au 2 S) oder stabiler Komplexe ([Au(CN)2]-), ist Au(I) wasserbeständig. Au(I) bevorzugt die lineare Koordination. Verwendung Goldlegierungen mit 70% Au, mehreren Pt-Metallen, Ag, Cu und Zn in der Dentaltechnik als Zahnersatz. Bemerkenswert für Gold ist seine Dehn- und Walzbarkeit (Blattgold)
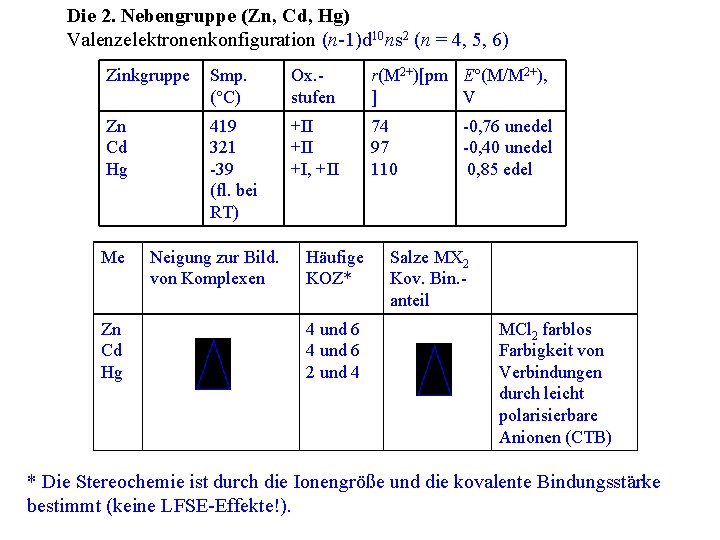
Die 2. Nebengruppe (Zn, Cd, Hg) Valenzelektronenkonfiguration (n-1)d 10 ns 2 (n = 4, 5, 6) Zinkgruppe Smp. (°C) Ox. stufen r(M 2+)[pm E°(M/M 2+), ] V Zn Cd Hg 419 321 -39 (fl. bei RT) +II +I, +II 74 97 110 Me Zn Cd Hg Neigung zur Bild. von Komplexen Häufige KOZ* 4 und 6 2 und 4 -0, 76 unedel -0, 40 unedel 0, 85 edel Salze MX 2 Kov. Bin. anteil MCl 2 farblos Farbigkeit von Verbindungen durch leicht polarisierbare Anionen (CTB) * Die Stereochemie ist durch die Ionengröße und die kovalente Bindungsstärke bestimmt (keine LFSE-Effekte!).

Zink Vorkommen Zinkspat (Zn. CO 3), Zinkblende (Zn. S) Gewinnung * Cd kommt in der Natur fast immer als Begleiter des Zn vor (Cd. S, Cd. CO 3).

Reaktionen An der Luft ist Zn beständig (Schutzschicht Zn. O und Zn(OH)2∙Zn. CO 3). Deshalb findet Verwendung für Dachbedeckungen, Verzinken von Eisenblech und Eisendraht. Zn löst sich in Säuren und Laugen: Zn + 2 H+ → Zn 2+ + H 2↑ Zn + 2 OH- + 2 H 2 O → [Zn(OH)4]2 - + H 2↑ Hochreines Zink wird nicht angegriffen (H 2 -Überspannung ≈ 0, 7 V, kinetische Hemmung für die Entladung der H 3 O+-Ionen auf der Zinkoberfläche). Versuch: Zn + verd. HCl → sehr schwache H 2 -Entwicklung Zn + Cu 2+ + verd. HCl → heftige H 2 -Entwicklung Erklärung: Zn + Cu 2+ → Zn 2+ + Cu↓

Kupfer scheidet sich auf dem Zink ab. Durch Verunreinigung bilden es sich Lokalelemente: Auf der Cu-Oberfläche besteht keine kinetische Hemmung für die Reduktion der Hydronium-Ionen. Lokalelemente sind wichtig bei der Korrosion. Schutzschichten auf Eisen aus Metallen, die edler als Eisen sind (Cr, Sn, Ni), beschleunigen bei ihrer Verletzung die Korrosion von Fe durch die Bildung eines Lokalelements. E°/V Zn/Zn 2+ -0, 76 Fe/Fe 2+ -0, 41 Sn/Sn 2+ -0, 14
![Verbindungen Zn(II)-sulfat-Heptahydrat [Zn(H 2 O)6]SO 4∙H 2 O Darstellung: Zn. O + H 2 Verbindungen Zn(II)-sulfat-Heptahydrat [Zn(H 2 O)6]SO 4∙H 2 O Darstellung: Zn. O + H 2](http://slidetodoc.com/presentation_image_h/1a3a2f6d9394a31e0bfc36932b8f0240/image-36.jpg)
Verbindungen Zn(II)-sulfat-Heptahydrat [Zn(H 2 O)6]SO 4∙H 2 O Darstellung: Zn. O + H 2 SO 4 → Zn. SO 4 + H 2 O Nur Zn(OH)2 von den Hydroxiden der 2. NG ist amphoter:

Verwendung Zn. S emittiert beim Bestrahlen mit UV-, g-Strahlen, Kathodenstrahlen sichtbares Licht. Dotierungen (etwa 1 : 104) mit Cu oder Ag-Verbindungen verbessern den Effekt und wirken als farbgebende Komponente. Farbfernsehen: Zn. S: Cu, Al (grün) Zn. S: Ag (blau) Zn. S wird als Weißpigment verwendet, im Gemisch mit Ba. SO 4 als Lithopone bekannt. Zn in galvanischen Elementen Zn-Mn. O 2 -Primärzelle (Georges Leclanche, 1860) Zink-Kohle-Batterie Trockenbatterie - der Elektrolyt, eine wässr. Lsg. von Zn. Cl 2 und NH 4 Cl, wird durch eine quellfähige Substanz, z. B. Mehl, immobilisiert.
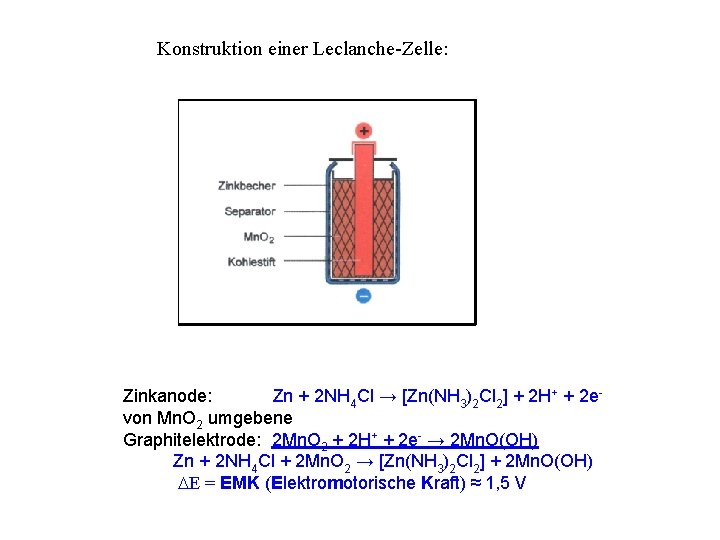
Konstruktion einer Leclanche-Zelle: Zinkanode: Zn + 2 NH 4 Cl → [Zn(NH 3)2 Cl 2] + 2 H+ + 2 evon Mn. O 2 umgebene Graphitelektrode: 2 Mn. O 2 + 2 H+ + 2 e- → 2 Mn. O(OH) Zn + 2 NH 4 Cl + 2 Mn. O 2 → [Zn(NH 3)2 Cl 2] + 2 Mn. O(OH) DE = EMK (Elektromotorische Kraft) ≈ 1, 5 V

Wideraufladbare Zn-Mn. O 2 -Zelle Die Reduktion zu Mn. II wird vermieden. Das erreicht man durch Limitierung der Zn-Aktivmasse. Anode(-): Zn + 4 OH- → [Zn(OH)4]2 - + 2 e. Kathode(+): 2 Mn. O 2 + 2 H 2 O + 2 e- → 2 Mn. O(OH) + 2 OH________________________ Zink ist essentiel für Menschen, Tiere, Pflanzen. Der Mensch enthält durchschnittlich 40 mg Zn pro kg (Bedarf ~ 22 mg Zn pro Tag). Zn 2+ ist ein elektrophiler Polarisator (Lewis-Säure):

Cadmium Die Chemie des Cd 2+ ist der des Zn 2+ sehr ähnlich, wenn auch kleine Unterschiede gibt, z. B. Cd(OH)2 ist nicht amphoter. Versuch:

Nachweis von Cd 2+ neben Cu 2+ Die Reaktion von CN- mit Cu 2+ ist vergleichbar mit der Reaktion des I- mit Cu 2+ (CN- = Pseudohalogenid): Cu 2+ + 2 CN- → Cu. CN↓ + 0, 5 (CN)2 (sehr giftig!) Im CN- Überschuß löst sich Cu. CN: Cu. CN + 3 CN- → [Cu(CN)4]3 Verwendung Korrosionschutz "Woodsches Metall": leicht schmelzende Legierung für Schmelzsicherung: 50% Bi, 25% Pb, 12, 5% Sn, 12, 5% Cd.

Quecksilber Hg besitzt eine Ausgeprägte Affinität zu Schwefel! Vorkommen, Gewinnung Zinnober (Hg. S) Vakuumdestillation Hg(II)-Verbindungen Hg 2+ + 2 OH- → Hg. O↓ + H 2 O (Hg 2+ bildet kein Hydroxid) gelber amorpfer Ndg. (krist. Hg. O ist rot gefärbt) Hg. Cl 2, Sublimat, lineare Moleküle mit kovalenten Bindungen (Cl-Hg-Cl), dissoziiert in wässr. Lsg. nur wenig in die Ionen. Hg. S Hg 2+ + S 2 - → Hg. S↓ schwarz Lp(Hg. S) = 1, 6 ∙ 10 -54 mol 2/l 2 Die Löslichkeit der Hg(II)-Verbindungen nimmt in folgender Reihe ab: Hg(NO 3)2 > Hg. Cl 2 > Hg. Br 2 > Hg. I 2 > Hg. S Die Abnahme der Löslichkeit lässt sich nach dem HSAB-Konzept erklären.

Hg. I 2 a)Hg. Cl 2 + 2 KI → Hg. I 2↓ + 2 Clrot a)Hg. I 2 ist dimorph und zeigt Thermochromie: c) Im Überschuß von I- löst sich das rote Hg. I 2 unter Bildung des farblosen Tetraiodomercurat(II)-Komplexes auf: Hg. I 2 + 2 I- → [Hg. I 4]2 d) Optische Thermometer rot schwarz
![Nesslers Reagenz Eine alkalische Lsg. von [Hg. I 4]2 - dient zum qualitativen und Nesslers Reagenz Eine alkalische Lsg. von [Hg. I 4]2 - dient zum qualitativen und](http://slidetodoc.com/presentation_image_h/1a3a2f6d9394a31e0bfc36932b8f0240/image-44.jpg)
Nesslers Reagenz Eine alkalische Lsg. von [Hg. I 4]2 - dient zum qualitativen und quantitativen Nachweis von NH 3 und Ammonium-Verbind. , wobei sich das schwerlösliche braune Iodid der Millonschen Base {[Hg 2 N]∞(OH) ∞} bildet. N. R. : Eine Lösung von 11 g KI und 15 g Hg. I 2 in 100 ml Wasser, die mit dem gleichen Vol. 6 M Na. OH vermischt ist. NH 3 + 2[Hg. I 4]2 - + 3 OH- → [Hg 2 N]I∙H 2 O↓ + 2 H 2 O + 7 Igelbbraune Lsg. → braune Flocken Nachweis von Hg(II) und Hg(I) Reduktion mit salzsaurer Sn. Cl 2 -Lsg. : 2 Hg. Cl 2 + Sn. Cl 3 - + Cl- → Hg 2 Cl 2↓ + [Sn. Cl 6]2 weiß Hg 2 Cl 2 + Sn. Cl 3 - + Cl- → 2 Hg↓ + [Sn. Cl 6]2 fein verteiltes Hg färbt die Lsg. grau

Hg(I)-Verbindungen Hg(I)-Salze enthalten das dimere Ion Hg 22+ (mit einer kovalenten Bindung zwischen den Hg-Atomen). Hg 22+ kann zu Hg 2+ und Hg disproportionieren: Hg 2 Cl 2 wird auch als schön schwarz bezeichnet, da bei der Behandlung mit NH 3 eine Schwarzfärbung sichtbar wird: Verwendung Bildung von Legierungen (Amalgame) zum Füllen von Barometern und Manometern Quecksilberlampen

Die 6. Nebengruppe Valenzelektronenkonfigurationen: Cr 3 d 54 s 1 Mo 4 d 55 s 1 W 5 d 46 s 2 Aufgrund der Lanthanoiden-Kontraktion sind die beiden schweren Elemente Mo und W einander recht ähnlich. Die Unterschiede zum Cr sind deutlich. Die maximale Oxidationszahl (OZ) ist +VI. Sie ist die stabilste OZ des Mo und W. Im Gegensatz zu den Wolframaten sind die Chromate daher starke Oxidationsmittel. Für Mo und W ist die Bildung komplizierter Polyanionen mit meist oktaedrischer Koordination typisch.

Beim Chrom gibt es nur wenige Spezies mit tetraedrischer Koordination. Die stabilste Oxidationsstufe des Chroms ist +III. Chrom(III) bildet zahlreiche oktaedrische Komplexverbindungen. Eine entsprechende Komplexchemie gibt es beim Mo und W nicht. Cr(II) wirkt reduzierend. Stabile Mo(II)- und W(II)-Verbindungen sind Clusterverbindungen, deren Stabilität durch Metall-Bindungen zustande kommt. Bei allen Metallen gibt es M(II)-Verbindungen mit Metall-Metall. Vierfachbindungen.

Chrom Vorkommen Chromit (Chromeisenstein) Fe. Cr 2 O 4 Darstellung Chrom ist das wichtigste Legierungselement für nichtrostende und hitzbeständige Stähle. Eisen-Chrom-Legierungen mit etwa 60% Cr erhält man durch Reduktion von Chromit Koks im Elektroofen: Diese Legierungen enthalten Carbide. Kohlenstoffarmes Ferrochrom wird durch Reduktion von Chromit Silicochrom (ca. 30% Si) gewonnen. Chrommetall wird aluminotermisch hergestellt: Cr 2 O 3 + 2 Al → Al 2 O 3 + 2 Cr Zur Verchromung von Stahl werden Cr(VI)-Lösungen, zur Gewinnung von Chrommetall Cr(III)-Lösungen elektrolysiert.

Eigenschaften: Das recht unedle Chrom (Cr → Cr 3+ + 3 e- E° = – 0, 74 V) löst sich leicht in nichtoxidierenden Säuren wie HCl unter H 2 -Entwicklung auf. Das Metall ist gegenüber starken Oxidationsmitteln wie konz. HNO 3 und sogar kaltes Königswasser durch die Bildung von sehr dichten Oxidhaut (Passivierung) inert. Verbindungen Oxidationsstufe +II (d 4): Cr(II)-Verb. sind starke Reduktionsmittel. Durch Abgabe eines Elektrons entsteht aus der d 4 -Konfiguration von Cr(II) die stabilste d 3 -Konfiguration von Cr(III). Cr + 2 HCl → Cr 2+ + H 2↑ + 2 Cl– Cr. Cl 2 ist in H 2 O stabil bei Luftausschluss, himmelblaue Lsg. durch [Cr(H 2 O)6]2+.
![Oxidationsstufe +III (d 3): Die stabilste OZ des Chroms ist +III. [Cr(H 2 O)6]3+ Oxidationsstufe +III (d 3): Die stabilste OZ des Chroms ist +III. [Cr(H 2 O)6]3+](http://slidetodoc.com/presentation_image_h/1a3a2f6d9394a31e0bfc36932b8f0240/image-50.jpg)
Oxidationsstufe +III (d 3): Die stabilste OZ des Chroms ist +III. [Cr(H 2 O)6]3+ - violett. [Cr(H 2 O)6]2(SO 4)3 und [Cr(H 2 O)6]Cl 3 reagieren sauer: Chrom(III)-chlorid, [Cr(H 2 O)6]Cl 3 löst sich in Wasser mit dunkelgrüner Farbe auf. Beim stehen färbt sich die Lsg. langsam heller blaugrün und schliesslich violett (Hydratations-isomerie): Beim Erwärmen spielt sich der umgekehrte Vorgang ab.

Cr(OH)3(amphoter): Redoxverhalten: Cr 3+ ist im sauren und neutralen Milieu stabil, nur stärkste Oxidationsmittel können Cr 3+ zu Chromat oxidieren. Im basischen Milieu kann Cr 3+ dagegen bereits durch milde Oxidationsmittel oxidiert werden.

Oxidationsschmelze In der alkalischen Schmelze wird Cr 3+ durch NO 3 - zu gelbem Chromat oxidiert: Cr 2 O 3 entsteht beim Verbrennen des Cr im O 2 oder durch Zersetzung von Ammoniumdichromat. Chemischer Vulkan: Cr(III)-Komplexe Die Elektronenkonfiguration d 3 liefert bei oktaedrischer Koordination eine große LFSE. Es gibt eine große Zahl stabiler Komplexe mit typische Farben. Die magnetischen Momente liegen beim „spin-only“-Wert, der für 3 ungepaarte Elektronen 3, 87 B. M. beträgt. Beispiele: [Cr(H 2 O)6]3+ violett, [Cr(NH 3)6]3+ gelb

Oxidationsstufe +VI (d 0): stabil nur in Oxoverbindungen (Ausnahme Cr. F 6), wirken alle sehr stark oxidierend. Cr. O 42 - Chromat gelb Cr 2 O 72 - Dichromat orange Cr. O 3 rot In Lsgen mit p. H > 6 liegt das tetraedrisch gebaute Cr. O 42 - vor. Zwischen p. H = 2 und p. H = 6 sind das Ion HCr. O 4 - und das Ion Cr 2 O 72 - im Gleichgewicht. p. H-abhängiges Gleichgewicht:

Dies wird bei der Ba 2+/Sr 2+-Trennung gebraucht. Aus einer Cr 2 O 72 - -Lsg. erzeugt man durch Einstellung eines bestimmten p. H-Wertes eine Cr. O 42 - -Konzentration, die zur Ausfällung des schweren löslichen Ba. Cr. O 4 (Lp = 8· 10 -11), nicht aber zur Überschreitung des größeren Löslichkeitsproduktes von Sr. Cr. O 4 (Lp = 3, 0∙ 10 -5) ausreicht. Bei Zusatz von konz. H 2 SO 4 zu Chromaten bildet sich das äußerst giftige Crom(VI)-oxid Cr. O 3, das wegen der leichten Sauerstoffabgabe ein sehr kräftiges Oxidationsmittel darstellt.

Saure Dichromatlösungen sind starke Oxidationsmittel (2 Cr 3+/Cr 2 O 72 -; E° = +1, 33 V)! Im alkalischen Bereich vorliegende Chromate oxidieren viel schwächer (Cr(OH)3/Cr. O 42 -; E° = 0, 13 V)! Die oxidative Eigenschaft der Chromate wird im Alkoholteströhrchen ausgenutzt: 2 Cr. O 42 - + 3 CH 2 OH + 10 H+ → 2 Cr 3+ + 3 CHO + 8 H 2 O gelb grün Nachweis als Chrom(VI)-peroxid, Cr. O 5: Cr(VI)-Ionen bilden in salpeter- bzw. schwefelsaurer Lsg. in der Kälte mit H 2 O 2 blaues Chrom(VI)-peroxid, Cr. O 5: Cr 2 O 72 - + 4 H 2 O 2 + 2 H+ → 2 Cr. O 5 + 5 H 2 O orange blau Die Reaktion ist für Cr(VI) spezifisch. Nach einiger Zeit schlägt die blaue Farbe in grün oder violett um: 4 Cr. O 5 + 12 H+ → 4 Cr 3+ + 6 H 2 O + 7 O 2↑ blau grün

Mit Ether kann Cr. O 5 aus der wässrigen Lsg. ausgeschütelt werden. Es entsteht das Cr. O 5(OEt 2)-Addukt, in dem das Cr. O 5 stabilisiert wird. Das Addukt hat eine verzerrt pentagonal-pyramidale Struktur: Cr-Carboxylate: Cr(II)-acetat war seit langem als anomal bekannt, weil es rot und fast diamagnetisch ist, während die einkernigen Cr(II)-Verbindungen blau oder violett und stark paramagnetisch sind. Später wurde gezeigt, dass das Acetat die folgende Struktur besitzt:
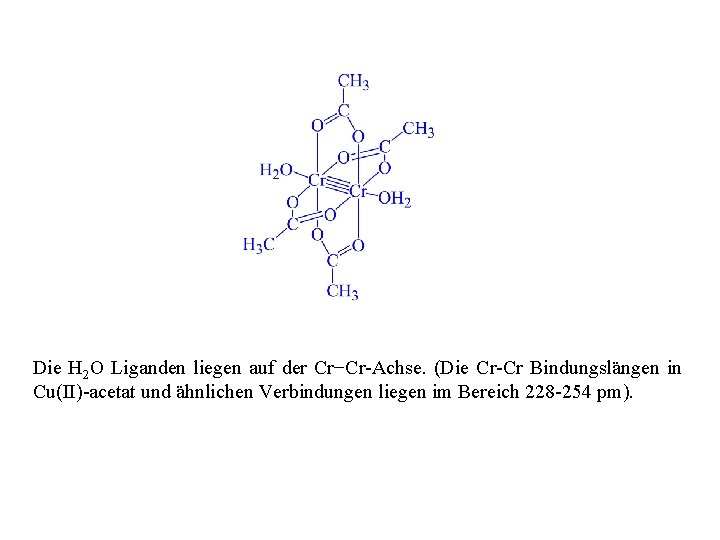
Die H 2 O Liganden liegen auf der Cr−Cr-Achse. (Die Cr-Cr Bindungslängen in Cu(II)-acetat und ähnlichen Verbindungen liegen im Bereich 228 -254 pm).

Molybdän und Wolfram Vorkommen Molybdänglanz Mo. S 2 Wulfenit (Gelbbleierz) Pb. Mo. O 4 Wolframit (Mn, Fe)WO 4 Scheelit Ca. WO 4 Darstellung Zuerst wird Mo. S 2 durch Rösten bei 400 -650°C in das Trioxid überführt. Mo. O 3 kann durch Sublimation bei 1200°C gereinigt werden. Dieses wird bei 1100°C mit H 2 zu Molybdän reduziert: Mo. O 3 + 3 H 2 → Mo + 3 H 2 O Scheelit wird mit konzentrierter HCl umgesetzt: Ca. WO 4 + 2 HCl → Ca. Cl 2 + WO 3∙H 2 O (Wolfram(VI)-oxidhydrat) WO 3∙H 2 O wird in WO 3 überführt und dies reduziert: WO 3 + 3 H 2 → W + 3 H 2 O

Oxide Mo. O 3 (weiss) und WO 3 (gelb) sind wasser- und säureunlöslich. In Alkalilaugen lösen sie sich unter Bildung der Ionen Mo. O 42 - und WO 42 -. Mo. O 2 (violett) und WO 2 (braun) sind diamagnetische metallisch leitende Verbindungen. Beim Erhitzen der Trioxide in Vakuum oder durch Reduktion der Trioxide mit den Metallen erhält man die zahlreichen stöchiometrischen Oxide mit nichtganzzahligen Oxidationszahlen. Sie sind intensiv violett oder blau gefärbt. Im Unterschied zu Chrom sind keine Oxide mit Oxidationszahlen < 4 bekannt. Isopolymolybdate, Isopolywolframate Die alkalischen Lösungen der Trioxide Mo. O 3 und WO 3 enthalten tetraedrische Mo. O 42 - und WO 42 - -Ionen. Aus stark sauren Lösungen kristallisieren die Oxidhydrate Mo. O 3· 2 H 2 O und WO 3∙ 2 H 2 O aus, die als „Molybdänsäure“ bzw. „Wolframsäure“ bezeichnet werden. Beim erwärmen wandeln sie sich in die Monohydrate um. Bei p. H-Werten zwischen diesen Extremen bilden sich polymere Anionen, die überwiegend aus Me. O 6 -Oktaedern aufgebaut sind.

Bei Mo erfolgt die Bildung der Polyanionen durch eine rasche Gleichgewichtseinstellung, beim W dauert die Gleichgewichtseinstellung oft Wochen. Polyanionen sind bei Mo und W verschieden. In Molybdatlösungen bilden sich – sobald der p. H-Wert unter 6 sinkt – die Polyanionen [Mo 7 O 24]6 -, [Mo 8 O 26]4 - und [Mo 36 O 112]8 -, z. B. : 7 Mo. O 42 - + 8 H+ = Mo 7 O 246 - + 4 H 2 O Mo 7 O 246 - + 4 H+ + Mo. O 42 - = Mo 8 O 264 - + 2 H 2 O In Wolframatlösungen kondensieren bei p. H ≈ 6 die WO 42 - - Ionen zunächst zu [HW 6 O 21]5 -, das sich langsam mit [H 2 W 12 O 42]10 - ins Gleichgewicht setzt. Bei p. H ≈ 4 bilden sich langsam [H 2 W 12 O 40]6 - -Ionen.

Heteropolyanionen In die Strukturen von Isopolyanionen können Heteroatome eintreten. So erhält man aus einer Lösung, die Mo. O 42 - - und HPO 42 - - Ionen enthält, beim Ansäuern das gelbe Heteropolyanion [PMo 12 O 40]3 -: Heteropolyanionen bilden eine große Verbindungsklasse. Die meisten sind Heteropolyanionen des Molybdäns und Wolframs mit mindestens 35 verschiedenen Heteroatomen. Die Heteroatome sind Nichtmetalle und Übergangsmetalle. Die freien Säuren und die Salze mit kleinen Kationen sind in Wasser gut löslich. Salze mit großen Kationen wie Cs+, Ba 2+ und Pb 2+ sind schwer löslich.
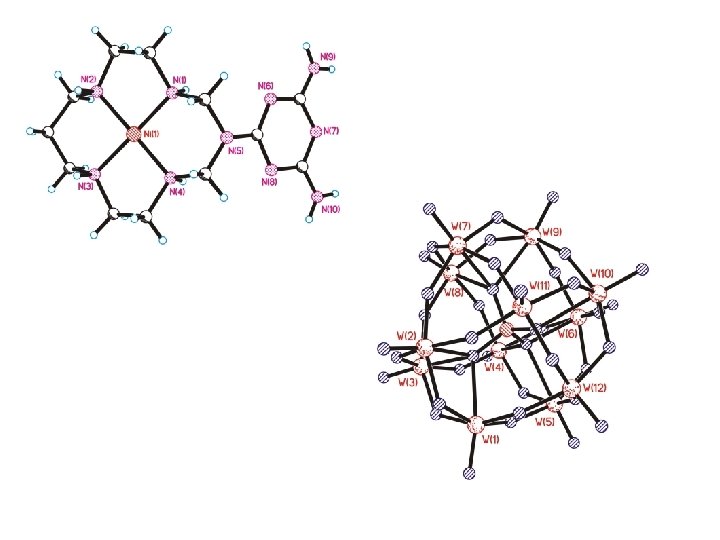
![[Cu(tet)(dmso)H 2 Si. Mo 12 O 40] [Cu(tet)(dmso)H 2 Si. Mo 12 O 40]](http://slidetodoc.com/presentation_image_h/1a3a2f6d9394a31e0bfc36932b8f0240/image-63.jpg)
[Cu(tet)(dmso)H 2 Si. Mo 12 O 40]

Bronzen Reduziert man Natrium-polywolframat mit H 2 bei Rotglut, erhält man eine Substanz, die wegen ihres metallischen, bronzeähnlichen Aussehens als Bronze bezeichnet wurde. Natriumwolframatbronzen sind nicht stöchiometrische Verbindungen der Zusammensetzung Nan. WO 3 ( 0 < n ≤ 1). Alle Alkalimetallwolframbronzen sind metallische Leiter. Wolframbronzen (Nan. WO 3 mit 0 < n ≤ 1) bilden auch folgende Metalle: Mg, Ca, Sr, Ba, Ga, In, Tl, Sn, Pb, Cu, Ag, Cd, Lanthanoide. Die analogen Alkalimetallmolybdänbronzen bilden sich nur unter hohem Druck.
- Slides: 64