Atypische mycobacterin in de setting van mucoviscidose Mieke

Atypische mycobacteriën in de setting van mucoviscidose Mieke Develter Dinsdag 27 april 2004 UZ Gasthuisberg

Mucoviscidose (cystic fibrosis CF) • meest frequente levensverkortende genetische aandoening bij de blanke populatie (1/2500) • autosomaal recessieve aandoening • mutatie in één enkel gen op de lange arm van chromosoom 7 coderend voor het CF transmembrane conductance regulator (CFTR) proteïne • veel mutaties beschreven, doch slechts een dozijn verantwoordelijk voor de meeste gevallen • aanwezigheid van F 508 verantwoordelijk voor de hogere frequentie van blanke tov andere rassen

Mucoviscidose (cystic fibrosis CF) • sterk visceuze secreties: respiratoire en gastrointestinale problemen • inflammatie van de luchtwegen vanaf jonge leeftijd • sputumculturen: multipele pathogenen, met voorspelbare, universele cascade van pathogenen in functie van leeftijd
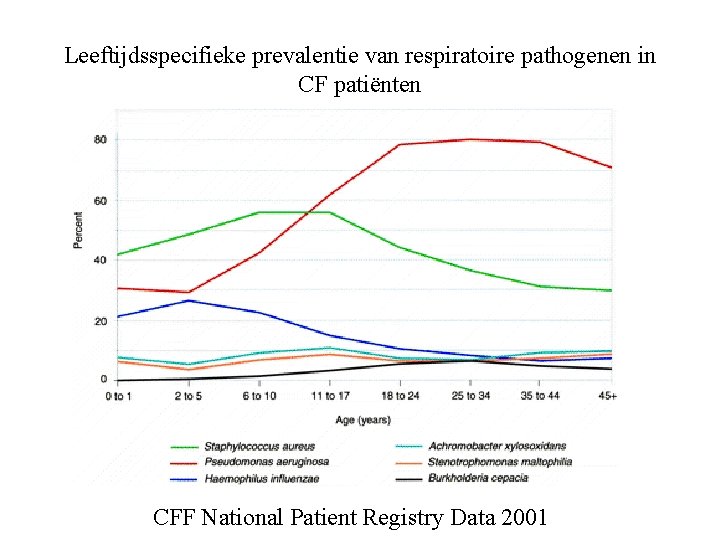
Leeftijdsspecifieke prevalentie van respiratoire pathogenen in CF patiënten CFF National Patient Registry Data 2001
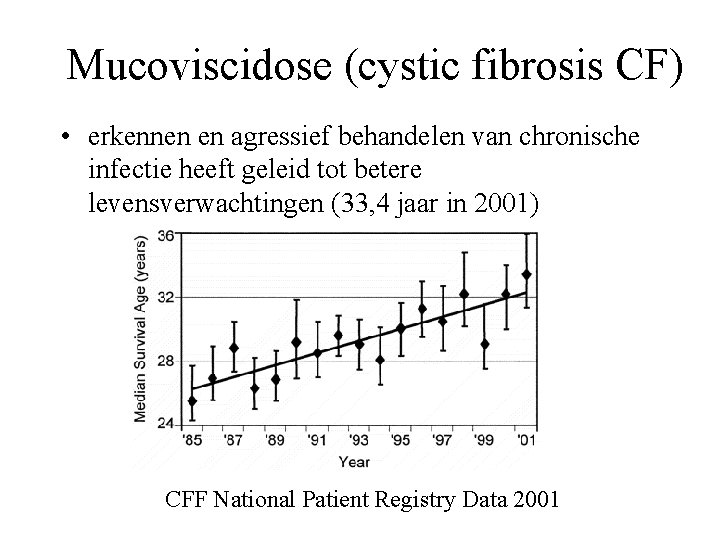
Mucoviscidose (cystic fibrosis CF) • erkennen en agressief behandelen van chronische infectie heeft geleid tot betere levensverwachtingen (33, 4 jaar in 2001) CFF National Patient Registry Data 2001

Mucoviscidose (cystic fibrosis CF) • bij deze toegenomen overleving, vond men in de monsters van de luchtwegen van CF- patiënten – multipele antibiotica resistente stammen van traditionele pathogenen zoals P. aeruginosa – het verschijnen van nieuwe, meer virulente pathogenen zoals B. cepacia complex – toenemend isoleren van organismen aanvankelijk als commensalen aanzien, zoals atypische mycobacteriën (nontuberculous mycobacteria (NTM))

Atypische mycobacteriën (nontuberculous mycobacteria NTM) • vrij snel geobserveerd na de ontdekking door Koch van de tuberkel bacil • zuur-vaste bacillen (Acid-Fast Bacilli: AFB) • water en grond-saprofieten • pas rond 1950 als humane pathogenen erkend • zeldzame overdracht van persoon op persoon • toename in prevalentie van NTM (CDC) • niet gekend of NTM-ziekte (vooral longziekte) snel na infectie of pas na een latentieperiode ontwikkelt • occasioneel oorzaak van primaire longziekte, maar vaker bij patiënten met onderliggende aandoeningen zoals AIDS, chronische longziektes, diabetes mellitus en behandeling met steroïden

NTM & CF • CF-patiënten hebben verhoogd risico op NTMinfectie omwille van – chronische longaandoening – diabetes mellitus – steroïden

NTM & CF • toenemend gebruik van onderhoudstherapie met macroliden: verdere studies zijn wel nodig voor lange termijn impact – anti-infectieus • • excellente biofilmpenetratie (P. aeruginosa) intracellulaire accumulatie in P. aeruginosa inhibitie proteïnesynthese verbeterde doding van P. aeruginosa – anti-inflammatoir effect ? • accumulatie in neutrofielen met impact op verschillende sleutelfuncties ? – fase III trial: verbeterde longfunctie, toename in gewicht, verminderd pulmonaire exacerbaties – mogelijke resistentie inductie bij atypische mycobacteriën

Atypische mycobacteriën (nontuberculous mycobacteria NTM) • taxonomie – traag groeiende • fotochromogenen (Runyoun groep I) oa M. kansasii • scotochromogenen (Runyoun groep II) oa M. scrofulaceum • nonfotochromogenen (Runyoun groep III) oa M. avium, M. intracellulare (MAC complex) – snel groeiende (Runyoun groep IV) oa M. fortuitum, M. chelonae, M. abscessus

Diagnostische criteria voor NTM longziekte (ATS 1997) 1. klinische criteria – – compatibele symptomen met deterioratie indien onderliggende aandoening exclusie van andere oorzaken als verklaring 2. radiologische criteria – RX-thorax • Infiltraten, cavitatie, noduli – HRCT (high-resolution computed tomography) • Noduli, bronchiëctasiën

Diagnostische criteria voor NTM longziekte (ATS 1997) 3. bacteriologische criteria – ten minste drie beschikbare sputa/bronchiale washes beschikbaar binnen 1 jaar • • drie positieve culturen met negatief uitstrijkje of twee positieve culturen met een positief uitstrijkje – één beschikbare bronchiale wash met onmogelijkheid om sputumstalen te verkrijgen • positieve cultuur of positief uitstrijkje – weefselbiopsie met positieve cultuur • voor diagnose van pulmonaire ziekte moet aan alle 3 de criteria voldaan zijn

Diagnostische criteria voor NTM longziekte (ATS 1997) • kliniek – symptomen zijn variabel en niet specifiek (chronische hoest, sputum productie, vermoeidheid, malaise, dyspnoe, koorts, hemoptoë, gewichtsverlies) • radiologie – geen specifieke diagnostische kenmerken • cultuur: essentieel voor diagnose

Critical appraisal • Patiënt: volwassen mucoviscidosepatiënt • Interventie: cultuur van mycobacteriën • Vergelijking: huidige decontaminatiemethode bij cultuur van atypische mycobacteriën met in de literatuur beschreven methodes voor specifieke decontaminatie bij mucoviscidosepatiënten • Outcome: heeft het opsporen van atypische mycobacteriën een invloed op de outcome van mucoviscidosepatiënten ?

Critical appraisal: bronnen • literatuurstudie • contact met andere referentiecentra van België voor mucoviscidose • nog lopende studie in Gasthuisberg

detectiemethodes huidtests: moleculaire diagnostiek: in ontwikkeling cultuur: gouden standaard, tijd zuurvaste kleuring: geen speciës identificatie mogelijk, minder gevoelig

decontaminatiemethodes NALC-Na. OH: meest gebruikt voor routine stalen oxaalzuur NALC-Na. OH gevolgd door oxaalzuur 2 -stapsdecontaminatie: 1. NALC-Na. OH 2. NALC-Na. OH gevolgd door oxaalzuur indien contaminatie

Analytische performantie 1. Pre-analytische factoren 2. Analytische factoren

Pre-analytische factoren • respiratoire stalen: ochtendstaal – – – opgehoest sputum: accurate indicator van lage luchtweg pathologie, geprefereerde bron van luchtwegsecreties bij mucoviscidosepatiënten hypertonisch zout geïnduceerd sputum: goed surrogaat voor staal van lagere luchtweg keel: geen optimale indicator van lage luchtweg pathologie (voor P. aeruginosa: goede specificiteit, maar slechte sensitiviteit) – BAL-vocht: meer sensitief dan keel bij patiënten die geen sputum ophoesten, maar • • invasief kostelijk beperkt tot 1 lob, mogelijk regionale aandoening missend kruis-contaminatie mogelijk met besmette bronchoscoop

Pre-analytische factoren • snel transport en inzetten van cultuur na afname – – steriel, lekvrij, wegwerp recipiënt geen preservatieven vereist voor robuste mycobacteriën onmiddellijk inzetten van cultuur bij transporttijd > 1 uur staalbewaring op 4°C gedurende maximum 24 uur – in labo: staalbewaring op 4°C (gedurende maximum 24 uur) voor het inzetten van het staal (vandaar voorkeur geen staalafname op donderdagavond of vrijdag)

Analytische factoren • meetbereik: zuur-vaste kleuring: (106 AFB/ml + AFB) (104 AFB/ml + AFB in 60%) • cultuur: (10 – 100 AFB/ml detectie) Turn Around Time (cultuur): 6 weken indien negatief, iets langer indien secundaire decontaminatie vereist is

Diagnostische performantie • literatuur – performantie van detectiemethodes – performantie van decontaminatiemethodes voor cultuur – prevalentie • andere referentiecentra mucoviscidose – prevalentie • nog lopende studie in Gasthuisberg
Performantie van detectiemethodes huidtests – algemeen: • veel gemeenschappelijke antigenen bij verschillende mycobacteriën speciës • extensieve kruisreacties – corticosteroïden gebruik • anergie

Performantie van detectiemethodes moleculaire diagnostiek: • • reeds voor M. tuberculosis en MAC complex in ontwikkeling voor andere atypische mycobacteriën sneller (6 u) in afwachting van meer probes voor NTM, voorlopig poging tot betere cultuur resultaten • in ontwikkeling op UZ Gasthuisberg (eventueel tegen lente 2005)

Performantie van detectiemethodes cultuur: gouden standaard: aanbeveling van één vast en één vloeibaar medium (CDC) – vaste bodem: • ei-media: bv Löwenstein-Jensen – goede houdbaarheid (verschillende maanden in koelkast) – goede isolatie van M. tuberculosis – minder betrouwbaar voor isolatie van andere mycobacteriën • agar-media: bv Middlebrook 7 H 11 en 7 H 10 – duur – beperkte houdbaarheid (1 maand in koelkast) – delicaat: excessieve warmte/licht kan deterioratie veroorzaken met vrijzetting van formaldehyde: toxisch voor mycobacteriën

Performantie van detectiemethodes cultuur: gouden standaard: aanbeveling van één vast en één vloeibaar medium (CDC) – vloeibaar medium: • radiometrische detectie: BACTEC 460 TB system – eerste systeem dat significant eerdere detectie van mycobacteriën toeliet – nu als “gouden standaard” aanzien: nieuwere systemen worden hiermee vergeleken • non-radiometrische detectie: bv MGIT 960 system (gebruik op UZ Gasthuisberg)

Performantie van detectiemethodes Vloeibare bodem radiometrische detectie: BACTEC 460 TB system • principe: -metabolisch verbruik van radiolabeled palmitinezuur 14 C-gelabeled CO 2: groei van mycobacteriën -12 B medium is erg arm aan voedinsstoffen, dus geen goede voedinsbodem voor de meeste bacteriën die het 14 C-substraat niet gebruiken • beperkingen – – radioactief materiaal manueel werk (laden en ontladen) potentieel risico van kruis contaminatie gebrek aan gecomputeriseerd data management

Performantie van detectiemethodes Vloeibare bodem: – non-radiometrische detectie: bv MGIT 960 system • principe: -fluorescentie-sensor technologie fluorescerend element is ingebed in bodem van MGIT-tube, dat aanvankelijk onderdrukt wordt door de aanwezige zuurstof, bij O 2 verbruik door bacteriën neemt de fluorescentie toe -gemodifieerde Middlebrook 7 H 9 (rijk medium) • voordelen – – geen radioactief materiaal volautomatisch continue monitoring (60’) niet invasieve aflezing die kruis-contaminatie en prikaccidenten voorkomt
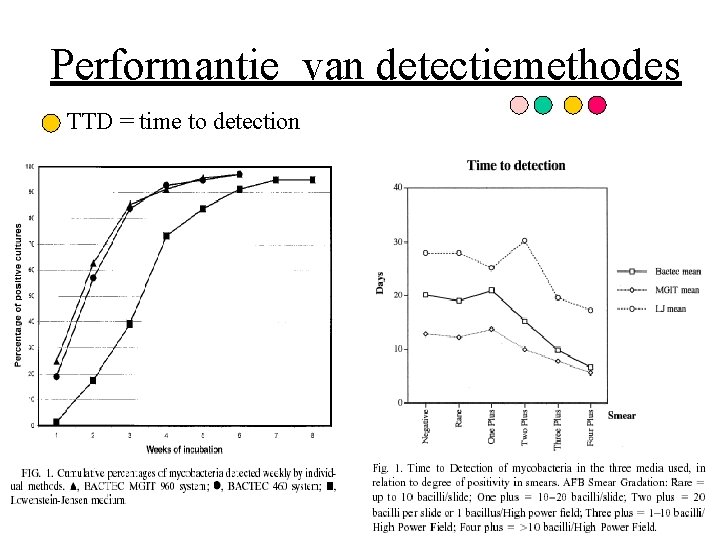
Performantie van detectiemethodes TTD = time to detection
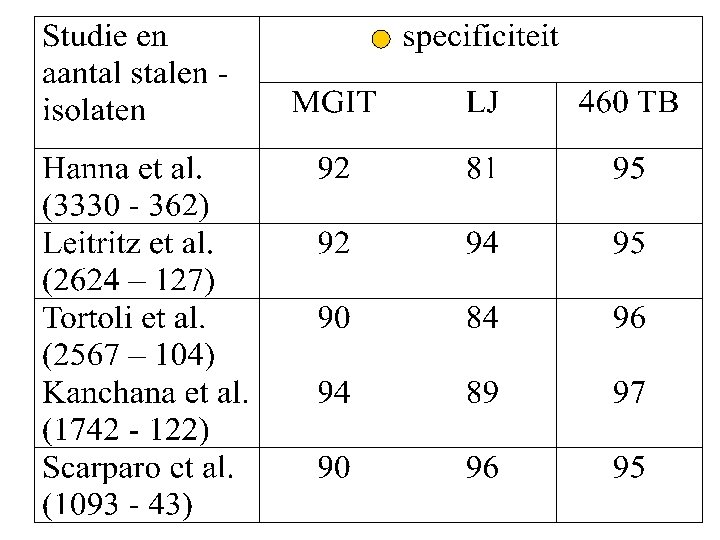
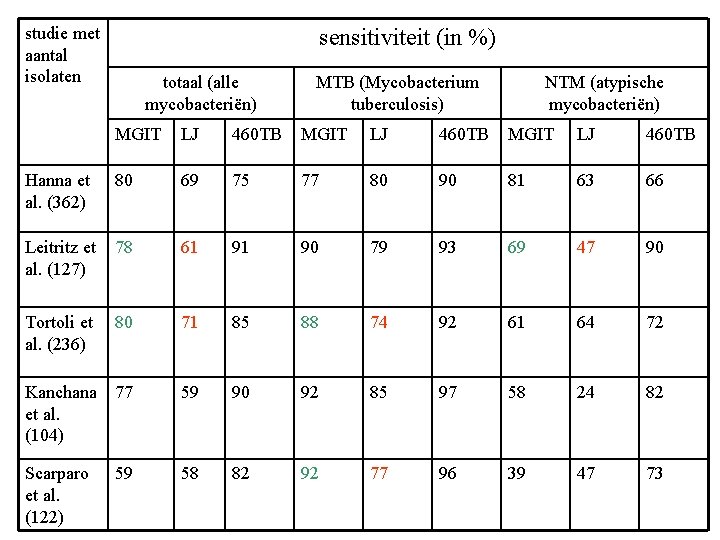
studie met aantal isolaten sensitiviteit (in %) totaal (alle mycobacteriën) MTB (Mycobacterium tuberculosis) NTM (atypische mycobacteriën) MGIT LJ 460 TB Hanna et al. (362) 80 69 75 77 80 90 81 63 66 Leitritz et al. (127) 78 61 91 90 79 93 69 47 90 Tortoli et al. (236) 80 71 85 88 74 92 61 64 72 Kanchana et al. (104) 77 59 90 92 85 97 58 24 82 Scarparo et al. (122) 59 58 82 92 77 96 39 47 73
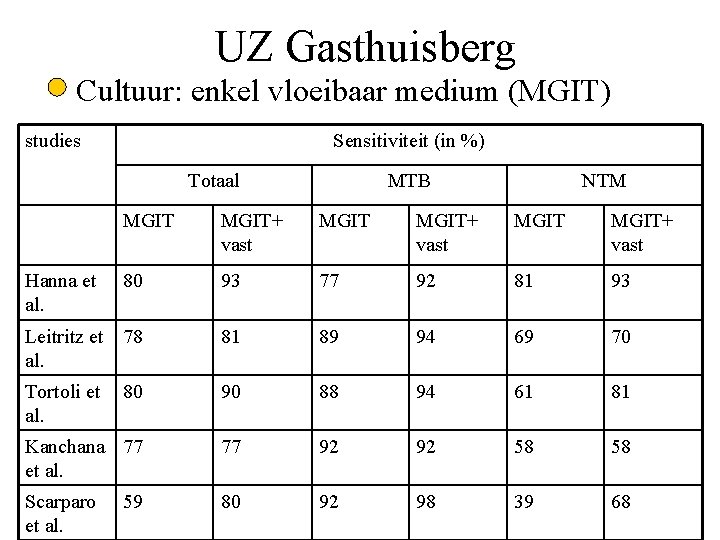
UZ Gasthuisberg Cultuur: enkel vloeibaar medium (MGIT) studies Sensitiviteit (in %) Totaal MTB NTM MGIT+ vast MGIT+ vast 80 93 77 92 81 93 Leitritz et 78 al. 81 89 94 69 70 Tortoli et al. 80 90 88 94 61 81 Kanchana 77 et al. 77 92 92 58 58 Scarparo et al. 80 92 98 39 68 Hanna et al. 59

Performantie van detectiemethodes zuurvaste kleuringen (Acid -Fast Bacilli AFB) – 2 types: • carbol-fuchsine (Ziehl-Neelsen of Kinyoun) – lichtmicroscoop: 300 velden bekijken (15’) • auramine-rhodamine fluorochroom: voorkeur – fluorescentiemicroscoop: kleinere vergroting: 30 velden bekijken (1, 5’) – verbeterde sensitiviteit – sneller – snel groeiende mycobacteriën (Runyon groep IV) kunnen < 10% zuurvast zijn en niet kleuren met fluorochroomkleuring – minder sensitief als cultuur (106 AFB/ml + AFB) (104 AFB/ml + AFB in 60%) – geen bepaling van speciës mogelijk

Performantie van decontaminatiemethodes voor cultuur • • NALC-Na. OH: meest gebruikt voor routine stalen oxaalzuur NALC-Na. OH gevolgd door oxaalzuur 2 -stapsdecontaminatie: 1. NALC-Na. OH 2. NALC-Na. OH gevolgd door oxaalzuur op reeds gegroeide cultuur indien contaminatie
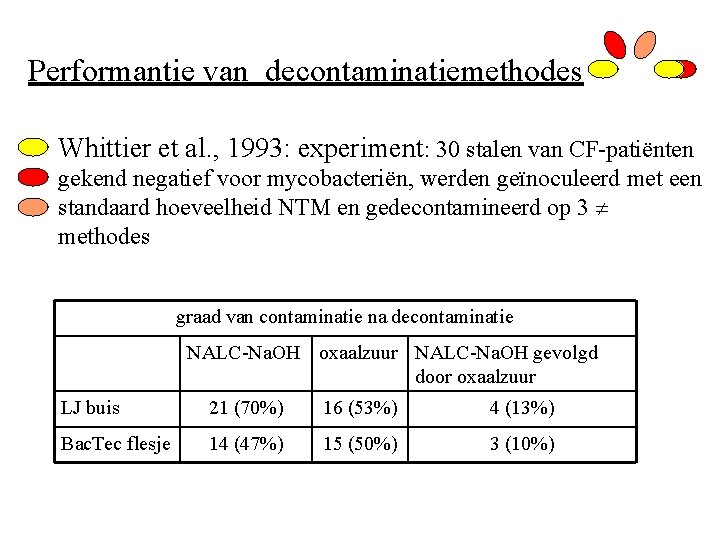
Performantie van decontaminatiemethodes • Whittier et al. , 1993: experiment: 30 stalen van CF-patiënten gekend negatief voor mycobacteriën, werden geïnoculeerd met een standaard hoeveelheid NTM en gedecontamineerd op 3 methodes graad van contaminatie na decontaminatie NALC-Na. OH oxaalzuur NALC-Na. OH gevolgd door oxaalzuur LJ buis 21 (70%) 16 (53%) 4 (13%) Bac. Tec flesje 14 (47%) 15 (50%) 3 (10%)
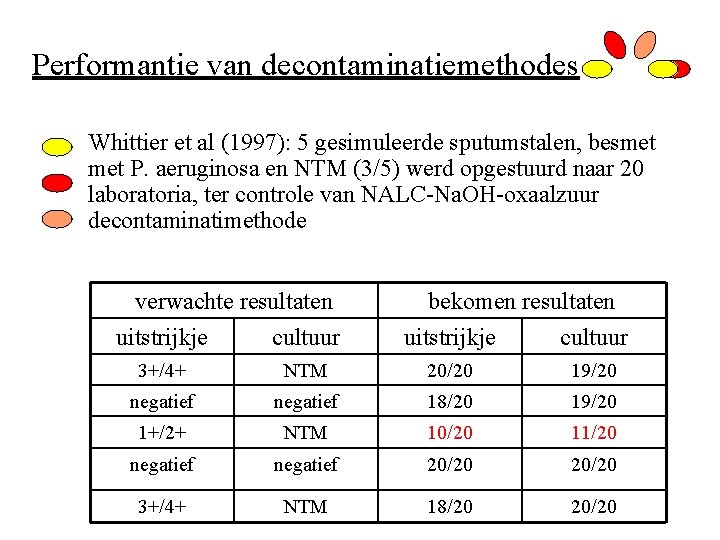
Performantie van decontaminatiemethodes Whittier et al (1997): 5 gesimuleerde sputumstalen, besmet P. aeruginosa en NTM (3/5) werd opgestuurd naar 20 laboratoria, ter controle van NALC-Na. OH-oxaalzuur decontaminatimethode verwachte resultaten uitstrijkje cultuur bekomen resultaten uitstrijkje cultuur 3+/4+ NTM 20/20 19/20 negatief 18/20 19/20 1+/2+ NTM 10/20 11/20 negatief 20/20 3+/4+ NTM 18/20 20/20
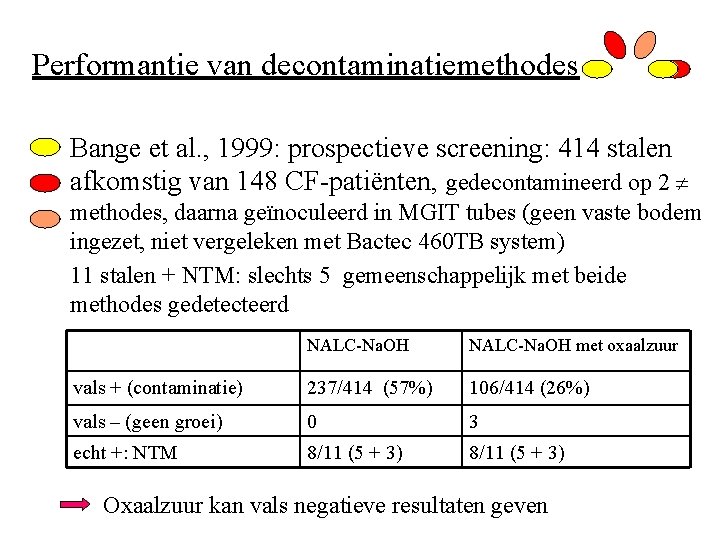
Performantie van decontaminatiemethodes • Bange et al. , 1999: prospectieve screening: 414 stalen afkomstig van 148 CF-patiënten, gedecontamineerd op 2 methodes, daarna geïnoculeerd in MGIT tubes (geen vaste bodem ingezet, niet vergeleken met Bactec 460 TB system) 11 stalen + NTM: slechts 5 gemeenschappelijk met beide methodes gedetecteerd NALC-Na. OH met oxaalzuur vals + (contaminatie) 237/414 (57%) 106/414 (26%) vals – (geen groei) 0 3 echt +: NTM 8/11 (5 + 3) Oxaalzuur kan vals negatieve resultaten geven
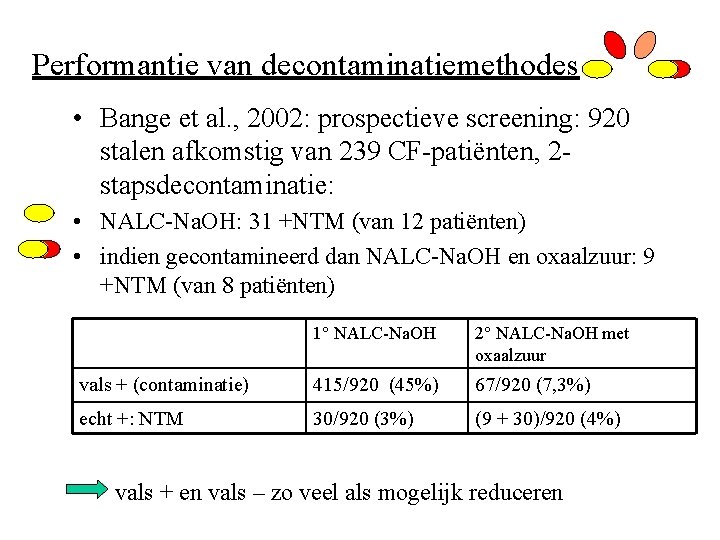
Performantie van decontaminatiemethodes • Bange et al. , 2002: prospectieve screening: 920 stalen afkomstig van 239 CF-patiënten, 2 stapsdecontaminatie: • NALC-Na. OH: 31 +NTM (van 12 patiënten) • indien gecontamineerd dan NALC-Na. OH en oxaalzuur: 9 +NTM (van 8 patiënten) 1° NALC-Na. OH 2° NALC-Na. OH met oxaalzuur vals + (contaminatie) 415/920 (45%) 67/920 (7, 3%) echt +: NTM 30/920 (3%) (9 + 30)/920 (4%) vals + en vals – zo veel als mogelijk reduceren
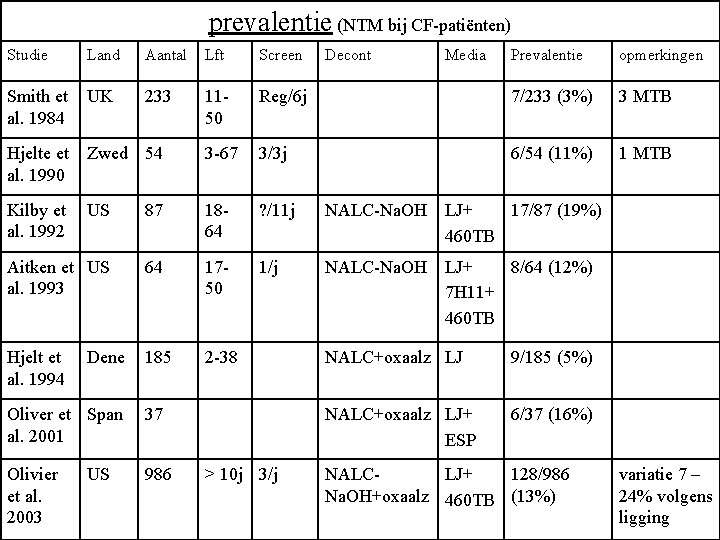
prevalentie (NTM bij CF-patiënten) Studie Land Aantal Lft Screen Smith et al. 1984 UK 233 1150 Hjelte et al. 1990 Zwed 54 Kilby et al. 1992 US Prevalentie opmerkingen Reg/6 j 7/233 (3%) 3 MTB 3 -67 3/3 j 6/54 (11%) 1 MTB 87 1864 ? /11 j NALC-Na. OH LJ+ 17/87 (19%) 460 TB Aitken et US al. 1993 64 1750 1/j NALC-Na. OH LJ+ 8/64 (12%) 7 H 11+ 460 TB Hjelt et al. 1994 185 2 -38 Dene Oliver et Span al. 2001 37 Olivier et al. 2003 986 US > 10 j 3/j Decont Media NALC+oxaalz LJ 9/185 (5%) NALC+oxaalz LJ+ ESP 6/37 (16%) NALCLJ+ 128/986 Na. OH+oxaalz 460 TB (13%) variatie 7 – 24% volgens ligging

Andere Belgische referentiecentra voor mucoviscidose • Prevalentie – AZ VUB • • sedert 2 jaar screening 1/jaar en bij klinische achteruitgang methode: 2 stapsdecontaminatie (Bange et al 2002) 3 patiënten met M. abscessus geen longtransplantatie indien M. abscessus – Centre Muco Erasme • • 150 patiënten (volwassenen) sedert 2 à 3 jaar screening 1/jaar 2 of 3 maal mycobacteriën geïsoleerd methode: NALC-Na. OH en bij contaminatie herhaling NALCNa. OH

Andere Belgische referentiecentra voor mucoviscidose - mucocentrum Antwerpen – St. Vincentiusziekenhuis (volw ptn) • cultuur mycobacteriën wordt regelmatig aangevraagd • methode: NALC-Na. OH • geen statistieken - universitair ziekenhuis Antwerpen (kinderen) • geen systematische screening, wel op indicatie en zeker indien bronchoscopie gebeurd is • methode: geen specifieke decontaminatiemethode (methode ontwikkeld door prof. Pattyn) • nog geen + resultaat

Andere Belgische referentiecentra voor mucoviscidose - UZ Gent • sedert 3 à 4 jaar screening 1/jaar • methode: NALC-Na. OH • nog geen + resultaat - CHR Citadelle • • 80 patiënten ( 35 volwassenen) sedert 4 jaar screening 1/jaar en bij klinische achteruitgang methode: Na. OH 2 atypische mycobacteriën geïsoleerd bij tieners

Andere Belgische referentiecentra voor mucoviscidose - cliniques St. Luc • 130 patiënten (38% volwassenen) • screening sedert 10 jaar • • niet systematisch, wel bij klinische acteruitgang hospitalisatie toename sputumproductie • methode: NALC-Na. OH , bij contaminatie oxaalzuur • 1 M. chelonae geïsoleerd

UZ Gasthuisberg – prospectieve studie bij (80) volwassen CF-patiënten – stalen van 30 patiënten • 10/30 redecontaminatie (2 -stapsdecontaminatie volgens Bange et al) – nog geen + resultaat

Klinische impact: diagnostisch • Kunnen andere testen vermeden, vervangen worden ? • Levert de test supplementaire en/of meer adekwate informatie, niet verkrijgbaar door andere onderzoeken ? – diagnose van NTM-infectie: ATS-criteria: voor diagnose van pulmonaire ziekte moet aan alle 3 de criteria voldaan zijn (klinisch, radiologisch, microbiologisch)

Klinische impact: therapeutisch • Kan een behandeling sneller gestart of juist vermeden worden door deze test ? – niet starten van onderhoudstherapie met macroliden indien cultuur + om resistentie te vermijden – sneller starten van antimycobacteriële therapie – vermijden van therapie voor andere pathogenen – soms voorwaarde voor transplantatie (echter geen contraindicatie volgens ATS) – vermijden van meer invasieve therapeutische opties (bv uitstellen van longtransplantatie, cfr. Oliver et al. , 2001)

Klinische impact: outcome • Kan een ziekte, complicatie, morbiditeit, mortaliteit vermeden worden door deze test ? – case reports: geen consensus • casussen met/zonder klinische deterioratie • casussen met/zonder klinische verbetering bij therapie – geen vergelijkende studies gevonden met bewezen verbeterde outcome wanneer gescreend wordt naar atypische mycobacteriën en deze ook behandeld worden indien klinisch geïndiceerd

Outcome: case reports • Smith et al (1984, UK): 223 patiënten 11 - 50 jaar follow up bij 3 patiënten met NTM • 1 beantwoordde niet aan therapie en overleed (autopsie) (M. fortuitum) • 1 ging klinisch beter na 3 maand therapie (M. chelonae) • 1 geen therapie toegediend (eenmalige isolatie NTM) • Hjelte et al (1990, Zweden): 54 patiënten 3 -67 jaar (3 MAC, 1 M. kansasii, 1 M. gordonae, 1 niet te classeren) impact: • bij aanvang: klinische deterioratie • follow up: klinische verbetering met aangepaste therapie

Outcome: case reports • Kilby et al (US 1992): 87 patiënten 18 - 64 jaar oud over 11 jaar opgevolgd (17 patiënten met NTM 11 met MAC 3 met M. chelonae 2 met zowel MAC als M. chelonae 1 met M. fortuitum) impact: geen correlatie met ernst aandoening • Aitken et al (1993, US): 64 patiënten 17 - 50 jaar oud over 1 jaar (8 patiënten met NTM: 7 met MAC en 1 met M. fortuitum) impact: tendens NTM+ patiënten lagere klinische scores

Outcome: case reports • Hjelt et al (1994, Denemarken): 185 patiënten 2 -38, 5 jaar (mediaan 15 jaar) over 1 jaar (3 -4 jaar follow up) (7 patiënten met herhaaldelijk NTM: 2 met MAC en 5 met M. abscessus) impact: • bij aanvang: 3/7 patiënten klinisch stabiel (1 MAC, 2 M. abscessus) • follow up: -bij 2/7 patiënten verdwijnt NTM spontaan (1 MAC) -bij 2/7 patiënten verbeterde kliniek onder therapie (simultane therapie voor andere pathogenen) (2 M. abscessus) -geen eradicatie bij 4/5 patiënten ondanks therapie

Outcome: case reports • Oliver et al (Spanje 2001): 37 patiënten impact: 3 patiënten met persisterende NTM • bij aanvang: klinische deterioratie voor en tijdens studie • follow-up: – 2/3 behandeld: » 1 klinische verbetering (M. chelonae) , zodat een inschrijving op de wachtlijst voor longtransplantatie geannuleerd kon worden » 1 duidelijke klinische verbetering (MAC) – 1/3 onbehandeld met stabiele longfunctie (M. chelonae)

Outcome: case reports • Olivier et al (US 2003): 986 CF-patiënten 10 jaar (± 10% van de US CF-populatie 10 jaar) 128/986 +NTM: MAC (72%) en M. abscessus (16%) – onderverdeling in groep +ATS criteria en - ATS criteria – impact: • bij aanvang: betere longfunctie bij NTM+ patiënten • korte termijn follow up (15 maand) – geen significante vermindering longfunctie – meer (progressie) abnormaliteiten HRCT bij groep +ATS criteria

Organisatorische en financiële impact • kostprijs: • cultuur: riziv forfait: 11, 04 € werkelijke kostprijs: 8, 99 € -indien geen secundaire decontaminatie -indien wel secundaire decontaminatie: duurder (waarschijnlijk ± dubbel)

To Do • studie afwachten • opleiding laboranten • aanpassingen op aanvraagbon nr. 3030 cultuur respiratoir specimen fungi 1754 sputum 45 1755 bronchus of endotrach. aspiraat 46 1756 bronchuslavage/BAL 47 1759 monster van mucoviscidosepatiënt 49 atypische mycobacteriën, enkel voor mucoviscidosepatiënt
- Slides: 54