Atualizao de Quimioterapia e Antiangiognicos Fernando Moura Oncologista










- Slides: 40

Atualização de Quimioterapia e Antiangiogênicos Fernando Moura Oncologista Clínico Hospital Israelita Albert Einstein – São Paulo 1 DIRETORIA COMERCIAL E MARKETING


Agenda • QT de 1 a Linha • QT de Manutenção • QT de 2 a Linha / Associação com Agentes Antiangiogênicos

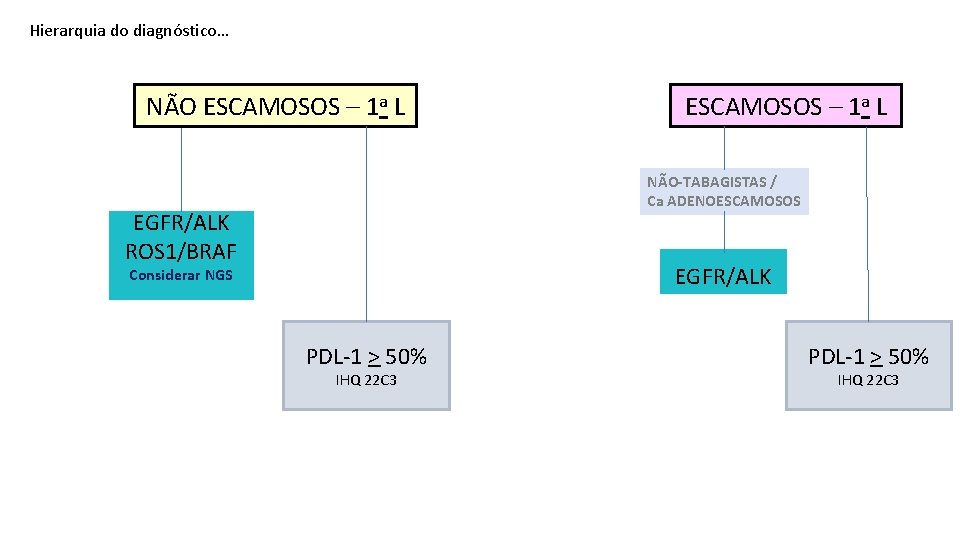
Hierarquia do diagnóstico… NÃO ESCAMOSOS – 1 a L NÃO-TABAGISTAS / Ca ADENOESCAMOSOS EGFR/ALK ROS 1/BRAF EGFR/ALK Considerar NGS PDL-1 > 50% IHQ 22 C 3

1ª Linha de Quimioterapia

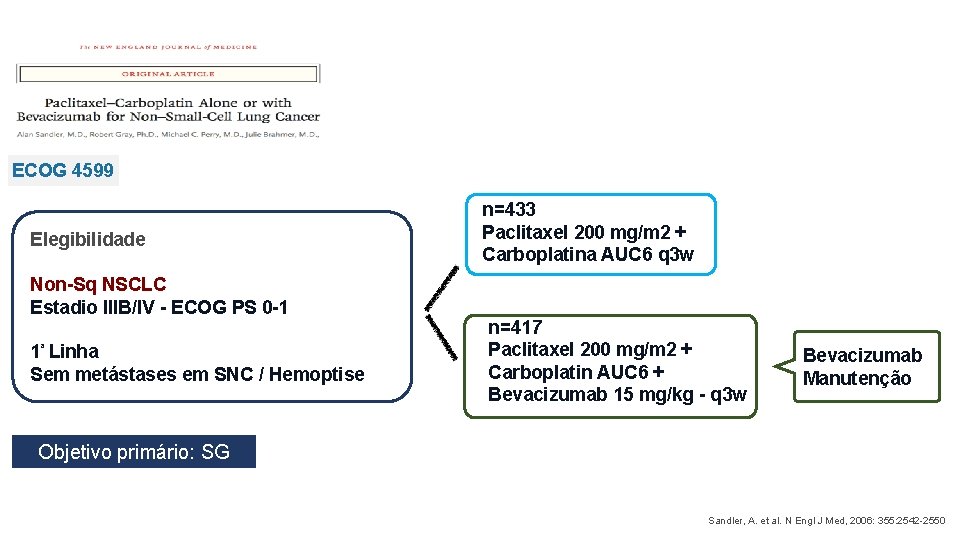
ECOG 4599 Elegibilidade Non-Sq NSCLC Estadio IIIB/IV - ECOG PS 0 -1 1ª Linha Sem metástases em SNC / Hemoptise n=433 Paclitaxel 200 mg/m 2 + Carboplatina AUC 6 q 3 w n=417 Paclitaxel 200 mg/m 2 + Carboplatin AUC 6 + Bevacizumab 15 mg/kg - q 3 w Bevacizumab Manutenção Objetivo primário: SG Sandler, A. et al. N Engl J Med, 2006: 355: 2542 -2550

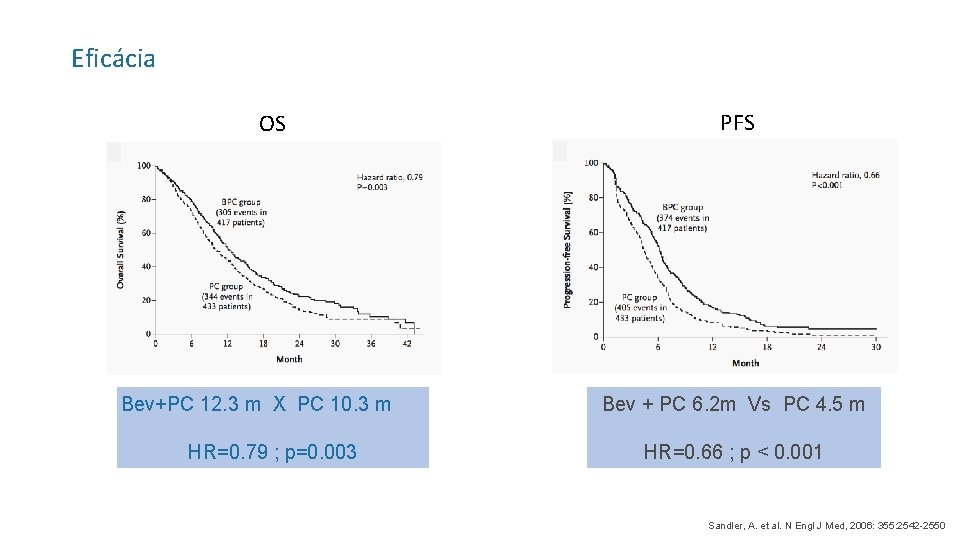
Eficácia OS Bev+PC 12. 3 m X PC 10. 3 m HR=0. 79 ; p=0. 003 PFS Bev + PC 6. 2 m Vs PC 4. 5 m HR=0. 66 ; p < 0. 001 Sandler, A. et al. N Engl J Med, 2006: 355: 2542 -2550

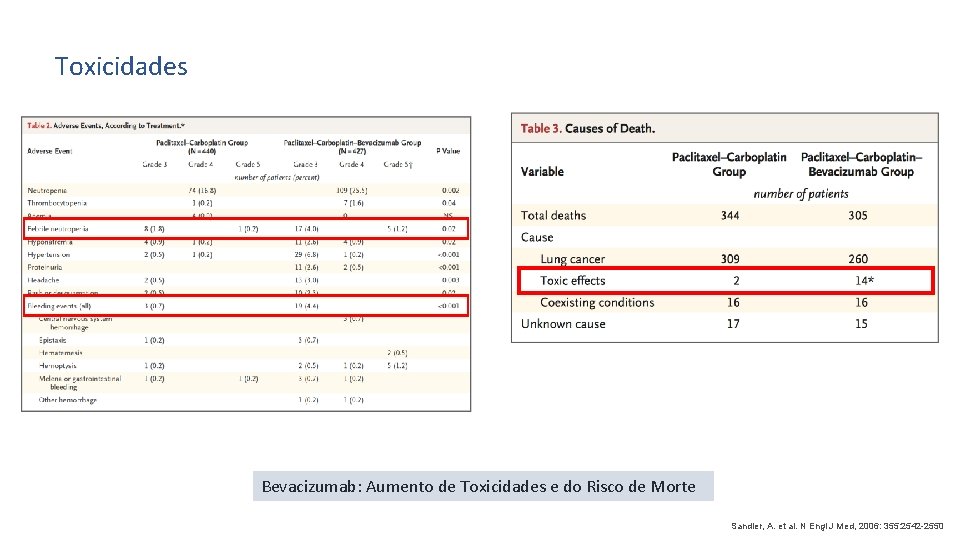
Toxicidades Bevacizumab: Aumento de Toxicidades e do Risco de Morte Sandler, A. et al. N Engl J Med, 2006: 355: 2542 -2550

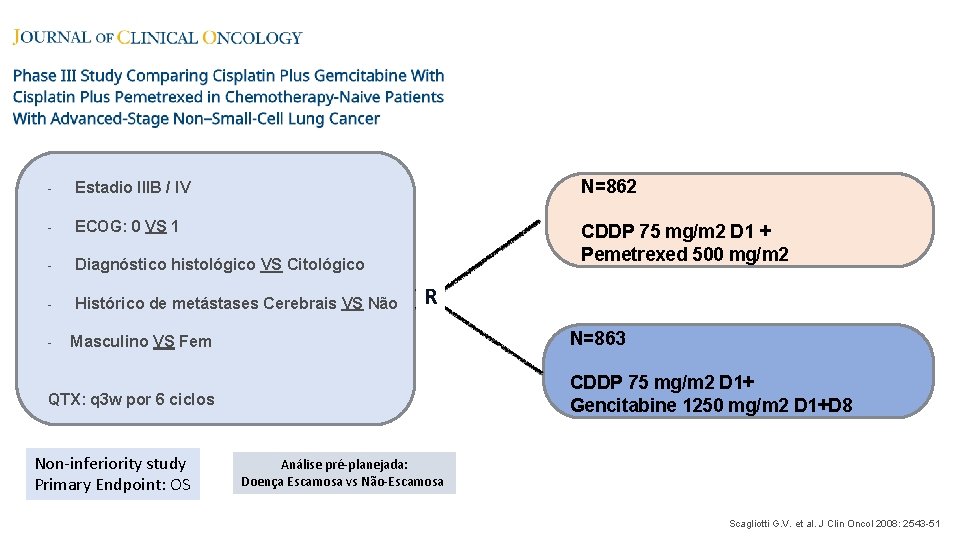
- Estadio IIIB / IV N=862 - ECOG: 0 VS 1 - Diagnóstico histológico VS Citológico CDDP 75 mg/m 2 D 1 + Pemetrexed 500 mg/m 2 - Histórico de metástases Cerebrais VS Não - R N=863 Masculino VS Fem CDDP 75 mg/m 2 D 1+ Gencitabine 1250 mg/m 2 D 1+D 8 QTX: q 3 w por 6 ciclos Non-inferiority study Primary Endpoint: OS Análise pré-planejada: Doença Escamosa vs Não-Escamosa Scagliotti G. V. et al. J Clin Oncol 2008: 2543 -51

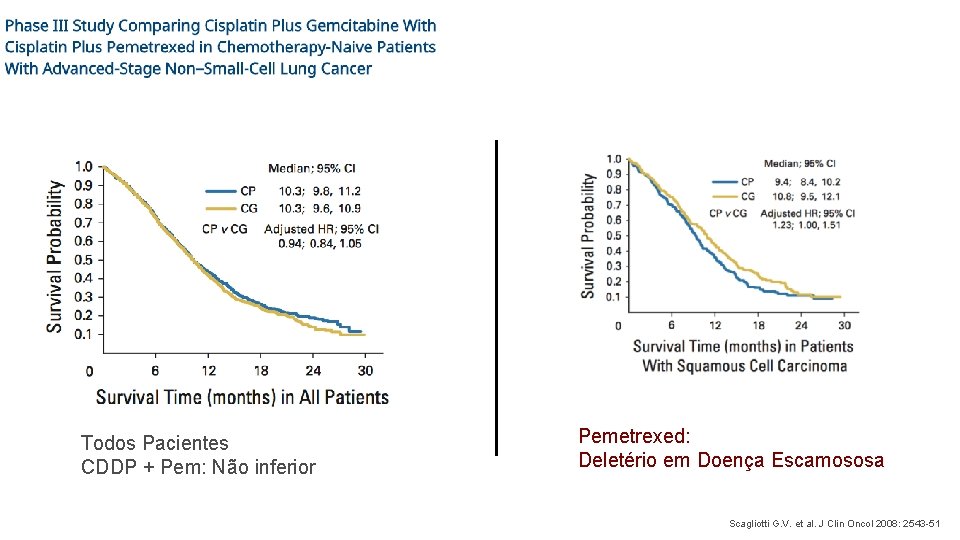
Todos Pacientes CDDP + Pem: Não inferior Pemetrexed: Deletério em Doença Escamososa Scagliotti G. V. et al. J Clin Oncol 2008: 2543 -51

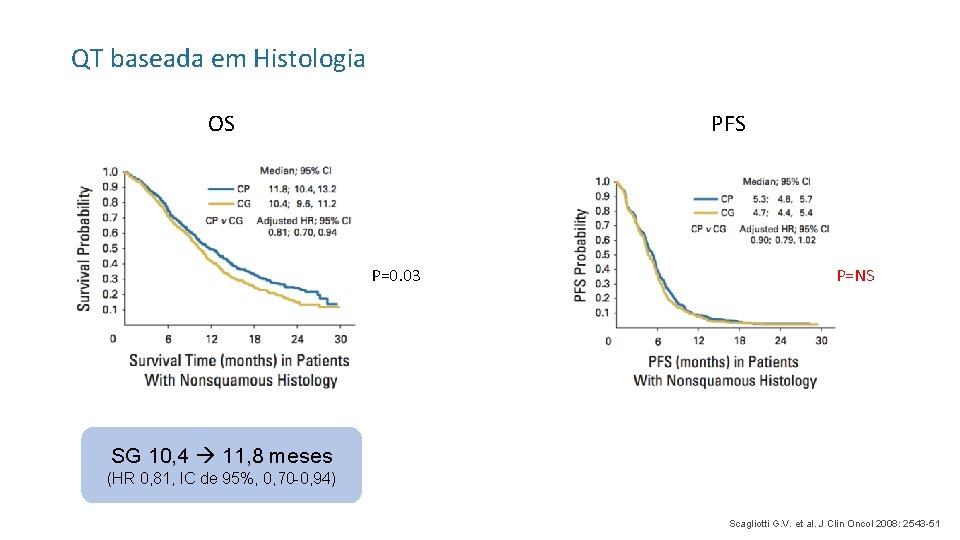
QT baseada em Histologia PFS OS P=0. 03 P=NS SG 10, 4 11, 8 meses (HR 0, 81, IC de 95%, 0, 70 -0, 94) Scagliotti G. V. et al. J Clin Oncol 2008: 2543 -51

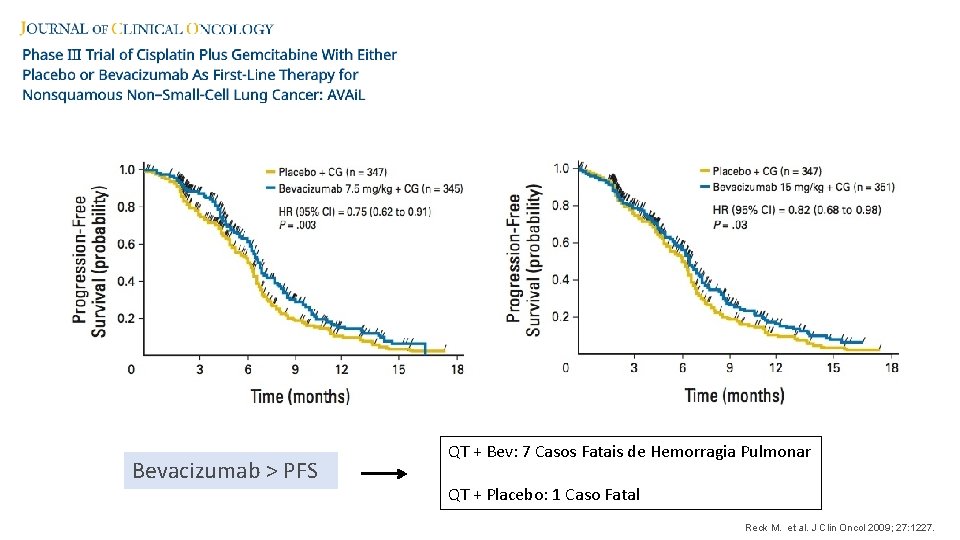
Bevacizumab > PFS QT + Bev: 7 Casos Fatais de Hemorragia Pulmonar QT + Placebo: 1 Caso Fatal Reck M. et al. J Clin Oncol 2009; 27: 1227.

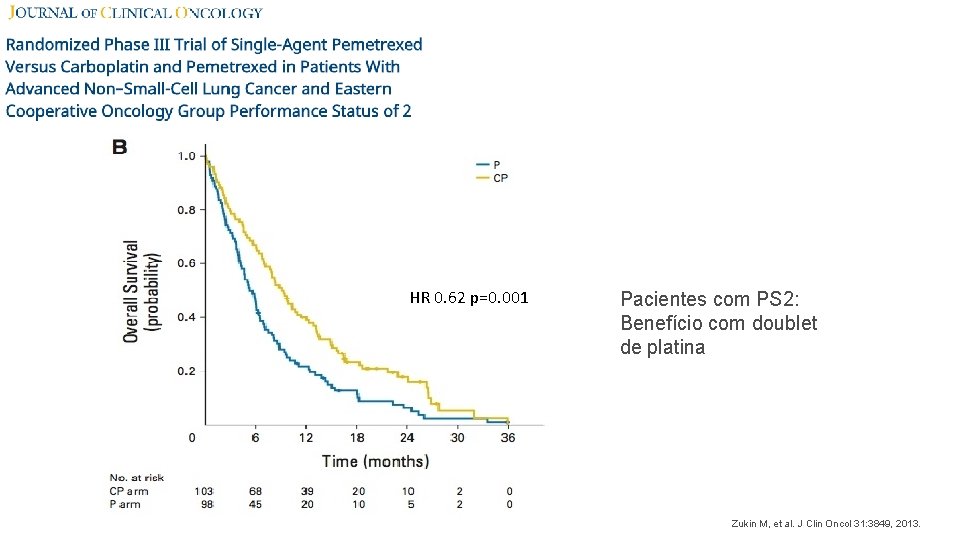
HR 0. 62 p=0. 001 Pacientes com PS 2: Benefício com doublet de platina Zukin M, et al. J Clin Oncol 31: 3849, 2013.


10 trials n=3973 pts Cochrane Database Systematic Review, Aug, 2013

Tratamento de Manutenção

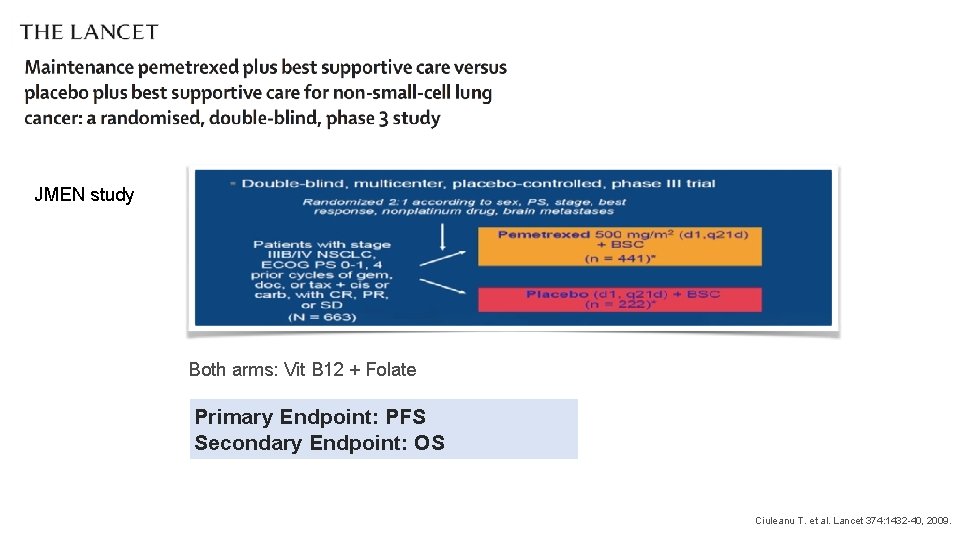
JMEN study Both arms: Vit B 12 + Folate Primary Endpoint: PFS Secondary Endpoint: OS Ciuleanu T. et al. Lancet 374: 1432 -40, 2009.

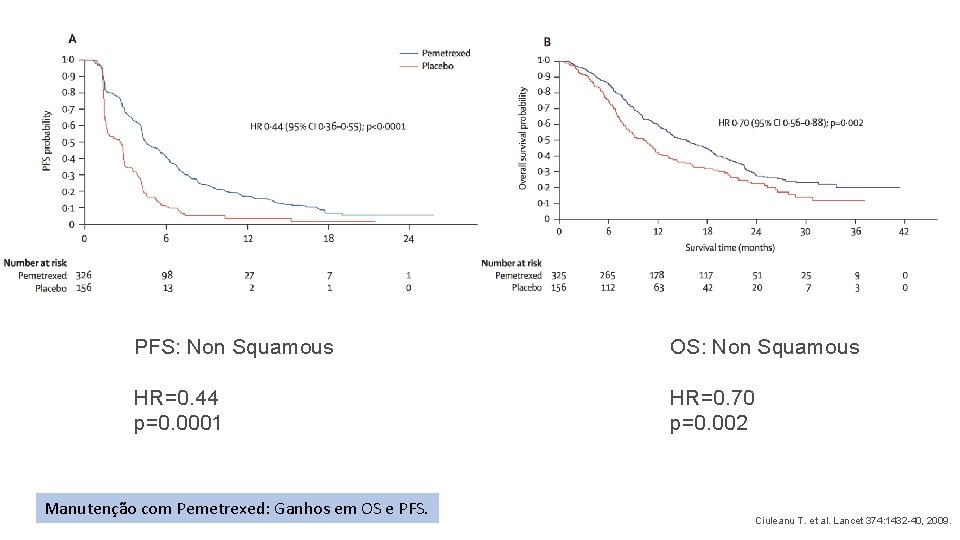
PFS: Non Squamous OS: Non Squamous HR=0. 44 p=0. 0001 HR=0. 70 p=0. 002 Manutenção com Pemetrexed: Ganhos em OS e PFS. Ciuleanu T. et al. Lancet 374: 1432 -40, 2009.

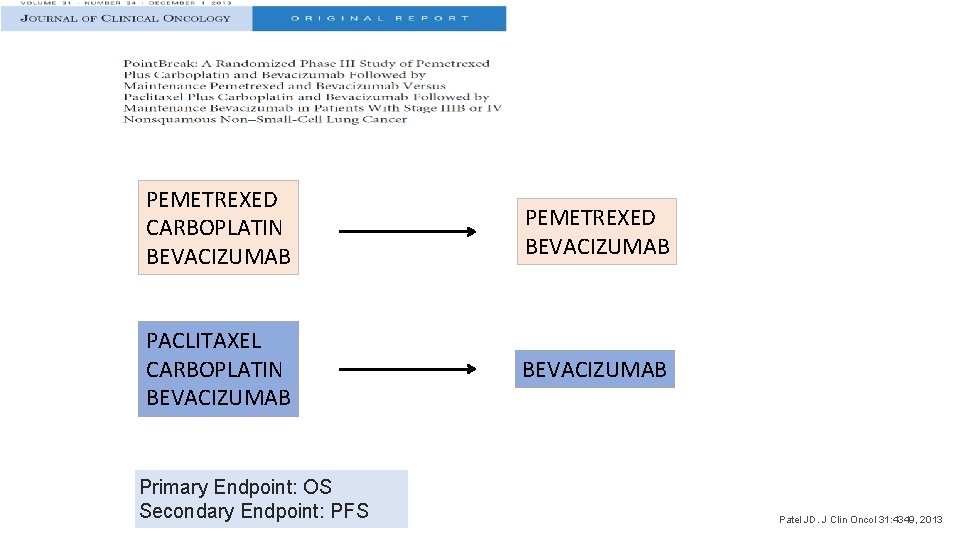
PEMETREXED CARBOPLATIN BEVACIZUMAB PEMETREXED BEVACIZUMAB PACLITAXEL CARBOPLATIN BEVACIZUMAB Primary Endpoint: OS Secondary Endpoint: PFS Patel JD. J Clin Oncol 31: 4349, 2013

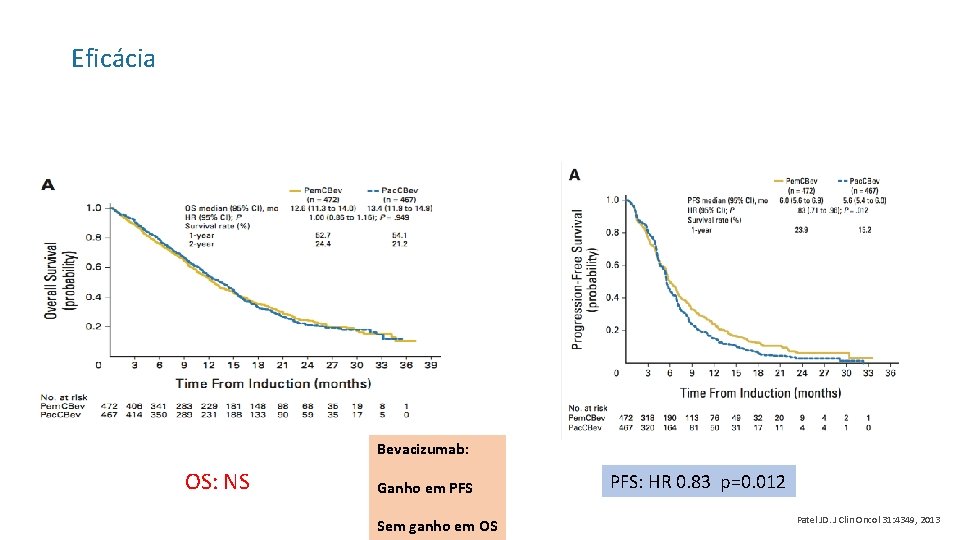
Eficácia Bevacizumab: OS: NS Ganho em PFS Sem ganho em OS PFS: HR 0. 83 p=0. 012 Patel JD. J Clin Oncol 31: 4349, 2013

2ª Linha de Quimioterapia

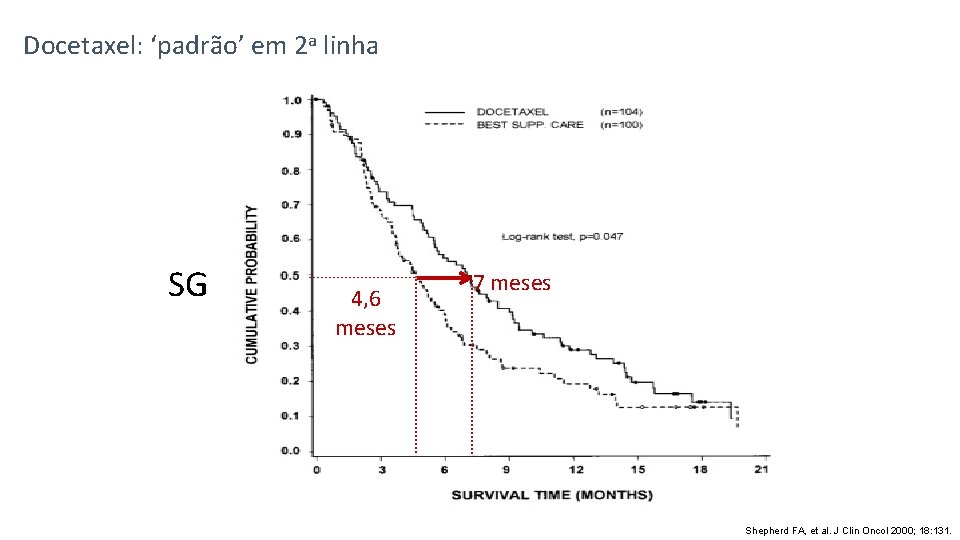
Docetaxel: ‘padrão’ em 2 a linha SG 4, 6 meses 7 meses Shepherd FA, et al. J Clin Oncol 2000; 18: 131.

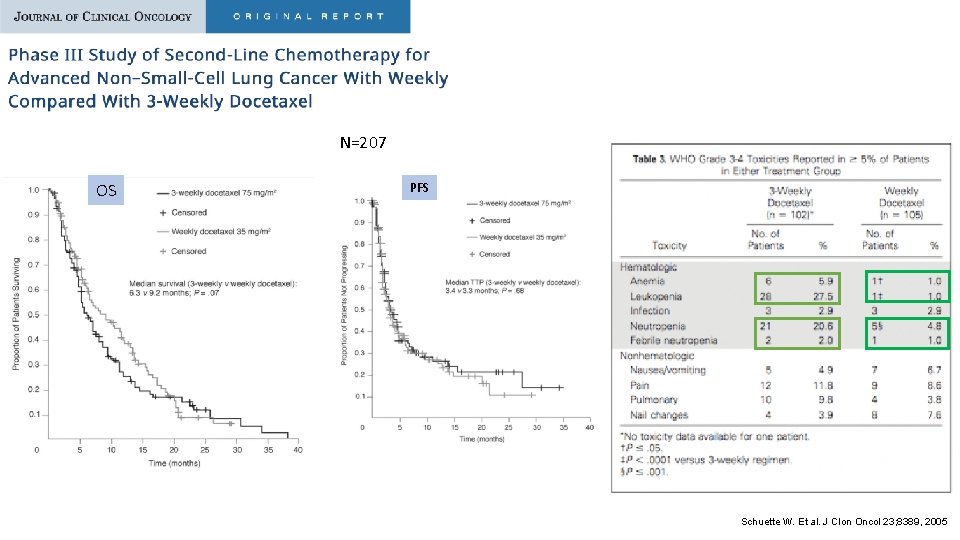
N=207 OS PFS Schuette W. Et al. J Clon Oncol 23; 8389, 2005

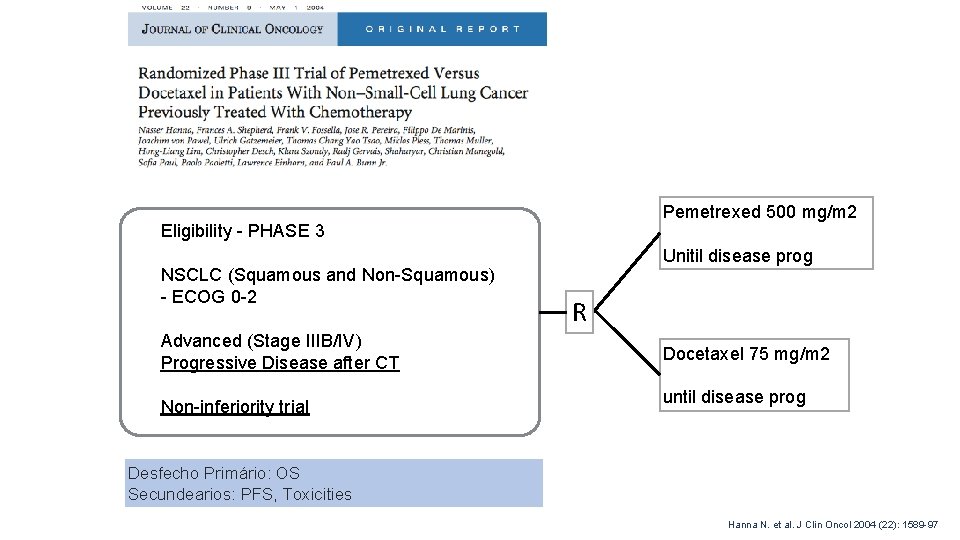
Pemetrexed 500 mg/m 2 Eligibility - PHASE 3 NSCLC (Squamous and Non-Squamous) - ECOG 0 -2 Advanced (Stage IIIB/IV) Progressive Disease after CT Non-inferiority trial Unitil disease prog R Docetaxel 75 mg/m 2 until disease prog Desfecho Primário: OS Secundearios: PFS, Toxicities Hanna N. et al. J Clin Oncol 2004 (22): 1589 -97

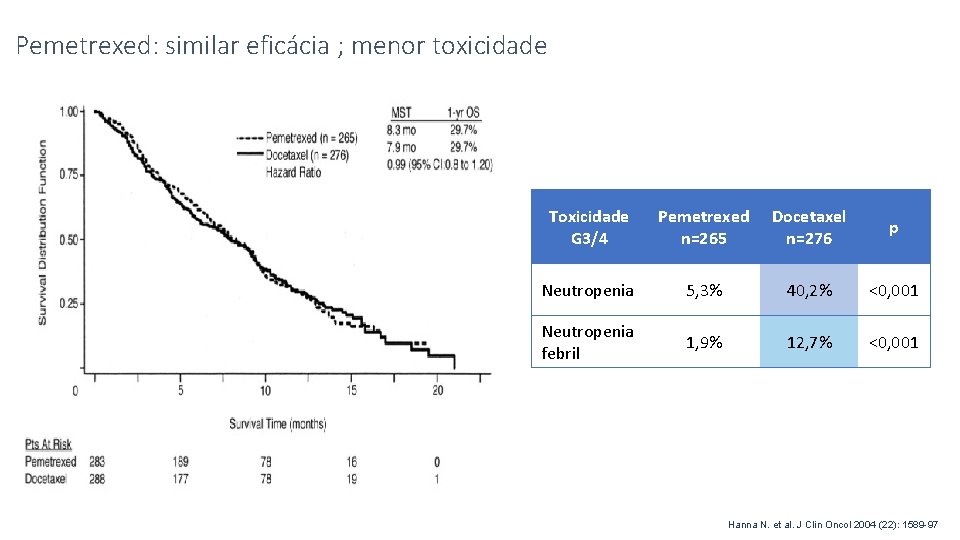
Pemetrexed: similar eficácia ; menor toxicidade Toxicidade G 3/4 Pemetrexed n=265 Docetaxel n=276 p Neutropenia 5, 3% 40, 2% <0, 001 Neutropenia febril 1, 9% 12, 7% <0, 001 Hanna N. et al. J Clin Oncol 2004 (22): 1589 -97

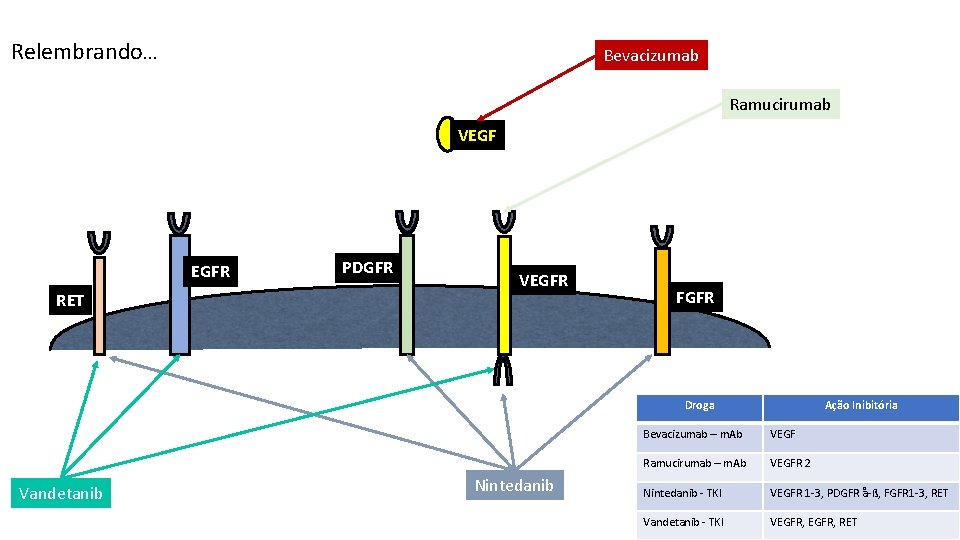
Relembrando… Bevacizumab Ramucirumab VEGF EGFR RET PDGFR VEGFR FGFR Droga Vandetanib Nintedanib Ação Inibitória Bevacizumab – m. Ab VEGF Ramucirumab – m. Ab VEGFR 2 Nintedanib - TKI VEGFR 1 -3, PDGFR å-ß, FGFR 1 -3, RET Vandetanib - TKI VEGFR, RET

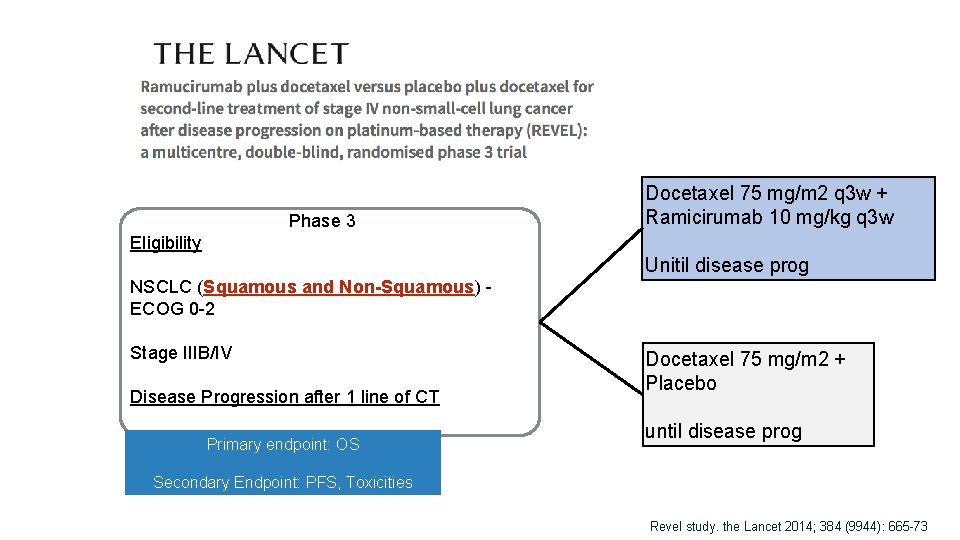
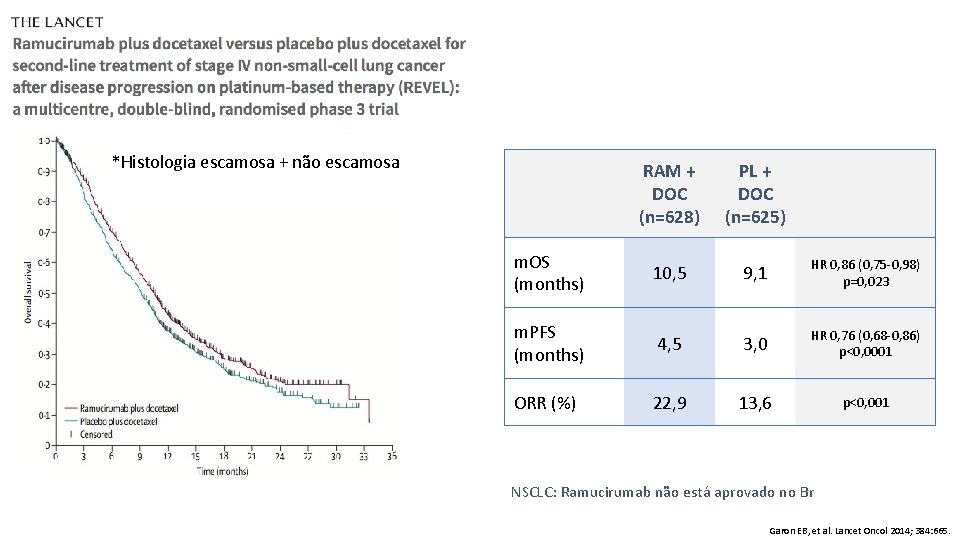
Phase 3 Docetaxel 75 mg/m 2 q 3 w + Ramicirumab 10 mg/kg q 3 w Eligibility Unitil disease prog NSCLC (Squamous and Non-Squamous) ECOG 0 -2 Stage IIIB/IV Disease Progression after 1 line of CT Primary endpoint: OS Docetaxel 75 mg/m 2 + Placebo until disease prog Secondary Endpoint: PFS, Toxicities Revel study. the Lancet 2014; 384 (9944): 665 -73

*Histologia escamosa + não escamosa RAM + DOC (n=628) PL + DOC (n=625) m. OS (months) 10, 5 9, 1 HR 0, 86 (0, 75 -0, 98) p=0, 023 m. PFS (months) 4, 5 3, 0 HR 0, 76 (0, 68 -0, 86) p<0, 0001 ORR (%) 22, 9 13, 6 p<0, 001 NSCLC: Ramucirumab não está aprovado no Br Garon EB, et al. Lancet Oncol 2014; 384: 665.

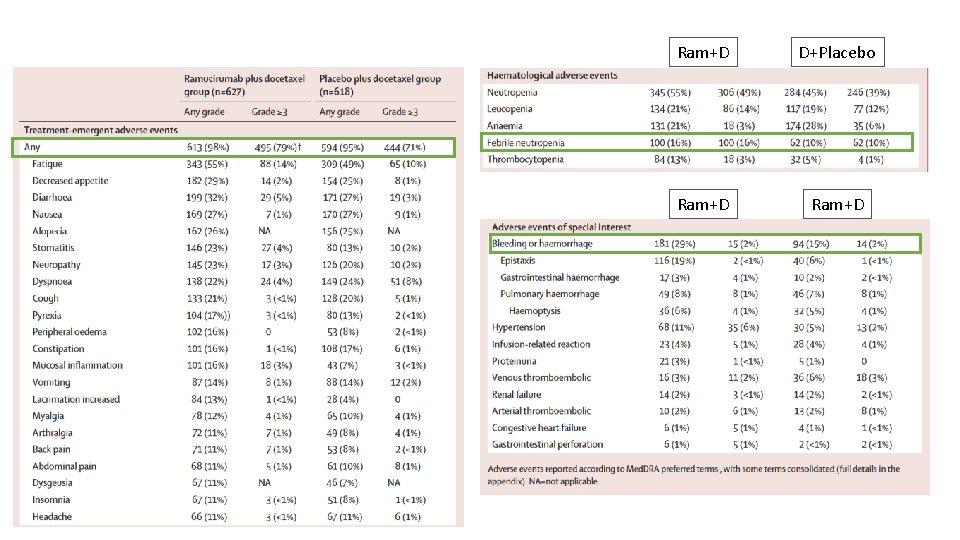
Ram+D D+Placebo Ram+D Toxicidades

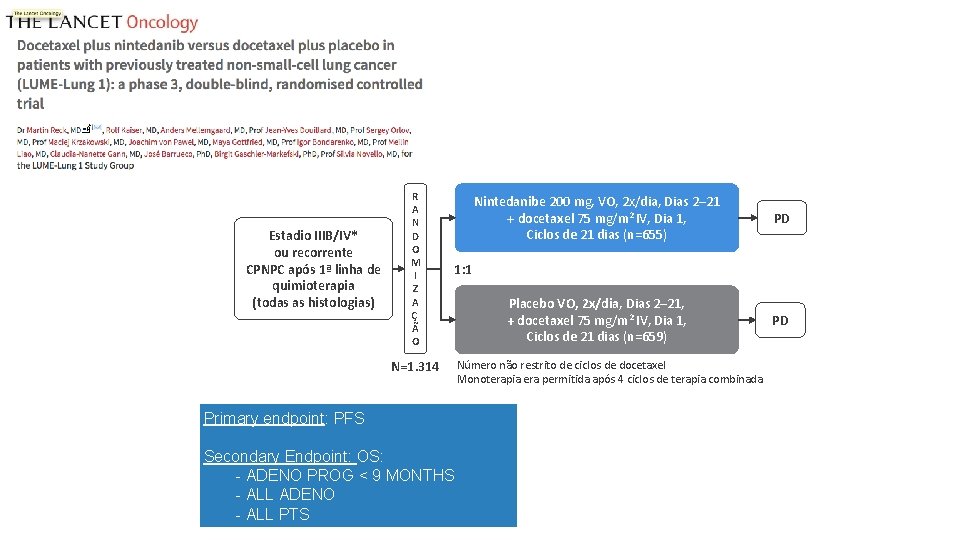
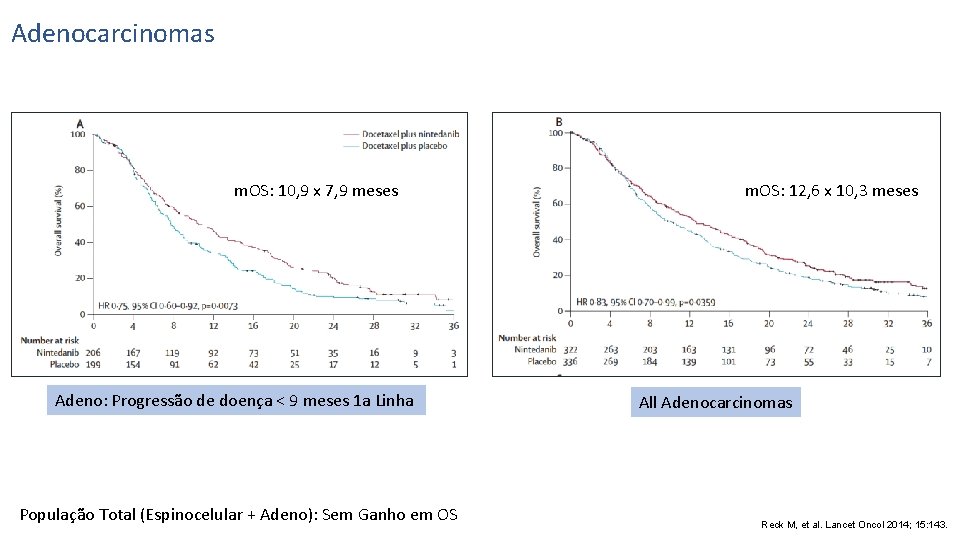
Estadio IIIB/IV* ou recorrente CPNPC após 1ª linha de quimioterapia (todas as histologias) R A N D O M I Z A Ç Ã O Nintedanibe 200 mg, VO, 2 x/dia, Dias 2– 21 + docetaxel 75 mg/m 2 IV, Dia 1, Ciclos de 21 dias (n=655) PD Placebo VO, 2 x/dia, Dias 2– 21, + docetaxel 75 mg/m 2 IV, Dia 1, Ciclos de 21 dias (n=659) PD 1: 1 N=1. 314 Primary endpoint: PFS Secondary Endpoint: OS: - ADENO PROG < 9 MONTHS - ALL ADENO - ALL PTS Número não restrito de ciclos de docetaxel Monoterapia era permitida após 4 ciclos de terapia combinada

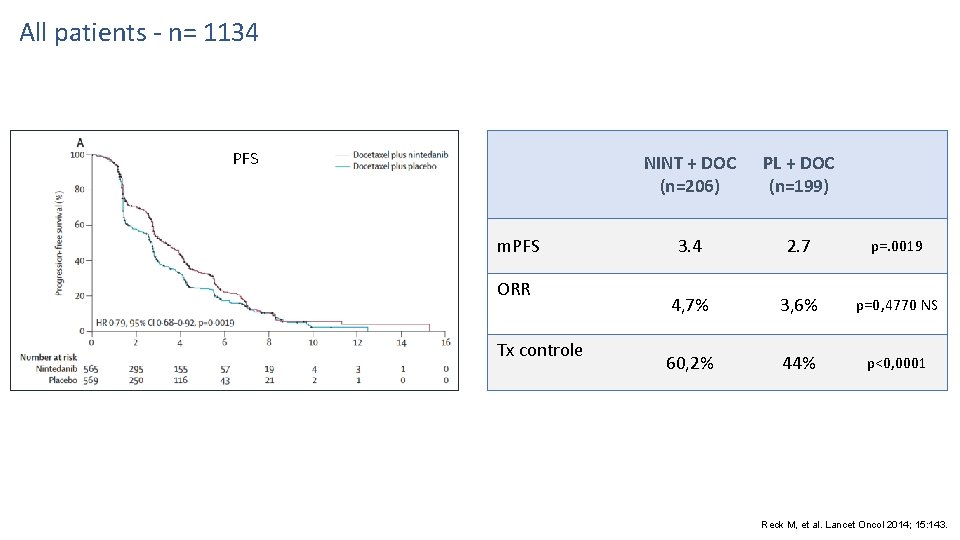
All patients - n= 1134 PFS m. PFS ORR Tx controle NINT + DOC (n=206) PL + DOC (n=199) 3. 4 2. 7 p=. 0019 4, 7% 3, 6% p=0, 4770 NS 60, 2% 44% p<0, 0001 Reck M, et al. Lancet Oncol 2014; 15: 143.

Adenocarcinomas m. OS: 10, 9 x 7, 9 meses Adeno: Progressão de doença < 9 meses 1 a Linha População Total (Espinocelular + Adeno): Sem Ganho em OS m. OS: 12, 6 x 10, 3 meses All Adenocarcinomas Reck M, et al. Lancet Oncol 2014; 15: 143.

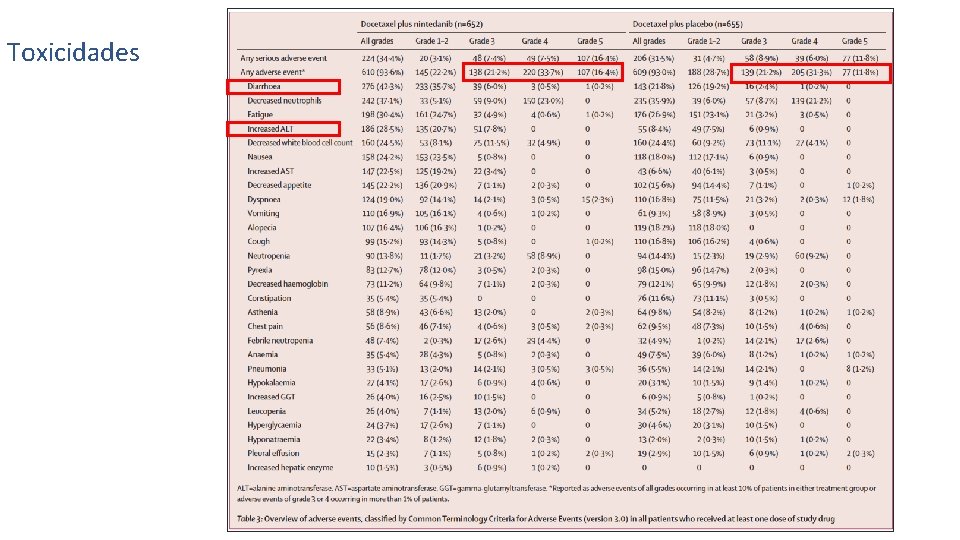
Toxicidades

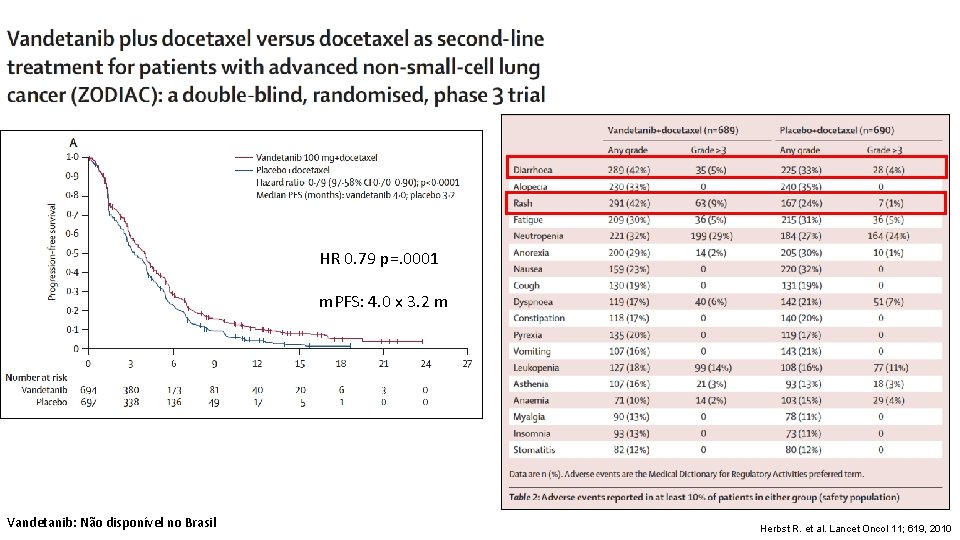
HR 0. 79 p=. 0001 m. PFS: 4. 0 x 3. 2 m Vandetanib: Não disponível no Brasil Herbst R. et al. Lancet Oncol 11; 619, 2010

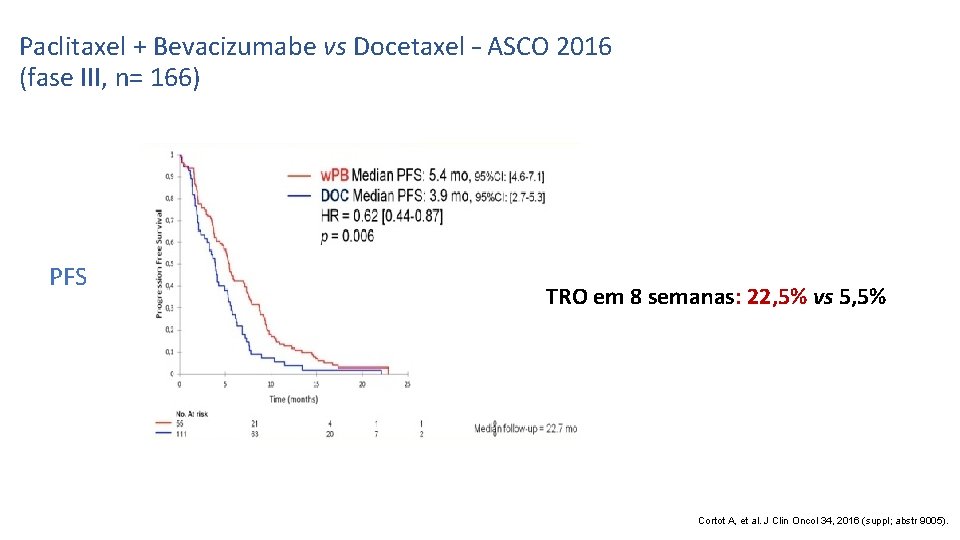
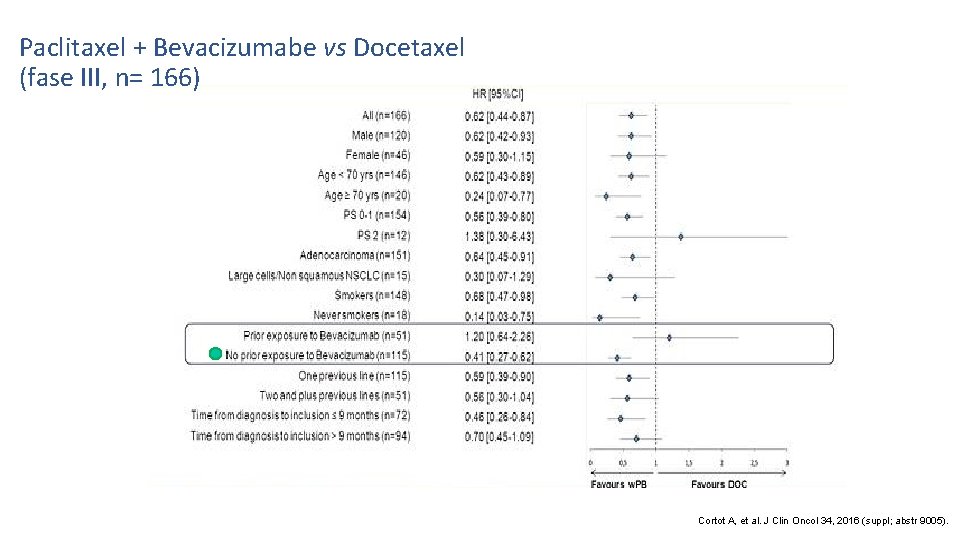
Paclitaxel + Bevacizumabe vs Docetaxel – ASCO 2016 (fase III, n= 166) PFS TRO em 8 semanas: 22, 5% vs 5, 5% Cortot A, et al. J Clin Oncol 34, 2016 (suppl; abstr 9005).

Paclitaxel + Bevacizumabe vs Docetaxel (fase III, n= 166) Cortot A, et al. J Clin Oncol 34, 2016 (suppl; abstr 9005).

Mensagens - Quimioterapia na doença metastática

Mensagens - Quimioterapia na doença metastática • QT com doublet de platina produz melhora de Qo. L e ganhos em OS. • Idosos e pacientes com PS 2: benefício em OS. • Adição de anti-angiogênicos em 1ªL e 2ªL produz ganhos em OS, às custas de maior toxicidade. • Manutenção: com Pemetrexed oferece ganhos em PFS e OS; com Bevacizumab ganhos em PFS.

Mensagens - Quimioterapia na doença metastática • QT com doublet de platina produz melhora de Qo. L e ganhos em OS. • Idosos e pacientes com PS 2: benefício em OS. • Adição de anti-angiogênicos em 1ªL e 2ªL produz ganhos em OS, às custas de maior toxicidade. • Manutenção: com Pemetrexed oferece ganhos em PFS e OS; com Bevacizumab ganhos em PFS.

Muito Obrigado f. moura@einstein. br 41 DIRETORIA COMERCIAL E MARKETING