ATOMO Laboratorio estivo di Fisica Moderna 2008 Modelli

ATOMO Laboratorio estivo di Fisica Moderna 2008

Modelli atomici – Democrito (460 a. C. ) ipotizza l’esistenza di particelle indivisibili chiamate “Atomi”. . . Modelli principali: • J. J. Thomson (1865 -1940) • E. Rutherford (1871 -1937) • N. Bohr (1885 -1962)

J. J. Thomson 1865 -1940 • Nasce a Cheetham • Scopre dei corpuscoli di carica negativa, chiamati elettroni • Nobel per la Fisica (1897) • Realizza primo spettrometro di massa (1912) => determinare rapporto e-/m • Scopre isotopi

Gli elettroni, carichi negativamente, sono distribuiti casualmente in una massa fluida di carica positiva.

E. Rutherford 1871 -1937 • Nasce a Brightwater • Nobel per la Chimica (1908) • Scopre nucleo atomico • Trasmuta elemento chimico in un altro • Avanza teorie sull’esistenza dei neutroni

Gli elettroni ruotano intorno al nucleo positivo secondo orbite circolari.

N. Bohr 1885 -1962 • Nasce a Copenaghen • Nobel per la fisica (1922) • Sviluppa il principio di complementarità • Fonda CERN di Ginevra

Quasi tutta la massa atomica è nel nucleo, attorno al quale ruotano gli elettroni su orbite ben definite che rappresentano i vari stadi di energia. L’elettrone può cadere da un’orbita di alta energia ad una di bassa energia, producendo un fotone.

Esperimento di Thomson: apparato e/m Verificare in modo sperimentale il rapporto e/m

Formula utilizzata La forza di Lorentz agisce perpendicolarmente alla velocità v e al campo magnetico B: F = ev. B F = ma = m v 2/R e/m = 2 V/ (BR)^2 e = carica elettrica m = massa elettrone V= voltaggio B = costante magnetica (7, 8 *10 -4) * intensità di corrente (I) R = raggio preciso (media del raggio dx e sx)
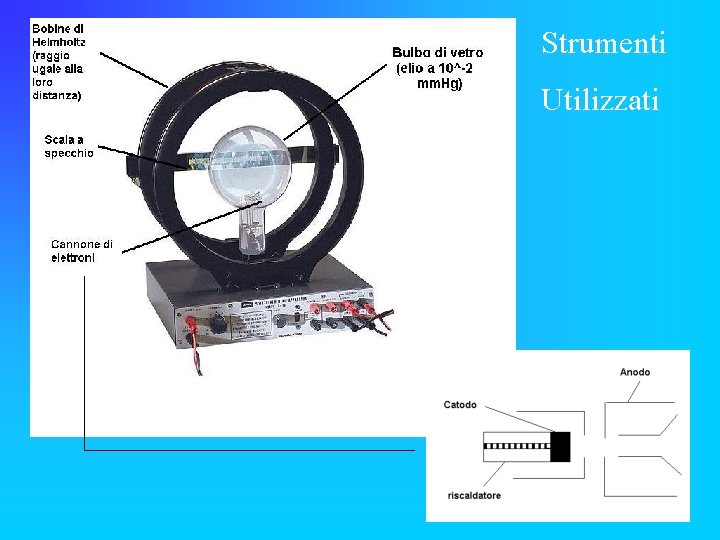
Strumenti Utilizzati

Lettura dello strumento Il passo più importante sta nel stabilire la lunghezza del raggio grazie al righello a specchio.

Procedimento Fascio di elettroni accelerato Azionamento bobine Scelta di un determinato valore di voltaggio e intensità elettrica Individuazione raggio sx e dx tramite scala a specchio raccolta dati Applicazione formula
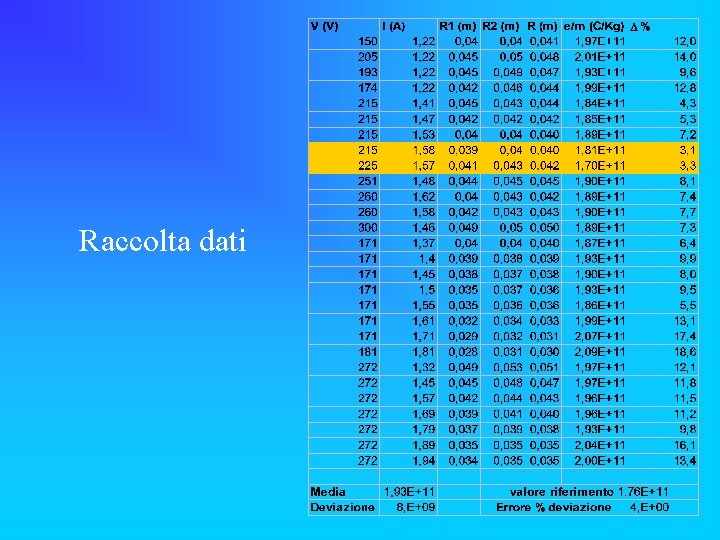
Raccolta dati

Errori sperimentali • Errata lettura dello strumento (parallasse) • Voltaggio o corrente troppo bassi o troppo alti • Mal posizionamento del cannone elettrico • Eventuali errori strumentali

Esperienza di RUTHERFORD (modello planetario) Apparato sperimentale utilizzato: sorgente radioattiva (Americio), lamina di alluminio, pompa a vuoto, cilindro a vuoto, rilevatore (fotodiodo a giunzione pn).

Modalità operative • Monto il dispositivo • Attraverso la pompa a vuoto pratico il vuoto nel cilindro • Collego ad un computer il rilevatore. • Posiziono la sorgente radioattive e la lamina di alluminio perpendicolarmente al rilevatore. • Tramite il rilevatore misuro la corrente che vi giunge proporzionale al numero di particelle che, dopo aver attraversato la lamina in un intervallo di tempo definito (60 s), lo colpiscono. • Mantenendo fisso il rilevatore ruoto la lamina e la sorgente di un certo angolo θ compreso tra ± 15° • Ripeto le operazioni precedenti più volte variando angolo.
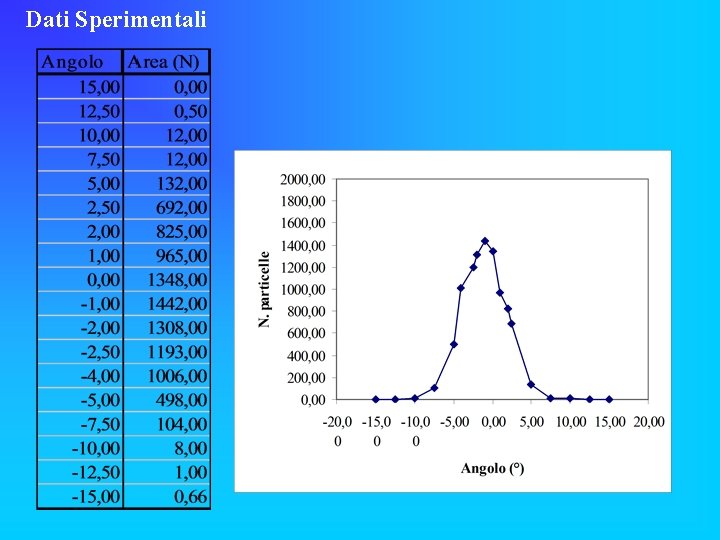
Dati Sperimentali

Curva Teorica

Osservazioni • La maggioranza delle particelle alfa prosegue in linea retta. • Alcune particelle sono deviate con un angolo diverso da 0. • Maggiore è l’angolo minore è la quantità di particelle rilevate. Conclusioni • Le particelle alfa(nuclei di elio) sono molto più piccoli dell'atomo, 10 -15. • La maggiore componente dell'atomo era lo spazio vuoto. • Non era concepibile una struttura atomica come quella rappresentata da Thomson.

Esperienza “Spettri a righe” Lo scopo dell'esperimento è quello di verificare la tesi di Bohr riguardante il modello atomico da lui proposto. nel 1913 per spiegare gli spettri a righe degli elementi.

Postulati del modello atomico di Bohr • Gli elettroni si muovono su orbite circolari attorno al nucleo • Un elettrone in moto su un orbita non irraggia • Le orbite sono soggette a una condizione di quantizzazione del momento angolare L = n h/2 p • Gli elettroni possono emettere o assorbire radiazioni elettromagnetiche quando passano da un’orbita all’altra E 2 - E 1 = hn H: costante di Plank = 6. 63*10^ -34 J*s

Gli spettri a righe Se si fornisce energia ad un elettrone, questo è in grado di emettere, sotto forma di radiazione luminosa, questa stessa energia, tornando nel suo stato fondamentale. Tale energia emessa viene poi assorbita su lastre o appositi strumenti e rappresentata nei cosiddetti spettri a righe. 2 tipi di spettri: -continuo: dispersione della luce bianca nelle sue componenti -discontinuo: assorbimento di determinate lunghezze d’onda da parte di un particolare elemento
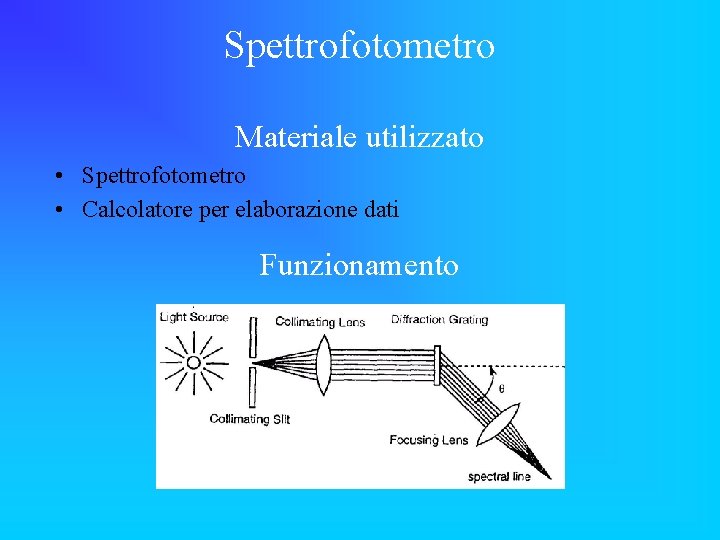
Spettrofotometro Materiale utilizzato • Spettrofotometro • Calcolatore per elaborazione dati Funzionamento

Descrizione dispositivo 1 2 3 5 7 6 4 -Lampada a spettro contenente per ogni prova un elemento differente (1) -Collimatore (2) -Lenti per focalizzare il fascio luminosos proveniente dalla lampada (3) -Base d’appoggio per lo strumento (4) -Sensore luminoso (5) -Sensore di posizione angolare (6) -Reticolo di diffrazione con fenditure di diverse grandezze (7)

Prove eseguite Sodio La radiazione luminosa della lampada a Sodio (Na) produce, una volta diffratta, uno spettro di righe colorate.
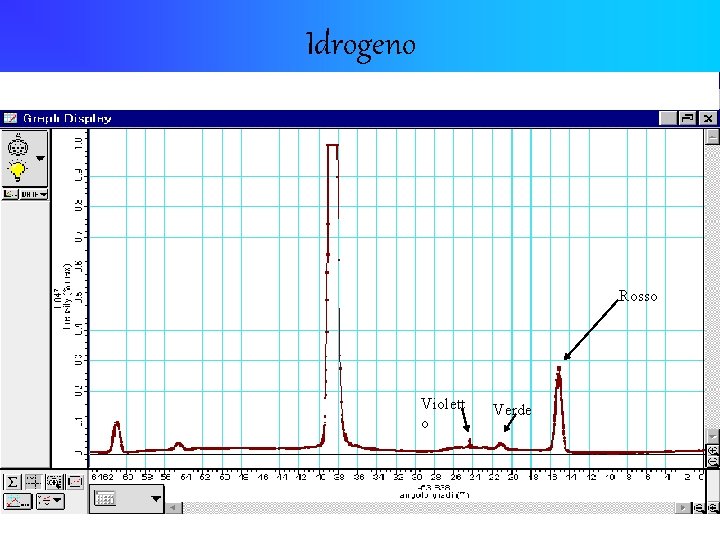
Idrogeno Rosso Violett o Verde
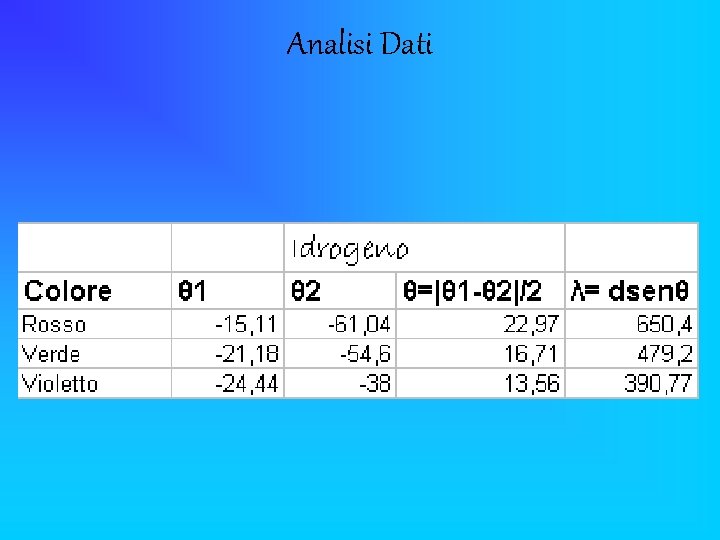
Analisi Dati
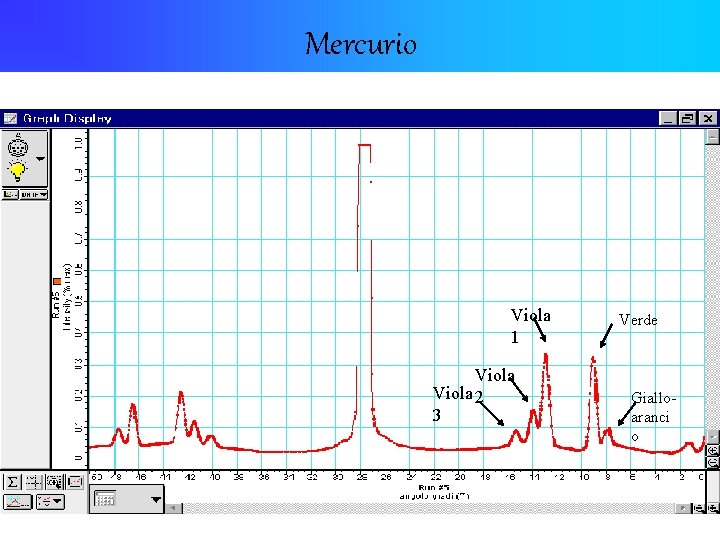
Mercurio Viola 1 Viola 2 3 Verde Gialloaranci o
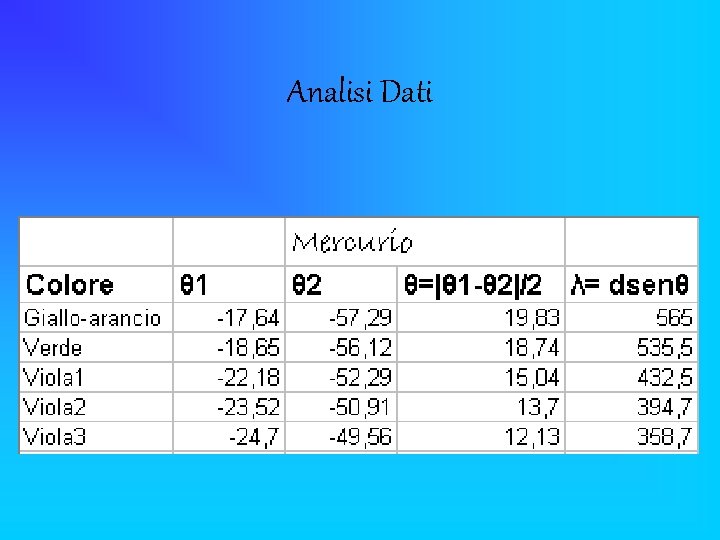
Analisi Dati

Kripton sensibilità x 10 IR 3 IR 4 IR 2 IR 1
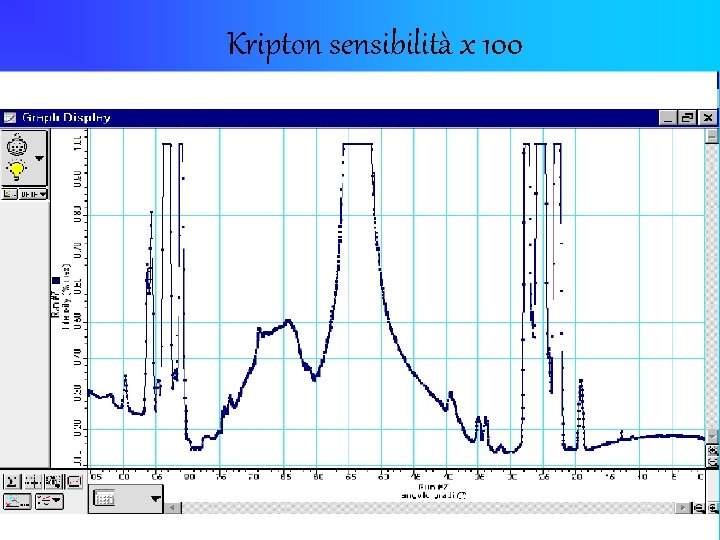
Kripton sensibilità x 100
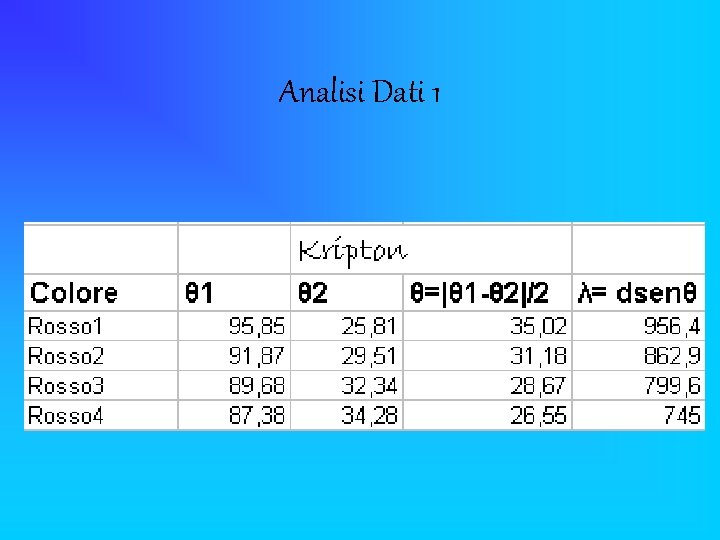
Analisi Dati 1
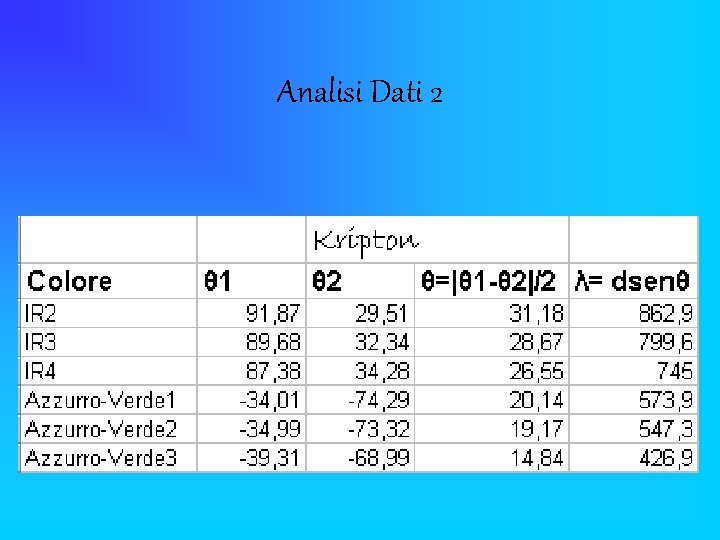
Analisi Dati 2

Conclusioni • Bohr, tramite l’esperienza degli spettri a righe riuscì a dimostrare la validità della sua teoria e dei suoi postulati e pose le basi per lo sviluppo della meccanica quantistica (energia quantizzata). • Esso dimostrò anche il raggio e l’energia dei livelli energetici sono calcolabili attraverso alcune formule matematiche. • Es: nel caso dell’Idrgoeno H • E 1 = E (n=1) = -13. 6 e. V 1 e. V = 1. 6*10^-19 J • R 1 = R (n=1) = 0. 529 A = 0. 5 * 10^-10 m = 5*10^-11 m

Gruppo Atomo • • • Bodini Laura Danelli Matteo Ghidelli Ruben Lancini Davide Madonini Claudio • • Manzoni Martina Medeghini Fabio Zangarini Maria Paola Zatti Nadia
- Slides: 36