ATOMER Hvordan er et atom bygd opp Atom

ATOMER Hvordan er et atom bygd opp?
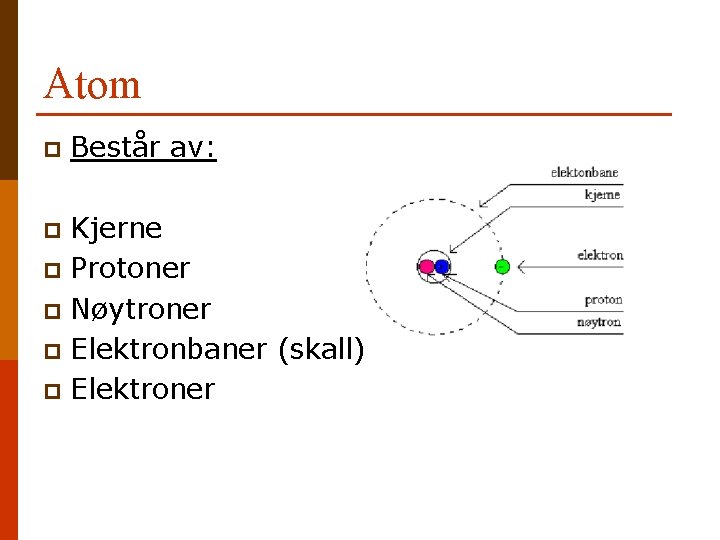
Atom p Består av: Kjerne p Protoner p Nøytroner p Elektronbaner (skall) p Elektroner p

Protoner, nøytroner og elektroner Protoner er elektrisk positivt ladet. p Nøytroner er nøytralt ladet. p Elektroner er negativt ladet. p

Størrelse Atomer er ekstremt små. p Ingen har noen gang har sett ett. p I en mynt er det ca 20 000 000 atomer. Hvis vi la disse atomene på en rekke, ville de gå nesten 60 000 ganger rundt jorda! p

Kjernen består av protoner og nøytroner som er i sentrumet av et atom. p Atomer med samme antall protoner tilhører samme grunnstoff p Atomer av samme grunnstoff, men med forskjellig antall nøytroner tilhører forskjellige isotoper. p

Rundt kjernen p Skall som heter K, L, M osv. p De tre innerste skallene har navna: - K-skallet plass til to elektroner - L-skallet plass til åtte elektroner - M-skallet plass til åtte elektroner -osv

p Elektroner svever i skallene (hvor mange elektroner avhenger av hvor stor kjernen er) - De beveger seg så fort at vi kan tenke på det som en sky.

Oktettregelen er at alle atomer vil få fylt opp det ytterste skallet. p For å få åtte elektroner så må to eller flere atomer binde seg sammen. p Da danner de ett molekyl. p
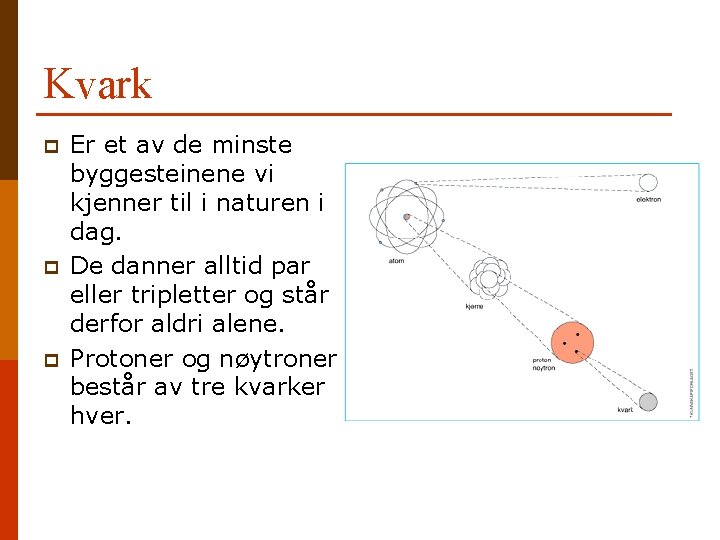
Kvark p p p Er et av de minste byggesteinene vi kjenner til i naturen i dag. De danner alltid par eller tripletter og står derfor aldri alene. Protoner og nøytroner består av tre kvarker hver.

Ion Et positivt ladet ion (kation) oppstår når et atom avgir elektroner. p Et negativt ladet ion (anion) oppstår når et atom tar opp elektroner. p

BINDINGER Hva er det og hva skjer?

Hva er det? p Atomene prøver alltid å fylle sitt ytterste skall. For å klare dette binder atomer seg sammen med andre atomer. Det er flere måter de kan binde seg sammen på.

To hovedgrupper Sterke bindinger – bindinger som er sterkt knyttet til hverandre og det er vanskelig å skille dem fra hverandre. p Svake bindinger – bindinger som ikke er så sterkt knyttet til hverandre og er lettere å skille. p
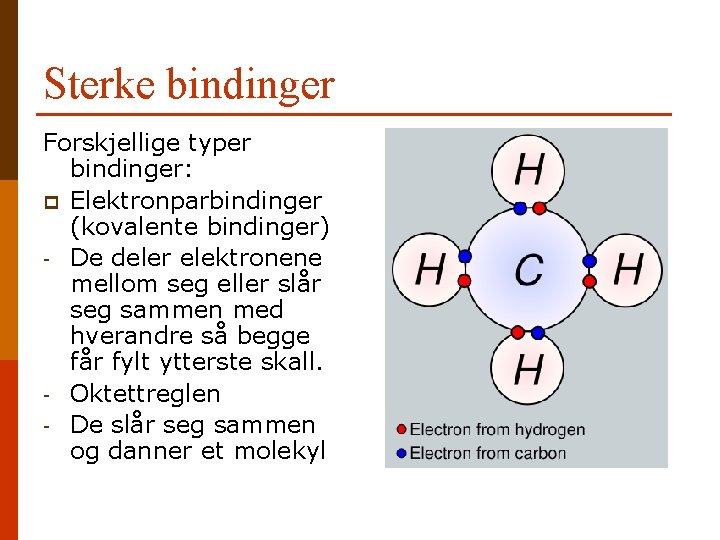
Sterke bindinger Forskjellige typer bindinger: p Elektronparbindinger (kovalente bindinger) - De deler elektronene mellom seg eller slår seg sammen med hverandre så begge får fylt ytterste skall. - Oktettreglen - De slår seg sammen og danner et molekyl

Hei, jeg er professor Atom Bind! Klikk på meg og deretter på F 2. Ha det gøy

Ionebindinger - I motsetning til elektronparbindinger stjeler det ene atomet elektroner fra det andre atomet slik at det også der oppnås oktettreglen - For at det skal være en ionebinding må begge atomene være ladde - Dvs. at det ene atomet har mistet ett elektron slik at det blir (+) og det andre har fått elektron ekstra slik at det blir (-)

Hei, her er igjen! Klikk på meg, deretter på Na. F molekylet ! Se og lær god fornøyelse
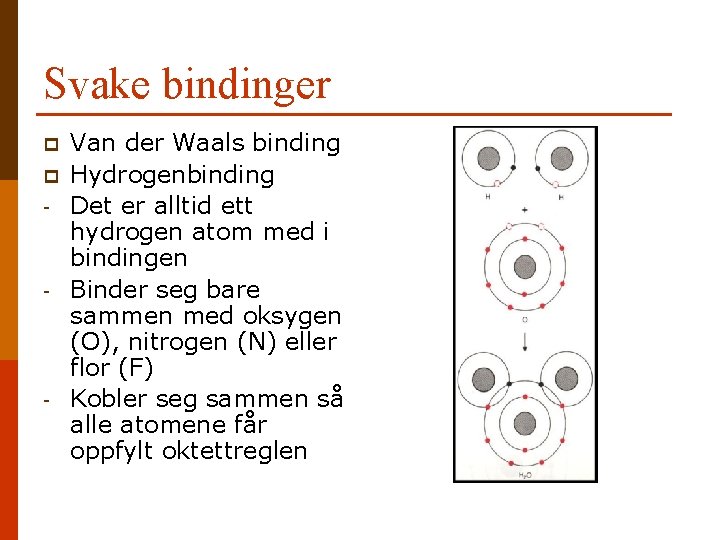
Svake bindinger p p - - - Van der Waals binding Hydrogenbinding Det er alltid ett hydrogen atom med i bindingen Binder seg bare sammen med oksygen (O), nitrogen (N) eller flor (F) Kobler seg sammen så alle atomene får oppfylt oktettreglen

Hei, her er jeg for siste gang. Denne gangen klikker du på meg også på HF. Hade bra
- Slides: 19