Atomer Elektroner Protoner Neutroner 0 Bohrs atommodell Periodiska
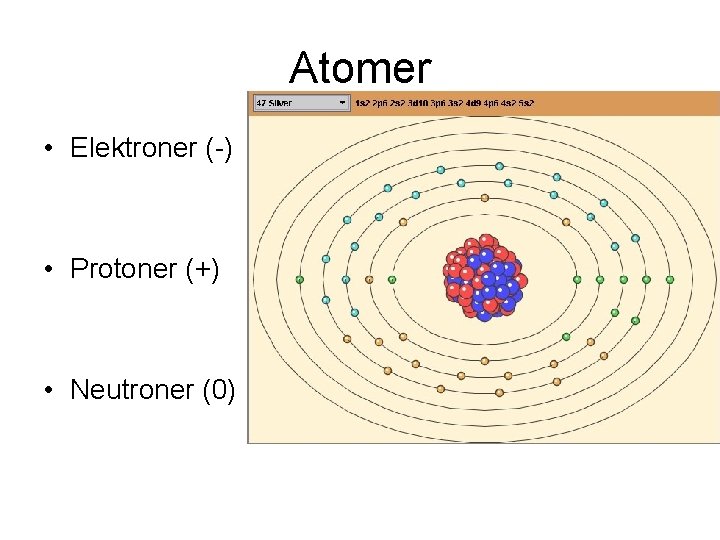
Atomer • Elektroner (-) • Protoner (+) • Neutroner (0)
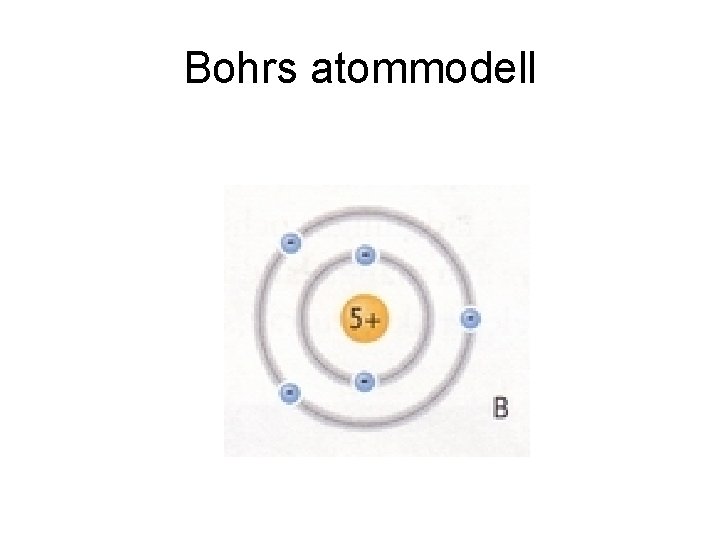
Bohrs atommodell
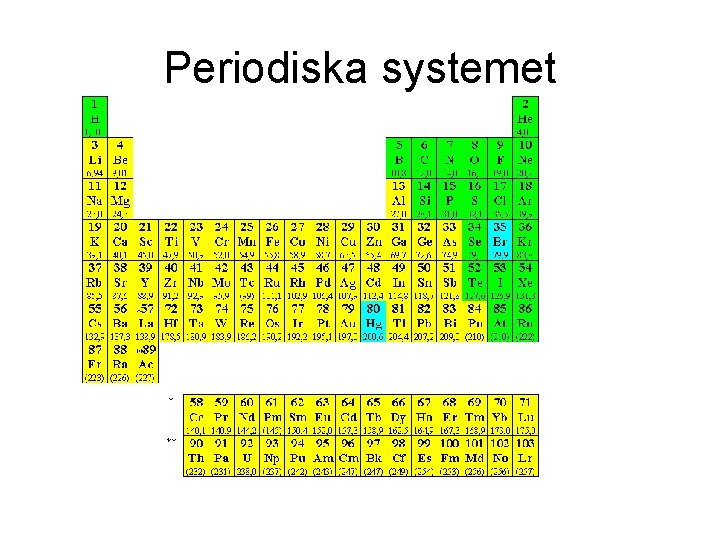
Periodiska systemet

Grupper och perioder • Alla grundämnen i samma grupp har lika många valenselektroner. • Alla ämnen i samma period har lika många elektronskal.
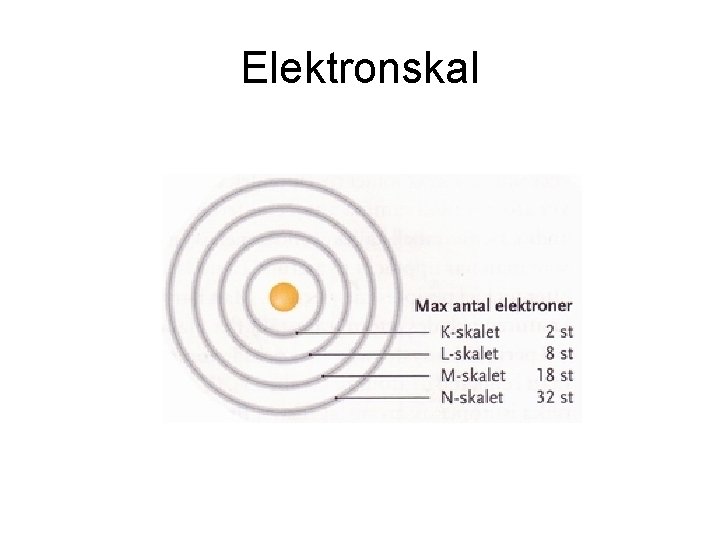
Elektronskal
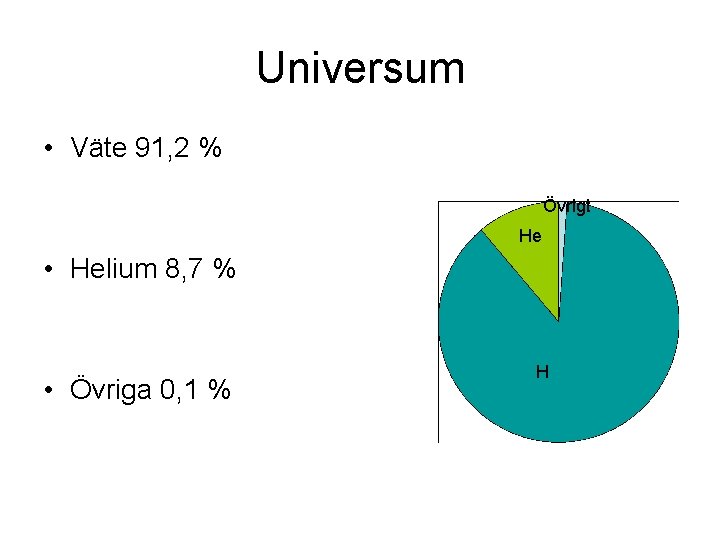
Universum • Väte 91, 2 % Övrigt He • Helium 8, 7 % • Övriga 0, 1 % H
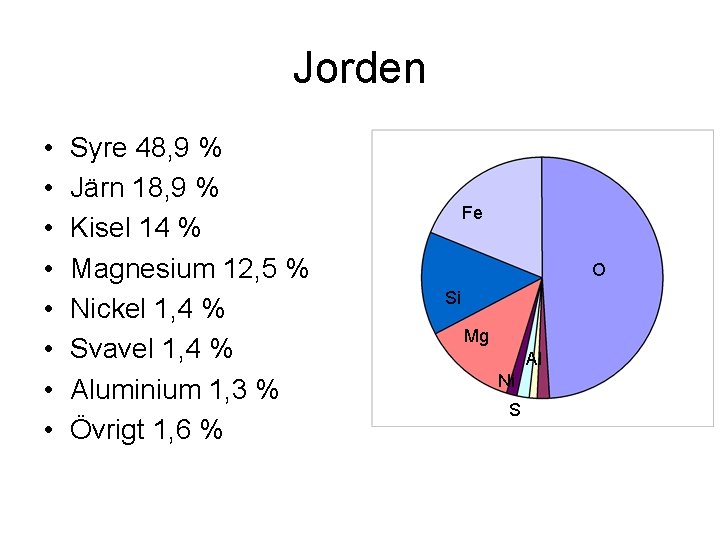
Jorden • • Syre 48, 9 % Järn 18, 9 % Kisel 14 % Magnesium 12, 5 % Nickel 1, 4 % Svavel 1, 4 % Aluminium 1, 3 % Övrigt 1, 6 % Fe O Si Mg Al Ni S
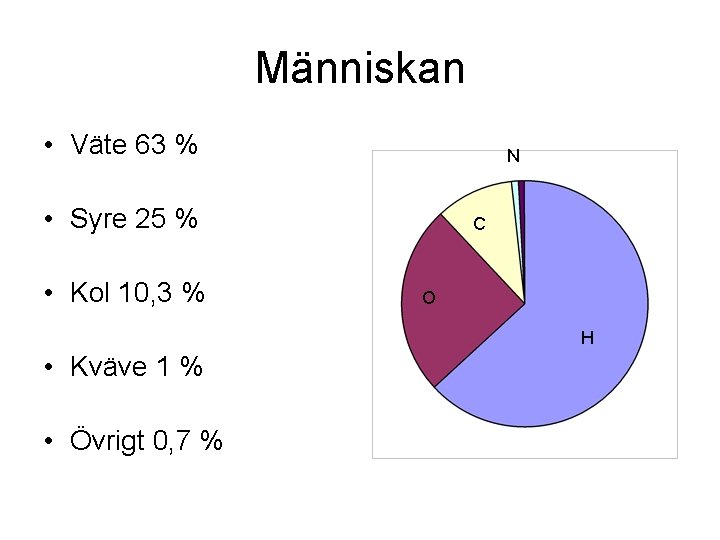
Människan • Väte 63 % N • Syre 25 % • Kol 10, 3 % C O H • Kväve 1 % • Övrigt 0, 7 %
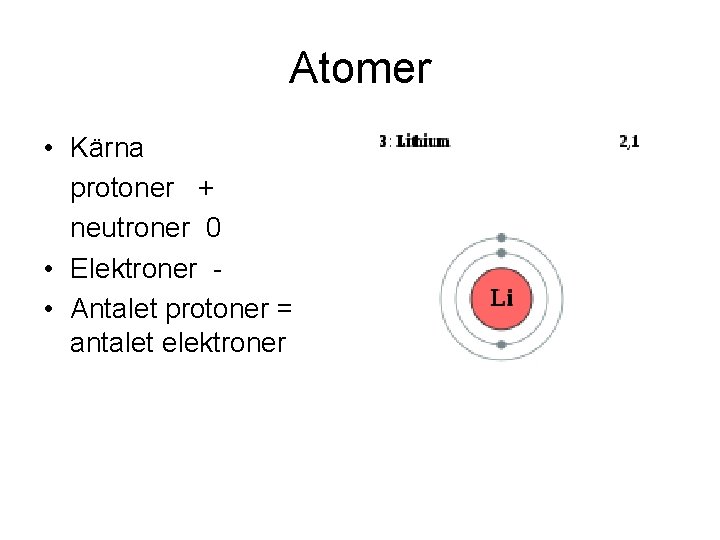
Atomer • Kärna protoner + neutroner 0 • Elektroner • Antalet protoner = antalet elektroner
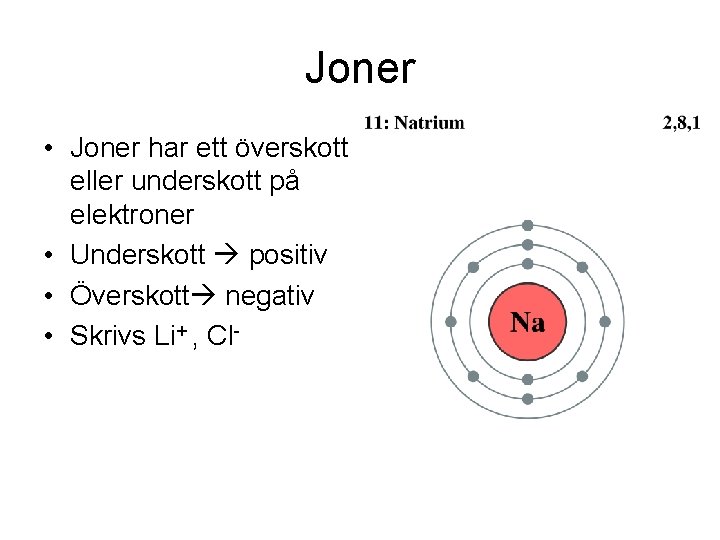
Joner • Joner har ett överskott eller underskott på elektroner • Underskott positiv • Överskott negativ • Skrivs Li+ , Cl-
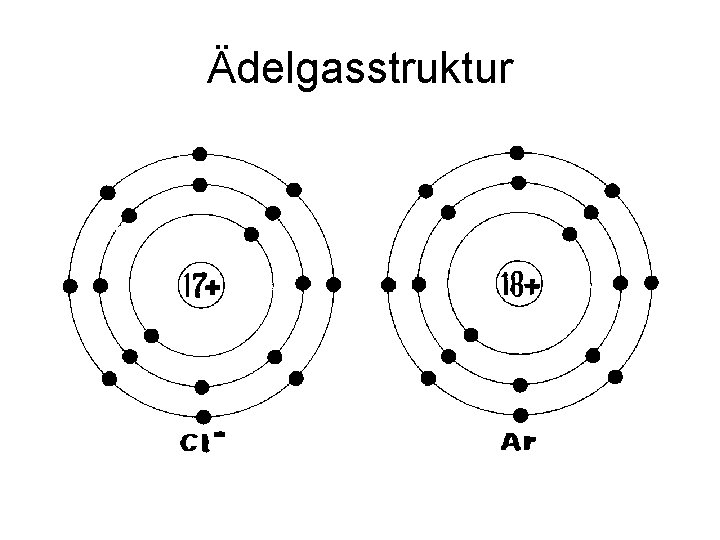
Ädelgasstruktur
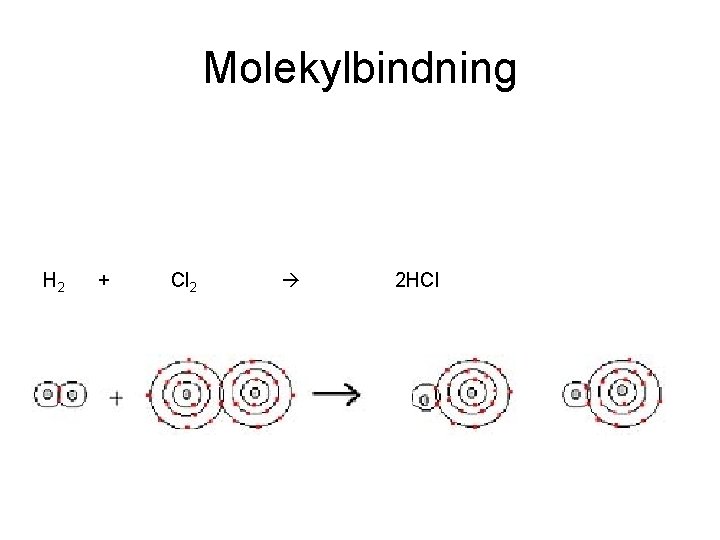
Molekylbindning H 2 + Cl 2 2 HCl
Vätemolekyl
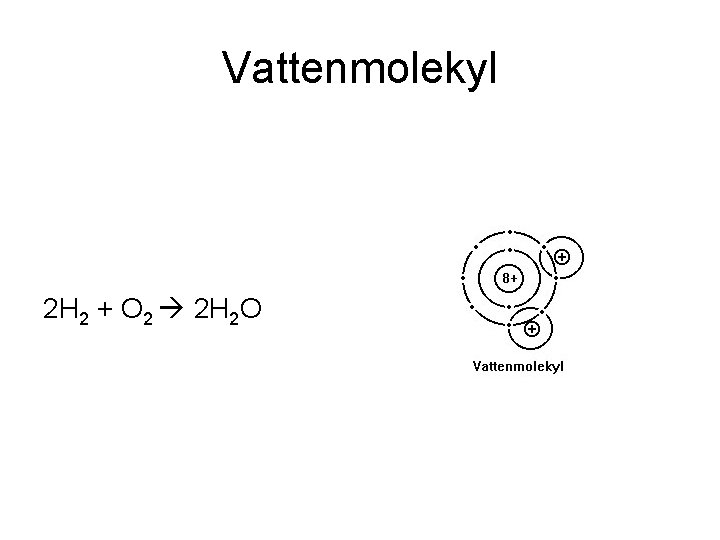
Vattenmolekyl 2 H 2 + O 2 2 H 2 O

Jonföreningar • Formelenhet ex Na. Cl • Delas upp i joner vatten • Kan bestå av sammansatta joner OH • Metallbindningar • Leder ström

Sammansatta joner
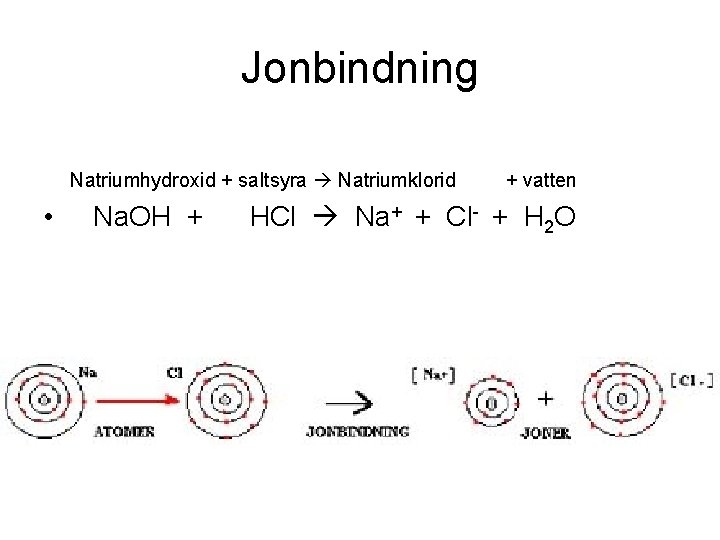
Jonbindning Natriumhydroxid + saltsyra Natriumklorid • Na. OH + + vatten HCl Na+ + Cl- + H 2 O
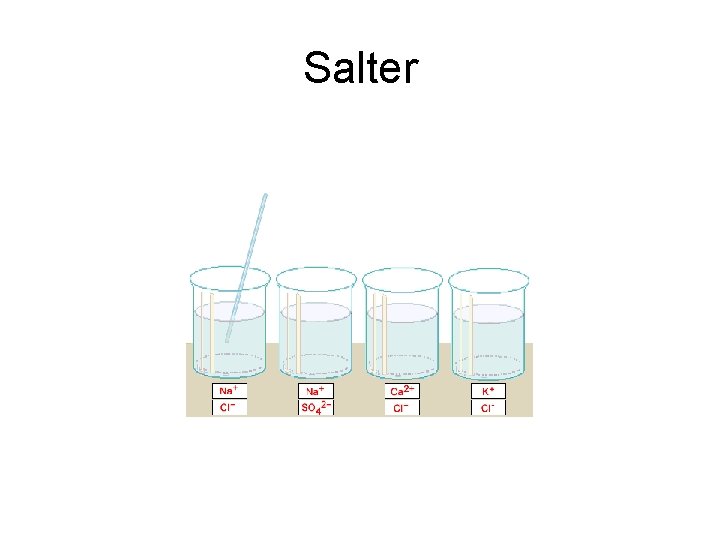
Salter

Salter • • • Vad tänker man på då man hör ordet salt? Vanligt salt-koksalt Na. Cl Salt lakrits Vägsalt Havssalt
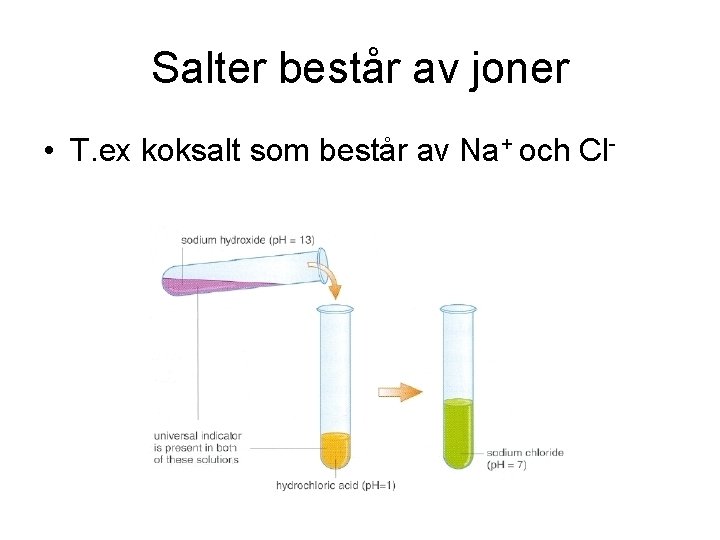
Salter består av joner • T. ex koksalt som består av Na+ och Cl-

Saltframställning • En bas och en syra-neutralisation • Metall reagerar med en syra • Metalloxid reagerar med en syra
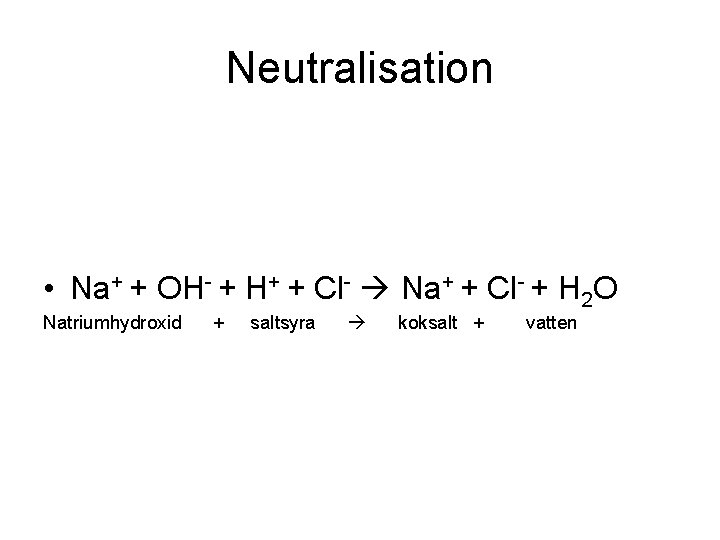
Neutralisation • Na+ + OH- + H+ + Cl- Na+ + Cl- + H 2 O Natriumhydroxid + saltsyra koksalt + vatten

Metall + syra • Zn + 2 H+ + 2 Cl- H 2 + Zn 2+ + 2 Cl. Zink + saltsyra vätgas + zinkklorid
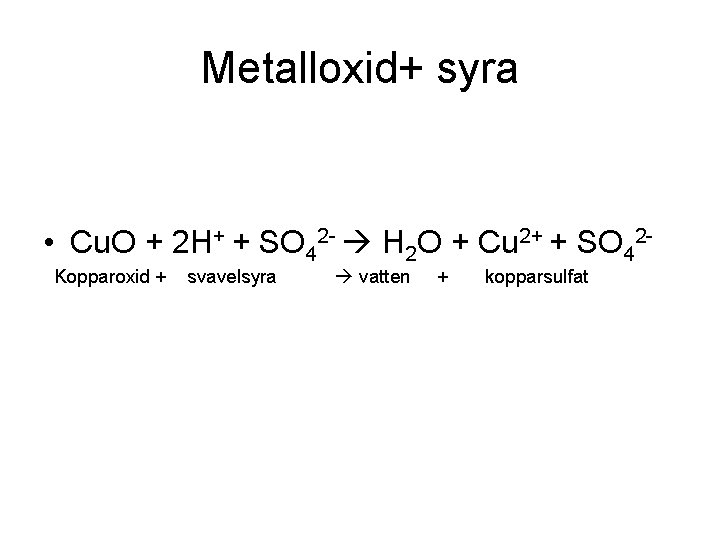
Metalloxid+ syra • Cu. O + 2 H+ + SO 42 - H 2 O + Cu 2+ + SO 42 Kopparoxid + svavelsyra vatten + kopparsulfat

Salters namn • • • Saltsyra Svavelsyra Salpetersyra Kolsyra Fosforsyra Klorider Sulfater Nitrater Karbonater Fosfater Cl. SO 42 NO 3 CO 32 PO 43 -

Några vanliga salter • Natriumklorid Na. Cl – koksalt Havsvatten Människokroppen • Bikarbonat Bakning • Handelsgödsel Kaliumnitrat KNO 3 Kalciumnitrat Ca(NO 3)2 Övergödning

Kalksten • Kalciumkarbonat Ca. CO 3 Kalksten Marmor Bränd kalk Släckt kalk

Hårt och mjukt vatten • • • Hårt vatten Kalkavlagringar Kalktvål Avhärdning Diskmaskiner

Gips • • Kalciumsulfat Ca. SO 4 Vatten molekyler ingår Gipsförband Gipsskivor

Salmiak • • Ammoniumklorid NH 4 Cl Salmiak Batterier Godis
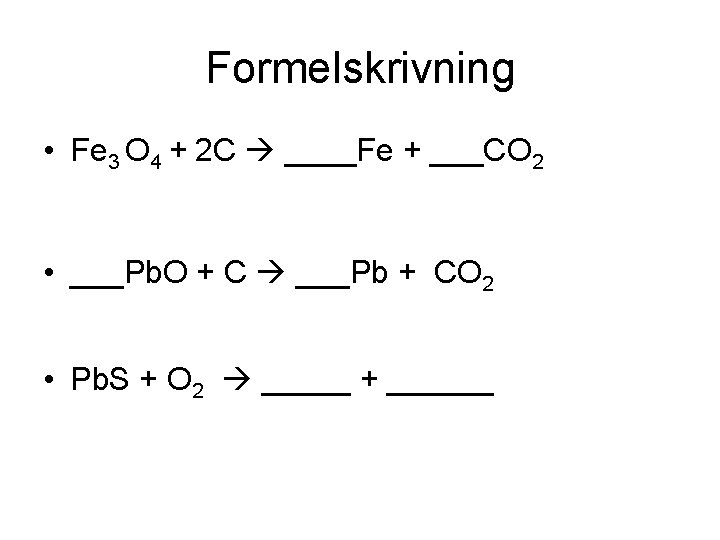
Formelskrivning • Fe 3 O 4 + 2 C ____Fe + ___CO 2 • ___Pb. O + C ___Pb + CO 2 • Pb. S + O 2 _____ + ______

Atommassa • Mäts i u (universella massenheten) = 1, 993 * 10 -23 g • Isotoper olika atommassa, men samma atomnummer • Kärnpartiklarna väger 1 u vardera • Atommassa ungefärligt masstal • Elektronernas massa försumbar

Formelmassa • Den sammanlagda massan för varje atom som ingår i en formel Ex Na. Cl formelmassa = 23 u + 35, 5 u = 58, 5 u

Mol • Lika många gram som atommassan eller formelmassan anger i u • En mol av ett ämne = 6 * 1023 atomer Ex 1 mol Na. Cl 23 g Na + 35, 5 g Cl
- Slides: 34