Atelier pratique Tocilizumab Certificat de Biothrapies 16 Juin

Atelier pratique Tocilizumab Certificat de Biothérapies 16 Juin 2012 Dr Hanan RKAIN SERVICE DE RHUMATOLOGIE, HOPITAL EL AYACHI, Pr N. HAJJAJ-HASSOUNI

• QUELLE EST LA NATURE DE TCZ?
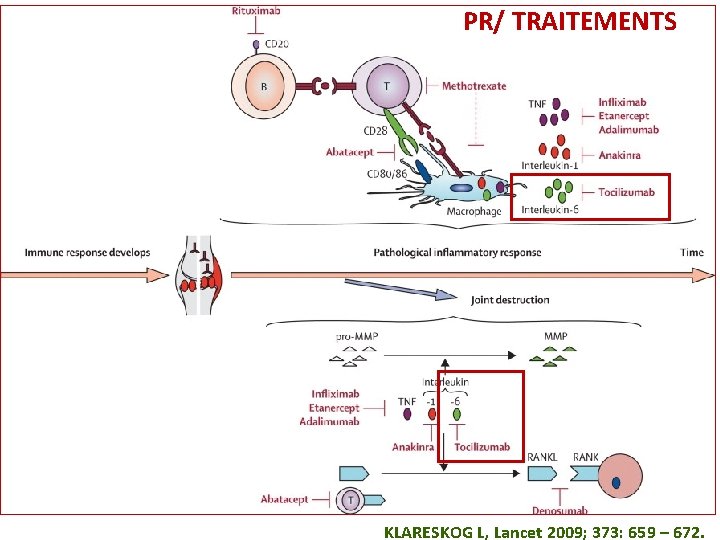
PR/ TRAITEMENTS KLARESKOG L, Lancet 2009; 373: 659 – 672.

1. Le Tocilizumab est un anticorps: q Murin q Humanisé q Chimérique
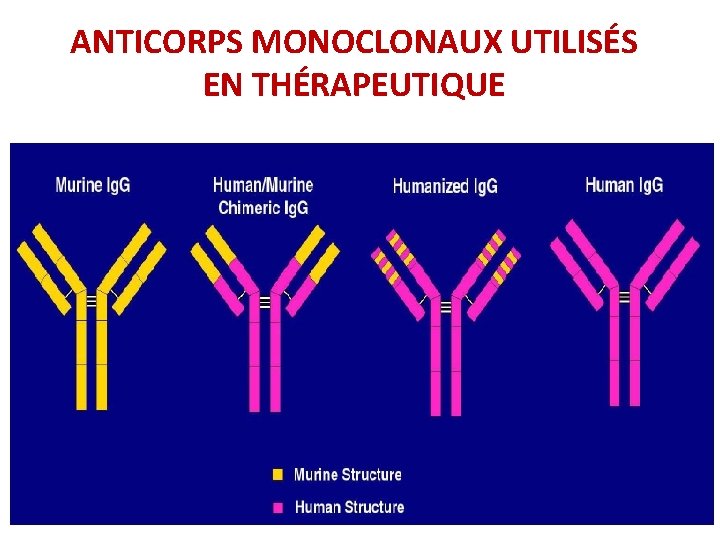
ANTICORPS MONOCLONAUX UTILISÉS EN THÉRAPEUTIQUE
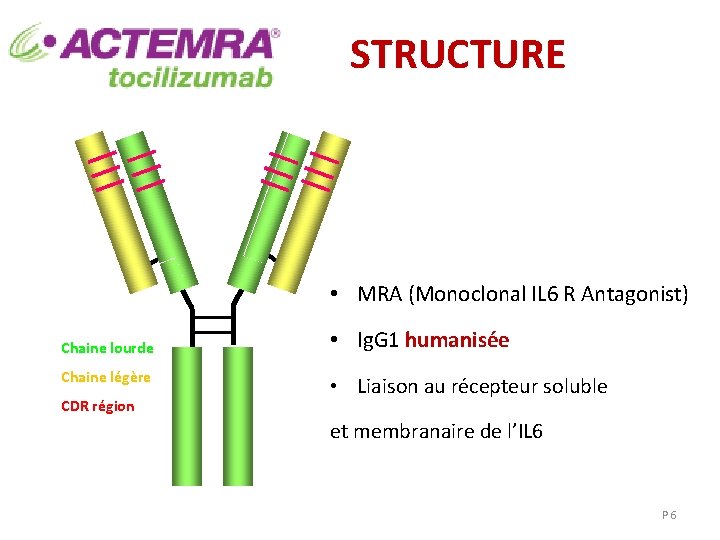
STRUCTURE • MRA (Monoclonal IL 6 R Antagonist) Chaine lourde Chaine légère CDR région • Ig. G 1 humanisée • Liaison au récepteur soluble et membranaire de l’IL 6 P 6
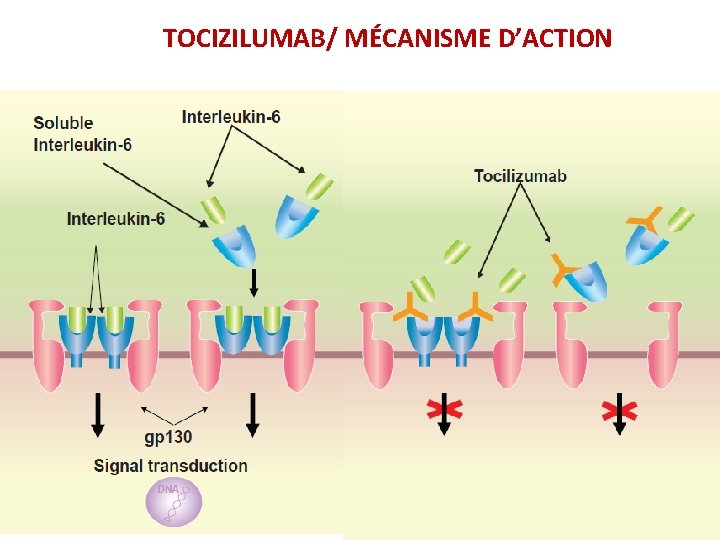
TOCIZILUMAB/ MÉCANISME D’ACTION

• QUELLES SONT LES INDICATIONS DE TCZ?

Indications q. Polyarthrite rhumatoïde q. Spondylarthrite ankylosante q. Arthrite idiopathique juvénile q. Sarcoïdose q. Maladie d’horton q. Syndrome de gougerot sjogren

Indications q. Polyarthrite rhumatoïde q. Spondylarthrite ankylosante q. Arthrite idiopathique juvénile q. Sarcoïdose q. Maladie d’horton q. Syndrome de gougerot sjogren

Indications § AMM Européenne, Japon § PR § Arthrite juvénile idiopathique forme polyarticulaire et systémique § AMM au Japon § Maladie de Still de l’adulte § Maladie de Castleman.

Le TCZ doit être associé à un DMARD et ne peut pas être utilisé en monothérapie q Oui q Non

2 Indications de TCZ/ PR • PR active, modérée à sévère : – En association au méthotrexate (MTX) chez les adultes qui ont eu soit une réponse inadéquate, soit une intolérance à au moins un traitement de fond (classique ou anti-TNF) ; – En monothérapie, en cas d’intolérance au MTX ou lorsque la poursuite du MTX est inadaptée.

2 Indications de TCZ/AIJ • PR active, modérée à sévère : – En association au méthotrexate (MTX) chez les adultes qui ont eu soit une réponse inadéquate, soit une intolérance à au moins un traitement de fond (classique ou anti-TNF) ; – En monothérapie, en cas d’intolérance au MTX ou lorsque la poursuite du MTX est inadaptée.
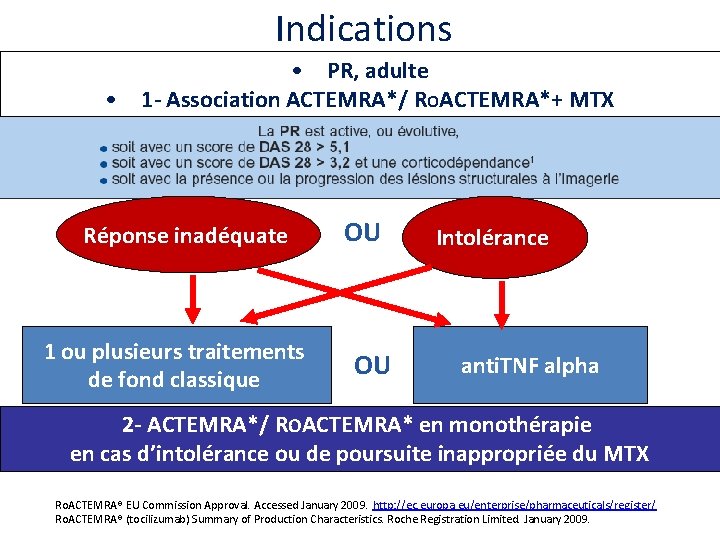
Indications • PR, adulte • 1 - Association ACTEMRA*/ ROACTEMRA*+ MTX Réponse inadéquate 1 ou plusieurs traitements de fond classique OU OU Intolérance anti. TNF alpha 2 - ACTEMRA*/ ROACTEMRA* en monothérapie en cas d’intolérance ou de poursuite inappropriée du MTX Ro. ACTEMRA® EU Commission Approval. Accessed January 2009. http: //ec. europa. eu/enterprise/pharmaceuticals/register/ Ro. ACTEMRA® (tocilizumab) Summary of Production Characteristics. Roche Registration Limited. January 2009.

• ET LE COUT DU TCZ?

COUT ANNUEL Le coût annuel du TCZ dépasse celui des anti-TNFα q. Oui qnon
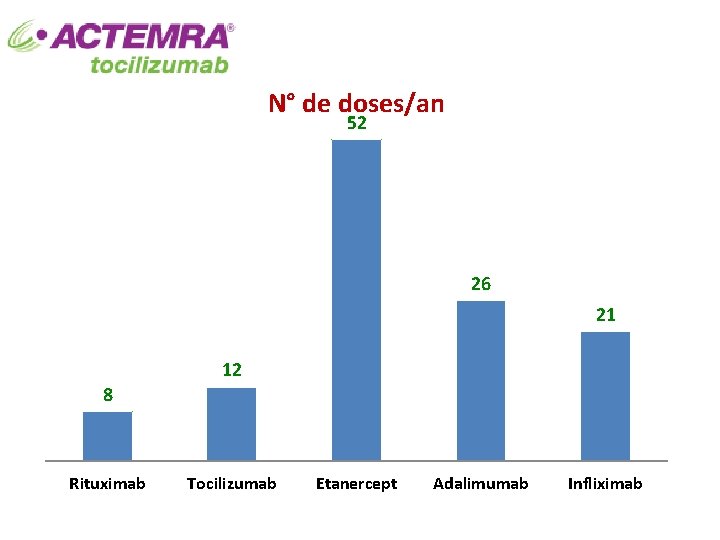
N° de doses/an 52 26 21 12 8 Rituximab Tocilizumab Etanercept Adalimumab Infliximab
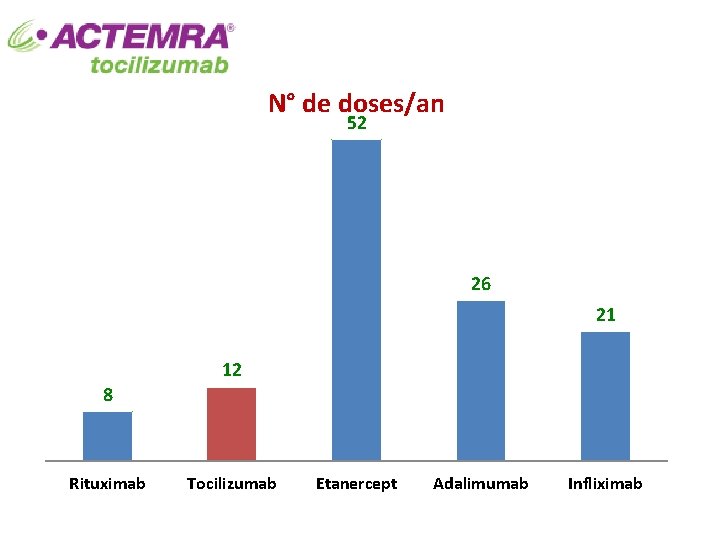
N° de doses/an 52 26 21 12 8 Rituximab Tocilizumab Etanercept Adalimumab Infliximab
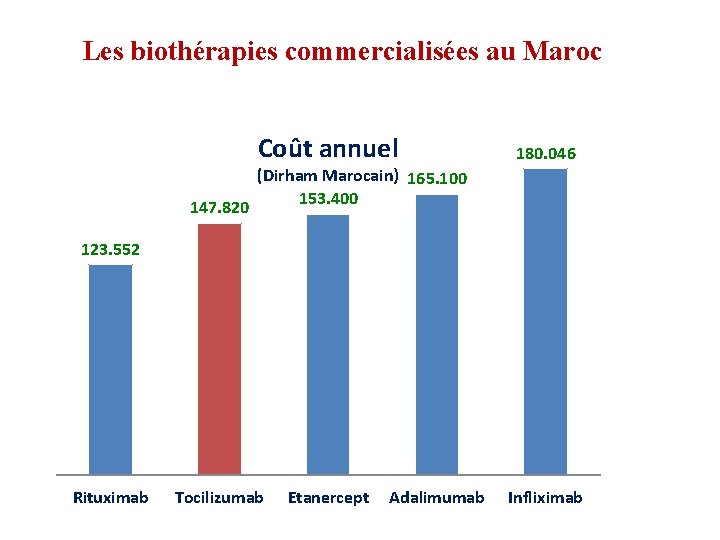
Les biothérapies commercialisées au Maroc Coût annuel 147. 820 180. 046 (Dirham Marocain) 165. 100 153. 400 123. 552 Rituximab Tocilizumab Etanercept Adalimumab Infliximab

• QUEL BILAN INITIAL?

Check up initial L’IDR est obligatoire q. Oui qnon

Bilan pré-thérapeutique initial check list Chercher systématiquement: • Contre-indications au TCZ; • Situations à risque ( précaution d’emploi).

Contre-indications • Allergie au produit; • Infection active sévère; • Néo< 5 ans; • Maladie cardiovx sévère non contrôlée.

Tuberculose § Interrogatoire, examen clinque; § IDR+ BK tubages ou crachats; § Quantiferon si IDR+; § Rx pulmonaire; § Dépistage et traitement de tuberculose active et latente.

Diverticulite § Interrogatoire, examen clinque; § ATCD de diverticulite ou intestinale; § Recher signes évocateurs. de d’ulcération

Terrains à FDR § Facteurs de risque de surinfection: diabète, diverticulose, etc § Antécédent de maladie cardiovasculaire; § ATCD de néoplasie.

Bilan pré-thérapeutique initial § NFS; § ASAT et ALAT; § Bilan lipidique avec taux cholestérol total, LDL, HDL, TG; § Sérologies hépatites B et C; § Radiographie du thorax; § Examens complémentaires à conseiller: sérologie HIV.
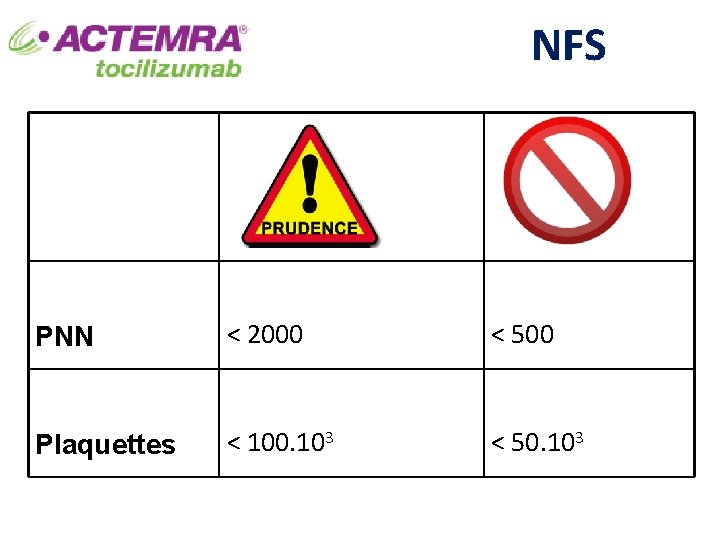
NFS PNN < 2000 < 500 Plaquettes < 100. 103 < 50. 103
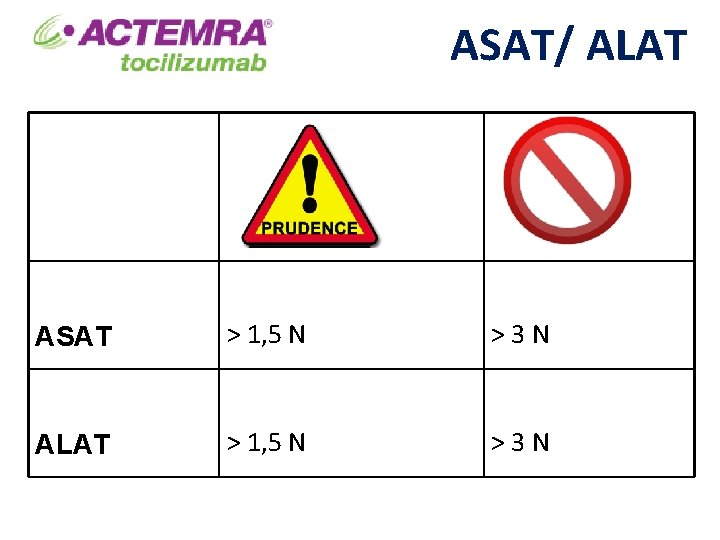
ASAT/ ALAT ASAT > 1, 5 N >3 N ALAT > 1, 5 N >3 N

Check up TCZ vs autres biothérapies Le check up du TCZ est le même que celui des anti-TNFα q. Oui q. Non

Faut-il prendre les mêmes précautions pour toutes les biothérapies ? Interrogatoire: ATCD Anti TNFα Rituximab Tocilizumab Cancer Tuberculose (contact personnel ou familial) Infections sévères, chroniques et/ou récidivantes (bactériennes, virales) IC sévère ou de maladie cardiovasculaire sévère non contrôlée Vaccin récent ( vivant: fièvre jaune, BCG) Grossesse, désir de grossesse SEP, Névrite optique ATCD de lymphome B n’est pas une CI Diverticulite

Faut-il prendre les mêmes précautions pour toutes les biothérapies ? Examen clinique Anti TNFα Rituximab Tocilizumab Infection évolutive: Fièvre, ADP Signes d’IC décompensée Signes orientant vers un cancer Signes d’auto-immunité HTA mal équilibrée ou pathologies cardiaques ischémiques Douleurs abdominales HTA, maladies CVx

Faut-il prendre les mêmes précautions pour toutes les biothérapies ? Examens complémentaires Anti TNFα Rituximab Tocilizumab NFS EPP Transaminases Sérologies hépatites B et C , sérologie VIH Rx thorax ECG En fonction de la clinique: panoramique dentaire, radiographies des sinus, ECBU IDR à la tuberculine 5 UI Recherche de BK AAN , anticorps anti-ADN natifs Dosage pondéral Ig IDR à la tuberculine 5 UI Recherche de BK Bilan lipidique

QUELS SONT LES POINTS CLES DE LA PERFUSION DE TCZ?

Perfusion § Doit être administrées en milieu hospitalier; § Sous étroit contrôle médical; § Pas de pré médication; § Tous moyens de réanimation immédiatement disponibles.
Flacons

Conservation § Conserver les flacons entre + 2 °C et + 8 °C (au réfrigérateur). § Conserver le conditionnement primaire dans l'emballage extérieur à l'abri de la lumière. § La solution diluée de TCZ pour perfusion est physiquement et chimiquement stable pendant 24 heures à 300 C et en condition strictement aseptique.

Dose à perfuser § Adulte: 8 mg/kg § Enfant: § Poids < 60 kg: Dose fixe= 480 mg § Poids> 60 kg: 8 mg/ kg sans dépasser 1, 2 g.

Matériel nécessaire § Poche 100 ml de chlorure de sodium à 0, 9%(9 mg/ml); § Seringues à usage unique; § Cathéter pour perfusion IV; § Compresses; § Garrot ; § Gants; § Alcool; § Médicaments: réaction allergique.
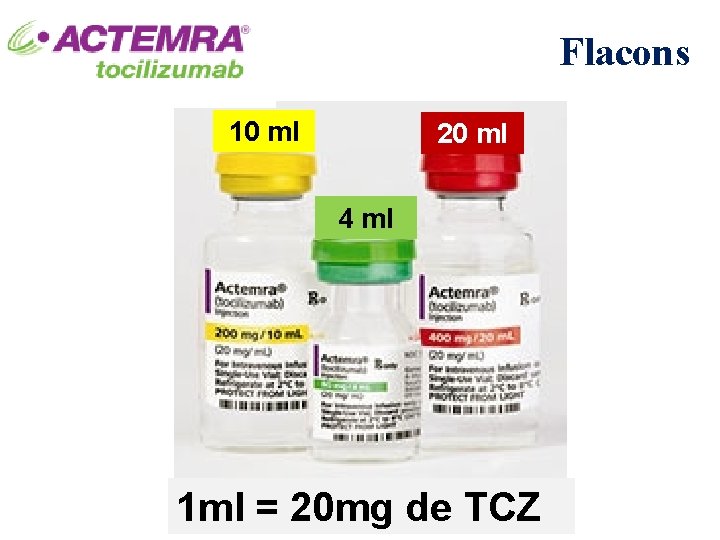
Flacons 10 ml 20 ml 4 ml 1 ml = 20 mg de TCZ

Perfusion Solution à température ambiante Asepsie: +++ 1. Prélever dose à administrer avec une seringue jetable A = 0, 8 mg/kg (1 ml=20 mg)= 0, 4 ml/kg 2. Avec une autre seringue jetable B: dans une poche pour perfusion de 100 ml de chlorure de sodium, retirer une quantité = quantité d’Actemra

Perfusion 3. Introduire dans cette poche la quantité d’Actémra prélevée dans la seringue A; 4. Mélanger avec précaution la solution, éviter la formation de mousse; 5. Contrôle visuel: particules , changement de coloration; 6. Jeter : restes de médicament non utilisés.

Perfusion • Kit pour perfusion unique; • Durée de la perfusion = 1 heure.

Perfusion Prémédication/ corticoïdes: q Obligatoire q Facultative

Pré-perfusion Reflexes obligatoires § Vérifier obligatoirement le checklist avant de démarrer chaque perfusion; § Vérifier que la prescription médicale et la CAT en cas de problème(s) sont présentes, claires et signées; § Réexpliquer au patient l’obligation de mentionner tout symptôme pouvant/ allergie.

Pré-Perfusion Demander au patient de vous signaler tout symptôme pouvant traduire une réaction allergique au produit: • Difficultés respiratoires ; • Gonflement de la langue et des lèvres; • Maux de tête ; • Chaleur et/ou de frissons; • Rougeurs et/ou prurit; • Nausées et/ou vomissements ; • Picotements du nez et/ou éternuements ; • Picotements dans la gorge; • Douleurs et/ou battements cardiaques anormalement rapides, etc…

Pré-Perfusion Situation 1 Perfusion pour la 1ère fois • Absence de facteurs prédicteurs de réactions a la perfusion • Pas de prémédication systématique Compte tenu du caractère exceptionnel des réactions à la perfusion
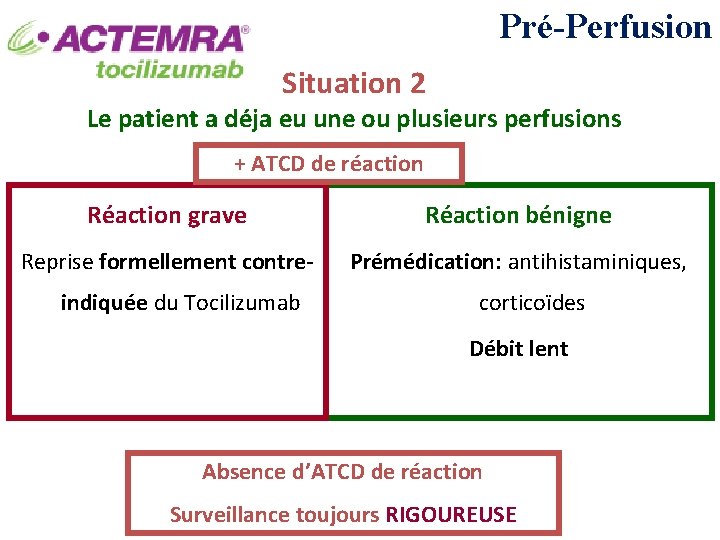
Pré-Perfusion Situation 2 Le patient a déja eu une ou plusieurs perfusions + ATCD de réaction Réaction grave Réaction bénigne Reprise formellement contre- Prémédication: antihistaminiques, indiquée du Tocilizumab corticoïdes Débit lent Absence d’ATCD de réaction Surveillance toujours RIGOUREUSE

Si survenue de réaction… Bénigne ou grave? . . . Bénigne • HTA (en cours), • Céphalées (en cours), • Rash, urticaire (au décours) Grave (0. 3%) • Réactions allergiques graves, • Anaphylaxie

Per-Perfusion Une réaction anaphylactique est un EI fréquent de la perfusion de TCZ? q Oui q Non

Per-Perfusion EI graves liés à la perfusion Réactions d’hypersensibilité (réactions allergiques graves) - Observées chez 0, 3% des patients; - Surtout entre la 2ème et la 5ème perfusion. Réactions anaphylactiques sévères - Observées chez 0, 2% des patients; - Plus fréquentes à la posologie de 4 mg/kg qu’à 8 mg/kg.
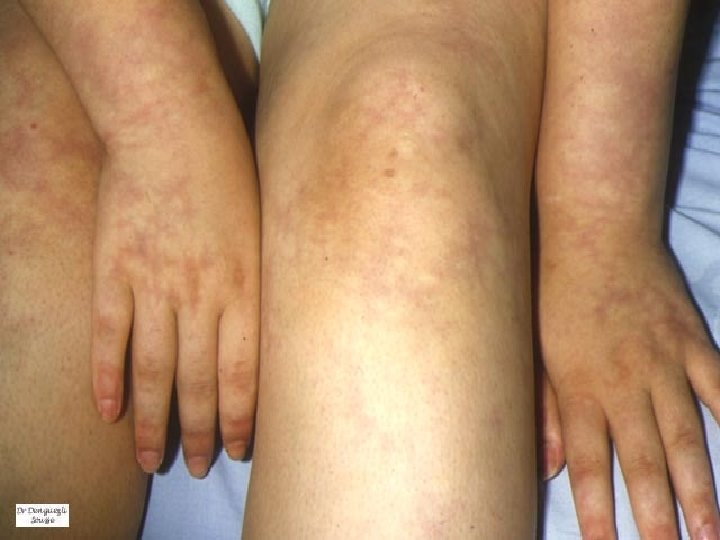
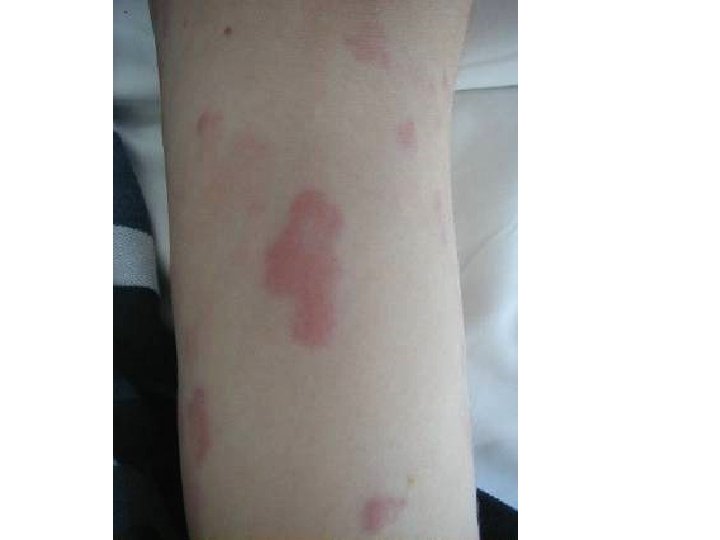
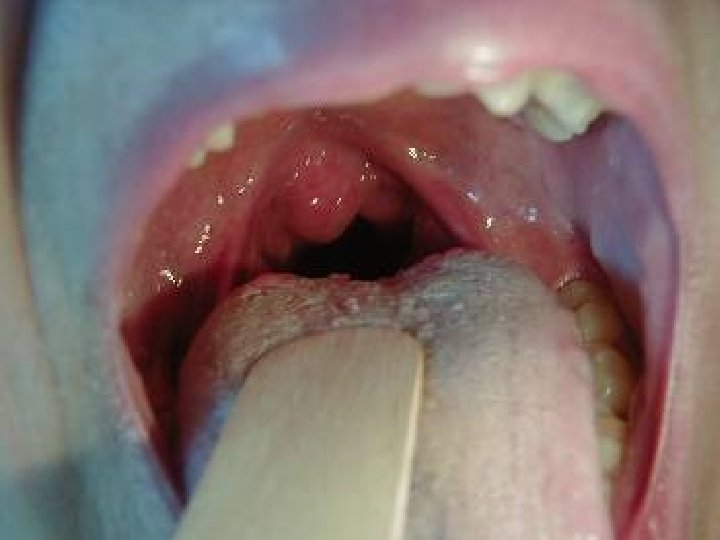
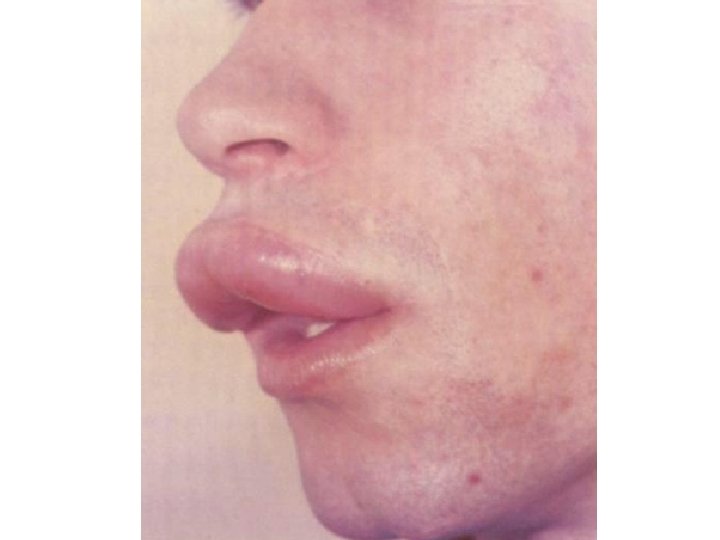
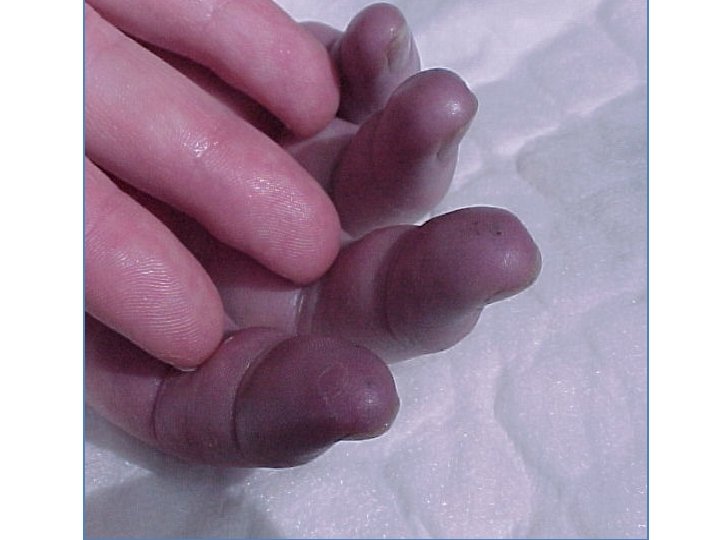
Cyanose
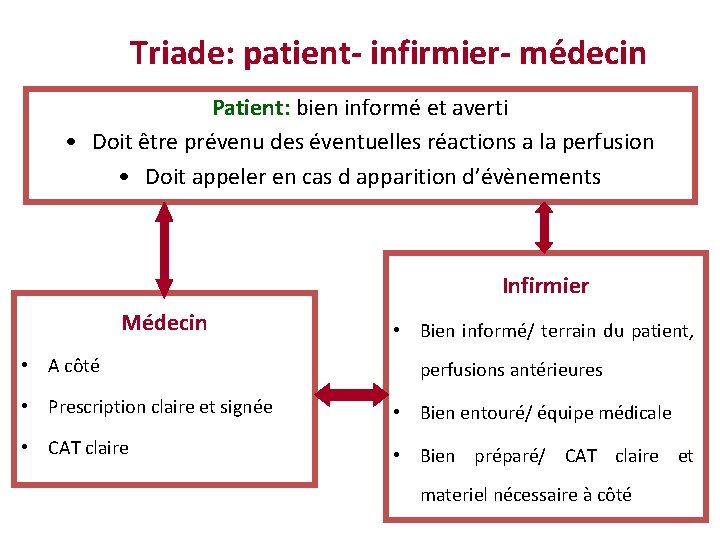
Triade: patient- infirmier- médecin Patient: bien informé et averti • Doit être prévenu des éventuelles réactions a la perfusion • Doit appeler en cas d apparition d’évènements Infirmier Médecin • A côté • Bien informé/ terrain du patient, perfusions antérieures • Prescription claire et signée • Bien entouré/ équipe médicale • CAT claire • Bien préparé/ CAT claire et materiel nécessaire à côté

Per-Perfusion CAT/ réaction allergique ? • Si symptômes RA mineure; on fera successivement les mesures suivantes: – arrêter la perfusion – administrer une demi ampoule d'atarax par voie IM ou IVL • Si des symptômes plus sévères – administration par voie parentérale de 1 mg/kg; d'équivalent prédnisone en 30 minutes; – surveiller l'évolution du patient.

Per-Perfusion CAT/ réaction allergique ? Si l'état du patient reste préoccupant : – Réanimation; – Oxygène nasal 2 l/min; – SS 0, 9% : 500 à 1000 ml en 20 min; – Adrénaline par voie sous cutanée à la dose ½ ampoule=½mg] à répéter éventuellement après 20 minutes;

Per-Perfusion Anaphylaxie/ Mots clés § Début rapide; § Peau, muqueuse; § Difficultés respiratoires; § Chute de la TA; § Symptômes de défaillance d’organes; § Adrénaline 0. 01 mg/ kg/ IM; § CI absolue de réintroduction.

Post-Perfusion Après résolution des signes, le patient • FAUX peut rentrer chez lui?

Post-Perfusion Après résolution des signes, le patient peut-il rentrer chez lui? • NON • Evolution biphasique: 5 à 20%; • Surveillance clinique de 12 heures.

EI bénins Post-Perfusion Très fréquents (plus de 1 patient sur 10): • Infections des voies respiratoires supérieures (toux et rhume), Fréquents (au moins 1 patient sur 100 et moins de 1 patient sur 10): • Infection pulmonaire, herpès, zona, infection cutanée, plaies buccales, éruption cutanée et démangeaisons, conjonctivite, maux de tête, sensations vertigineuses, augmentation de la pression artérielle, douleur de l’estomac,

• COMMENT FAIRE POUR LE BILAN DE SUIVI?

SURVEILLANCE CLINIQUE • Interrogatoire et examen clinique minutieux; • Fièvre peut manquer; • CRP et VS: peu ou pas d’utilité; • Éducation et information des patients.

Bilan de suivi • Tolérance: per et post-perfusion; • Efficacité: VS et CRP tous les 3 mois; • Structural: tous les ans;

Bilan avant chaque perfusion • NFS; • ALAT/ ASAT; • Bilan lipidique avant la 3ème perfusion: cholestérol total, LDL-cholestérol, HDL-cholestérol et triglycérides.

Juger l’efficacité • Si la baisse du DAS 28 < 0, 6 à 12 semaines, il n’est pas recommandé de poursuivre le traitement.

• CAT/ ANOMALIES DU BILAN BIOLOGIQUE DE SUIVI?

SUIVI DES PNN/ NFS Valeur labo PNN (cellules x 109/l ) CAT PNN: >1 +Maintenir dose PNN: [0. 5 -1] (par contrôle dosage) + Interrompre TCZ + Quand valeur arrive, >1 passer dose 4 mg/kg puis augmenter à 8 mg/kg si l’état clinique le permet. ANC <0. 5 Arrêter TCZ
![SUIVI DES PLAQUETTES/ NFS Valeur labo PLQ (cellules x 103/μl) [50 -100] <50 CAT SUIVI DES PLAQUETTES/ NFS Valeur labo PLQ (cellules x 103/μl) [50 -100] <50 CAT](http://slidetodoc.com/presentation_image_h/e8fcfd822359e17ea5373c71b40b61e5/image-72.jpg)
SUIVI DES PLAQUETTES/ NFS Valeur labo PLQ (cellules x 103/μl) [50 -100] <50 CAT + Interrompre TCZ +Quand tx >100 x 103/μl résumer TCZ à 4 mg/kg, puis augmenter dose à 8 mg/kg selon l’état clinque Arrêter TCZ

SUIVI DES ALAT et ASAT Valeur labo CAT >1 - 3 x limite sup Normale + Modification dose MTX si appropriée. + Si persistance augmentation tjr >1 to 3, réduire dose TCZ à 4 mg/kg ou interrompre TCZ jusqu’à normalisation AST/ALT + Reprendre avec 4 mg/kg ou 8 mg/kg, selon l’état clinique 3 -5 N (confirmé par contrôle dosage) +Interrompre TCZ jusqu’à <3 x N + Quand valeur arrive <3 x ULN, passer dose 4 mg/kg ou 8 mg/kg dose + Si taux persiste >3 x ULN, arrêter TCZ >5 x limite sup Normale arrêter TCZ

SUIVI DU BILAN LIPIDIQUE Valeur labo CAT >1 - 3 x limite sup Normale + Modification dose MTX si appropriée. + Si persistance augmentation tjr >1 to 3, réduire dose TCZ à 4 mg/kg ou interrompre TCZ jusqu’à normalisation AST/ALT + Reprendre avec 4 mg/kg ou 8 mg/kg, selon l’état clinique 3 -5 N (confirmé par contrôle dosage) +Interrompre TCZ jusqu’à <3 x N + Quand valeur arrive <3 x ULN, passer dose 4 mg/kg ou 8 mg/kg dose + Si taux persiste >3 x ULN, arrêter TCZ >5 x limite sup Normale arrêter TCZ

SUIVI DU BILAN LIPIDIQUE CAT/ dyslipidémie : - Ne pas arrêter le TCZ; - Dépister les autres facteurs de risque cardiovasculaire.

Dyslipidémie FDR CVX NON § Traitement diététique en § OUI § Statines de façon précoce; monothérapie pour une période § Diététique §Posologie faible afin d’optimiser de 3 mois, § Contrôle après. § Statines si besoin §La fluvastatine, la pravastatine et la rosuvastatine. §Correction des autres facteurs de Bilan de surveillance: 1/ mois tous les 3 puis 6 mois. risque

SUIVI DU BILAN LIPIDIQUE § Si persistance taux lipides augmenté: introduction statines; § Avis endocrino; § Gestion selon guidelines local et ou international pour PEC dyslipidémie.

TCZ ET DESIR DE GROSSESSE?

Contraception • Efficace chez le couple; • Délai de 3 mois entre la dernière perfusion et la conception.

• SOINS DENTAIRES/ TCZ?

Soins dentaires Soins appropriés avant de débuter le TCZ 1. Soins usuels (caries, détartrage) : Pas d’arrêt du tocilizumab, antibioprophylaxie. 2. Soins à risque infectieux (extraction, granulome apical, abcès. . ) : Arrêt du TCZ avant soins dentaires, d’au moins 4 semaines+ antibioprophylaxie. 3. Implants : Pas d’arrêt du TCZ, aux risques infectieux potentiels.

• CHIRURGIE/ TCZ?

Chirurgie programmée § Durée d’arrêt du tocilizumab avant l’intervention d’au moins 4 semaines;

Chirurgie en urgence • Arrêt du traitement par tocilizumab ; • Antibiothérapie prophylactique de couverture en cas de chirurgie à risque septique (exemple : péritonite); • Surveillance rigoureuse post-opératoire (état local du site opératoire et symptômes douloureux); • Reprise du traitement autorisée uniquement après cicatrisation (et arrêt d’une éventuelle antibiothérapie) et en l’absence d’infection.

VACCINS/ TCZ?

VACCINS 2 grandes catégories de vaccins Vivant atténué BCG, Fièvre jaune, Rougeole-Oreillons-Rubéole (ROR), Polio par voie buccale (réservé uniquement aux situations épidémiques), Varicelle. Inactivés ou composés d’un antigène Grippe, Pneumocoque, Méningocoque, Haemophilus influenza, Hépatites A et B, Pentacoq (Diphtérie-Tétanos. Poliomyélite-Coqueluche. Haemophilus influenza b), Fièvre typhoïde, Polio par voie injectable.

VACCINS Inactivés ou composés d’un antigène Vivant atténué § Arrêter le traitement au §Vaccination pourra être faite à moins 70 jours avant le vaccin tout moment; (5 demi-vies) § Attendre au minimum 2 §Pas de report de la perfusion du semaines et idéalement 4 tocilizumab. semaines après la vaccination avant de tocilizumab. reprendre le

VACCINS CAS PARTICULIERS § Vaccination des pèlerins; § Vaccination des voyageurs; § Epidémies : méningococcies, choléra…

Vaccins méningococciques • Le vaccin méningococcique A, C, Y, W 135: Mencevax°, Menvéo° (conjugué) – imposée par les autorités saoudiennes – Pour le pelerinage de La Mecque – depuis 1987 – valable au 10ème jour pendant 3 ans • Vaccin méningococcique A+C • Séjour en ceinture de la méningite si conditions de contact étroit avec la population locale • Si travail secteur santé ou réfugiés

VACCINS Vivant atténué BCG, Fièvre jaune, Rougeole-Oreillons-Rubéole (ROR), Polio par voie buccale (réservé uniquement aux situations épidémiques), Varicelle. Inactivés ou composés d’un antigène Grippe, Pneumocoque, Méningocoque, Haemophilus influenza, Hépatites A et B, Pentacoq (Diphtérie-Tétanos. Poliomyélite-Coqueluche. Haemophilus influenza b), Fièvre typhoïde, Polio par voie injectable.

VACCINS Inactivés ou composés d’un antigène Vivant atténué § Arrêter le traitement au §Vaccination pourra être faite à moins 70 jours avant le vaccin tout moment; (5 demi-vies) § Attendre au minimum 2 §Pas de report de la perfusion du semaines et idéalement 4 tocilizumab. semaines après la vaccination avant de tocilizumab. reprendre le
La fièvre jaune § Règlement sanitaire international; § Centre agréé, carnet international; § Exigible à partir de 1 an; § Valide au 10ème jour pendant 10 ans; § Valide le jour même d'un rappel; § Afrique, Amérique du sud, guyane française.
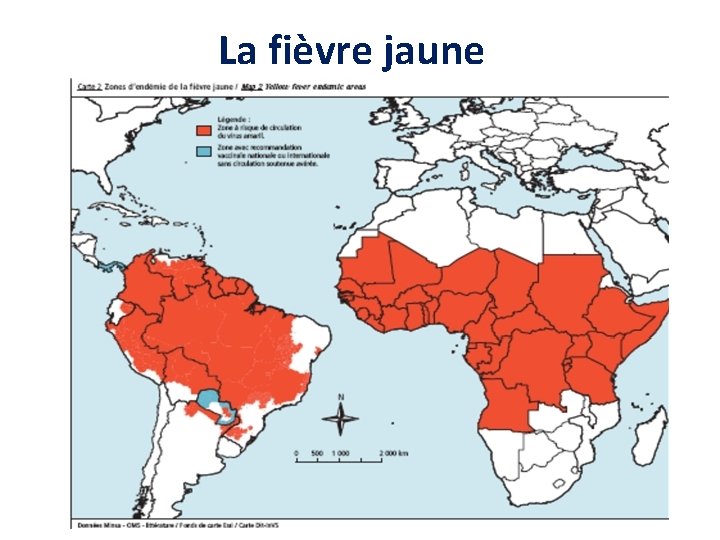
La fièvre jaune

VACCINS Vivant atténué BCG, Fièvre jaune, Rougeole-Oreillons-Rubéole (ROR), Polio par voie buccale (réservé uniquement aux situations épidémiques), Varicelle. Inactivés ou composés d’un antigène Grippe, Pneumocoque, Méningocoque, Haemophilus influenza, Hépatites A et B, Pentacoq (Diphtérie-Tétanos. Poliomyélite-Coqueluche. Haemophilus influenza b), Fièvre typhoïde, Polio par voie injectable.

VACCINS Inactivés ou composés d’un antigène Vivant atténué § Arrêter le traitement au §Vaccination pourra être faite à moins 70 jours avant le vaccin tout moment; (5 demi-vies) § Attendre au minimum 2 §Pas de report de la perfusion du semaines et idéalement 4 tocilizumab. semaines après la vaccination avant de tocilizumab. reprendre le

Typhoïde • Cas pour 100 000 voyageurs : – Mexique 0 - 13 – Maroc : 0 – 7 – Inde : 27 – 81 +++ Connor et al , Lancet Infect Dis 2005

Typhoïde • Adulte et enfant au-dessus de 2 ans en zone d'endémie; • Séjours prolongés ou mauvaises conditions; • Protection acquise 50 -80%; • Durée d’immunité 3 ans.

VACCINS Vivant atténué BCG, Fièvre jaune, Rougeole-Oreillons-Rubéole (ROR), Polio par voie buccale (réservé uniquement aux situations épidémiques), Varicelle. Inactivés ou composés d’un antigène Grippe, Pneumocoque, Méningocoque, Haemophilus influenza, Hépatites A et B, Pentacoq (Diphtérie-Tétanos. Poliomyélite-Coqueluche. Haemophilus influenza b), Fièvre typhoïde, Polio par voie injectable.

VACCINS Inactivés ou composés d’un antigène Vivant atténué § Arrêter le traitement au §Vaccination pourra être faite à moins 70 jours avant le vaccin tout moment; (5 demi-vies) § Attendre au minimum 2 §Pas de report de la perfusion du semaines et idéalement 4 tocilizumab. semaines après la vaccination avant de tocilizumab. reprendre le

Rage? ? ?

• INTERRACTIONS MEDICAMENTEUSES ET TCZ
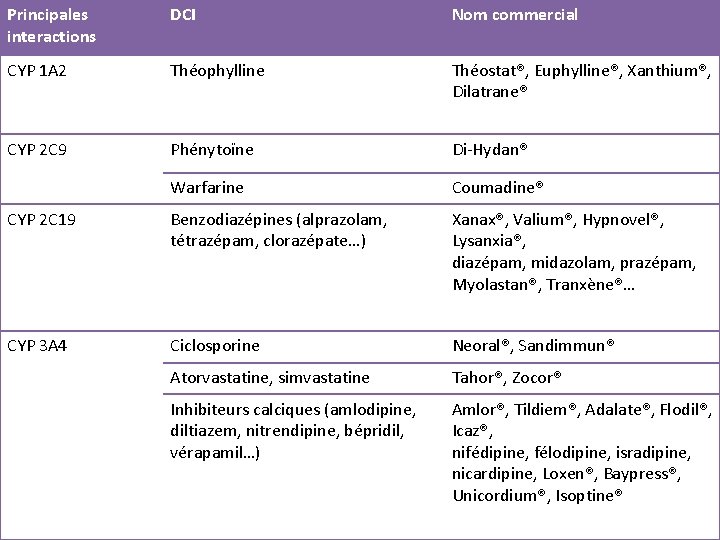
Principales interactions DCI Nom commercial CYP 1 A 2 Théophylline Théostat®, Euphylline®, Xanthium®, Dilatrane® CYP 2 C 9 Phénytoïne Di-Hydan® Warfarine Coumadine® CYP 2 C 19 Benzodiazépines (alprazolam, tétrazépam, clorazépate…) Xanax®, Valium®, Hypnovel®, Lysanxia®, diazépam, midazolam, prazépam, Myolastan®, Tranxène®… CYP 3 A 4 Ciclosporine Neoral®, Sandimmun® Atorvastatine, simvastatine Tahor®, Zocor® Inhibiteurs calciques (amlodipine, diltiazem, nitrendipine, bépridil, vérapamil…) Amlor®, Tildiem®, Adalate®, Flodil®, Icaz®, nifédipine, félodipine, isradipine, nicardipine, Loxen®, Baypress®, Unicordium®, Isoptine®

Interactions médicamenteuses • Adaptation des posologies de ces traitements à l’instauration et à l’arrêt de TCZ.
- Slides: 103