ATARAX I LAtarax Gnralits Introduction Formes pharmaceutiques Composition


















- Slides: 24

. ATARAX®

I) L’Atarax ® : Généralités. * Introduction. * Formes pharmaceutiques. * Composition.

*INTRODUCTION. Médicament des laboratoires UCB PHARMA. Répartition géographique : Europe : Atarax ® Etats-Unis : Atarax ® Japon : Atarax P ® Commercialisation : depuis 1956. AMM française : 16 août 1988.

*Formes Pharmaceutiques. 30 Comprimés pelliculés bisécables/boîte. 2 plaquettes thermoformées. 15 comprimés/plaquettes thermoformées. Prix (en ville) : 3. 37 € Remboursement : 65% Autres présentations : ATARAX 25 mg Comprimé pelliculé sécable Boîte de 150. ATARAX 100 mg Comprimé pelliculé sécable Boîte de 30. ATARAX 100 mg Comprimé pelliculé sécable Boîte de 150. ATARAX 10 mg/5 ml Sirop Boîte de 50 Flacons de 200 ml. ATARAX 10 mg/5 ml Sirop Flacon de 200 ml. ATARAX 100 mg/2 ml Solution injectable Boîte de 100 Ampoules de 2 ml. ATARAX 100 mg/2 ml Solution injectable Boîte de 6 Ampoules de 2 ml.

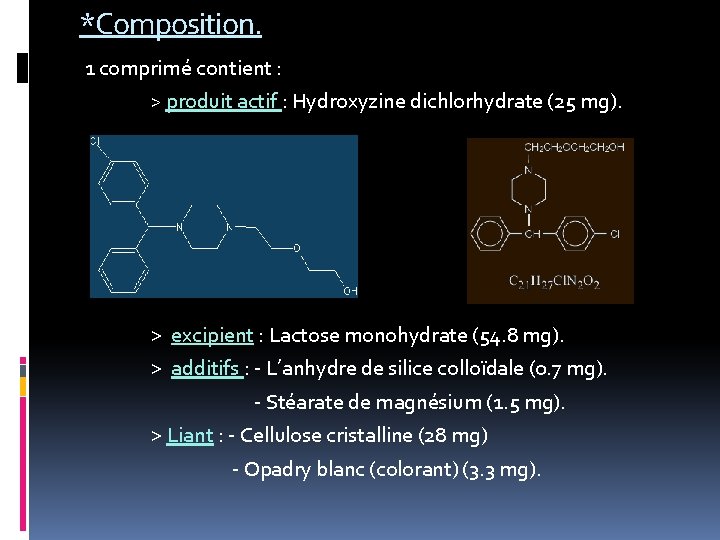
*Composition. 1 comprimé contient : > produit actif : Hydroxyzine dichlorhydrate (25 mg). > excipient : Lactose monohydrate (54. 8 mg). > additifs : - L’anhydre de silice colloïdale (0. 7 mg). - Stéarate de magnésium (1. 5 mg). > Liant : - Cellulose cristalline (28 mg) - Opadry blanc (colorant) (3. 3 mg).

II) Propriétés pharmacologiques. * Propriétés pharmacodynamique. * Classes pharmacothérapeutiques. * Propriétés pharmacocinétiques.

*Propriétés pharmacodynamiques. Hydroxyzine = 1 -(p-chloro-a-phénylbenzyl)-4 -(2 hydroxyéthyl)pipérazine Structure 3 D de l’hydroxyzine. C 21 H 27 Cl. N 2 O 2 Dérivé de la pipérazine. antihistaminique antagoniste des récepteurs H 1. Effet sédatif. Activité sur les symptômes d’anxiété. Réf. officielle : Rectificatif AMM française 30/08/2006.

*Classes pharmacothérapeutiques. Antihistaminique H 1. Antiprurigineux. Anxiolytique. Anticholinergique. Sédatif.

*Propriétés pharmacocinétiques. Absorption. absorption rapide Pic plasmatique : 2 h après la prise de comprimé. Concentration maximale plasmatique : 30 ng/ml. Distribution. Volume apparent de distribution : 16 L/Kg (adulte). Diffusion : - cutané - Barrière hémato-encéphalique.

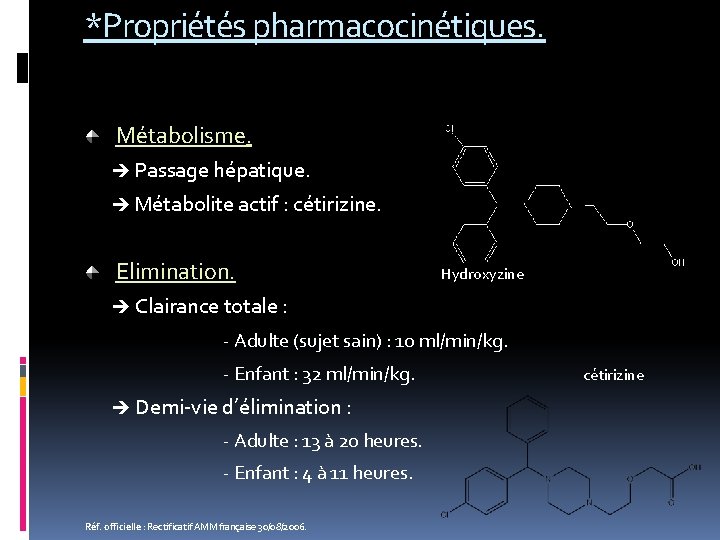
*Propriétés pharmacocinétiques. Métabolisme. Passage hépatique. Métabolite actif : cétirizine. Elimination. Hydroxyzine Clairance totale : - Adulte (sujet sain) : 10 ml/min/kg. - Enfant : 32 ml/min/kg. Demi-vie d’élimination : - Adulte : 13 à 20 heures. - Enfant : 4 à 11 heures. Réf. officielle : Rectificatif AMM française 30/08/2006. cétirizine

III) Indications thérapeutiques. * Posologie. 12 semaines de traitement. Sur ordonnance.

*Posologie. Prise pendant ou entre les repas. Existence de 10 schémas posologiques. Selon pathologies : - Adulte : 25 à 300 mg/jour. - Enfant 6 à 15 ans : adapter mg/Kg/jour. Exemple : Traitement contre urticaire. Dose minimale : 50 mg/jour. Dose maximale : 100 mg/jour. Ref. officielle : Rectificatif AMM française 30/08/2006.

IV) Mécanisme d’action. * Antihistaminique H 1. * Autres actions : > Antiprurigineux. > Anxiolytique. > Anticholinergique. > Sédatif. Ref. officielle : Rectificatif AMM française 30/08/2006.

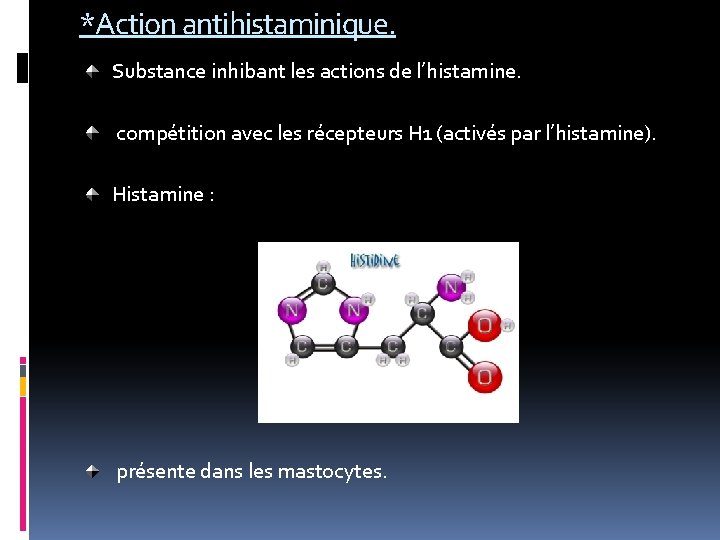
*Action antihistaminique. Substance inhibant les actions de l’histamine. compétition avec les récepteurs H 1 (activés par l’histamine). Histamine : présente dans les mastocytes.

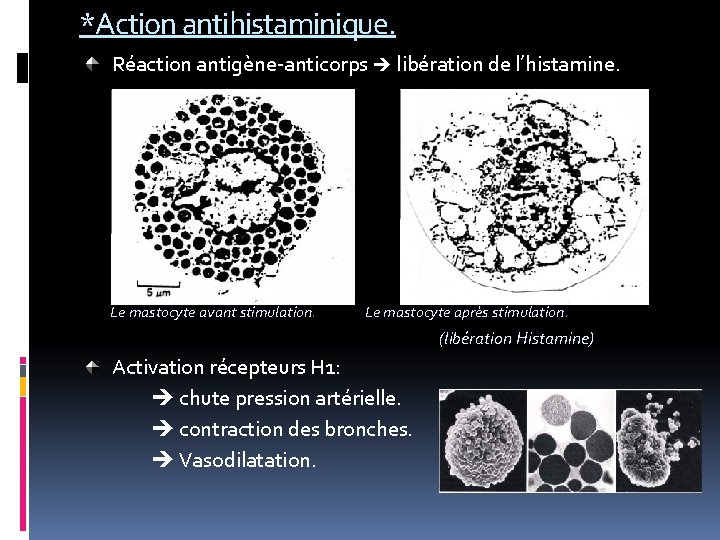
*Action antihistaminique. Réaction antigène-anticorps libération de l’histamine. Le mastocyte avant stimulation. Le mastocyte après stimulation. (libération Histamine) Activation récepteurs H 1: chute pression artérielle. contraction des bronches. Vasodilatation.

*Autres actions : plusieurs familles chimiques (pipérazine. . . ). Autres propriétés pour la classification : sédatifs du système nerveux central. Effets anticholinergiques. Antiprurigineux. Anxiolytique.

V) Contre-indications. * Contre-indiqué. * Déconseillé.

* Contre-indiqué: Hypersensibilité. Liées à l'effet anticholinergique : Glaucome à angle fermé. rétention urinaire. intolérance au fructose, de syndrome de malabsorption du glucose et du galactose. Ref. officielle : Rectificatif AMM française 30/08/2006.

* Déconseillé: chez les patients présentant des troubles cognitifs ou un syndrome confusionnel. Allaitement : en l'absence de données. Grossesse : effet tératogène chez l’animal. Absorption de boissons alcoolisées. Association de ce médicament à des médicaments provoquant une réaction antabuse. Ref. officielle : Rectificatif AMM française 30/08/2006.

VI) Précautions et effets. * Précautions d’emplois. * Effets indésirables.

* Précaution d’emplois: Chez enfant : effets sur le système nerveux central. Insuffisance hépatique et/ou rénale sévère Accumulation Chez les sujets âgés : Allongement de la demi-vie d'élimination. Effets anticholinergiques. Ref. officielle : Rectificatif AMM française 30/08/2006.

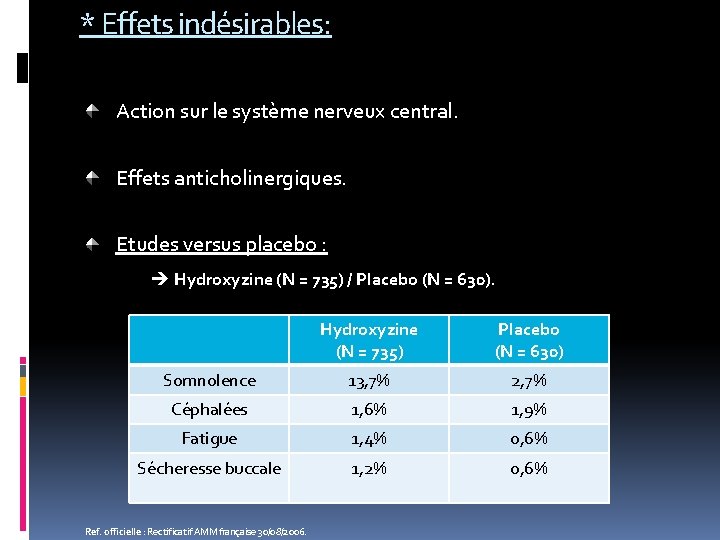
* Effets indésirables: Action sur le système nerveux central. Effets anticholinergiques. Etudes versus placebo : Hydroxyzine (N = 735) / Placebo (N = 630). Hydroxyzine (N = 735) Placebo (N = 630) Somnolence 13, 7% 2, 7% Céphalées 1, 6% 1, 9% Fatigue 1, 4% 0, 6% Sécheresse buccale 1, 2% 0, 6% Ref. officielle : Rectificatif AMM française 30/08/2006.

* Effets indésirables: Réactions cutanées. Manifestations allergiques. Effets psychiatriques. Effets neurologiques. Effets ophtalmologiques. Effets cardiovasculaires. Effets gastro-intestinaux. Effets urologiques.

VII) Conclusions. Atarax® - Plusieurs effets thérapeutiques. - Substance active : Hydroxyzine dichlorhydrate. - Pas d’automédication. - Chiffre d’affaires (2006) : € 45 millions.