Asztma genetikai httere Dr Szalai Csaba 2008 mrcius

Asztma genetikai háttere Dr. Szalai Csaba 2008. március 1. Tüdőgyógyászati továbbképzés, Soroksár

Az öröklődés, genetikai háttér vizsgálata Módszerek • Családi halmozódás vizsgálata pl. ikerkutatások • Szegregációs analízis • Founder populációk vizsgálata • Beteg-egészséges (Case-control) vizsgálatok

Az öröklődés vizsgálata Eredmények • Egypetéjű ikreknél az asztma konkordanciája magasabb mint két nem rokon ember között: • Asztma λs=2, 0 (CF: 500; IDDM: 15; NIDDM: 3, 5, Skrizofénia: 8, 6) • Imprinting jelenség: A két szülőtől kapott génpár közül, szigorúan meghatározott módon csak az egyik szülőé fejeződik ki.

• 11. 750 ikerpár vizsgálatakor a szénanáthára való hajlamért 36%-ban genetikai faktorok, 57%-ban a közös környezet volt a felelős, 11%-ban egyéb (2006).

Teljes genom szűrések • Mikroszatellita analízis, pl. : (TA)n, vagy (CAG)n • SNP: single nucleotide polymorphism pl. : • CAGGATAGGCATG • CAGGATTGGCATG Kromoszóma

Humán vizsgálatok • >600 asszociációs vizsgálat: >120 gén, de csak 10 gén >10 független vizsgálatban • Teljes genomszűrés: 20 régióval találtak kapcsolatot • Pozícionális klónozás: 7 gén • Teljes genom asszociációs vizsgálat: 1 gén (ORMDL 3)

Asztma genomszűrések eredményei

2 -es kromoszóma • IL-1 géncsalád: α és β: akut fázis válasz, T sejtek és monocita/makrofág aktiválása • Citotoxikus T limfocita asszociált antigén-4 (CTLA-4) (2 q 33): magas Ig. E, bizonyos haplotípusok: asztma

Citokin génklaszter

5 q 31 -q 33 • IL-4, IL-13, GM-CSF: B sejtek átkapcsolása Ig. E termelésre, Th 2 válasz kiváltása Emelkedett Ig. E szint, asztma • IL-5: Eozinophil felszabadítása a csontvelőből, eotaxin (eozinofil kemoattraktáns) termelés fokozása Asztma, bronchiális hiperreaktivitás

CD 14 • CD 14: . Szerepet játszik a T 1/Th 2 egyensúly kialakulásában. Bakteriális LPS kötő receptor. -159 C/T polimorfizmus: A CC homozigóta: Csökkent s. CD 14 szint (s= solubilis), csökkent CD 14 sűrűség monocitákon, emelkedett Ig. E szint, több pozitív bőrpróba (vs TT). Magyarázat: CD 14 -LPS kapcsolat IL-12 termelést vált ki, segít az élet korai szakaszában a Th 1 válasz kialakulásában. Alacsonyabb CD 14 -gyel Th 2 válasz felé billenhet az egyensúly. Ez magyarázhatja a gyermekkori fertőzés és az atópia közötti inverz kapcsolatot.
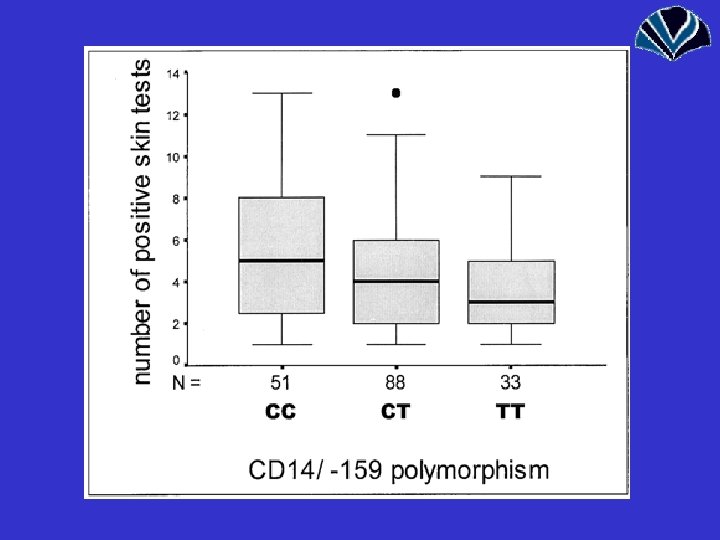

Francia vizsgálat • CD 14 -159 TT: kb. 2 x-es kockázatcsökkenés atópiára és allergiás rhinitisre • Korai életkorban a farmon való élet szintén 2 x kockázatcsökkenés • A CS 14 -159 TT + farmon való élet: 45 x-ös kockázatcsökkenés

6 p 21. 3 • Az MHC tartomány: MHC II (HLA-D) allergénpeptidek prezentációja a “jobb” vagy “rosszabb” bemutatás más citokineket termelő Th sejtek aktivációját, tehát erősebb vagy gyengébb allergiás immunválaszt eredményez. Parlagfű Amb 5 allergénjére reagáló fehérek 97, 5%-a: DR 2. 2; nem reagáló: 22% DR 2. 2; Amb 6, Der 1 és Der 2. • TNFα: Gyulladási választ közvetítése Asztma
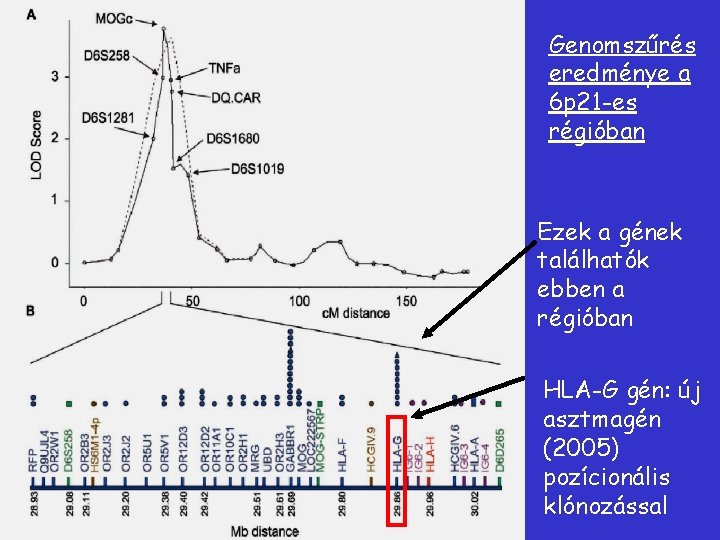
Genomszűrés eredménye a 6 p 21 -es régióban Ezek a gének találhatók ebben a régióban HLA-G gén: új asztmagén (2005) pozícionális klónozással

HLA-G • Fő szerepe: gátolja a magzat kilökődését terhességben • Gátolja a Th 1 -es immunválaszt • -964 GG gyerekek akkor hajlamosak bronchiális hiperreakcióra, ha az anyjuknak is van. • -964 AA gyerekek 60% atópiás, a GG gyerekek 41% atópiás
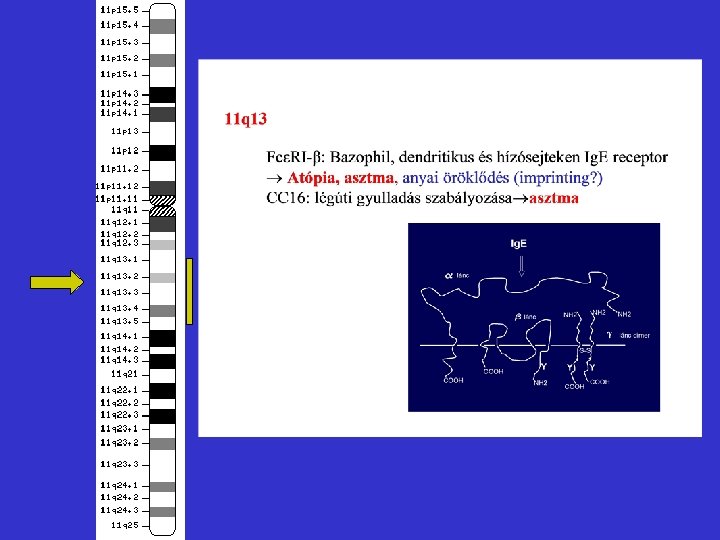

16 p 21 • IL-4 R: IL-4 -nek (és az a alegység az IL-13 -nak is) receptora Atópia, asztma • Ile 50 Val az extracelluláris doménben helyezkedik el, valin esetén a receptor erősebben köti az IL-4 -t. A Glu 576 Arg polimorfizmus a jelátviteli intermedierekhez való kötődést változtatja meg. Mindkét esetben a receptor felerősödött jelátvitelét tapasztalták. • Az 576 -os arginin atópiára hajlamosító hatása domináns, míg az 50 -es valin autoszomális recesszív öröklődést mutat.

17 q 11. 2 • RANTES, MCP-1, eotaxin: Leukociták gyulladáshoz vonzása (kemokinek): fontos szerep asztmában • MCP-1 -2518 A/G Asztma • RANTES -403 G/A; -28 C/G Emelkedett asztma hajlam
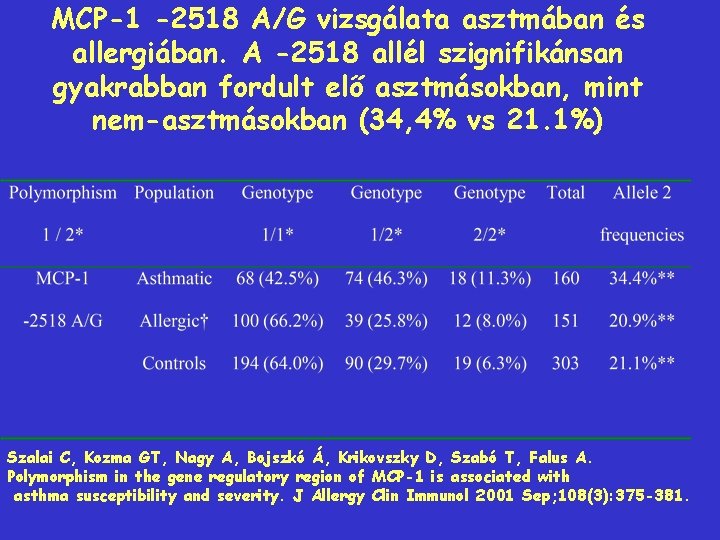
MCP-1 -2518 A/G vizsgálata asztmában és allergiában. A -2518 allél szignifikánsan gyakrabban fordult elő asztmásokban, mint nem-asztmásokban (34, 4% vs 21. 1%) Szalai C, Kozma GT, Nagy A, Bojszkó Á, Krikovszky D, Szabó T, Falus A. Polymorphism in the gene regulatory region of MCP-1 is associated with asthma susceptibility and severity. J Allergy Clin Immunol 2001 Sep; 108(3): 375 -381.
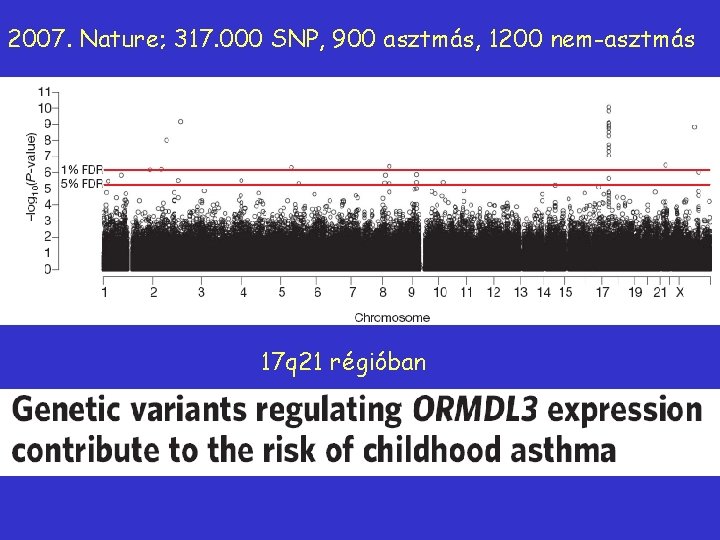
2007. Nature; 317. 000 SNP, 900 asztmás, 1200 nem-asztmás 17 q 21 régióban

Farmakogenomika/genetika • Két fontos terület: • Terápiás célpontok azonosítása genomikai/genetikai eszközökkel • Az egyének közötti genetikai különbségek hogyan befolyásolják a gyógyszerekre adott választ.
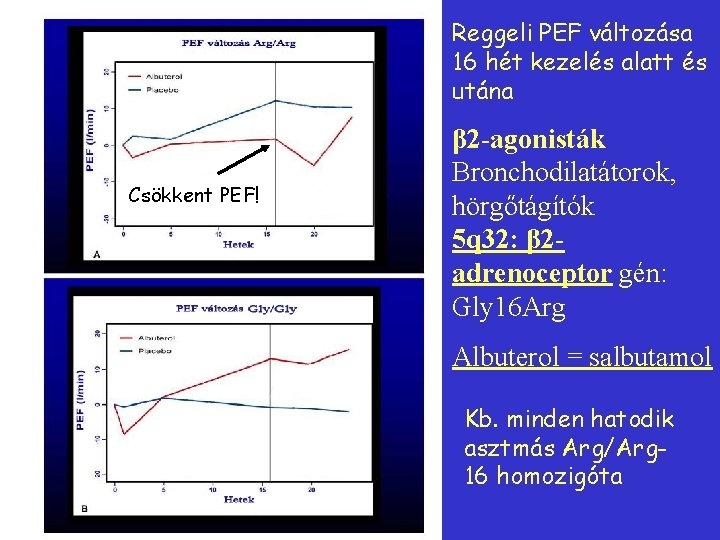
Reggeli PEF változása 16 hét kezelés alatt és utána Csökkent PEF! β 2 -agonisták Bronchodilatátorok, hörgőtágítók 5 q 32: β 2 adrenoceptor gén: Gly 16 Arg Albuterol = salbutamol Kb. minden hatodik asztmás Arg/Arg 16 homozigóta

Leukotrién antagonisták 5 -lipoxigenáz (5 -LO) • A gén promoterében található egy ismétlődő (tandem szekvencia (5’GGGCGG 3’), ami egy Sp 1 transzkripciós faktor kötő motívum. A vad típusban ebből 5 van, a variánsban 3 (12 bp deléció). • A 3 -as génvariációról kimutatták, hogy befolyásolja az asztma kezelésére kifejlesztett antileukotrién ABT-761 hatását.
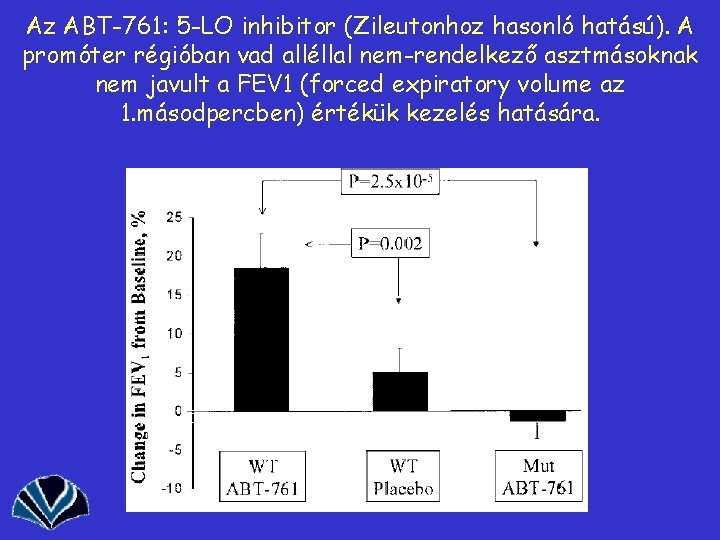
Az ABT-761: 5 -LO inhibitor (Zileutonhoz hasonló hatású). A promóter régióban vad alléllal nem-rendelkező asztmásoknak nem javult a FEV 1 (forced expiratory volume az 1. másodpercben) értékük kezelés hatására.

Leukotrién C 4 szintáz • -444 A/C promóter polimorfizmus • C mutáció egy újabb transzkripciós kötőhelyet hoz létre megnövekedett transzkripció erősebb hajlam asztmára. • A C allél gyakoribb aszpirin-intoleráns asztmásokban (asztmások 3 -8%-a) • Zafirlukast (leukotrién receptor antagonista) kezelésre a C alléllal rendelkezők reagáltak jobban. Valószínűleg magasabb a leukotrién C 4 szintjük, s ennek csökkentése jobban csökkenti az asztmatikus tüneteket.
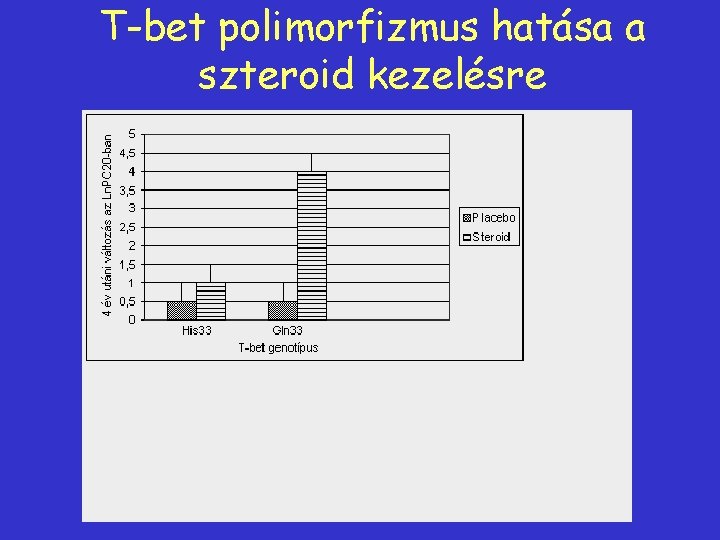
T-bet polimorfizmus hatása a szteroid kezelésre

Probléma, módszer • A dohányfüst expozíciónak kitett csecsemőkben nőtt-e a későbbi asztma kialakulásának kockázata, és ha igen, azt milyen kromoszómarégiókon található gének befolyásolták? • ETS = environmental tobacco smoke (kb. passzív dohányzás) • Collaborative Study for the Genetics of Asthma (CSGA); USA-fehéreket vizsgált • 144 család, melyben legalább egy asztmás testvérpár van több család 3 generációs. • Kérdés dohányzott-e valaki a családban amikor kisbaba volt? • 323 markert vizsgáltak autoszómákon

Eredmények • Az 5 q karon a b 2 -AR, az IL-4 és az IL-13 géneket tartalmazó szakaszon detektálták a legmagasabb LOD-számot (= logarithm of odds; a kapcsoltság mértékére használt érték (itt az asztma, a csecsemőkori “passzív dohányzás és a genetikai variációk között)).

Gén-környezet asszociációs vizsgálat (dohányzás asztma) • A β 2 adrenoceptor arginin-16 homozigóta dohányzóknak közel 8 -szoros az esélyük arra, hogy asztmásak legyenek, összehasonlítva a nemdohányzó glicin-16 homozigótákkal. • Magyarázat: Gly 16 homozigótáknak kevesebb a b 2 adrenerg receptoruk: a dohányfüst kevésbé hat rájuk. A jobban reagáló Arg 16 receptor száma valószínűleg a füst hatására erőteljesen leregulálódik.
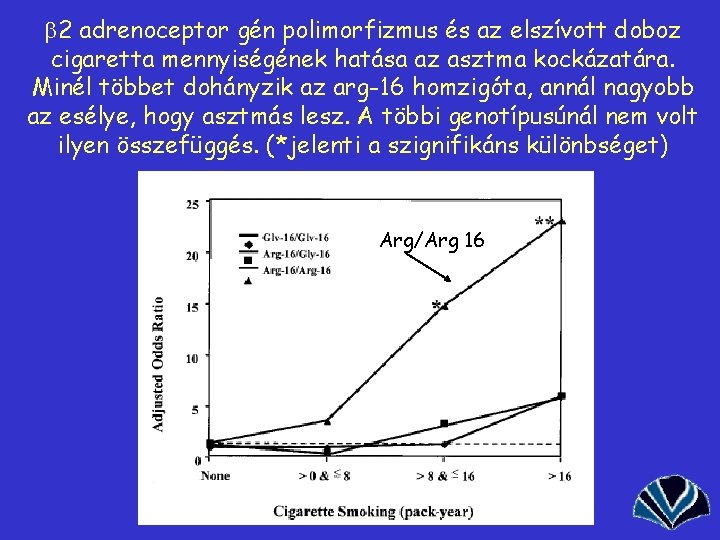
b 2 adrenoceptor gén polimorfizmus és az elszívott doboz cigaretta mennyiségének hatása az asztma kockázatára. Minél többet dohányzik az arg-16 homzigóta, annál nagyobb az esélye, hogy asztmás lesz. A többi genotípusúnál nem volt ilyen összefüggés. (*jelenti a szignifikáns különbséget) Arg/Arg 16

Köszönöm a figyelmet!
- Slides: 32