ASTLER VE BAZLAR NDEKLER Asit ve Baz Kavram

ASİTLER VE BAZLAR

İÇİNDEKİLER • • • Asit ve Baz Kavramı Asit ve Bazların Kuvvetliliği Ph ve POH Kavramı Ph Deneyi Kaynakça Hazırlayan
Asit ve Baz Kavramı ASİT VE BAZ TANIMLARI Arrhenius Asit-Baz Tanımı Bronsted-Lowry Asit-Baz Tanımı Lewis Asit-Baz Tanımı

Arrhenius Asit-Baz Tanımı • Suya H 3 O+ (hidronyum) katyonu veren maddeler ASİT • Suya OH- (hidroksit) anyonu veren maddeler BAZ denir. HCl Na. OH H+ + Cl. Na+ + OH-
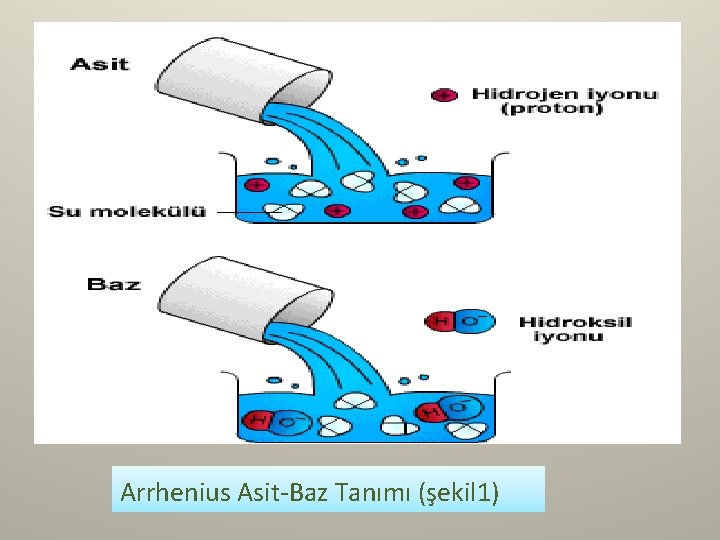
Arrhenius Asit-Baz Tanımı (şekil 1)
![Arrhenius Asit-Baz Tanımı • Asitler suda H+ oluşturduklarından suyun [H+] ni artırırlar. • Bazlar Arrhenius Asit-Baz Tanımı • Asitler suda H+ oluşturduklarından suyun [H+] ni artırırlar. • Bazlar](http://slidetodoc.com/presentation_image_h2/41aefdb238640d9a66cd5519691b4f21/image-6.jpg)
Arrhenius Asit-Baz Tanımı • Asitler suda H+ oluşturduklarından suyun [H+] ni artırırlar. • Bazlar suyun [OH–] ni artıran maddelerdir. • Arrhenius'e göre asitler HX , bazlar MOH genel formülüne sahiptir.

Bronsted-Lowry Asit-Baz Tanımı • Bronsted ve Lowry asitleri ve bazları biraz daha genel anlamda tanımlamıştır. Bunlara göre; Asit: Karşısındaki maddeye H+ verebilen Baz: Karşısındaki maddeden H+ alabilen (veya H+ bağlayabilen) maddedir.
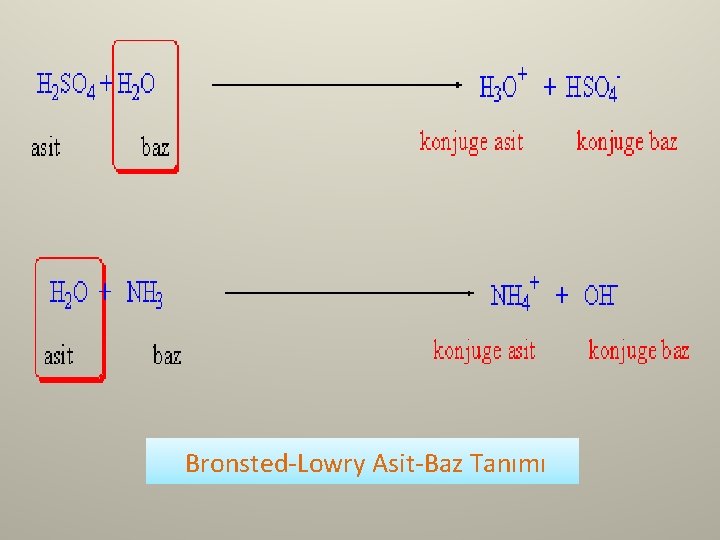
Bronsted-Lowry Asit-Baz Tanımı

Bronsted-Lowry Asit-Baz Tanımı • Bronsted - Lowry'ye göre bir tepkimede bir asit-baz çifti tepkimeye girerek yeni bir asit baz çifti oluşturmaktadır. Girenler tarafında asit olan madde H+ iyonunu kaybederek baza; baz olan madde H+ kazanarak aside dönüşmektedir. Bu teoride aralarında H+ kadar fark olan asit- baz çiftine eşlenik (konjuge) asit-baz çifti denir.

Lewis Asit-Baz Tanımı • Asit: elektron nokta yapısında elektron boşluğu bulunduran ve dolayısıyla elektron çifti bağlayabilen, • Baz: elektron nokta yapısında ortaklanmamış elektron çifti bulunduran ve dolayısıyla elektron çifti verebilen maddedir
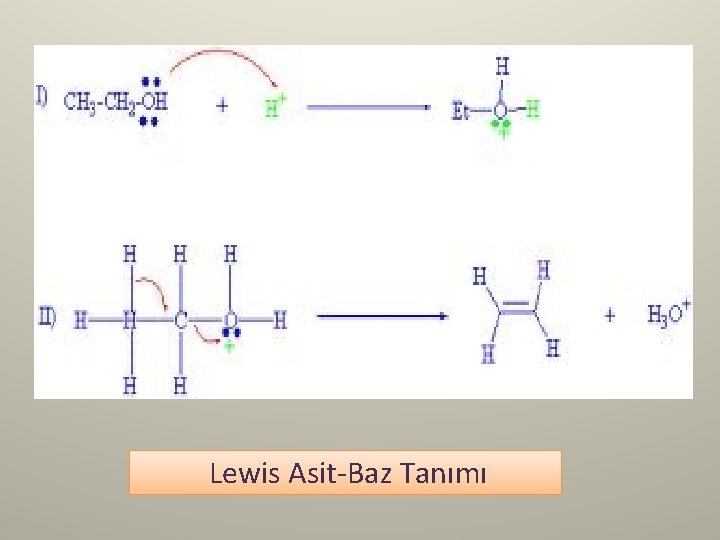
Lewis Asit-Baz Tanımı

ASİT VE BAZLARIN KUVVETLİLİĞİ

Kuvvetli Asit ve Bazlar

Kuvvetli Asitler ve Bazlar • su icinde tamamen veya tamamina yakini cozunen asitlerdir. • ph değerleri küçük olan asitlerdir. • Örneğin ; HCl HNO 3 H 2 SO 4 Na. OH KOH

Zayıf Asitler ve Bazlar • Tamamen iyonlaşmayan asitlere ve bazlara zayıf asit veya baz denir. Zayıf asitler HA, zayıf bazlarda B ile gösterilir. HA + H 2 O ↔ H 3 O+ + A 2 H 2 O ↔ H 3 O+ + OH-

Kuvvetli Asit ve Bazların Hesabı

Günlük hayattan asitler
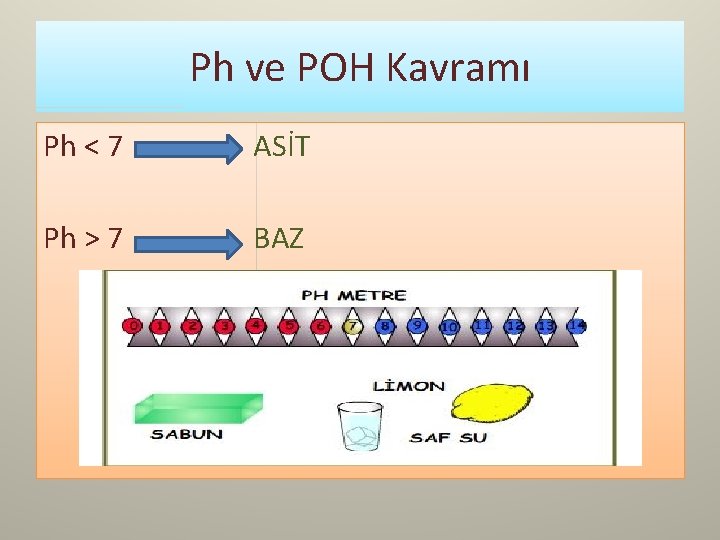
Ph ve POH Kavramı Ph < 7 ASİT Ph > 7 BAZ
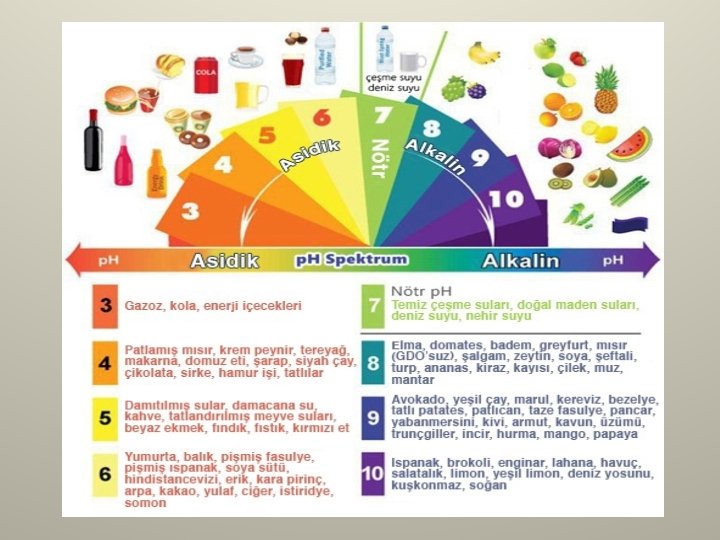
![Ph ve POH Kavramı • p. H = –log[H+] • p. OH = –log[OH–] Ph ve POH Kavramı • p. H = –log[H+] • p. OH = –log[OH–]](http://slidetodoc.com/presentation_image_h2/41aefdb238640d9a66cd5519691b4f21/image-20.jpg)
Ph ve POH Kavramı • p. H = –log[H+] • p. OH = –log[OH–] • p. H + p. OH = 14 eşitlikleri yardımıyla bir çözeltinin [H+] derişimi ya da [OH] derişimi bilinirse p. H’ı ya da p. OH’sı, p. H’ı ya da p. OH’ı bilinen bir çözeltinin [H+] derişimi ya da [OH–] derişimi bulunur.

PH DENEYİ

Kaynakça • www. kimyaevi. com. tr • www. ekimya. com. tr • www. fenokulu. com. tr

Yusuf Can ÇOBAN Kimya Öğretmenliği
- Slides: 23