asticov zloenie ltok Atm Stavba atmu Histria Pred

Časticové zloženie látok Atóm, Stavba atómu

História § Pred asi 2400 rokmi grécky filozof DEMOKRITOS nazval najmenšie častice látok atómami (grécky „atomos“ – nedeliteľný). § Vyslovil názor, že všetko je zložené z maličkých častíc – atómov.

V roku 1808 anglický chemik J. DALTON vypracoval vedeckú predstavu o zložení látok z atómov a experimentálne potvrdil existenciu atómov.
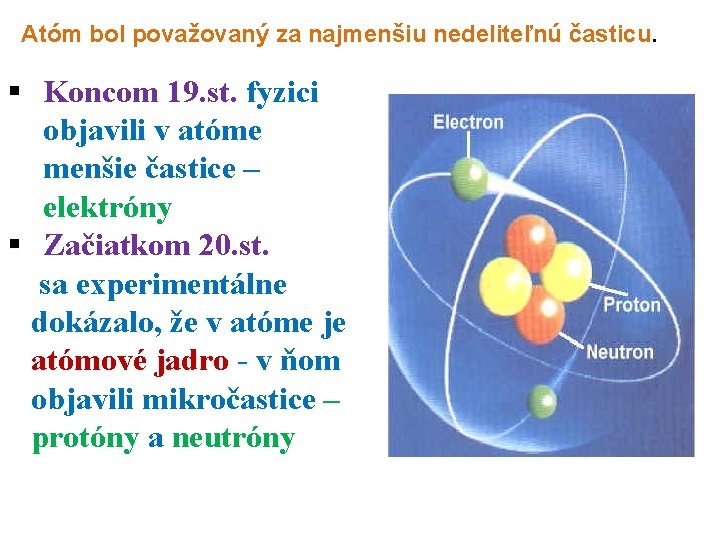
Atóm bol považovaný za najmenšiu nedeliteľnú časticu. § Koncom 19. st. fyzici objavili v atóme menšie častice – elektróny § Začiatkom 20. st. sa experimentálne dokázalo, že v atóme je atómové jadro - v ňom objavili mikročastice – protóny a neutróny
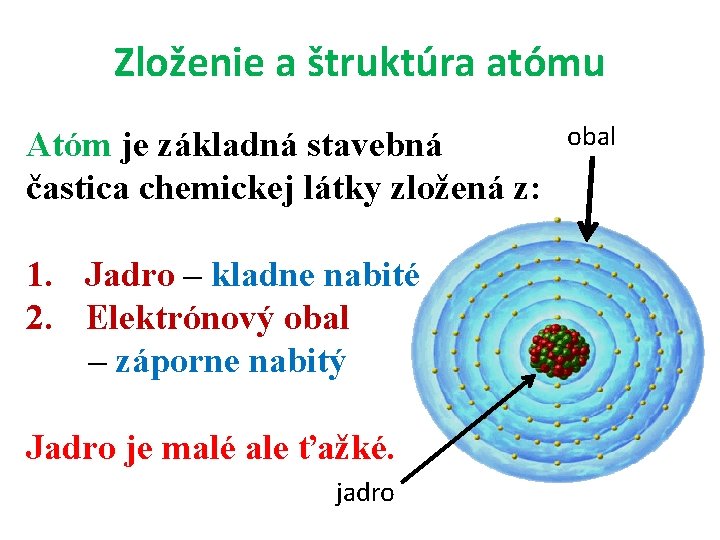
Zloženie a štruktúra atómu Atóm je základná stavebná častica chemickej látky zložená z: 1. Jadro – kladne nabité 2. Elektrónový obal – záporne nabitý Jadro je malé ale ťažké. jadro obal
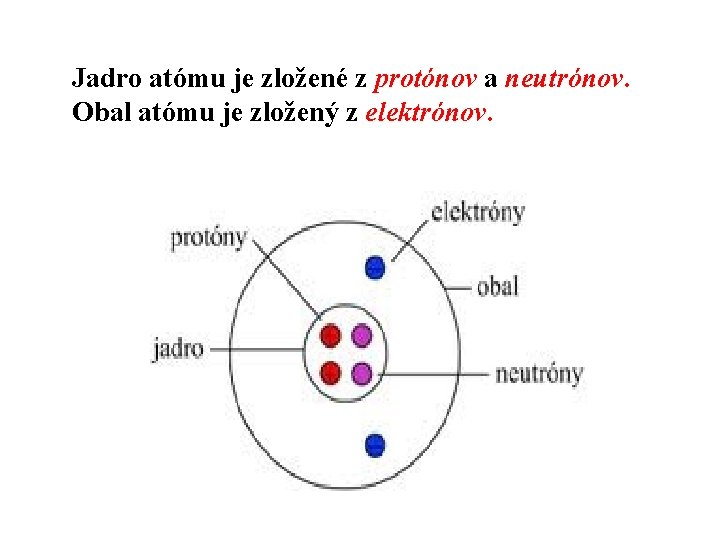
Jadro atómu je zložené z protónov a neutrónov Obal atómu je zložený z elektrónov
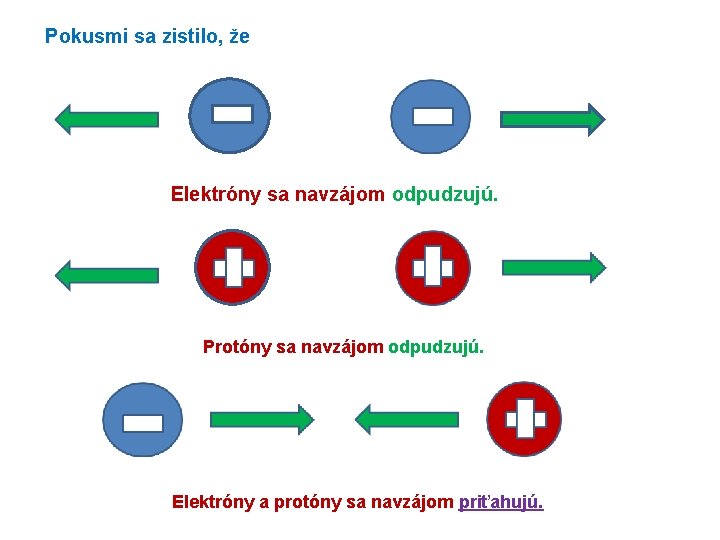
Pokusmi sa zistilo, že Elektróny sa navzájom odpudzujú. Protóny sa navzájom odpudzujú. Elektróny a protóny sa navzájom priťahujú.

• O časticiach, ktoré navzájom na seba pôsobia elektrickými silami, hovoríme, že majú elektrické vlastnosti, alebo tiež že majú elektrický náboj. • Neutrón je mikročastica bez elektrického náboja. ( n 0) • Protón je mikročastica s najmenším kladným elektrickým nábojom ( p +) • Elektrón je mikročastica s najmenším záporným elektrickým nábojom ( e - )
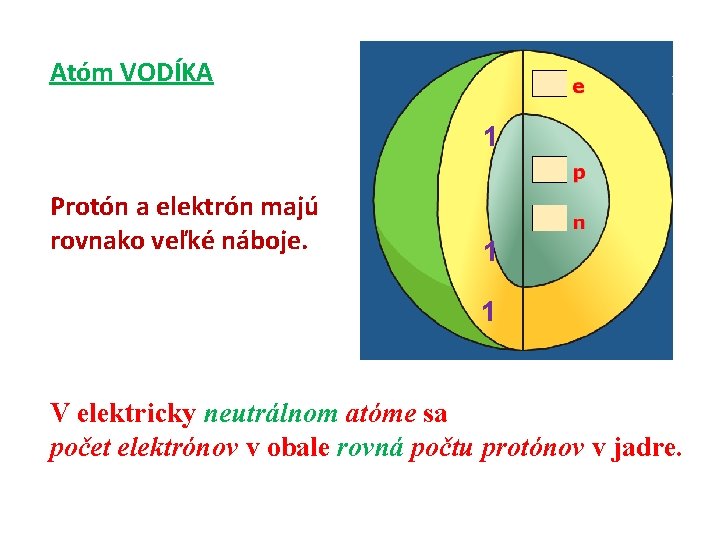
Atóm VODÍKA 1 Protón a elektrón majú rovnako veľké náboje. 1 1 V elektricky neutrálnom atóme sa počet elektrónov v obale rovná počtu protónov v jadre.

Napr. : uhlík 6 C obsahuje 6 p+ a 6 ekyslík 8 O obsahuje 8 p+ a 8 eÚloha: Koľko p+ a e- obsahuje: a) vápnik b) horčík 20 Ca 12 Mg
Modely atómu

Thomsonov model: ( pudingový model ) J. J. Thomson, 1907 § atómy sú guľôčky z kladne nabitej látky, v ktorej sú rozložené elektróny tak, aby celok bol stabilný a elektricky neutrálny. § Tento model si možno jednoducho predstaviť tak, že kladne nabitú hmotu nám predstavuje puding a záporne elektróny budú hrozienkami. Odtiaľ názov pudingový model atómu.
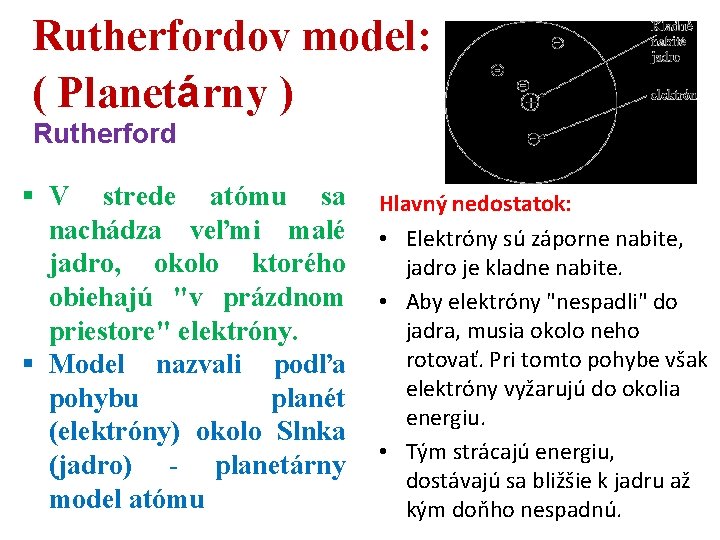
Rutherfordov model: ( Planetárny ) Rutherford § V strede atómu sa nachádza veľmi malé jadro, okolo ktorého obiehajú "v prázdnom priestore" elektróny. § Model nazvali podľa pohybu planét (elektróny) okolo Slnka (jadro) - planetárny model atómu Hlavný nedostatok: • Elektróny sú záporne nabite, jadro je kladne nabite. • Aby elektróny "nespadli" do jadra, musia okolo neho rotovať. Pri tomto pohybe však elektróny vyžarujú do okolia energiu. • Tým strácajú energiu, dostávajú sa bližšie k jadru až kým doňho nespadnú.
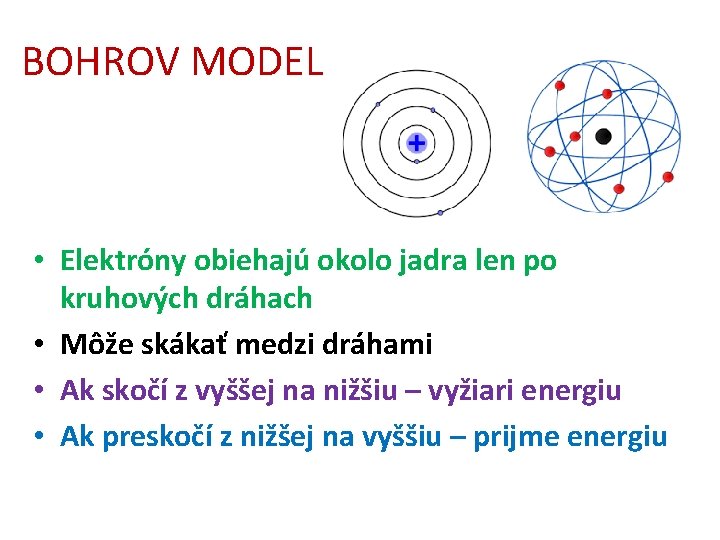
BOHROV MODEL • Elektróny obiehajú okolo jadra len po kruhových dráhach • Môže skákať medzi dráhami • Ak skočí z vyššej na nižšiu – vyžiari energiu • Ak preskočí z nižšej na vyššiu – prijme energiu

SOMMERFELDOV MODEL • Elektróny sa pohybujú po elipsovitých dráhach • V strede je jadro

KVANTOVO – MECHANICKÝ MODEL • Nemožno vypočítať dráhu a rýchlosť elektrónu • Má duálny charakter: vČastica v. Vlna • ORBITAL – priestor, kde sa s 99, 99% pravdepodobnosťou vyskytuje

Ste šikovní a ja vám Ďakujem za pozornosť prajem pekný deň
- Slides: 17