Aspects rglementaire BPF et organisationnel dun laboratoire de

Aspects réglementaire (BPF) et organisationnel d’un laboratoire de Contrôle de Qualité Dr Houamria Hamza 1

PLAN Introduction Ressources humaines Personnel Responsabilités Les missions du Pharmaciens Responsable De Contrôle de la Qualité Tâches partagées chef de production/ Responsable de contrôle de la Qualité Formation Conception des locaux et Matériel Locaux et Matériel Stockage des réactifs Documentation BPF nécessaire Equipement Flux matières premières Programme de suivi de la stabilité Hygiène du personnel Sécurité 2

Introduction (1) Le contrôle de la qualité fait partie des bonnes pratiques de fabrication ; il concerne l’échantillonnage, l’établissement de spécifications et l’analyse, ainsi que l’organisation, l’établissement des documents et des procédures de libération qui garantissent que des essais nécessaires et appropriés ont bien été effectués, que les matières premières et les articles de conditionnement ne sont pas libérés pour la fabrication, ni les produits finis libérés en vue de leur vente ou de leur distribution, avant que leur qualité n’ait été jugée satisfaisante. 3

Introduction (2) Le contrôle de la qualité ne se limite donc pas aux activités de laboratoire, mais doit participer à toutes les décisions qui peuvent concerner la qualité du produit. L’indépendance du contrôle de la qualité par rapport à la production est un élément fondamental de son bon fonctionnement. 4
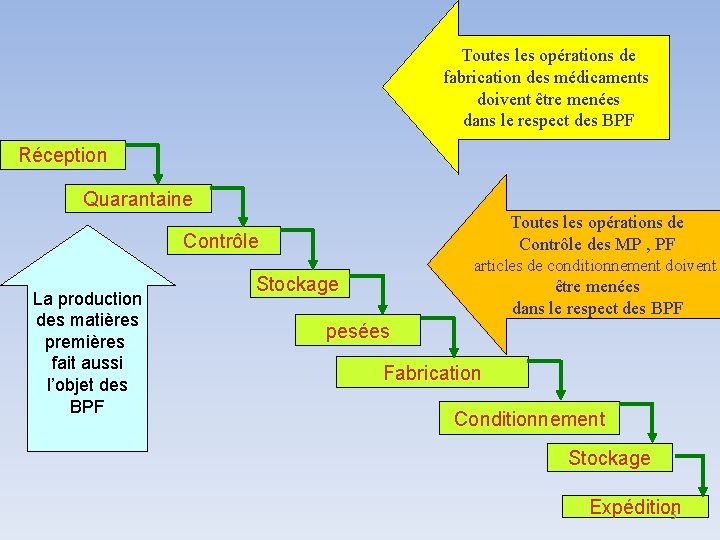
Toutes les opérations de fabrication des médicaments doivent être menées dans le respect des BPF Réception Quarantaine Toutes les opérations de Contrôle des MP , PF Contrôle La production des matières premières fait aussi l’objet des BPF articles de conditionnement doivent Stockage être menées dans le respect des BPF pesées Fabrication Conditionnement Stockage Expédition 5

Ressources humaines (1) Chaque personne doit comprendre les responsabilités qui attribuées. lui sont Ces responsabilités doivent être mises par écrit ( « fiches de fonction » ). Le personnel doit connaître les BPF ( la formation initiale et continue est une exigence). 6

Ressources humaines (2) • Le personnel du Département de Contrôle de la Qualité est composé de : Opérateurs Analystes : Diplômes supérieurs (ingénieur ou DES) Pharmacien chargé du Contrôle de la Qualité • Le champ d’activité de chaque agent est définit dans sa fiche de fonction et fiches de postes établie par rapport à l’organigramme Département de Contrôle de la Qualité. 7

Personnel (1) Le laboratoire doit: disposer d’un personnel d’encadrement et d’un personnel technique ayant l’autorité et les moyens nécessaires pour effectuer leurs tâches. avoir mis en place une politique et une procédure garantissant la confidentialité des informations. définir, à l’aide d’organigrammes, la structure organisationnelle et gestionnaire du laboratoire, sa place dans l’organisation mère. 8

Personnel (2) assurer une supervision suffisante du personnel, y compris des stagiaires, par des personnes connaissant bien les méthodes et procédures d’analyses et/ou d’étalonnages, de validation et de vérification. préciser les responsabilités, la hiérarchie et les relations entre les différents membres du personnel d’encadrement, d’exécution. 9
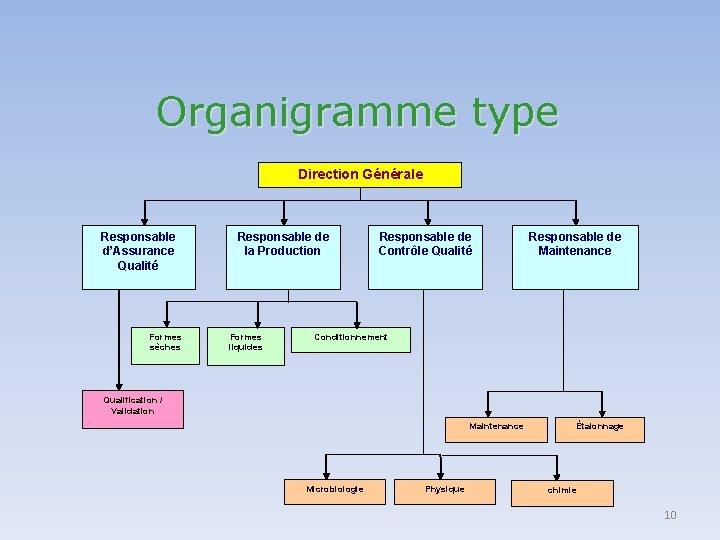
Organigramme type Direction Générale Responsable d’Assurance Qualité Formes sèches Responsable de la Production Formes liquides Responsable de Contrôle Qualité Responsable de Maintenance Conditionnement Qualification / Validation Maintenance Microbiologie Physique Étalonnage chimie 10

Responsabilités Les postes clés selon les BPF sont: Pharmacien responsable / DT. Responsable de Production. Responsable de Contrôle de la Qualité. Responsable de l’Assurance qualité. 11

Les missions du Pharmacien Responsable De Contrôle de la Qualité(1) Le chef du département du contrôle de la qualité assume généralement les tâches suivantes : accepter ou refuser les matières premières, les articles de conditionnement et les produits intermédiaires, vrac et finis approuver les spécifications, les instructions d'échantillonnage, les méthodes d'analyse et les autres procédures de contrôle de la qualité évaluer les dossiers de lot. 12

Les missions du Pharmacien Responsable De Contrôle de la Qualité(2) vérifier que tous les contrôles requis ont bien été effectués. agréer et contrôler les sous-traitants chargés des analyses. vérifier que la formation initiale et continue requise pour son personnel est assurée et adaptée aux besoins. contrôler l'entretien de son service, de ses locaux et de son matériel 13

Tâches partagées Responsable de Production/ Responsable de Contrôle de la Qualité (I) (I Approbation des procédures écrites et des autres documents, y compris les modifications; Surveillance et contrôle de l’environnement en fabrication; Hygiène dans l’usine; Les Validations des procédés; La Formation; 14

Tâches partagées Responsable de Production/ Responsable de Contrôle de la Qualité (II) (II Agrément et contrôle des fournisseurs; le choix et la surveillance des conditions de stockage des produits. toute auto-inspection, enquête et prise d'échantillons en vue de surveiller les facteurs qui peuvent influencer la qualité des produits. l'archivage des dossiers. Agrément et contrôle des fabricants sous-traitants; 15

Le personnel du département de contrôle de la qualité doit avoir accès aux zones de production pour prélever les échantillons et effectuer les investigations nécessaires. le personnel non formé ne devraient pas de préférence pénétrer dans les zones de production et de contrôle de la qualité. Si cela s'avérait indispensable, une information suffisante devrait leur être donnée au préalable, en particulier au sujet de l'hygiène personnelle et des éventuelles exigences en matière de vêtements protecteurs. Ces personnes doivent alors être toujours accompagnées. 16

Formation 17

• Le personnel doit recevoir, initialement puis de façon répétée, une formation, dont l’efficacité est vérifiée, comprenant: les aspects théoriques et pratiques du concept d’assurance de la qualité et de bonnes pratiques de fabrication. les exigences particulières pour la fabrication des médicaments expérimentaux: • Le fabricant doit assurer la formation de tout le personnel appelé à pénétrer dans les zones de production ou dans les laboratoires de contrôle (personnel technique, d'entretien et de nettoyage inclus) A côté de cette formation de base sur la théorie et la pratique des bonnes pratiques de fabrication, les membres du personnel nouvellement recrutés doivent recevoir une formation appropriée aux tâches qui leurs sont attribuées. 18

Les programmes de formation doivent être disponibles et approuvés, selon le cas, soit par le chef de production, soit par le chef du contrôle de la qualité. Les procès-verbaux des séances de formation doivent être conservés. Il convient d'assurer une formation spéciale aux personnes travaillant dans les zones où les contaminations peuvent constituer un risque particulier, par exemple les zones d'atmosphère contrôlée ou les zones où sont manipulés des produits hautement actifs, toxiques, infectieux ou sensibilisants. 19

Conception des locaux et Matériel 20

Locaux et Matériel • Les locaux doivent être conçus, construits, équipés et entretenus en vue d'empêcher: l'entrée d'insectes et d'autres animaux l'entrée de personnes non autorisées • Les locaux et le matériel doivent être situés, adaptés et entretenus de façon à: Diminuer au maximum les risques d’erreurs ou confusions Minimiser la possibilité d’altération des produits (ambiance contrôlée) Éviter les contaminations croisées. 21

Éviter, de façon générale, toute atteinte à la qualité des produits. Permettre un nettoyage et un entretien efficaces en vue a éviter le dépôt de poussières ou de saletés. L'éclairage, la température, l'humidité et la ventilation doivent être appropriés afin de ne pas affecter, directement ou indirectement, ni les médicaments durant leur fabrication et leur stockage, ni le bon fonctionnement du matériel. Les zones de production, de stockage et de contrôle de la qualité ne doivent pas être utilisées comme lieu de passage par le personnel qui n’y travaille pas. 22

Stockage des Réactifs (1) Les stocks de réactifs doivent être entreposés dans un lieu de stockage dans des conditions appropriées (température ambiante, au réfrigérateur ou au congélateur). Tous les réactifs et produits chimiques, y compris les solvants et les produits utilisés dans les analyses et dosages, doivent être de qualité appropriée. Les réactifs doivent être achetés auprès de fournisseurs reconnus et agréés et être accompagnés du certificat d’analyse et de la fiche de sécurité du matériel. L’étiquetage des réactifs doit clairement précisés. 23

Stockage des Réactifs (2) Code d’achat………………. Fabricant: ……………. Désignation: ……………. Concentration: …………………. Masse brute initiale……………. . Date d’ouverture du Récipient……. Date d’expiration: ……………. . Instructions pour le stockage: ……… 24

Stockage des Réactifs (3) L’étiquetage des solutions de réactifs préparées au laboratoire en précisant: a) La nature b) la date de préparation et les initiales du technicien ou analyste c) la date de péremption d) la concentration Règles de mise en stock : Les réactifs sont mis en stock selon leurs compatibilités réactives et selon une gestion alphabétique qui facilite le repérage et l’identification de l’emplacement du réactif. 25

Tableau des incompatibilités de stockage des Réactifs 26

Tableau des incompatibilités de stockage des Réactifs 27

28

Documentation BPF nécessaire (1): Spécifications: décrivent en détail les exigences auxquelles doivent se conformer les produits et composants utilisés ou obtenus au cours de la fabrication. Elles servent de base à l’évaluation de la qualité. . Procédures: (également connues sous le nom de « procédures opératoires standardisées » ou POS) donnent les indications nécessaires à la réalisation de certaines opérations. Protocoles: donnent des instructions pour exécuter et enregistrer certaines opérations particulières. 29

Documentation BPF nécessaire (2): Certificats d’analyse: fournissent un résumé de l’ensemble des résultats des contrôles réalisés sur les échantillons de produits ou de composants 1 ainsi qu’une évaluation de leur conformité aux spécifications établies les rapports et/ou les certificats d’analyse ; les données concernant la surveillance de l’environnement, lorsque cela s’impose ; les enregistrements obtenus lors de validation des méthodes de contrôle. les procédures et les enregistrements concernant l’étalonnage des instruments et la maintenance du matériel 30

Documentation BPF nécessaire (3): Tout document du contrôle de la qualité concernant un lot doit être conservé un an après la date de péremption du lot et au moins 5 ans après la certification du lot. Il est conseillé de conserver certaines données (par exemple : les résultats d’analyses, les rendements, les données de surveillance de l’environnement) de façon à permettre l’étude de leur évolution dans le temps. 31

Documentation BPF nécessaire (4): Enregistrements: apportent la preuve des différentes actions entreprises pour démontrer la conformité aux instructions par exemple les opérations, les anomalies et investigations et permettent de retracer l’historique de chacun des lots fabriqués y compris du point de vue de leur distribution. Ces documents incluent l’ensemble des données brutes qui sont utilisées pour créer d’autres enregistrements. Qualification de la conception (QC) Ensemble documenté d’activités définissant les spécifications fonctionnelles et opérationnelles de l’instrument et les critères de sélection du vendeur, sur la base de l’usage auquel l’instrument est destiné. 32

Equipement(1) • Les équipements importants ou essentiels doivent être accompagnés d’un «cahier de route» (log book) mentionnant, selon le cas: toutes les validations les étalonnages • les opérations d’entretien, de nettoyage ou de réparation, avec les dates et le nom des personnes ayant effectué ces opérations. 33

Equipement (2) Le matériel de fabrication et de contrôle doit être conçu, installé et entretenu en fonction de sa destination. Le matériel doit être installé de façon à éviter tout risque d'erreur ou de contamination Le matériel de mesure, de pesée, d'enregistrement et de contrôle doit être étalonné et vérifié à intervalles définis et par des méthodes appropriées. Les comptes rendus de ces contrôles doivent être conservés. 34

Equipement (3) les appareils utilisés pour l’obtention de données chimiques et physiques doivent occuper un emplacement correct. 35

Flux matières premières §Le Département de Contrôle de la Qualité est subdivisé en plusieurs unités fonctionnelles : Logistique de Contrôle de la Qualité Laboratoire de Contrôle Qualité Chimique Laboratoire de Contrôle Qualité Physique Laboratoire de Contrôle Qualité Microbiologique. 36

Contrôle des échantillons : • Clients : • Le Département de Contrôle de la Qualité (DCQ) répond aux demandes autres département pour le Contrôle de la Qualité de différents échantillons(MP, PF, Articles de conditionnement, …) Les demandeurs potentiels sont par ordre décroissant : La production, L’industrialisation (Développement), L’achat l’assurance qualité • Par ailleurs une correspondance logique entre le demandeur et la nature de l’échantillon doit être vérifiée, en l’absence de laquelle (ou dans le cas d’absence de justificatif) un rapport de déviation est émis et un refus de prélèvements doit être confirmé. 37

Demande d’analyse (1) La DPA : demande de prélèvements et d’analyse est un document émis par le client et envoyée au DCQ pour être réceptionné au niveau de la LCQ. La DPA selon le cas peut être: accompagnée d’échantillon c’est le cas de la production (vrac et pré mélanges et PSF formes sèches), l’industrialisation (prélèvements d’étude de stabilité). Un personnel dédié est en charge de ces prélèvements. Autrement, seule la DPA est reçue à la LCQ. 38

Demande d’analyse (2) Dans le cas de réception d’une DPA seule, le responsable LCQ avec l’aide de l’agent de prélèvement organise dans le cadre d’un programme hebdomadaire de prélèvements toute l’activité d’échantillonnage des lots reçus. Echantillon de référence : échantillon d’un lot de matière première, d’article de conditionnement ou de produit fini, conservé pour être analysé pendant toute la durée de vie du lot concerné 39

Demande d’analyse (3) Echantillon modèle : échantillon de produit fini dans son conditionnement final. Il est conservé pour identification, en tant que de besoin pendant toute la durée de vie du lot concerné. Durée de conservation: Les échantillons de référence et les échantillons modèles de chaque lot de produit fini doivent être conservés pendant au moins un an après la date de péremption. Les échantillons de matières premières (autres que les solvants, les gaz ou l’eau utilisés dans les procédés de fabrication) doivent être conservés pendant au moins deux ans après la libération du produit 40

L’échantillon de référence doit être d’une taille suffisante pour permettre de réaliser au moins deux analyses complètes en conformité avec le dossier d’autorisation de mise sur le marché, évalué et approuvé par les autorités compétentes. 41

Prélèvements : Un agent de prélèvements est mandaté pour réaliser les prélèvements. une procédure et un local de prélèvements et d’échantillonnage sont dédiés. Acheminement des Prélèvements : Le transfert des prélèvements doit se faire en respectant les conditions adéquates et en protégeant l’échantillon des conditions environnementales (température, humidité, lumière. En règle générale dans une glacière dûment étiqueté) Réception : Le LCQ réceptionne les DPA seules ou accompagnée d’échantillon, ensuite les échantillons sont transférés aux laboratoires destinataires 42

Chaque échantillon est analysé selon la procédure de contrôle correspondante et en vigueur, par un technicien qualifié, avec une méthode validée et avec un équipement qualifié, calibré et contrôlé, en respectant les 5 M. Collecte des résultats d’essais: Le dossier est repris et minutieusement vérifié et organisé, si toutes les analyses demandées sont exécutées et le contrôle en totalité achevée un bulletin d’analyse sera édité, Le dossier ainsi que le bulletin d’analyses seront vérifiés par le Pharmacien Chargé du Contrôle de la Qualité et transmit au Département d’Assurance de la Qualité. 43
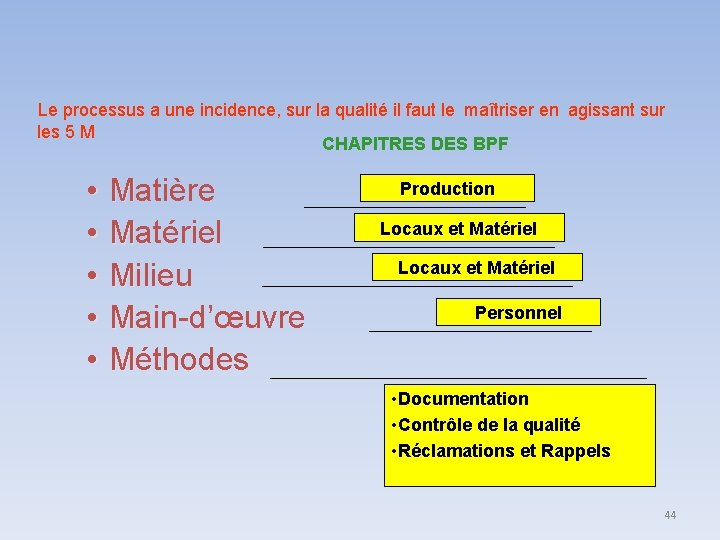
Le processus a une incidence, sur la qualité il faut le maîtriser en agissant sur les 5 M CHAPITRES DES BPF • • • Matière Matériel Milieu Main-d’œuvre Méthodes Production Locaux et Matériel Personnel • Documentation • Contrôle de la qualité • Réclamations et Rappels 44
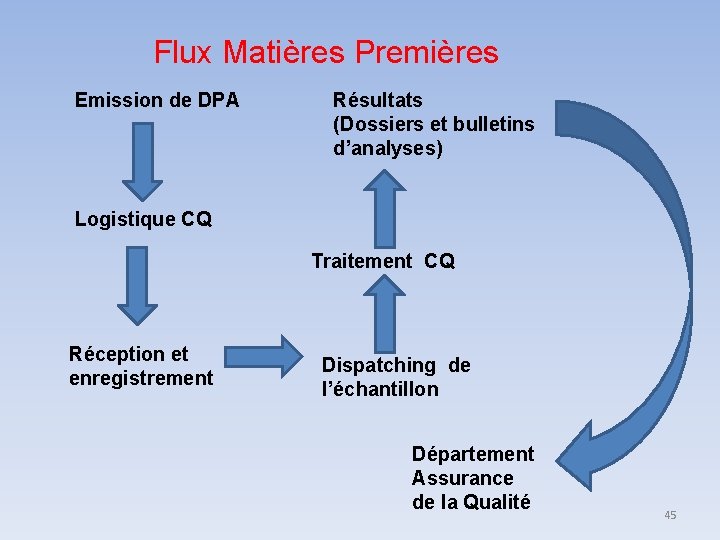
Flux Matières Premières Emission de DPA Résultats (Dossiers et bulletins d’analyses) Logistique CQ Traitement CQ Réception et enregistrement Dispatching de l’échantillon Département Assurance de la Qualité 45

Programme de suivi de la stabilité L’objet du programme de suivi de la stabilité est de surveiller le produit pendant toute sa durée de validité et de déterminer s’il est, et si on s’attend à ce qu’il reste, toujours conforme aux spécifications définies dans les conditions de stockage indiquées sur L’étiquetage. Le programme de suivi de la stabilité doit être établi dans un protocole écrit et les résultats doivent faire l’objet d’un rapport. Les équipements utilisés pour mener ce programme (notamment les enceintes climatiques) doivent être qualifiés. 46

Hygiène du personnel Des programmes détaillés consacrés à l'hygiène doivent être établis et adaptés aux différents besoins de l'entreprise. Ils doivent comporter des procédures relatives à la santé, à l'hygiène et à l'habillage du personnel. Les procédures doivent être comprises et observées de façon stricte par toute personne appelée à pénétrer dans les zones de fabrication et de contrôle. Les programmes d'hygiène doivent être promus par la direction et discutés de façon approfondie au cours de séances de formation. 47

Sécurité Les instructions générales et particulières relatives à la sécurité doivent être à la disposition de chaque membre du personnel. la mise à disposition des fiches de sécurité pour le personnel avant l’exécution des analyses. interdiction de fumer, de manger et de boire dans le laboratoire. la fourniture du matériel de premiers secours et la formation du personnel aux techniques de premiers secours, aux soins d’urgence et à l’utilisation des antidotes. 48
- Slides: 48