ASPECTOS MOLECULARES DEL CNCER DE COLON HEREDITARIO JAVIER


















- Slides: 51

ASPECTOS MOLECULARES DEL CÁNCER DE COLON HEREDITARIO JAVIER GODINO Hospital Clínico “Lozano Blesa”. Zaragoza Servicio de Oncología Médica, I+CS

• Introducción - Cáncer colorrectal. + Aspectos moleculares del Cáncer colorrectal. + Cáncer esporádico, familiar y hereditario. • Síndromes polipósicos. - Ligados a APC: PAF; PAFA - Ligados a MYH: MAP - Otras poliposis. • Síndromes no polipósicos - HNPCC es un término equívoco - Síndrome de Lynch. Asociado a defectos en MMR - Cáncer colorrectal familiar tipo X. No asociado a MMR • Genes de baja penetrancia: Cáncer familiar • Genes modificadores.

INTRODUCCIÓN

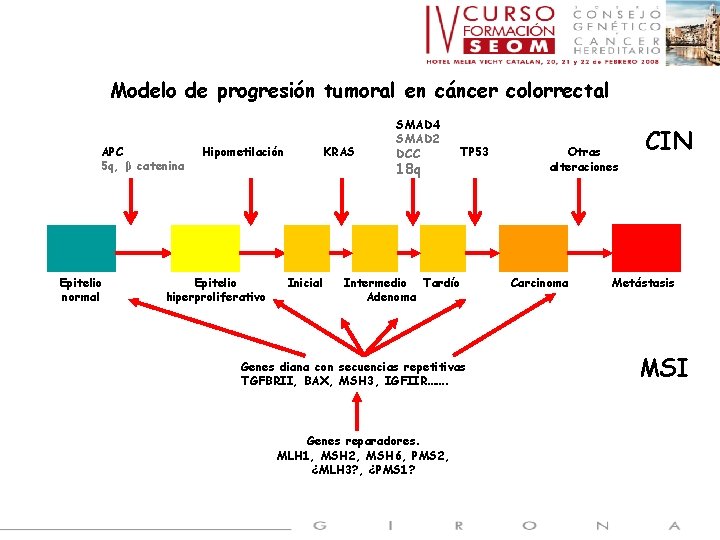
Modelo de progresión tumoral en cáncer colorrectal APC 5 q, β catenina Epitelio normal Hipometilación Epitelio hiperproliferativo KRAS Inicial SMAD 4 SMAD 2 DCC 18 q TP 53 Intermedio Tardío Adenoma Genes diana con secuencias repetitivas TGFBRII, BAX, MSH 3, IGFIIR……. Genes reparadores. MLH 1, MSH 2, MSH 6, PMS 2, ¿MLH 3? , ¿PMS 1? Otras alteraciones Carcinoma CIN Metástasis MSI

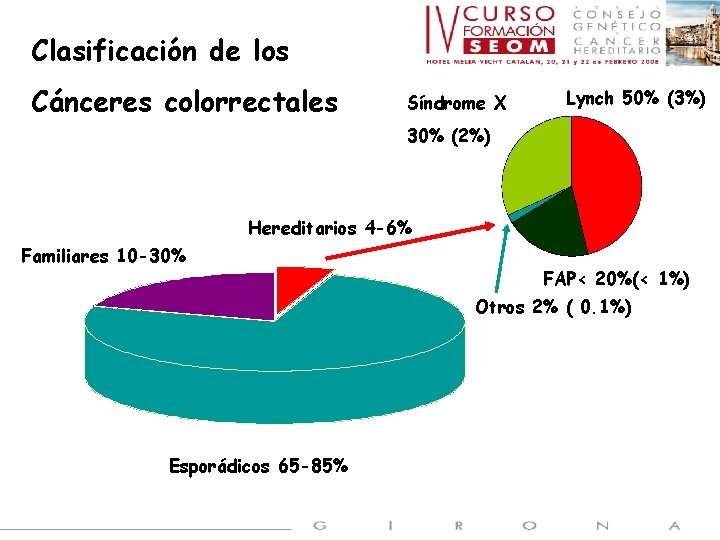
Clasificación de los Cánceres colorrectales Síndrome X Lynch 50% (3%) 30% (2%) Hereditarios 4 -6% Familiares 10 -30% FAP< 20%(< 1%) Otros 2% ( 0. 1%) Esporádicos 65 -85%

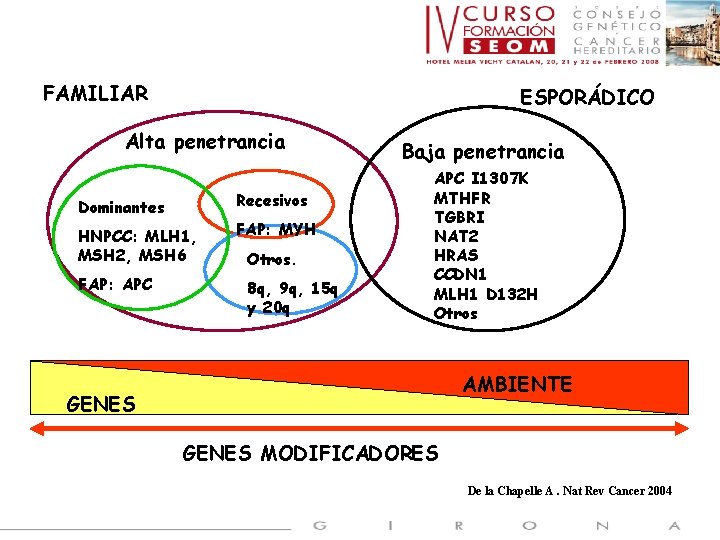
FAMILIAR ESPORÁDICO Alta penetrancia Recesivos Dominantes HNPCC: MLH 1, MSH 2, MSH 6 FAP: APC FAP: MYH Otros. 8 q, 9 q, 15 q y 20 q Baja penetrancia APC I 1307 K MTHFR TGBRI NAT 2 HRAS CCDN 1 MLH 1 D 132 H Otros AMBIENTE GENES MODIFICADORES De la Chapelle A. Nat Rev Cancer 2004

SÍNDROMES POLIPÓSICOS

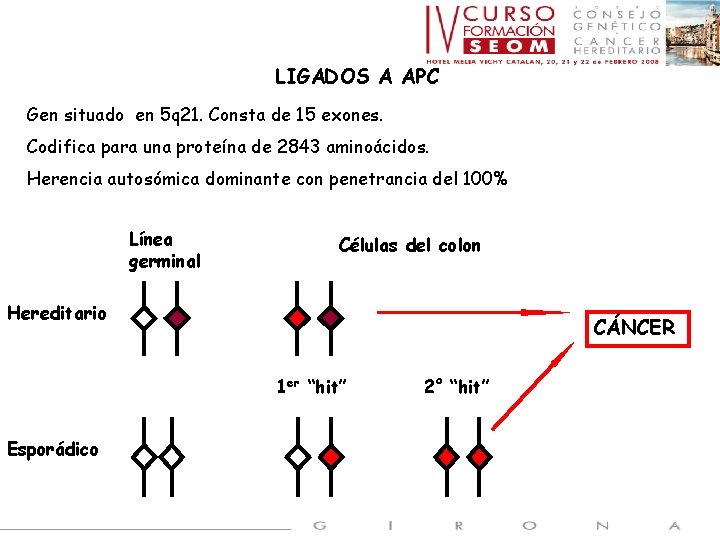
LIGADOS A APC Gen situado en 5 q 21. Consta de 15 exones. Codifica para una proteína de 2843 aminoácidos. Herencia autosómica dominante con penetrancia del 100% Línea germinal Células del colon Hereditario CÁNCER 1 er “hit” Esporádico 2º “hit”

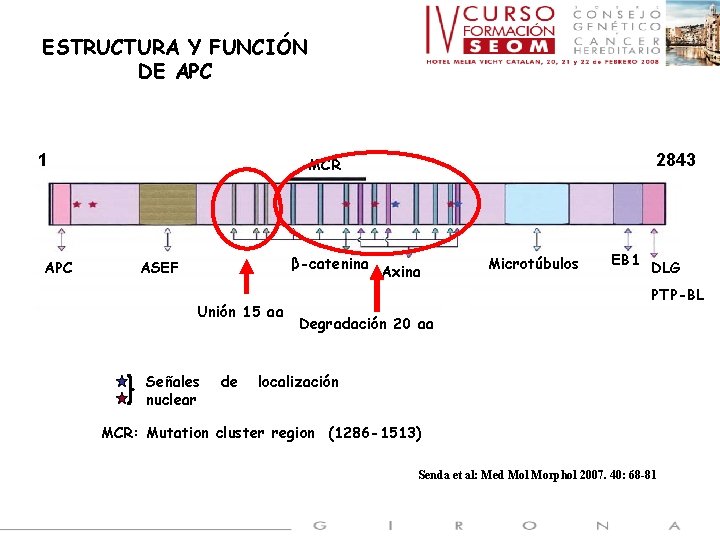
ESTRUCTURA Y FUNCIÓN DE APC 1 APC 2843 MCR β-catenina ASEF Unión 15 aa Señales nuclear de Axina Microtúbulos EB 1 DLG PTP-BL Degradación 20 aa localización MCR: Mutation cluster region (1286 -1513) Senda et al: Med Mol Morphol 2007. 40: 68 -81

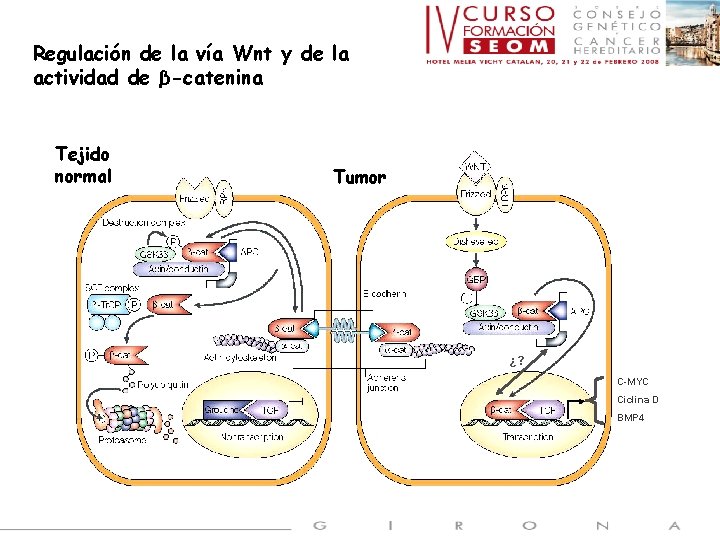
Regulación de la vía Wnt y de la actividad de β-catenina Tejido normal Tumor ¿? C-MYC Ciclina D BMP 4

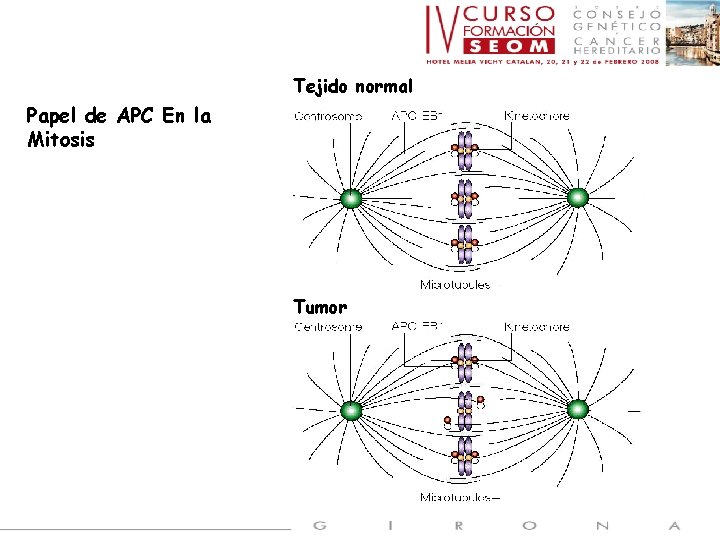
Tejido normal Papel de APC En la Mitosis Tumor

OTRAS FUNCIONES DE APC • Control de la migración celular. Unión a ASEF y microtúbulos. • Regulación de la adhesión celular. Unión DLG. • Mantenimiento de la polarización celular: Unión a DLG y microtúbulos. • Control del ciclo celular. Mediante su unión a DLG.

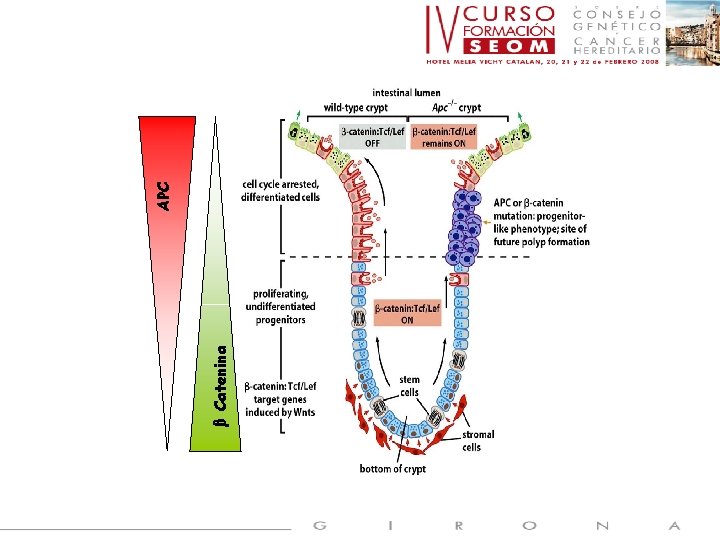
β Catenina APC

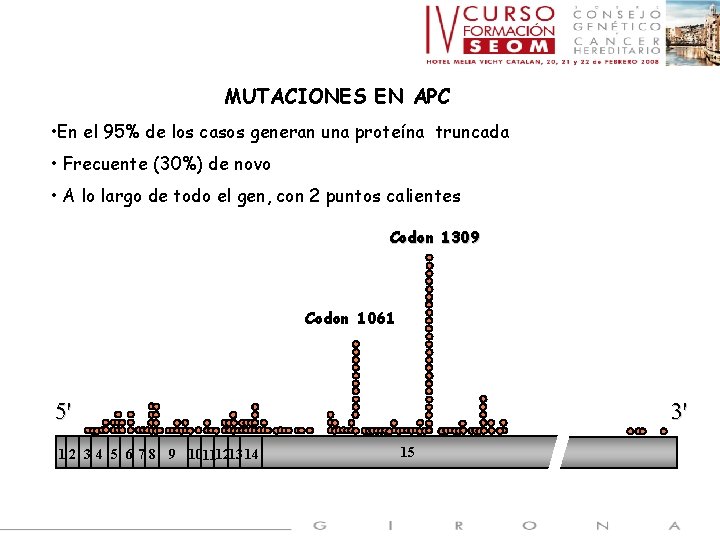
MUTACIONES EN APC • En el 95% de los casos generan una proteína truncada • Frecuente (30%) de novo • A lo largo de todo el gen, con 2 puntos calientes Codon 1309 Codon 1061 5' 1 2 3 4 5 6 7 8 9 10111213 14 3' 15

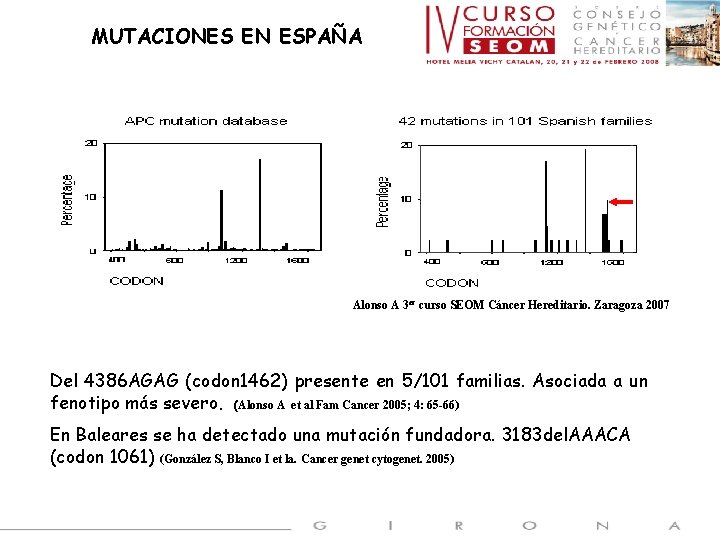
MUTACIONES EN ESPAÑA Alonso A 3 er curso SEOM Cáncer Hereditario. Zaragoza 2007 Del 4386 AGAG (codon 1462) presente en 5/101 familias. Asociada a un fenotipo más severo. (Alonso A et al Fam Cancer 2005; 4: 65 -66) En Baleares se ha detectado una mutación fundadora. 3183 del. AAACA (codon 1061) (González S, Blanco I et la. Cancer genet cytogenet. 2005)

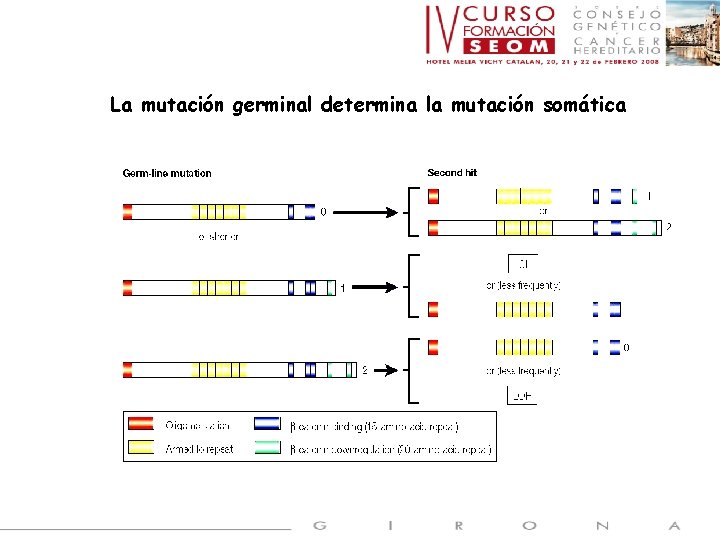
La mutación germinal determina la mutación somática

EXPRESIÓN CLÍNICA DE MUTACIONES EN APC. • Poliposis adenomatosa familiar (PAF). Incidencia (1/10. 000 -1/7000) + Mas de 100 pólipos en la 2 -3 década de vida. + CCR en un 100% de los casos hacia los 35 años, localización distal + Manifestaciones extracolónicas: Osteomas, HCEPR, Tumores desmoides, Pólipos gástricos y duodenales, hepatoblastoma, cáncer papilar de tiroides (síndrome de Gardner, síndrome de Turcot). + En un 90% de los casos asociado a mutaciones en APC.

EXPRESIÓN CLÍNICA DE MUTACIONES EN APC. • Poliposis adenomatosa familiar atenuada (PAFA). + Entre 10 -100 pólipos con aparición mas tardía (± 15 años). + Se han descrito manifestaciones extracolónicas. + Sólo en un 20% de los casos asociado a mutaciones en APC. + Mas frecuentes las mutaciones “de Novo” + “Tercer Hit” Mutación germinal CÁNCER 2º Hit 3 er Hit

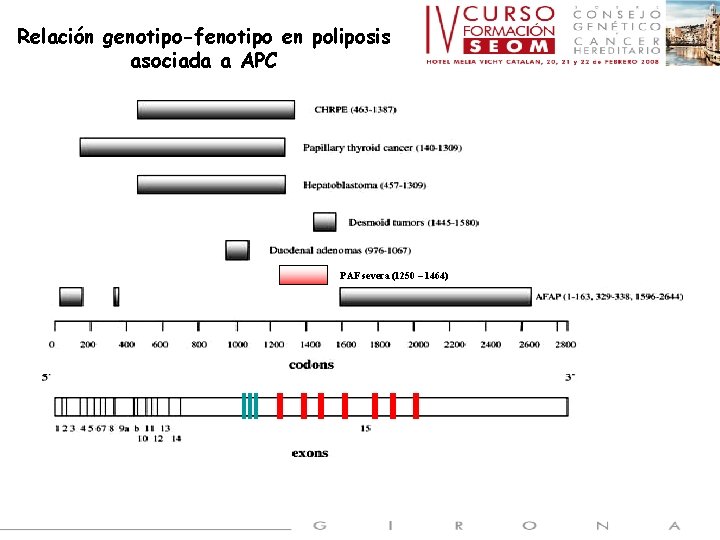
Relación genotipo-fenotipo en poliposis asociada a APC PAF severa (1250 – 1464)

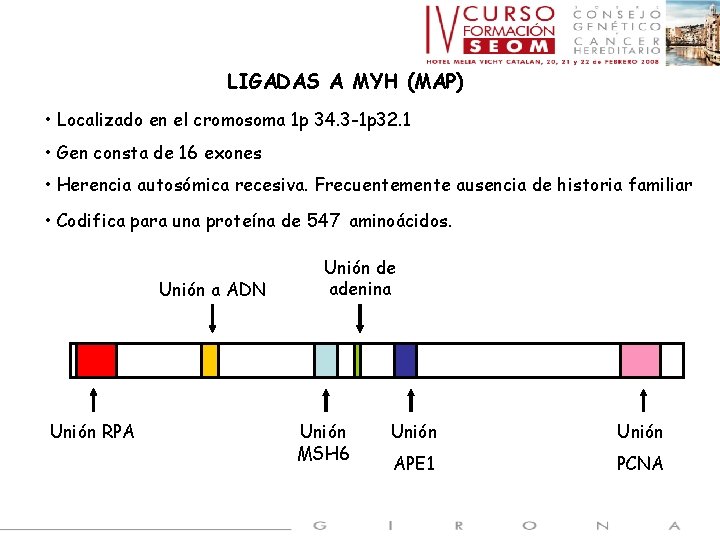
LIGADAS A MYH (MAP) • Localizado en el cromosoma 1 p 34. 3 -1 p 32. 1 • Gen consta de 16 exones • Herencia autosómica recesiva. Frecuentemente ausencia de historia familiar • Codifica para una proteína de 547 aminoácidos. Unión a ADN Unión RPA Unión de adenina Unión MSH 6 Unión APE 1 PCNA

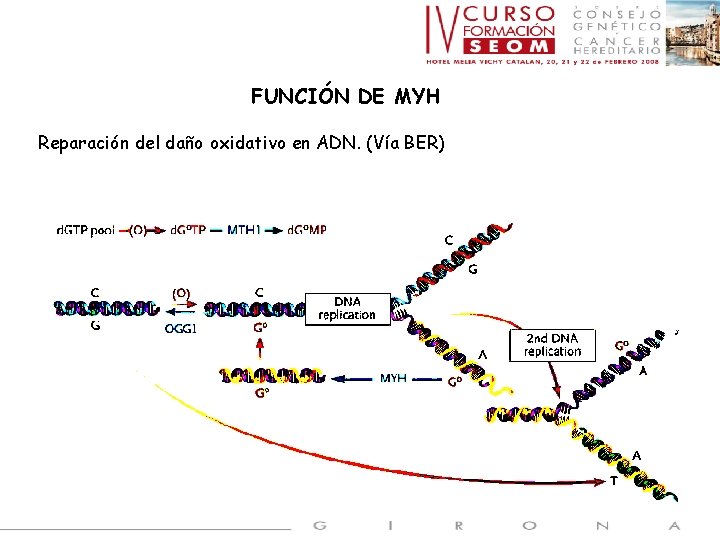
FUNCIÓN DE MYH Reparación del daño oxidativo en ADN. (Vía BER)

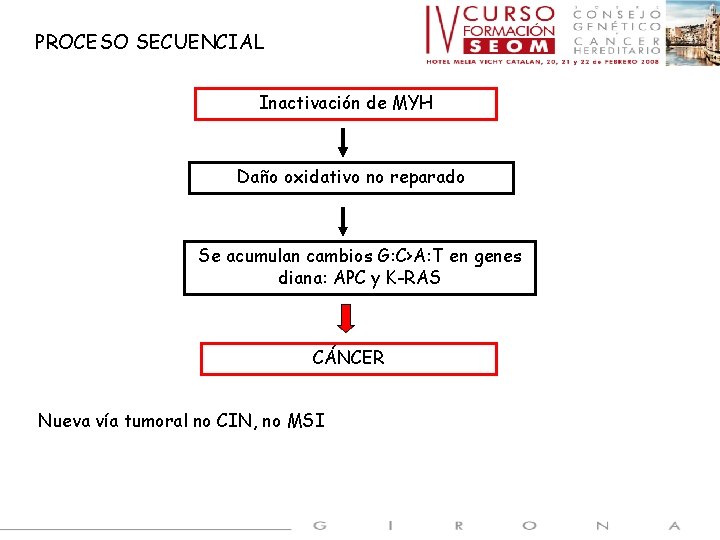
PROCESO SECUENCIAL Inactivación de MYH Daño oxidativo no reparado Se acumulan cambios G: C›A: T en genes diana: APC y K-RAS CÁNCER Nueva vía tumoral no CIN, no MSI

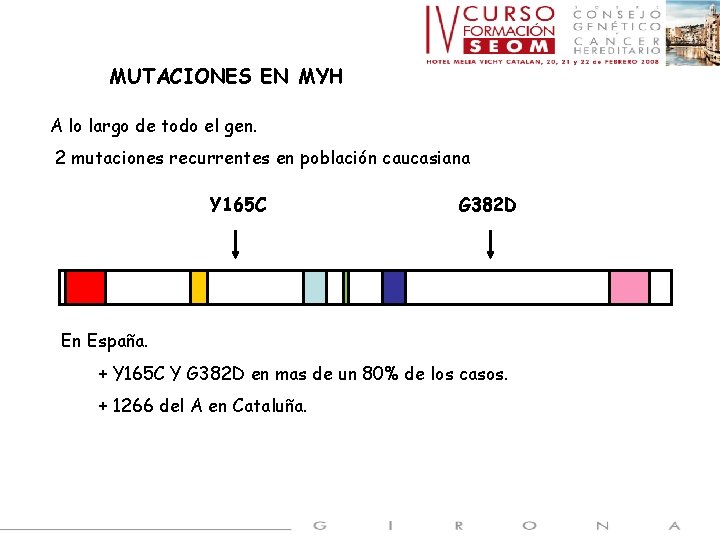
MUTACIONES EN MYH A lo largo de todo el gen. 2 mutaciones recurrentes en población caucasiana Y 165 C G 382 D En España. + Y 165 C Y G 382 D en mas de un 80% de los casos. + 1266 del A en Cataluña.

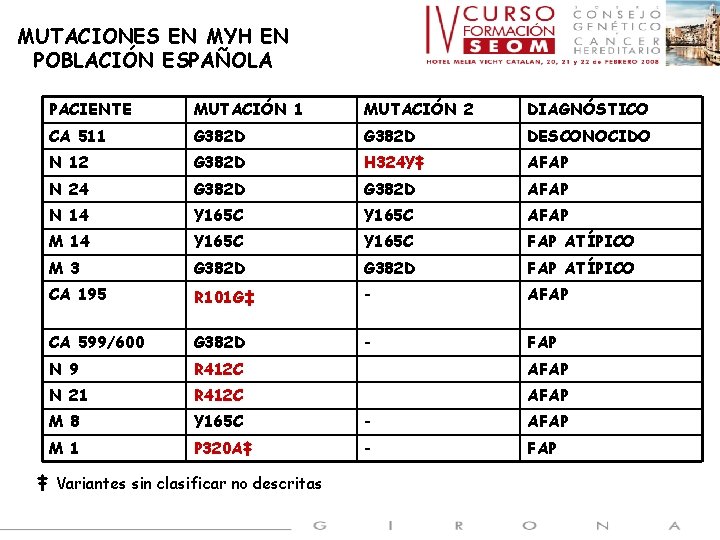
MUTACIONES EN MYH EN POBLACIÓN ESPAÑOLA PACIENTE MUTACIÓN 1 MUTACIÓN 2 DIAGNÓSTICO CA 511 G 382 D DESCONOCIDO N 12 G 382 D H 324 Y‡ AFAP N 24 G 382 D AFAP N 14 Y 165 C AFAP M 14 Y 165 C FAP ATÍPICO M 3 G 382 D FAP ATÍPICO CA 195 R 101 G‡ - AFAP CA 599/600 G 382 D - FAP N 9 R 412 C AFAP N 21 R 412 C AFAP M 8 Y 165 C - AFAP M 1 P 320 A‡ - FAP ‡ Variantes sin clasificar no descritas

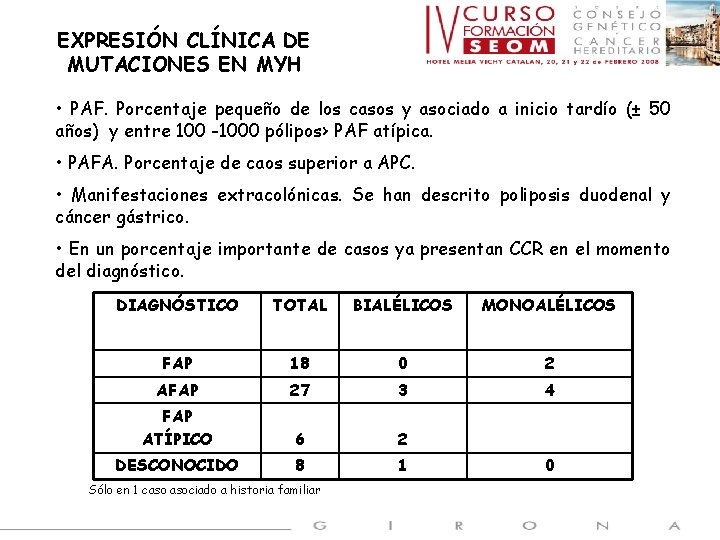
EXPRESIÓN CLÍNICA DE MUTACIONES EN MYH • PAF. Porcentaje pequeño de los casos y asociado a inicio tardío (± 50 años) y entre 100 -1000 pólipos› PAF atípica. • PAFA. Porcentaje de caos superior a APC. • Manifestaciones extracolónicas. Se han descrito poliposis duodenal y cáncer gástrico. • En un porcentaje importante de casos ya presentan CCR en el momento del diagnóstico. DIAGNÓSTICO TOTAL BIALÉLICOS MONOALÉLICOS FAP 18 0 2 AFAP 27 3 4 FAP ATÍPICO 6 2 DESCONOCIDO 8 1 Sólo en 1 caso asociado a historia familiar 0

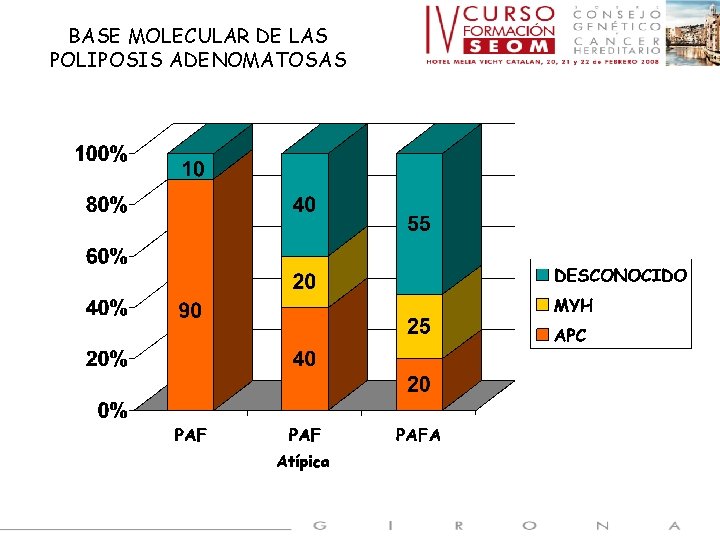
BASE MOLECULAR DE LAS POLIPOSIS ADENOMATOSAS Atípica

OTROS SÍNDROMES POLIPÓSICOS • Poliposis Hamartomatosas. + Mutaciones asociados a aumento del riesgo de CCR y herencia Autosómica Dominante. - Poliposis familiar juvenil. En un 80% de los casos se asocian en mutaciones en SMAD 4 o BMPR 1. - Síndrome de Peutz-Jeghers. Asociado a mutaciones en LKB 1. + Asociadas a mutaciones en PTEN. Patrón de herencia incierto, asociación a riesgo de CCR poco claro. - Síndrome de Cowden - Sindrome de Bannayan-Riley- Rubalcaba.

OTROS SÍNDROMES POLIPÓSICOS • Poliposis con adenomas serrados. + Nueva vía tumorogénica. Mutaciones en BRAF, hipermetilación, MSI-V. + Poliposis serrada. + Poliposis Hiperplásica familiar. Sin base molecular conocida + Poliposis mixta familiar. Herencia autosómica dominante, asociada al locus CRAC 1

SINDROMES NO POLIPÓSICOS

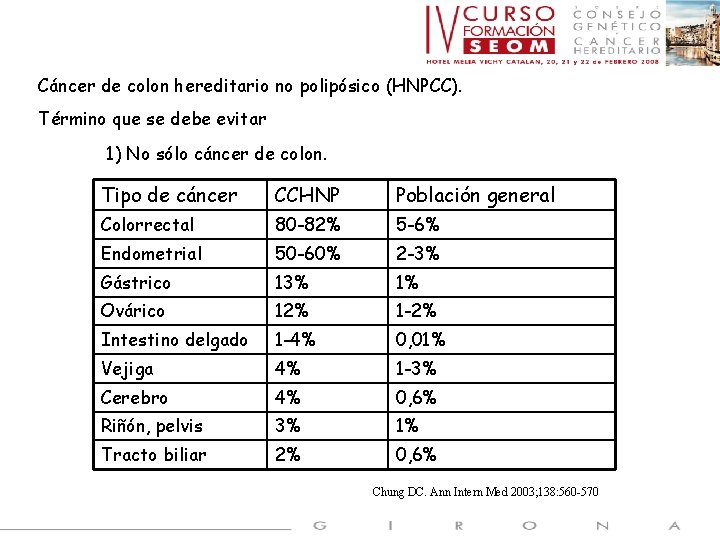
Cáncer de colon hereditario no polipósico (HNPCC). Término que se debe evitar 1) No sólo cáncer de colon. Tipo de cáncer CCHNP Población general Colorrectal 80 -82% 5 -6% Endometrial 50 -60% 2 -3% Gástrico 13% 1% Ovárico 12% 1 -2% Intestino delgado 1 -4% 0, 01% Vejiga 4% 1 -3% Cerebro 4% 0, 6% Riñón, pelvis 3% 1% Tracto biliar 2% 0, 6% Chung DC. Ann Intern Med 2003; 138: 560 -570

2) Denominación clínica sin una base molecular única. - Se puede confundir con ciertos casos de poliposis atenuada - Probablemente englobe 2 síndromes de base molecular diferente. + Asociado a fallos en la reparación de errores producidos en la replicación del ADN (MMR) : Síndrome de Lynch. + Síndrome de cáncer de colon familiar tipo X: No asociado a fallos en MMR

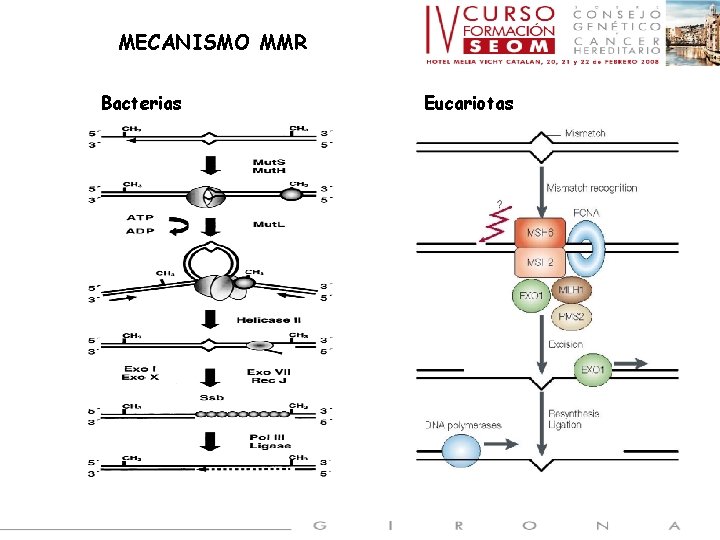
MECANISMO MMR Bacterias Eucariotas

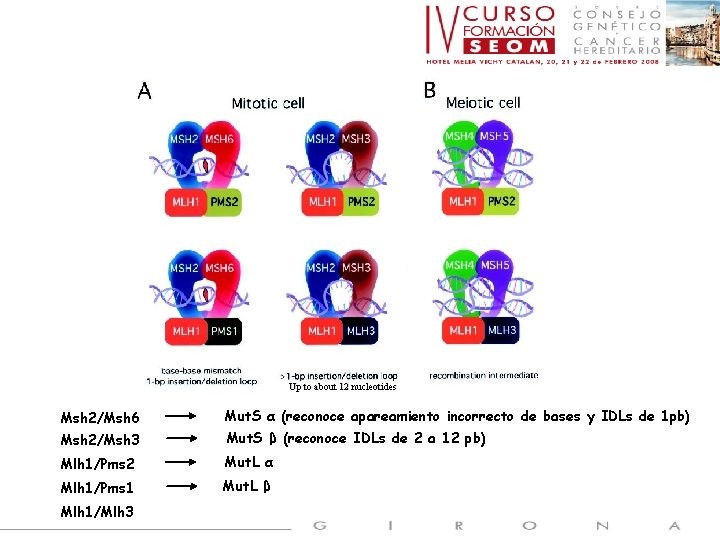
Up to about 12 nucleotides Msh 2/Msh 6 Mut. S α (reconoce apareamiento incorrecto de bases y IDLs de 1 pb) Msh 2/Msh 3 Mut. S β (reconoce IDLs de 2 a 12 pb) Mlh 1/Pms 2 Mut. L α Mlh 1/Pms 1 Mut. L β Mlh 1/Mlh 3

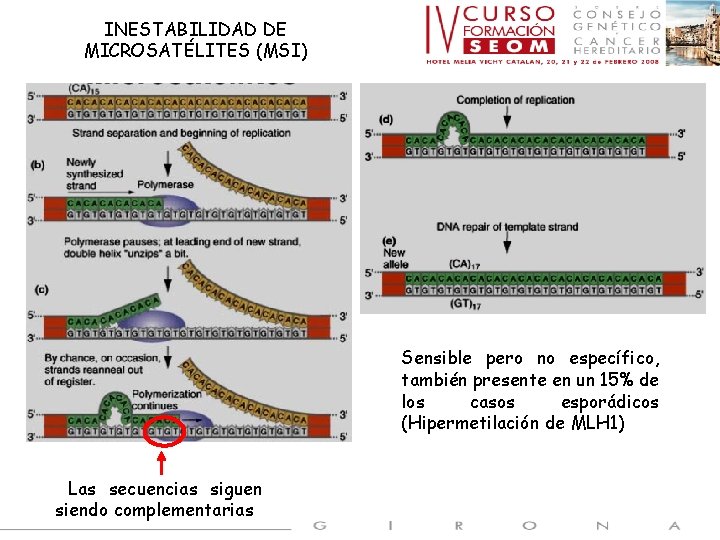
INESTABILIDAD DE MICROSATÉLITES (MSI) Sensible pero no específico, también presente en un 15% de los casos esporádicos (Hipermetilación de MLH 1) Las secuencias siguen siendo complementarias

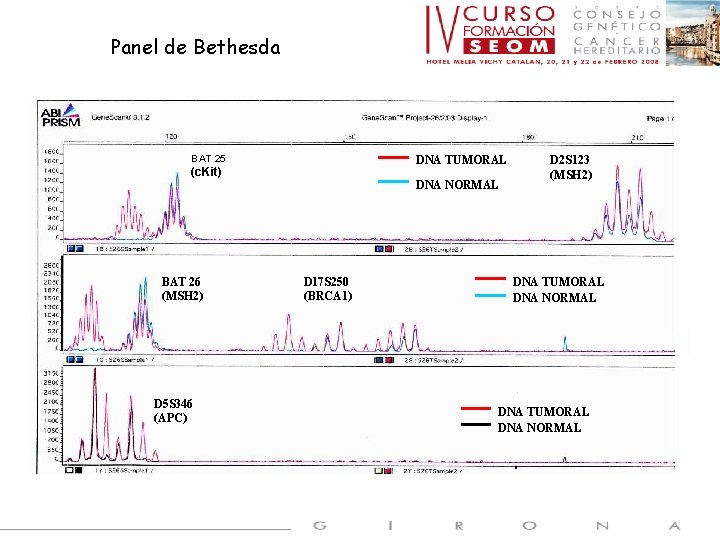
Panel de Bethesda BAT 25 DNA TUMORAL (c. Kit) BAT 26 (MSH 2) D 5 S 346 (APC) DNA NORMAL D 17 S 250 (BRCA 1) D 2 S 123 (MSH 2) DNA TUMORAL DNA NORMAL

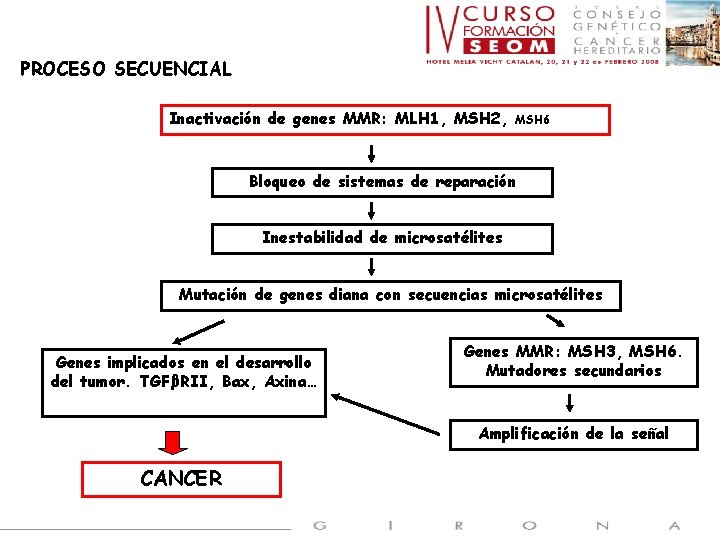
PROCESO SECUENCIAL Inactivación de genes MMR: MLH 1, MSH 2, MSH 6 Bloqueo de sistemas de reparación Inestabilidad de microsatélites Mutación de genes diana con secuencias microsatélites Genes implicados en el desarrollo del tumor. TGFβRII, Bax, Axina… Genes MMR: MSH 3, MSH 6. Mutadores secundarios Amplificación de la señal CANCER

Genes diana de inestabilidad en Síndrome de Lynch GEN FUNCIÓN TGFβRII Receptor de TGFβ ± 80% Adenoma BAX Factor pro-apoptótico ± 50% Adenoma MSH 3 MMR ± 40% Carcinoma MSH 6 MMR ± 25% Carcinoma Axina 2 Via Wnt ± 25% Adenoma TCF 4 Via Wnt ± 40% Adenoma RIZ 1 Apoptosis, ciclo celular ± 25% Adenoma IGFIIR Receptor de IGFII ± 20% Adenoma PTEN Via de PI 3 K ± 20% Adenoma PTHL 3 Metabolismo del Ca 2+ ± 80% Carcinoma ACTVR 2 Receptor de la Activina ± 70% Adenoma * En CCR PORCENTAJE* ESTADIO*.

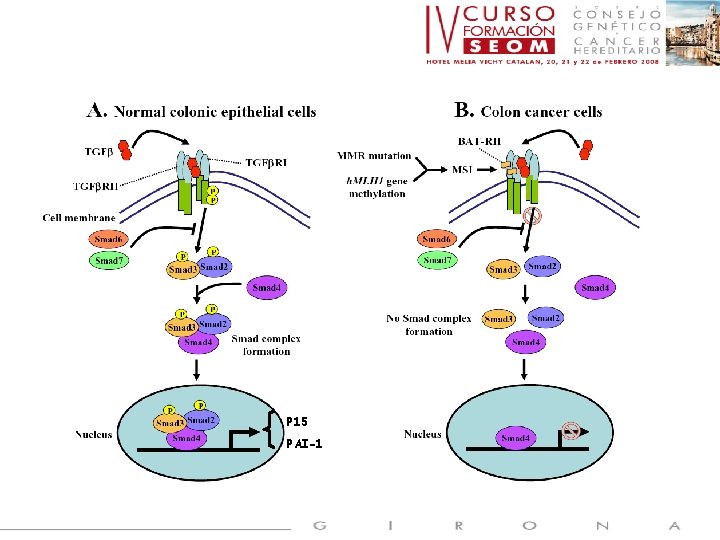
P 15 PAI-1

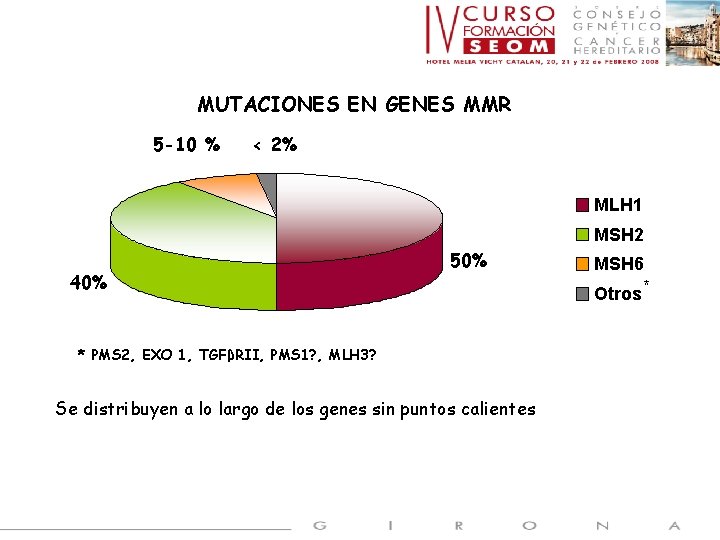
MUTACIONES EN GENES MMR 5 -10 % < 2% MLH 1 MSH 2 40% 50% * PMS 2, EXO 1, TGFβRII, PMS 1? , MLH 3? Se distribuyen a lo largo de los genes sin puntos calientes MSH 6 Otros *

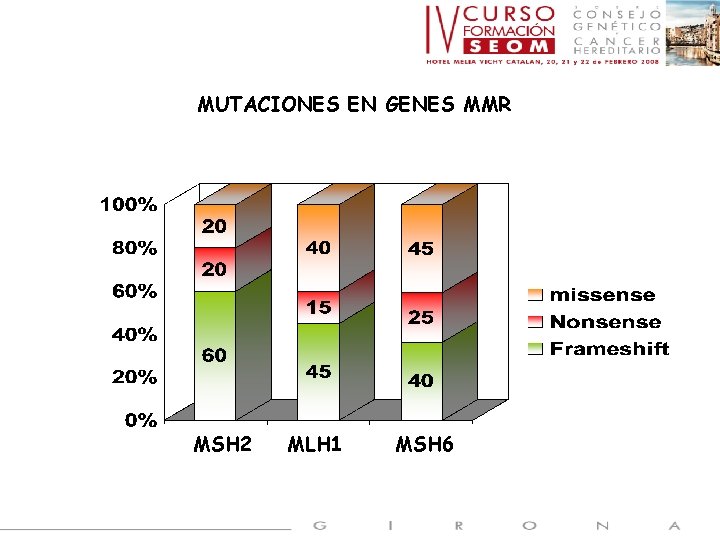
MUTACIONES EN GENES MMR MSH 2 MLH 1 MSH 6

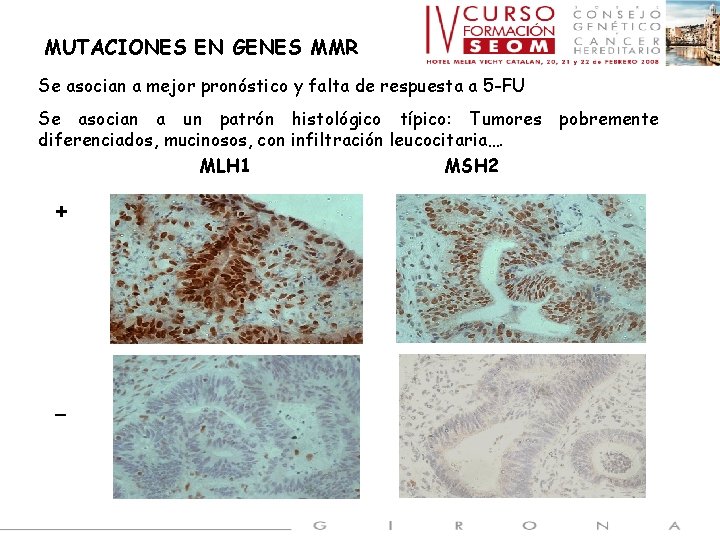
MUTACIONES EN GENES MMR Se asocian a mejor pronóstico y falta de respuesta a 5 -FU Se asocian a un patrón histológico típico: Tumores pobremente diferenciados, mucinosos, con infiltración leucocitaria…. MLH 1 MSH 2 + _

CLÍNICA ASOCIADA A MUTACIONES EN GENES MMR. Incluye: Endometrio, Ovario, gástrico, intestino delgado, tracto urinario, tracto biliar, páncreas, cerebro y glándulas sebáceas CCR fundamentalmente proximal

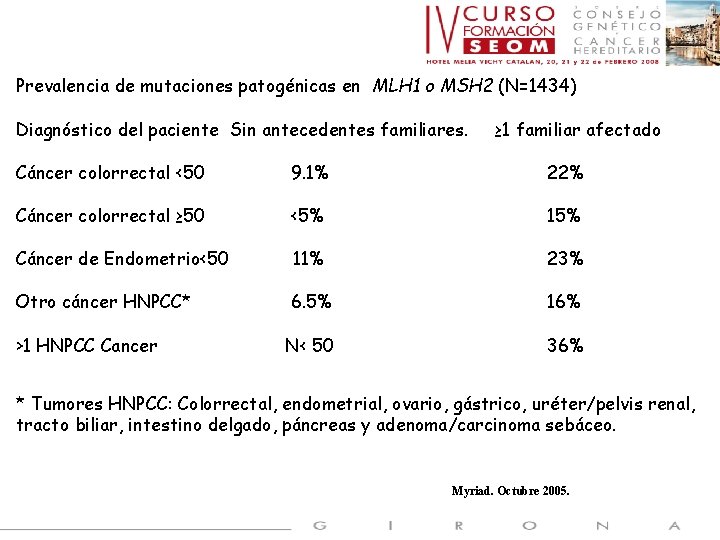
Prevalencia de mutaciones patogénicas en MLH 1 o MSH 2 (N=1434) Diagnóstico del paciente Sin antecedentes familiares. ≥ 1 familiar afectado Cáncer colorrectal <50 9. 1% 22% Cáncer colorrectal ≥ 50 <5% 15% Cáncer de Endometrio<50 11% 23% Otro cáncer HNPCC* 6. 5% 16% >1 HNPCC Cancer N< 50 36% * Tumores HNPCC: Colorrectal, endometrial, ovario, gástrico, uréter/pelvis renal, tracto biliar, intestino delgado, páncreas y adenoma/carcinoma sebáceo. Myriad. Octubre 2005.

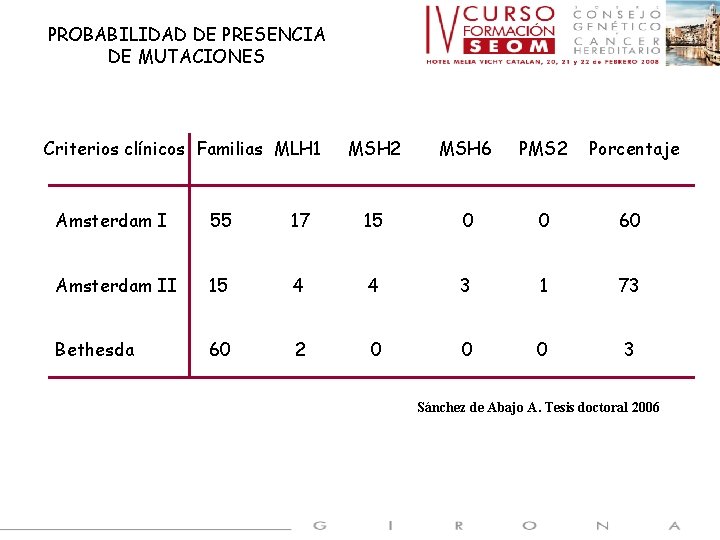
PROBABILIDAD DE PRESENCIA DE MUTACIONES Criterios clínicos Familias MLH 1 MSH 2 MSH 6 PMS 2 Porcentaje Amsterdam I 55 17 15 0 0 60 Amsterdam II 15 4 4 3 1 73 Bethesda 60 2 0 0 0 3 Sánchez de Abajo A. Tesis doctoral 2006

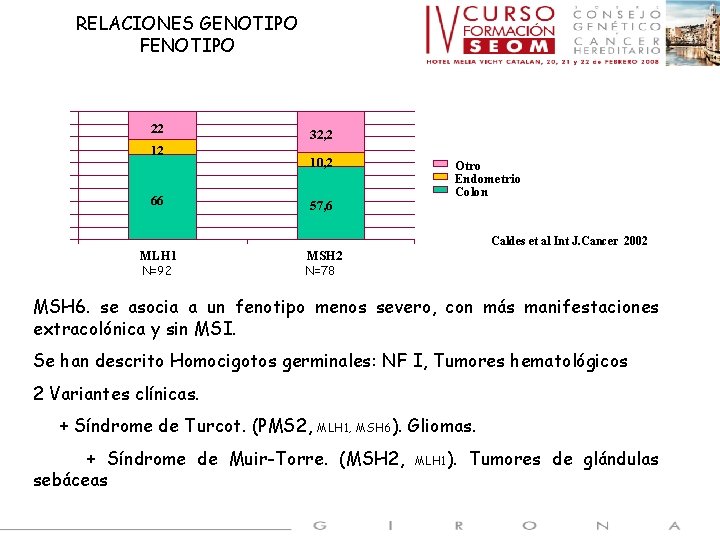
RELACIONES GENOTIPO FENOTIPO 53, 7 22 12 66 32, 2 10, 2 57, 6 Otros Endometrio Colon 30, 5 Caldes et al Int J. Cancer 2002 MLH 1 N=92 MSH 2 N=78 MSH 6. se asocia a un fenotipo menos severo, con más manifestaciones extracolónica y sin MSI. Se han descrito Homocigotos germinales: NF I, Tumores hematológicos 2 Variantes clínicas. + Síndrome de Turcot. (PMS 2, MLH 1, MSH 6 ). + Síndrome de Muir-Torre. (MSH 2, sebáceas Gliomas. MLH 1). Tumores de glándulas

CÁNCER COLORRECTAL FAMILIAR TIPO X • Características clínicas comparadas con síndrome de Lynch. . + Menor incidencia CCR + No predominio de colon proximal + No predominio de mucinosos, pobremente diferenciados + No se asocia a tumores extracolónicos. + Edad aparición de tumores más tardía Lindor NM et al JAMA 2005

CÁNCER COLORRECTAL FAMILIAR TIPO X • Características Moleculares. + No asociado a alteraciones en MMR + Contenido DNA aneuploide: CIN en al menos un 40% de los casos. + Patrón de mutaciones en KRAS y p 53 intermedia entre CIN y MSI + Vía Wnt no afectada: No hay presencia de β-catenina intranuclear Sánchez de Abajo A et al. Clin Cancer Res 2007. Abdel-Raman WM et al. Oncogene 2005

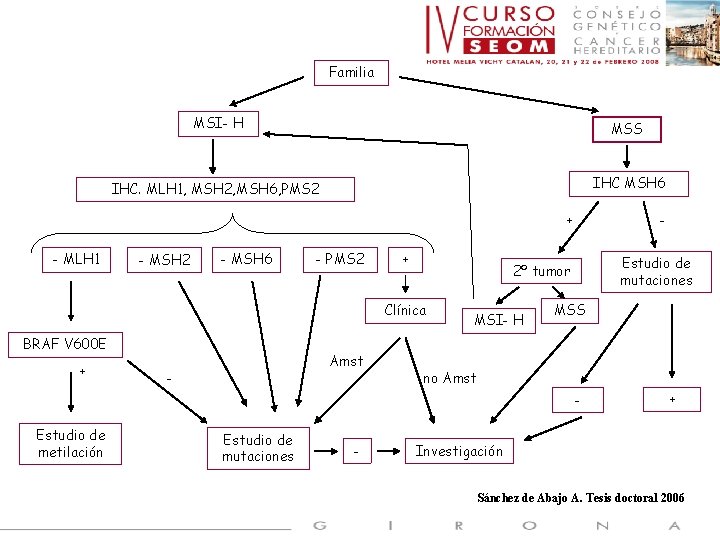
Familia MSI- H MSS IHC. MLH 1, MSH 2, MSH 6, PMS 2 IHC MSH 6 + - MLH 1 - MSH 2 - MSH 6 - PMS 2 + + Amst - Estudio de mutaciones 2º tumor Clínica BRAF V 600 E - MSI- H MSS no Amst - Estudio de metilación Estudio de mutaciones - + Investigación Sánchez de Abajo A. Tesis doctoral 2006

ALELOS DE BAJA PENETRANCIA • Asociados a cáncer familiar y esporádico. • Riesgo de cáncer asociado bajo pero prevalencia alta Explican un porcentaje elevado de tumores Gen Alelo APC 1307 K 5 -7 (Ashkenazis) 1. 5 -2. 2 3 -7% TGFβR 1 6 ala 14 (Caucasianos) 1. 2 3% HRAS 1 VNTR 1 -6 (Caucasianos) 2. 5 1 -8% MTHFR 677 V 32 -43 (Caucasianos) 0. 75 - Ash 0. 8 (Ashkenazis) 2. 4 1% BLM Frecuencia Riesgo relativo Porcentaje de CCR atribuible • Otros genes con alelos asociados a CCR. NAT 2, CHECK 2, CCND 1 • ¿Alelos en genes de alta penetrancia (APC I 1307 Q, MLH 1 D 132 H) • ¿Heterozigotos para MYH?

ALELOS DE BAJA PENETRANCIA Búsquedas genómicas. + Se estudian simultáneamente mas de 300. 000 SNPs distribuidos a lo largo de todo el genoma y se compara frecuencias en casos y controles. + 8 q 24: Fuerte evidencia de asociación. También asociado a mayor riesgo de cáncer de próstata. + 9 p 24, 3 q 21 -q 24.

GENES MODIFICADORES • Gran variabilidad fenotípica para una misma mutación, incluso, dentro de la misma familia Factores genéticos. • Los modelos animales no se corresponden con lo que pasa en humanos. • Se han identificado algunos alelos que varían el fenotipo. + PAF. Varían la severidad - NAT 1 - NAT 2. Acetiladores rápidos. + Síndrome de Lynch. Varía la edad de diagnóstico. - CCND 1 - IGF-1 - p 53 - CYP 1 A 1 - GSTT 1, GSTM 1