Asocijacije Autor Jelena Muci HEMIJSKE VEZE Autor Jelena












- Slides: 21

Asocijacije Autor: Jelena Mucić



HEMIJSKE VEZE Autor: Jelena Mucić

VEZE? romantična a ka ja tajn wi-fi a genetska n v r o a neraskidiva d b binsk jl u kratka a veza luka politička krvna a prijateljska bračna n v i n a j terne t i poslovna n drugarska e l e z a z e periodična v radio postojana dnevna a b lasaobraćajna s duga telefonska

HEMIJSKE VEZE ZAŠTO NASTAJU HEMIJSKE VEZE? KO GRADI HEMIJSKE VEZE? KAKVE SU TO SILE PRIVLAČENJA? DA LI SU TO STABILNE VEZE?

Odgovor tražimo u PSE

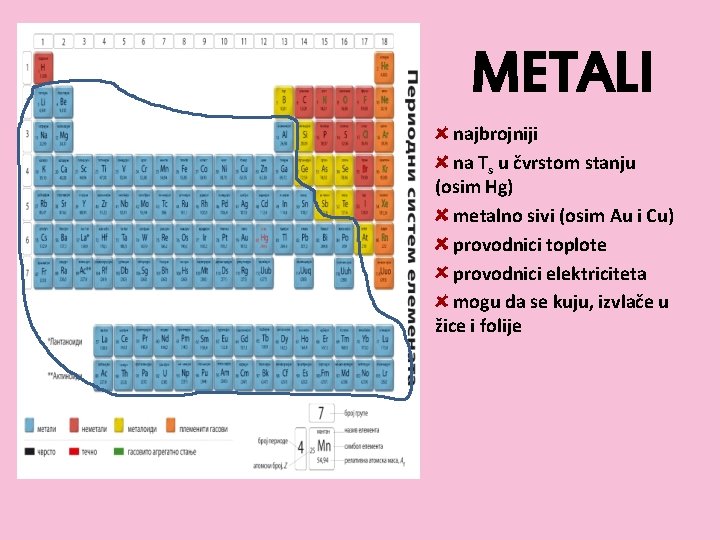
METALI najbrojniji na Ts u čvrstom stanju (osim Hg) metalno sivi (osim Au i Cu) provodnici toplote provodnici elektriciteta mogu da se kuju, izvlače u žice i folije

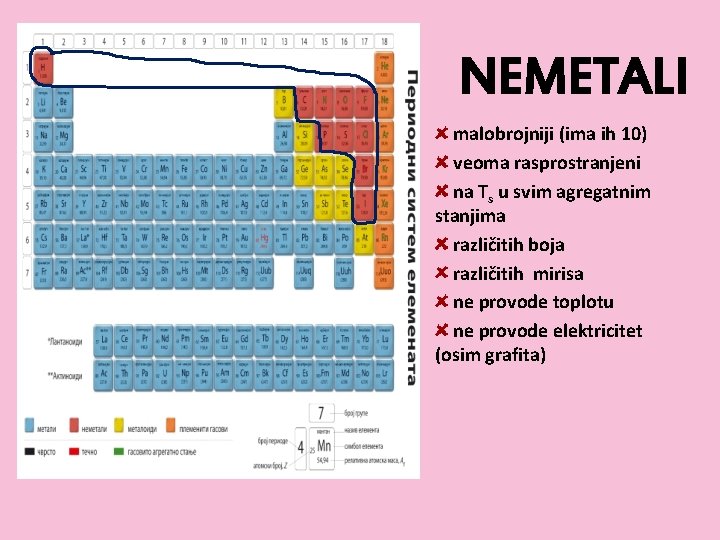
NEMETALI malobrojniji (ima ih 10) veoma rasprostranjeni na Ts u svim agregatnim stanjima različitih boja različitih mirisa ne provode toplotu ne provode elektricitet (osim grafita)

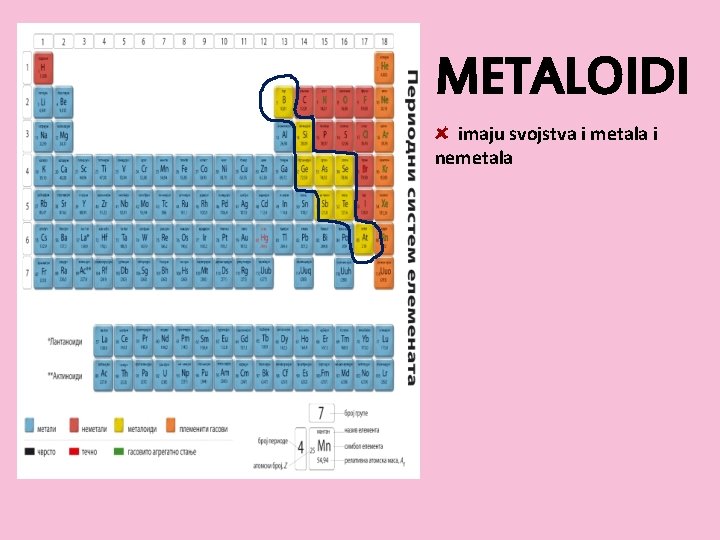
METALOIDI imaju svojstva i metala i nemetala

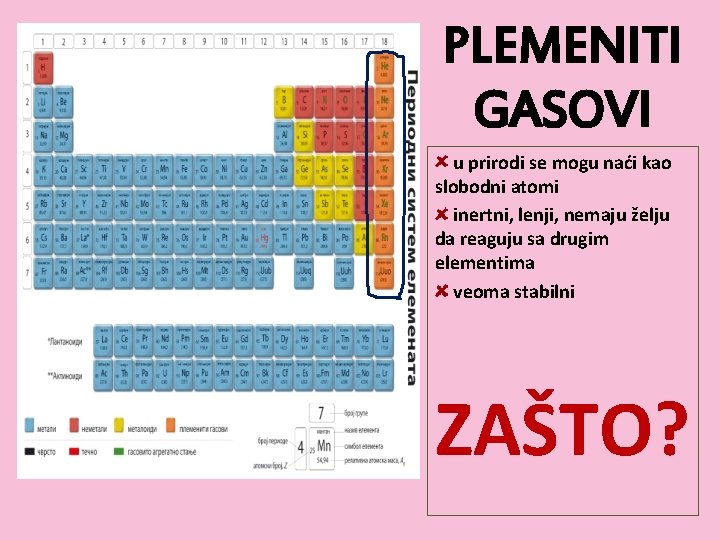
PLEMENITI GASOVI u prirodi se mogu naći kao slobodni atomi inertni, lenji, nemaju želju da reaguju sa drugim elementima veoma stabilni ZAŠTO?

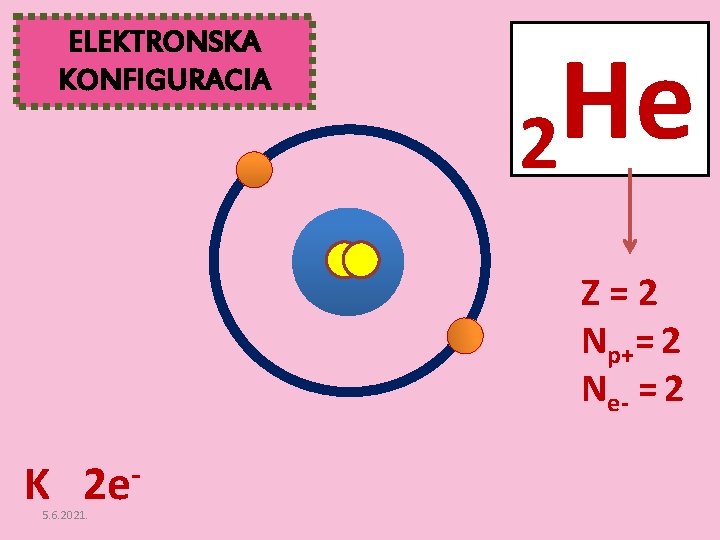
ELEKTRONSKA KONFIGURACIA He 2 Z=2 Np+= 2 Ne- = 2 K 2 e 5. 6. 2021.

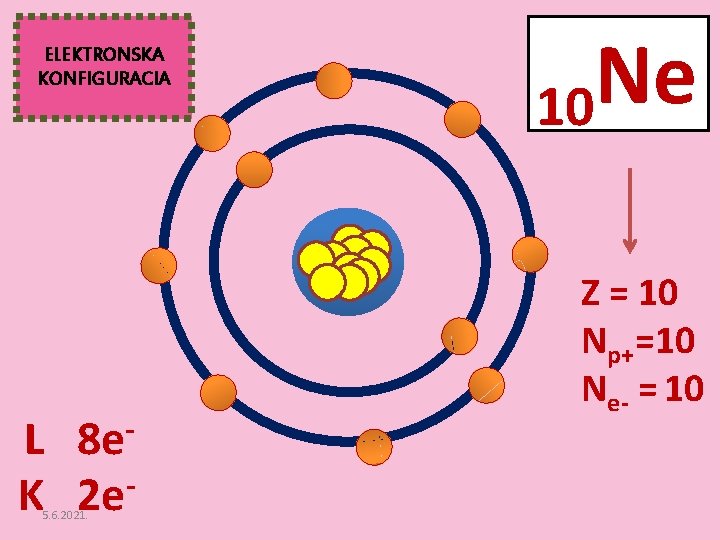
ELEKTRONSKA KONFIGURACIA 8 e L K 2 e 5. 6. 2021. Ne 10 Z = 10 Np+=10 Ne- = 10

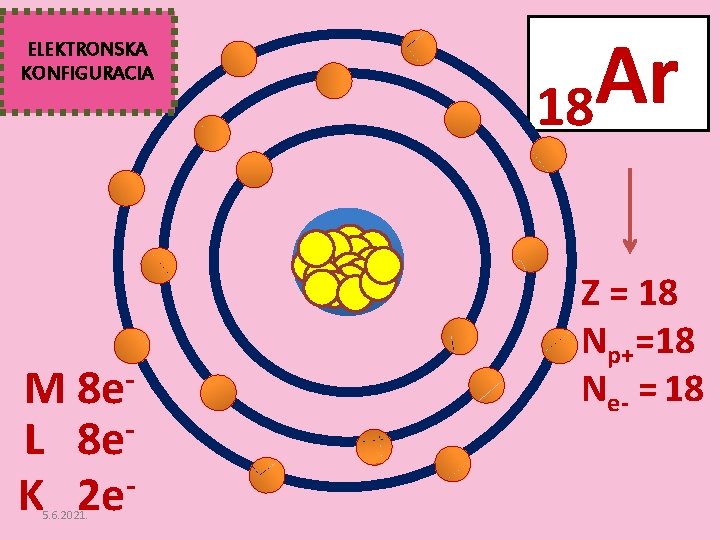
ELEKTRONSKA KONFIGURACIA M 8 e. L 8 e K 2 e 5. 6. 2021. Ar 18 Z = 18 Np+=18 Ne- = 18

ELEKTRONSKA KONFIGURACIA • poslednji energetski nivo plemenitih gasova popunjen je maksimalnim brojem elektrona helijum- dva, a ostali osam dublet oktet Sve u prirodi teži da postigne što veću stabilnost! Svi elementi teže da postignu stabilnu elektronsku konfiguraciju najbližeg plemenitog gasa

STABILNOST stalno kretanje čestica supstanci, sudaranje zbog težnje da se postigne što niža energija, odnosno da se postigne elektronska konfiguracija najbližeg plemenitog gasa, dolazi do pregrupisavanja i stvaranja stabilnijih celina u stabilne celine povezuje se najmanje dva atoma istog ili različitog hemijskog elementa, a broj ovih atoma može biti i po nekoliko hiljada MOLEKULI su stabilne celine udruženih atoma

MOLEKULI atomi u molekulima više nisu nezavisni jedni od drugih slobodan atom se predstavlja simbolom H, Na, K, Mg 2 H – dva atoma vodonika KOEFICIJENT molekule predstavljamo hemijskim formulama H 2 O, Na. Cl, C 6 H 12 O 6 INDEKS

HEMIJSKA FORMULA Hemijska formula ima dvojako značenje: * KVALITATIVNO – pokazuje o kojoj supstanci je reč i od kojim atoma se sastoji molekul * KVANTITATIVNO – pokazuje odnos broja atoma pojedinih elemenata u tom molekulu i predstavljaju jedan molekul te supstance

HEMIJSKA FORMULA 7 H 2 SO 4 - sedam molekula sumporne kiseline 7 – koeficijent 2, 4 – indeksi jedan molekul sumporne kiseline ima 2 atoma vodonika, jedan atom sumpora i četiri atoma kiseonika H 2 SO 4 ( H, H, S, O, O) sedam molekula sumporne kiseline ima 7 x 2=14 H, 7 x 1=7 S, 7 x 4=28 O, ukupno 49 atoma

VRSTA VEZE Privlačne sile koje drže čestice na okupu nazivaju se hemijske veze atomi mogu graditi molekule: * udruživanjem svojih valentnih elektrona sa elektronima drugih atoma u zajedničke elektronske parove KOVALENTNA VEZA - grade je nemetali među sobom * primanjem ili otpuštanjem elektrona JONSKA VEZA - grade je metali i nemetali

Ovo je OKSITOCIN – molekul ljubavi Još ne znate kakve su hemijske veze unutar ovog molekula, ali ne sumnjam da ste uspeli da se zaljubite!