Asitler ve Bazlar 2 ASTBAZ TANIMI Arrhenius Asit

Asitler ve Bazlar
2 ASİT-BAZ TANIMI Arrhenius Asit - Baz. Tanımı Bronsted Lowry Asit-Baz Tanımı Lewis Asit. Baz Tanımı 08. 05. 2014
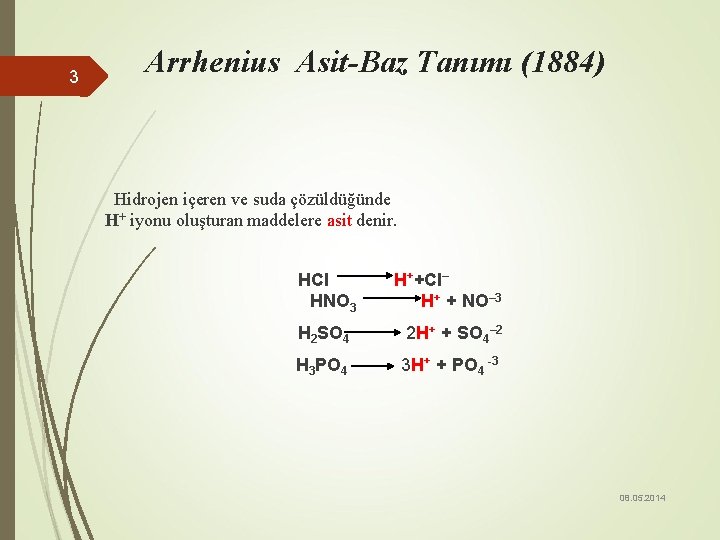
3 Arrhenius Asit-Baz Tanımı (1884) Hidrojen içeren ve suda çözüldüğünde H+ iyonu oluşturan maddelere asit denir. HCI HNO 3 H++Cl– H+ + NO– 3 H 2 SO 4 2 H+ + SO 4– 2 H 3 PO 4 3 H+ + PO 4 -3 08. 05. 2014

4 Bronsted-Lowry Asit-Baz Tanımı (1923) Proton (H+ )iyonu verme eğiliminde olan maddelere asit denir. HCl + H 2 O Cl– + H 3 O+ Asit + Baz + Asit Proton (H+ ) iyonu alma eğiliminde olan maddelere baz denir. NH 3 + H 2 O NH 4+ + OHBaz + Asit + Baz 08. 05. 2014
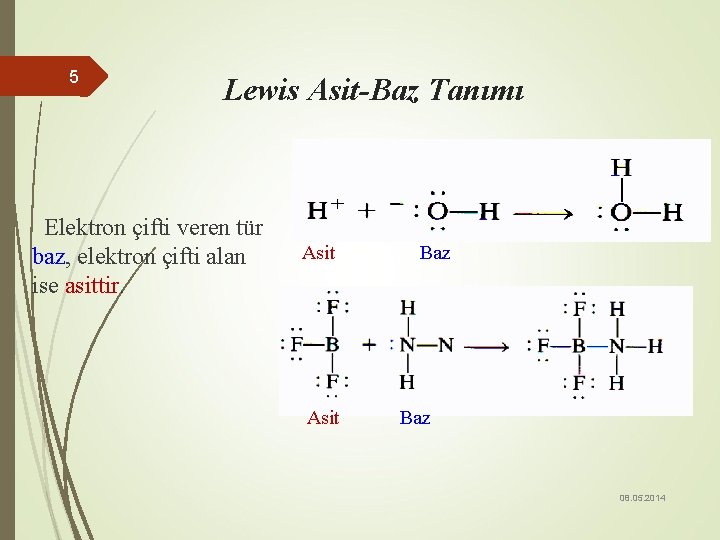
5 Lewis Asit-Baz Tanımı Elektron çifti veren tür baz, elektron çifti alan ise asittir. Asit Baz 08. 05. 2014
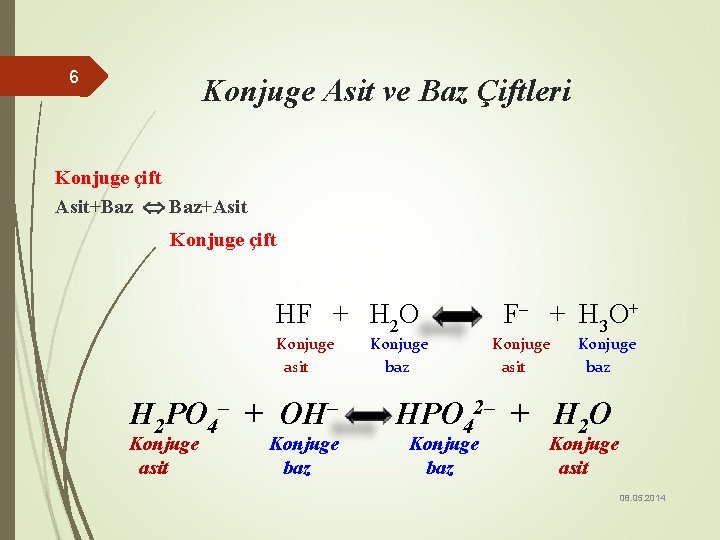
6 Konjuge Asit ve Baz Çiftleri Konjuge çift Asit+Baz Baz+Asit Konjuge çift HF + H 2 O Konjuge asit H 2 PO 4– + OH– Konjuge asit Konjuge baz F– + H 3 O+ Konjuge asit Konjuge baz HPO 42– + H 2 O Konjuge baz Konjuge asit 08. 05. 2014

7 Asit Ve Bazların Kuvveti Elektrolit Suda ve bazı çözücülerde çözündüğü zaman iyonlaşarak elektriği ileten çözeltilere elektrolit denir. Kuvvetli elektrolitler bir çözücüde tamamen, zayıf elektrolitler ise kısmen iyonlaşır. 08. 05. 2014

8 Asit Ve Bazların Kuvveti Kuvvetli Asit Kuvvetli baz Suda tamamen iyonlaşan asitlere kuvvetli asit denir. Suda tamamen iyonlaşan bazlara kuvvetli baz denir. HCl, HBr, HI, HF , HCN, HNO 3, H 2 SO 4 Na. OH, KOH, Li. OH, Rb. OH, Cs. OH 08. 05. 2014

9 Asit Ve Bazların Kuvveti Zayıf Asitler Zayıf bazlar Suda kısmen iyonlaşan bazlara denir. asitlere denir. Örnek; (RCOOH), CH 3 COOH (NH 3) Aminler C 6 H 5 COOH, H 2 S, H 2 CO 3, (RNH 2, R 2 NH, R 3 N), H 2 SO 3 CH 3 CH 2 NH 2, (CH 3)2 H, (C 3 H 7)3 N, C 5 H 5 N 08. 05. 2014

10 Asitlerin Özellikleri 1 - Sulu çözeltileri elektrik akımını iletir. 2 - Sulu çözeltilerinin tatları ekşidir (limon, sirke gibi). 3 - Turnusol kağıdının rengini maviden kırmızıya dönüştürürler. 4 - Sulu çözeltilerine, (suda çözündüklerinde) hidrojen iyonu (H+) verirler. 5 - Plastik ve camlara etki edemezler. 6 - Saf haldeyken elektrik akımını iletmezler. 7 - Yakıcı özelliktedirler. 8 - Bazlarla birleşerek nötrleşirler ve tuz ile su oluşturup ısı açığa çıkarırlar. Nötrleşme tepkimeleri ekzotermiktir. 9 - Aktif Metallerle tepkimeye girerek metal tuzu oluştururlar ve H 2 (hidrojen) gazı açığa çıkarırlar. 08. 05. 2014

11 Asitin Değerliği Bir asitin değerliği suya verdiği H+ iyonu miktarına yada (H) sayısına bağlıdır. HCl → H+ + Cl- (1 değerlikli) HNO 3 → H+ + NO 3 - (1 değerlikli) H 2 SO 4 → 2 H+ + SO 4 -2 (2 değerlikli) H 3 PO 4 → 3 H+ + PO 4 -3 (3 değerlikli) Not: Asitlerin üzerine su ilave edilmez. 08. 05. 2014
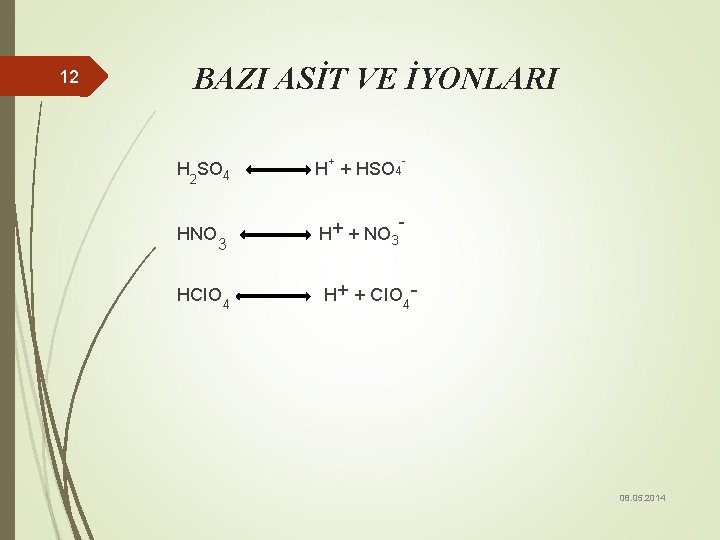
12 BAZI ASİT VE İYONLARI - + H 2 SO 4 H + HSO 4 HNO + H + NO 3 HCIO 4 3 H+ + CIO 4 - 08. 05. 2014

13 Günlük Hayatta Kullanılan Bazı Asitler Sirke, seyreltik bir asetik asit(CH 3 COOH) çözeltisidir. Araba akülerinde sülfürik asit (H 2 SO 4) kullanılır. Nitrik asit (HNO 3 ), boya ve gübre yapımında kullanılır. Temizlikte kullanılan tuz ruhu seyreltik hidroklorik asit (HCl)çözeltisidir. 08. 05. 2014

14 Bazların Özellikleri Baz içine fenolftalein çözeltisi damlatıldığında, baz pembe renk alır. Fenolftalein asit içine konulduğunda asitin rengini değiştirmez. Bazlar da asitler gibi suda iyonlarına ayrıştıkları için elektrik akımını iletir. Na. OH ve KOH kuvvetli bazlardır. Kuvvetli bazlar metallere ve dokulara tahriş edici etki yapar. Amonyağın buharı göze, burna ve solunum yoluna zarar verir. 08. 05. 2014

15 08. 05. 2014

16 08. 05. 2014

17 Günlük Hayatta Bazların Kullanım Alanları Sodyum hidroksit ( Na. OH ) sabun yapımında kullanılır. Bu yüzden sabun ağzımıza ve gözümüze değdiğinde acı verir. Diş macunu ve şampuanlarda da baz olduğu için acı tat verir. Amonyaklı sıvı maddeler, yağ ve kireç sökücü olarak ev temizleyicilerinde kullanılır. 08. 05. 2014

18 Bazların Değerliği Bir bazın değerliği suya verdiği OH- iyonunun miktarına yada yapısındaki OH sayısına bağlıdır. Na. OH KOH Ca(OH)2 Al(OH)3 - Na+ + OH (1 değerlikli ) K+ + OH (1 değerlikli ) Ca+2 + 2 OH (2 değerlikli ) Al+3 + 3 OH (3 değerlikli ) 08. 05. 2014
![Asit ve Baz Derecesinin Belirlenmesi Eğer ; çözeltide [ H ] > [OH-] ise Asit ve Baz Derecesinin Belirlenmesi Eğer ; çözeltide [ H ] > [OH-] ise](http://slidetodoc.com/presentation_image/48bbbb6aa1f0fe93544bc9fc0caf4397/image-19.jpg)
Asit ve Baz Derecesinin Belirlenmesi Eğer ; çözeltide [ H ] > [OH-] ise bu çözelti asidiktir. + Bir çözeltide içindeki asit ya da baz derecesini belirleyen H+ ya da OHiyonu miktarıdır. Eğer ; çözeltide [ H ] = [OH-] ise bu çözelti nötrdür. + Eğer ; çözeltide [OH + ] > [ H ] ise bu çözelti baziktir.

20 p. H Ölçüsü Bir sıvı çözeltideki asit miktarı, p. H ölçüsü olarak adlandırılan bir yöntemle tespit edilir. Bunun için p. H kâğıdı ya da p. H metre aleti kullanılır. p. H kâğıdı çözeltinin asitlik derecesine göre renk değiştirir. p. H ölçüsüne göre çözeltinin asitliği 0 - 14 arasında değerlendirilir. 08. 05. 2014
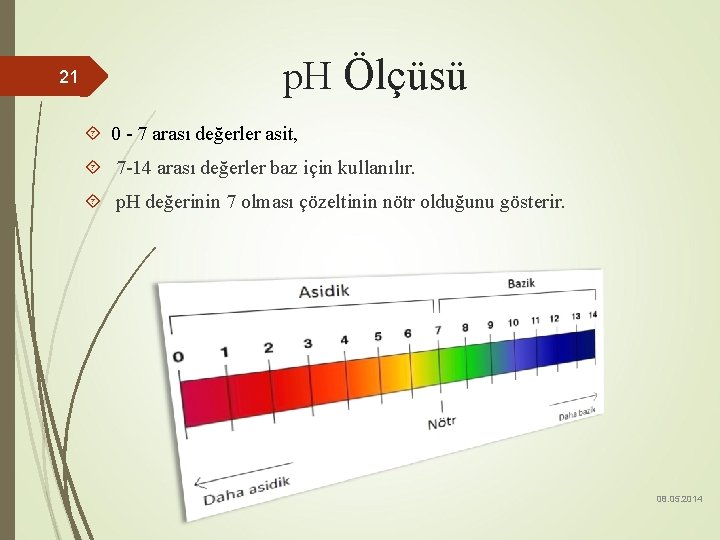
21 p. H Ölçüsü 0 - 7 arası değerler asit, 7 -14 arası değerler baz için kullanılır. p. H değerinin 7 olması çözeltinin nötr olduğunu gösterir. 08. 05. 2014

Ph Nedir? 22 p. H , bir çözeltinin asitlik veya bazlık derecesini tarif eden ölçü birimidir. 0'dan 14'e kadar olan bir skalada ölçülür. p. H teriminde p; eksi logaritmanın matematiksel sembolünden ve H ise Hidrojenin kimyasal formülünden türetilmişlerdir. p. H = - log[H 3 O+] H 2 O(s) + H 2 O(s) veya p. H = - log[H+] + H 3 O +OH - -14 2 + K[H 2 O] Ksu = [H 3 O ][OH ] = 1. 0 × 10 (25 o. C ) 08. 05. 2014

23 p. H Saf suda Hidronyum iyonu ve Hidroksil iyonu konsantrasyonları eşittir. [H 3 O+] = [OH-] = 1. 0 x 10 -7 (25°C) p. H < 7. 00 asidik çözeltiler p. H = 7. 00 nötr çözeltiler p. H > 7. 00 bazik çözeltiler 08. 05. 2014

24 p. H Hesaplamaları Kuvvetli Asit ve Bazlarda Kuvvetli asitlerde p. H direkt kuvvetli asitten gelen H+ iyonu konsantrasyonu kullanarak hesaplanır. Burada suyun iyonlaşmasından gelen H+ ve OH- iyonları ihmal edilir. ıf Asit ve Bazlarda Zayıf asit ve bazlarda asitlik veya bazlık denge sabiti kullanılır. Burada suyun iyonlaşmasından gelen H+ ve OH- iyonları duruma göre ihmal edilir veya edilmez. 08. 05. 2014

25 Zayıf Asit ve Bazlarda İyonlaşma Zayıf asit ve bazlarda asitlik veya bazlık denge sabiti kullanılır. HA(aq) + H 2 O(s) Ka = [H 3 O+] [A-] [HA] CH 3 COOH + H 2 O Ka= H 3 O+(aq) + A (aq) H 3 O+ + CH 3 COO- [H 3 O+] [CH 3 COO-] [CH 3 COOH] 08. 05. 2014
- Slides: 25